Ćwiczenie # 1. Plik wejściowy dla czasteczki N 2. Omówienie elementów pliku wejściowego
|
|
|
- Franciszek Kowalik
- 6 lat temu
- Przeglądów:
Transkrypt
1 Ćwiczenie # 1. Obliczenia metoda Hartree-Focka dla czasteczek N 2 i O 2 Wykonamy dziś obliczenia energii elektronowej dla cząsteczek N 2 i O 2 metodą Hartree-Focka (HF). Dla zamkniętopowłokowej cząsteczki N 2 wykorzystamy wariant tej metody z restrykcją spinową (RHF, ang. restricted HF), natomiast dla otwartopowłokowej cząsteczki O 2 wariant bez restrykcji spinowej (UHF, ang. unrestricted HF). Obejrzymy orbitale molekularne oraz wykonamy optymalizację geometrii. Jednym z podstawowych celów tego ćwiczenia jest zaznajomienie się z programami Gaussian i MOLDEN, jak również z typowymi procedurami (przygotowywanie pliku wejściowego, uruchamianie obliczeń, analiza pliku wynikowego, wizualizacja orbitali, oglądanie przebiegu optymalizacji geometrii) oraz ważnymi pojeciami (metoda Hartree-Focka w wariancie RHF i UHF, procedura SCF, energia orbitalna, energia całkowita (energia elektronowa) i przyczynki do niej, orbitale molekularne, układ zamkniętopowłokowy i otwartopowłokowy, zanieczyszczenie spinowe w metodzie UHF). Plik wejściowy dla czasteczki N 2 Przykładowy plik wejściowy dla programu Gaussian, definiujący obliczenia energii metodą RHF w bazie 6-31G(d) dla cząsteczki N 2 w eksperymentalnej geometrii (odległość N N wynosi Å): #P RHF/6-31G(d) GFInput Pop=Full IOP(6/80=1) obl. energii metoda RHF dla N2 w geometrii eksperymentalnej 0 1 N N Omówienie elementów pliku wejściowego Powyższy przykład jest jednym z najprostszych, a bardziej zaawansowane elementy poznamy w trakcie kolejnych ćwiczeń. Pełne omówienie składni pliku wejściowego można znaleźć w dokumentacji programu Gaussian. Na początku pliku wejściowego znajduje się sekcja kierujaca (ang. route section), którą poznajemy po początkowym znaku #. W sekcji kierującej umieszczamy słowa kluczowe definiujące sposób prowadzenia obliczeń, stosowaną metodę chemii kwantowej, bazę funkcyjną, itd. #P (P bezpośrednio po znaku #) włącza bardziej szczegółowe raportowanie wyników obliczeń w stosunku do domyślnego, normalnego poziomu (#N); RHF/6-31G(d) jest to specyfikacja metody obliczeniowej (tu: metoda RHF) i bazy funkcyjnej (tu: 6-31G(d)). Więcej o bazach funkcyjnych i ich oznaczeniach dowiemy się w jednym z kolejnych ćwiczeń. Symbol metody i bazy są zawsze rozdzielone znakiem / (bez odstępów). GFInput oznacza, że w pliku wynikowym znajdzie się definicja używanej baza funkcyjnej. Umożliwi to późniejszą wizualizację orbitali molekularnych w programie MOLDEN. 1
2 Pop skrót od Population. To słowo kluczowe kontroluje sposób wyświetlania orbitali molekularnych oraz wykonanie tzw. analiz populacyjnych. W przykładzie powyżej mamy Pop z opcją Full, co oznacza że żądamy wypisywanie współczynników rozwinięcia orbitali molekularnych oraz wykonania pełnej analiza populacyjnej metodą Mullikena. Uwaga: zapisy Pop=Full, Pop(Full), jak również Pop=(Full) są równoważne. Gdy do słowa kluczowego chcielibyśmy przekazać kilka opcji, robimy to następująco: Pop(Full,Hirshfeld,ThreshOrbital=5) Mniejsza w tej chwili o znaczenie tych opcji; chodzi tylko o zilustrowanie składni. IOP od ang. internal option; pozwala zmienić wewnętrzne opcje programu Gaussian w celu uzyskania niestandardowej funkcjonalności (której nie można uzyskać za pomocą zwykłych słów kluczowych). Tutaj mamy zapis IOP(6/80=1), czyli w warstwie 6 zmieniamy opcję nr 80, nadając jej wartość 1. Jak można sprawdzić w podręczniku IOP-ów (plik PDF, str. 116), oznacza to że zostaną obliczone ładunki Löwdina i rzędy wiązań Mayera (domyślnie nie są liczone). Uwaga: słowo kluczowe IOP jest zwykle stosowane przez zaawansowanych użytkowników i nie należy go nadużywać. Początkujący zwykle nie muszą z niego korzystać, a jeśli już, to zwykle wystarczy im zaledwie kilka dobrze sprawdzonych opcji. Kolejnym elementem pliku wejściowego jest sekcja tytułowa. Jest to zwięzły, zrozumiały dla użytkownika opis prowadzonych obliczeń. Tytuł jest zawsze wymagany, choć nie jest interpretowany przez program. Dalej następuje specyfikacja czasteczki, czyli zdefiniowanie układu molekularnego, dla którego wykonamy obliczenia. W pierwszej linii podajemy ładunek (tu: 0) i multipletowość spinową (tu: 1). 1 Następnie (bez robienia pustej linii) definiujemy geometrię cząsteczki. W powyższym przykładzie geometria jest podana we współrzędnych wewnętrznych (Z-matrix), ale można też użyć współrzędnych kartezjańskich (XYZ). Wykonanie obliczeń W dowolnym edytorze tekstu przygotuj wejściowy do obliczeń energii dla cząsteczki N 2 w zadanej geometrii, o zawartości jak wyżej i zapisz go pod odpowiednią nazwą z rozszerzeniem.inp (np. n2.inp). W celu uruchomienia obliczeń, wydaj komendę: rung09 n2.inp Uwaga: w przypadku dłuższych obliczeń warto dodać znak & na końcu komendy (tzn. np. g09 n2.inp &). Dzięki temu zadanie uruchomi się w tle i będzie można wydawać inne komendy w trakcie trwania obliczeń. Te obliczenia są jednak bardzo krótkie i dlatego (chwilowo) nie ma takiej potrzeby. 1 Pojęcie ładunku cząsteczki powinno być zupełnie jasne (tutaj: ładunek 0, bo mamy cząsteczkę obojętną; dla jonu jednododatniego mielibyśmy ładunek 1; dla jonu jednoujemnego 1, itd). Natomiast multipletowość wyraża się wzorem: m = 2S + 1 = n u + 1, gdzie S to wypadkowy spin elektronowy cząsteczki, który wynika ze zliczenia spinów wszystkich niesparowanych elektronów (w liczbie n u ), stąd druga postać wzoru. Dla zamkniętopowłokowej cząsteczki wszystkie elektrony są sparowane, zatem: n u = 0, S = 0, m = 1. O takim stanie spinowym mówimy inaczej: stan singletowy. Z kolei gdy n u = 2, to S = 1, a multipletowość wynosi 3 i mówimy o stanie trypletowym; gdy n u = 1, to S = 1/2, a multipletowość wynosi 2 i mówimy o stanie dubletowym; gdy S = 3/2, multipletowość wynosi 4 i mówimy o stanie kwartetowym, itd. Mulitpletowość charakteryzuje stopień zdegenerowania stanu spinowego w nieobecności pola magnetycznego i przy zaniedbaniu sprzężenia spinowo-orbitalnego. Dla ustalonej liczby kwantowej S, magnetyczna liczba spinowa M S może bowiem przyjmować 2S +1 wartości (M S = S, S +1,...,S 1,S), które (przy braku pola magnetycznego) odpowiadają tej samej energii. 2
3 Plik wynikowy dla czasteczki N 2 Po zakończeniu obliczeń obejrzyj zawartość pliku wynikowego z końcówką.log. Do podejrzenia zawartości pliku tekstowego najlepiej użyć polecenia less <nazwa pliku>. 2 (Ewentualnie można też otworzyć plik.log w edytorze tekstu, uważając aby nie zmodyfikować jego zawartości. Ale stanowczo polecam less). W początkowej części pliku wynikowego zwróć uwagę na powtórzoną specyfikacje geometrii oraz informację o grupie symetrii cząsteczki rozpoznanej przez program (linia zaczynająca się od Full point group). Odczytaj również wartość energii odpychania jader w zadanej geometrii (linia zaczynająca się od: nuclear repulsion energy). Dalej zwróć szczególną uwagę na komunikat przypominający ten: SCF Done: E(RHF) = A.U. after 8 cycles Informuje on o uzbieżnieniu procedury SCF (ang. Self Consistent Field) w podanej liczbie cykli. Odczytaj energię elektronowa (zwaną też w tym kontekście energią całkowitą) w ramach przybliżenia RHF. Nieco niżej znajdziesz też informacje o przyczynkach do energii elektronowej: energia kinetyczna elektronów (KE), energia potencjalna odziaływania elektronów z jądrami (PE), energia potencjalna odpychania elektronów (EE). Zanotuj wartości tych przyczynków, oblicz ich sumę i wytłumacz, dlaczego ta suma nie jest równa energii całkowitej. Przejrzyj informacje o orbitalach molekularnych (MO), które znajdziesz poniżej komunikatu: Molecular Orbital Coefficients. Orbitale molekularne podane są kolumnami, przedstawiającymi ich współczynniki rozwinięcia na funkcje bazy, tzn. orbitale atomowe (AO). 3 Na górze każdej kolumny jest podana symetria danego orbitalu (reprezentacja nieprzywiedlna grupy symetrii cząsteczki, wg której transformuje), informacja czy jest obsadzony (O), czy wirtualny (V), oraz energia orbitalna (wartość własna operatora Focka, stąd określenie Eigenvalues). Zanotuj informacje o symetriach i energiach dla wszystkich zajętych oraz dwóch najniższych wirtualnych orbitali. Zwróć szczególną uwagę na AO partycypujące w MO nr 5, 6 i 7. Czy potrafisz wytłumaczyć, dlaczego niektóre współczynniki rozwinięcia są dokładnie równe zero? Zwróć też uwagę na różnicę w energii między orbitalami 1 i 2 oraz kolejnymi. Przeglądnij wyniki analizy populacyjnej, które znajdziesz poniżej komunikatu Gross orbital populations. Zwróć uwagę na ułamkowe, lecz niezerowe obsadzenia orbitali d (XZ, YZ). Odczytaj rzad wiazania w ujęciu Mayera (Atomic Valencies and Mayer Atomic Bond Orders). Jak obliczony rząd wiązania ma się do intuicji chemicznej / wzoru elektronowego Lewisa? Wczytaj plik wynikowy do programu MOLDEN wydając komendę: gmolden n2.log & (zwróć uwagę na końcowy znak &). Aby wyświetlić kontury orbitali molekularnych: Kliknij na przycisk Dens.Mode. Program przejdzie w tryb wizualizacji MO i gęstości elektronowej (density mode); powrót do trybu molekularnego (molecular mode) umożliwia przycisk Mol.Mode. Kliknij na przycisk PlotPlane (z menu Miscellaneous); w nowo wyświetlonym okienku wydaj komendę edge=10 [Enter] i zamknij to okienko. W ten sposób lepiej dopasujemy do rozmiarów cząsteczki wirtualny sześcian, w którym obliczane są wartości orbitali. Następnie kliknij Space (z menu Plot Mode); rekomendowana wartość konturu: Pomoc dot. polecenia less. Przewijanie: strzałki, wyszukiwanie w przód: /wzorzec [Enter], wyszukiwanie wstecz:?wzorzec [Enter], pomoc: h, wyjście: q). Warto też zapoznać się z komendą grep do wyszukiwania wzorców; przykłady jej wykorzystania znajdują się na stronie WWW z dokumentacją do ćwiczeń. 3 Zgodnie z istotą metody LCAO-MO, każdy MO jest przybliżany jako liniowa kombinacja dostępnych AO. 3
4 A C B D E Rysunek 1: Położenie interesujących przycisków w okienku Molden Control programu gmolden po przejściu do trybu density mode: A przycisk Orbital (wyświetli okienko z listą orbitali), B przycisk Space (orbitale będą wizualizowane w postaci konturów), C przycisk przełączający między renderowaniem grafiki OpenGL a Xwindows, D przycisk Plot Plane, E przycisk umożliwiający powrót do trybu molecular mode. Kliknij na przycisk z obrazkami brył 3D (Switch between OpenGL and Xwindows rendering). Umożliwia uzyskanie realistycznych, trójwymiarowych konturów orbitali, które można łatwo obracać. Przycisk Orbital (z menu Plot Function) otworzy okienko, w którym można wybrać z listy interesujący nas orbital. Rysunek 1 ukazuje położenie potrzebnych przycisków w okienku Molden Control programu gmolden (już po przejściu do trybu density mode). Obejrzyj orbitale 1 9, zanotuj ich symetrię (σ, π) oraz charakter (wiążący, antywiążący). Obliczenia energii dla czasteczki O 2 Stan podstawowy cząsteczki O 2 jest otwartopowłokowy. Liczba elektronów o spinie α jest o 2 większa niż liczba elektronów o spinie β, czyli cząsteczka posiada 2 niesparowane elektrony i spin całkowity S = 1. Innymi słowy, stan podstawowy jest trypletem. Ponieważ metoda RHF nie pozwala 4
5 opisać struktury elektronowej układów otwartopowłokowych, zastosujemy metodę UHF (spinowo nieograniczony wariant metody Hartree-Focka). Na bazie pliku wejściowego dla cząsteczki N 2, przygotuj plik do obliczeń energii dla cząsteczki O 2 w eksperymentalnej geometrii (odległość O O 1.21 Å) w metodzie UHF, w bazie 6-31G(d). Przygotowując plik, pamiętaj aby poprawnie zdefiniować: geometrię cząsteczki (rodzaj atomów, odległość); ładunek i multipletowość; metodę obliczeniową i bazę. Po zakończeniu obliczeń przeglądnij plik wynikowy. Sprawdź, czy procedura SCF uzbieżniła się, zapisz wartość obliczonej energii elektronowej, długość rzutu spinu na kierunek z (<Sz>) oraz wartość średnią (spodziewaną) kwadratu spinu (<S**2>). Zwróć uwagę, że dla metody UHF mamy dwa zestawy orbitali molekularnych w zależności od spinu elektronu (Alpha / Beta Molecular Orbital Coefficients) Porównaj energię i współczynniki rozwinięcia dla odpowiadające orbitali 8α vs 8β oraz 9α vs 9β. Obejrzyj również kontury tych orbitali w programie MOLDEN. Czy odpowiadające sobie orbitale α i β są identyczne? Jeśli nie, czy są przynajmniej do siebie podobne? Jaka jest symetria (σ, π) i jaki charakter (wiążący, antywiążący) tych orbitali? Skąd widać, że te orbitale są pojedynczo obsadzone w stanie podstawowym O 2? Optymalizacja geometrii dla czasteczki O 2 Dotychczas wykonaliśmy obliczenia energii w zadanej geometrii. W tej chwili, dla wybranej przez nas metody i bazy funkcyjnej, wyznaczymy geometrię optymalną, czyli odpowiadającą minimum energii w funkcji współrzędnych. Oczywiście, geometria optymalna zależy od metody i bazy stosowanej w obliczeniach; nie jest tożsama z rzeczywistą geometrią cząsteczki (wyznaczoną eksperymentalnie), chociaż oczekujemy, że powinna być jej przybliżeniem Na bazie dotychczasowego pliku inputowego, przygotuj nowy plik wejściowy do optymalizacji geometrii. Metodę (UHF) i bazę (6-31G(d)) pozostaw bez zmian. W nowym pliku musi się znaleźć słowo kluczowe Opt, oznaczające optymalizację geometrii. Zadbaj o właściwą nazwę pliku (np. o2_opt.inp), jak również nie zapomnij nadać obliczeniom jakiegoś zrozumiałego tytułu. Po zakończeniu obliczeń odszukaj w pliku wynikowym (np. o2_opt.log) komunikat o treści -- Stationary point found. informujący o znalezieniu punktu stacjonarnego (w tym przypadku chodzi o minimum). Odczytaj poniżej tego komunikatu optymalną długość wiązania. Wydaj komendę: grep SCF Done o2_opt.log i zwróć uwagę, że w przypadku optymalizacji geometrii komunikat SCF Done pojawia się wielokrotnie. Zanotuj końcową energię po optymalizacji geometrii. Plik wynikowy z optymalizacji geometrii obejrzyj w programie MOLDEN. Aby zobaczyć przebieg optymalizacji geometrii wybierz przycisk Geom.conv. z menu Convergence, a następnie przycisk Movie z menu Select Point. Zmierz długość wiązania wybierając Distance z menu Calculated, klikając na dwa interesujące nas atomy. Przetestuj opcję Monitor umożliwiającą śledzenie długości wybranego wiązania w trakcie optymalizacji geometrii. Zanotuj długość wiązania optymalną dla metody UHF/6-31G(d). 5
6 Co powinno być w sprawozdaniu? Zwięzła informacja, jakie obliczenia przeprowadzono, jakimi metodami, w jakiej bazie, dla jakich cząsteczek, czy optymalizowano geometrię, a jeśli nie, dla jakiej geometrii wykonano obliczenia. Proszę nie kopiować fragmentów instrukcji, ale napisać własnymi słowami. Zapisane wyniki obliczeń dla cząsteczki N 2, zgodnie z instrukcją. Proszę nie kopiować fragmentów pliku wynikowego, ale zestawić najważniejsze informacje i opisać po polsku (używając poprawnych określeń, np. energia elektronowa, nie elektroniczna ), pamiętając o podaniu jednostek energii i długości wiązania oraz o właściwym zaokrągleniu podawanych wielkości. Schemat drabinka orbitali molekularnych (MOs) dla cząsteczki N 2, z zaznaczonymi energiami, symetriami (σ, π) i charakterem (wiążący, antywiążący) dla każdego MO z zakresu od 1 do 9. Dla cząsteczki N 2 w geometrii eksperymentalnej, proszę obliczyć sumę energii orbitalnych dla 14 elektronów. Obliczoną wielkość proszę porównać z sumą energii kinetycznej (KE) i potencjalnej elektronów (PE + EE). Proszę wytłumaczyć przyczynę rozbieżności. (Pomocne może być przyjrzenie się wzorom na energie orbitalne i energię całkowitą w metodzie HF). Wyniki i analiza dla cząsteczki O 2 w geometrii eksperymentalnej oraz wynik optymalizacji geometrii dla tej cząsteczki. Wyjaśnienie struktury elektronowej cząsteczki O 2 (czy jest otwartoczy zamkniętopowłokowa, jaki jest jej stan spinowy, ile niesparowanych elektronów i na których orbitalach?). Porównanie znalezionych wartości Ŝz i Ŝ2 z wartościami teoretycznymi 4 oraz wyjaśnienie wyniku tego porównania. Uwaga: energie w plikach wynikowych są podane w jednostkach atomowych Hartree (skrót E h lub a.u., od atomic units). W razie potrzeby można łatwo przeliczyć energie w a.u. na inne jednostki, np. 1 a.u. = ev = kcal/mol. Sugerowana dokładność przy podawaniu wyników obliczeń: długości wiązań Å kąty: 0.1 energie całkowite w a.u.: 10 5 a.u. energie względne w kcal/mol: 0.1 kcal/mol energie względne w ev: 0.01 ev rzędy wiązań, ładunki atomowe: Dokładność typowych metod chemii kwantowej dla względnych energii (np. energia produktów reakcji wzgledem substratów reakcji), jest rzędu 1 kcal/mol lub nieco gorsza. Główną przyczyną błedów są daleko idące przybliżenia w samych metodach chemii kwantowej (jak również uproszczenia co do modelu, którym próbujemy wytłumaczyć dane eksperymentalne). Nie należy mieć złudzenia, że przez zapisanie wyników obliczeń z bardzo dużą ilością miejsc po przecinku zapewnimy wysoką dokładność wyników obliczeń względem danych eksperymentalnych! Literatura (1) L. Piela Idee Chemii Kwantowej, wyd. PWN, str (2) F. Jensen Introduction to Computational Chemistry, wyd. Wiley, str Tzn. z wartościami dla wspólnego stanu własnego operatorów Ŝz i Ŝ2, który jest opisany liczbami kwantowymi S = 1, M S = S. 6
Ćwiczenie 3. Spektroskopia elektronowa. Etylen. Trypletowe przejścia elektronowe *
 Ćwiczenie 3 Spektroskopia elektronowa. Etylen. Trypletowe przejścia elektronowe * 1 Ćwiczenie 3 Spektroskopia elektronowa. Etylen. Trypletowe przejścia elektronowe * I. Narysuj etylen a) Wybierz Default
Ćwiczenie 3 Spektroskopia elektronowa. Etylen. Trypletowe przejścia elektronowe * 1 Ćwiczenie 3 Spektroskopia elektronowa. Etylen. Trypletowe przejścia elektronowe * I. Narysuj etylen a) Wybierz Default
Teoria Orbitali Molekularnych. tworzenie wiązań chemicznych
 Teoria Orbitali Molekularnych tworzenie wiązań chemicznych Zbliżanie się atomów aż do momentu nałożenia się ich orbitali H a +H b H a H b Wykres obrazujący zależność energii od odległości atomów długość
Teoria Orbitali Molekularnych tworzenie wiązań chemicznych Zbliżanie się atomów aż do momentu nałożenia się ich orbitali H a +H b H a H b Wykres obrazujący zależność energii od odległości atomów długość
Atomy wieloelektronowe
 Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
Ćwiczenie 5. Wyznaczanie widm IR i Ramana formaldehydu oraz obliczenia za pomocą pakietu Gaussian 03W
 Ćwiczenie 5 Wyznaczanie widm IR i Ramana formaldehydu oraz obliczenia za pomocą pakietu Gaussian 03W Co powinieneś umieć przed zajęciami Jak obliczyć energię oscylatora harmonicznego, klasycznego i kwantowego?
Ćwiczenie 5 Wyznaczanie widm IR i Ramana formaldehydu oraz obliczenia za pomocą pakietu Gaussian 03W Co powinieneś umieć przed zajęciami Jak obliczyć energię oscylatora harmonicznego, klasycznego i kwantowego?
że w wyniku pomiaru zmiennej dynamicznej A, której odpowiada operator αˆ otrzymana zostanie wartość 2.41?
 TEST. Ortogonalne i znormalizowane funkcje f i f są funkcjami własnymi operatora αˆ, przy czym: α ˆ f =. 05 f i α ˆ f =. 4f. Stan pewnej cząstki opisuje 3 znormalizowana funkcja falowa Ψ = f + f. Jakie
TEST. Ortogonalne i znormalizowane funkcje f i f są funkcjami własnymi operatora αˆ, przy czym: α ˆ f =. 05 f i α ˆ f =. 4f. Stan pewnej cząstki opisuje 3 znormalizowana funkcja falowa Ψ = f + f. Jakie
Podstawy chemii obliczeniowej
 Podstawy chemii obliczeniowej Anna Kaczmarek Kędziera Katedra Chemii Materiałów, Adsorpcji i Katalizy Wydział Chemii UMK, Toruń Elementy chemii obliczeniowej i bioinformatyki 2015 Plan wykładu 15 godzin
Podstawy chemii obliczeniowej Anna Kaczmarek Kędziera Katedra Chemii Materiałów, Adsorpcji i Katalizy Wydział Chemii UMK, Toruń Elementy chemii obliczeniowej i bioinformatyki 2015 Plan wykładu 15 godzin
c) prawdopodobieństwo znalezienia cząstki między x=1.0 a x=1.5 jest równe
 TEST 1. Ortogonalne i znormalizowane funkcje f 1 i f są funkcjami własnymi operatora, przy czym: f 1 =1.05 f 1 i f =.41 f. Stan pewnej cząstki opisuje znormalizowana funkcja 1 3 falowa = f1 f. Jakie jest
TEST 1. Ortogonalne i znormalizowane funkcje f 1 i f są funkcjami własnymi operatora, przy czym: f 1 =1.05 f 1 i f =.41 f. Stan pewnej cząstki opisuje znormalizowana funkcja 1 3 falowa = f1 f. Jakie jest
Cząsteczki. 1.Dlaczego atomy łącz. 2.Jak atomy łącz. 3.Co to jest wiązanie chemiczne? Jakie sąs. typy wiąza
 Cząsteczki 1.Dlaczego atomy łącz czą się w cząsteczki?.jak atomy łącz czą się w cząsteczki? 3.Co to jest wiązanie chemiczne? Co to jest rząd d wiązania? Jakie sąs typy wiąza zań? Dlaczego atomy łącz czą
Cząsteczki 1.Dlaczego atomy łącz czą się w cząsteczki?.jak atomy łącz czą się w cząsteczki? 3.Co to jest wiązanie chemiczne? Co to jest rząd d wiązania? Jakie sąs typy wiąza zań? Dlaczego atomy łącz czą
Rzędy wiązań chemicznych
 Seminarium Magisterskie Rzędy wiązań chemicznych w ujęciu Teorii Komunikacji Opracowanie Dariusz Szczepanik Promotor Dr hab. Janusz Mrozek Rzędy wiązań chemicznych w ujęciu Teorii Komunikacji Plan prezentacji
Seminarium Magisterskie Rzędy wiązań chemicznych w ujęciu Teorii Komunikacji Opracowanie Dariusz Szczepanik Promotor Dr hab. Janusz Mrozek Rzędy wiązań chemicznych w ujęciu Teorii Komunikacji Plan prezentacji
Modelowanie molekularne
 Ck08 Modelowanie molekularne metodami chemii kwantowej Dr hab. Artur Michalak Zakład Chemii Teoretycznej Wydział Chemii UJ Wykład 10 http://www.chemia.uj.edu.pl/~michalak/mmod2007/ Podstawowe idee i metody
Ck08 Modelowanie molekularne metodami chemii kwantowej Dr hab. Artur Michalak Zakład Chemii Teoretycznej Wydział Chemii UJ Wykład 10 http://www.chemia.uj.edu.pl/~michalak/mmod2007/ Podstawowe idee i metody
Zadanie 1. Stosowanie stylów
 Zadanie 1. Stosowanie stylów Styl to zestaw elementów formatowania określających wygląd: tekstu atrybuty czcionki (tzw. styl znaku), akapitów np. wyrównanie tekstu, odstępy między wierszami, wcięcia, a
Zadanie 1. Stosowanie stylów Styl to zestaw elementów formatowania określających wygląd: tekstu atrybuty czcionki (tzw. styl znaku), akapitów np. wyrównanie tekstu, odstępy między wierszami, wcięcia, a
Liczby kwantowe n, l, m l = 0 l =1 l = 2 l = 3
 Liczby kwantowe Rozwiązaniem równania Schrödingera są pewne funkcje własne, które można scharakteryzować przy pomocy zestawu trzech liczb kwantowych n, l, m. Liczby kwantowe nie mogą być dowolne, muszą
Liczby kwantowe Rozwiązaniem równania Schrödingera są pewne funkcje własne, które można scharakteryzować przy pomocy zestawu trzech liczb kwantowych n, l, m. Liczby kwantowe nie mogą być dowolne, muszą
Wykład 5: Cząsteczki dwuatomowe
 Wykład 5: Cząsteczki dwuatomowe Wiązania jonowe i kowalencyjne Ograniczenia teorii Lewisa Orbitale cząsteczkowe Kombinacja liniowa orbitali atomowych Orbitale dwucentrowe Schematy nakładania orbitali Diagramy
Wykład 5: Cząsteczki dwuatomowe Wiązania jonowe i kowalencyjne Ograniczenia teorii Lewisa Orbitale cząsteczkowe Kombinacja liniowa orbitali atomowych Orbitale dwucentrowe Schematy nakładania orbitali Diagramy
Mechanika kwantowa. Jak opisać atom wodoru? Jak opisać inne cząsteczki?
 Mechanika kwantowa Jak opisać atom wodoru? Jak opisać inne cząsteczki? Mechanika kwantowa Elektron fala stojąca wokół jądra Mechanika kwantowa Równanie Schrödingera Ĥ E ψ H ˆψ = Eψ operator różniczkowy
Mechanika kwantowa Jak opisać atom wodoru? Jak opisać inne cząsteczki? Mechanika kwantowa Elektron fala stojąca wokół jądra Mechanika kwantowa Równanie Schrödingera Ĥ E ψ H ˆψ = Eψ operator różniczkowy
KARTA PRZEDMIOTU. Informacje ogólne WYDZIAŁ MATEMATYCZNO-PRZYRODNICZY. SZKOŁA NAUK ŚCISŁYCH UNIWERSYTET KARDYNAŁA STEFANA WYSZYŃSKIEGO W WARSZAWIE
 1 2 4 5 6 7 8 8.0 Kod przedmiotu Nazwa przedmiotu Jednostka Punkty ECTS Język wykładowy polski Poziom przedmiotu podstawowy K_W01 2 wiedza Symbole efektów kształcenia K_U01 2 umiejętności K_K01 11 kompetencje
1 2 4 5 6 7 8 8.0 Kod przedmiotu Nazwa przedmiotu Jednostka Punkty ECTS Język wykładowy polski Poziom przedmiotu podstawowy K_W01 2 wiedza Symbole efektów kształcenia K_U01 2 umiejętności K_K01 11 kompetencje
Fizyka atomowa r. akad. 2012/2013
 r. akad. 2012/2013 wykład VII - VIII Podstawy Procesów i Konstrukcji Inżynierskich Fizyka atomowa Zakład Biofizyki 1 Spin elektronu Elektrony posiadają własny moment pędu L s. nazwany spinem. Wartość spinu
r. akad. 2012/2013 wykład VII - VIII Podstawy Procesów i Konstrukcji Inżynierskich Fizyka atomowa Zakład Biofizyki 1 Spin elektronu Elektrony posiadają własny moment pędu L s. nazwany spinem. Wartość spinu
Budowa atomu. Izotopy
 Budowa atomu. Izotopy Zadanie. atomu lub jonu Fe 3+ atomowa Z 9 masowa A Liczba protonów elektronów neutronów 64 35 35 36 Konfiguracja elektronowa Zadanie 2. Atom pewnego pierwiastka chemicznego o masie
Budowa atomu. Izotopy Zadanie. atomu lub jonu Fe 3+ atomowa Z 9 masowa A Liczba protonów elektronów neutronów 64 35 35 36 Konfiguracja elektronowa Zadanie 2. Atom pewnego pierwiastka chemicznego o masie
Geometria cząsteczek wieloatomowych. Hybrydyzacja orbitali atomowych.
 Geometria cząsteczek wieloatomowych. Hybrydyzacja orbitali atomowych. Geometria cząsteczek Geometria cząsteczek decyduje zarówno o ich właściwościach fizycznych jak i chemicznych, np. temperaturze wrzenia,
Geometria cząsteczek wieloatomowych. Hybrydyzacja orbitali atomowych. Geometria cząsteczek Geometria cząsteczek decyduje zarówno o ich właściwościach fizycznych jak i chemicznych, np. temperaturze wrzenia,
Budowa atomów. Atomy wieloelektronowe Układ okresowy pierwiastków
 Budowa atomów Atomy wieloelektronowe Układ okresowy pierwiastków Model atomu Bohra atom zjonizowany (ciągłe wartości energii) stany wzbudzone jądro Energia (ev) elektron orbita stan podstawowy Poziomy
Budowa atomów Atomy wieloelektronowe Układ okresowy pierwiastków Model atomu Bohra atom zjonizowany (ciągłe wartości energii) stany wzbudzone jądro Energia (ev) elektron orbita stan podstawowy Poziomy
Inżynieria Biomedyczna. Wykład XII
 Inżynieria Biomedyczna Wykład XII Plan Wiązania chemiczne Teoria Lewisa Teoria orbitali molekularnych Homojądrowe cząsteczki dwuatomowe Heterojądrowe cząsteczki dwuatomowe Elektroujemność Hybrydyzacja
Inżynieria Biomedyczna Wykład XII Plan Wiązania chemiczne Teoria Lewisa Teoria orbitali molekularnych Homojądrowe cząsteczki dwuatomowe Heterojądrowe cząsteczki dwuatomowe Elektroujemność Hybrydyzacja
Chemia Ogólna wykład 1
 Chemia Ogólna wykład 1 Materia związki chemiczne cząsteczka http://scholaris.pl/ obojętne elektrycznie indywiduum chemiczne, złożone z więcej niż jednego atomu, które są ze sobą trwale połączone wiązaniami
Chemia Ogólna wykład 1 Materia związki chemiczne cząsteczka http://scholaris.pl/ obojętne elektrycznie indywiduum chemiczne, złożone z więcej niż jednego atomu, które są ze sobą trwale połączone wiązaniami
Ćwiczenie 4: Modelowanie reakcji chemicznych. Stan przejściowy.
 Ćwiczenie 4: Modelowanie reakcji chemicznych. Stan przejściowy. Celem ćwiczenia jest wymodelowanie przebiegu reakcji chemicznej podstawienia nukleofilowego zachodzącego zgodnie z mechanizmem SN2. Wprowadzenie:
Ćwiczenie 4: Modelowanie reakcji chemicznych. Stan przejściowy. Celem ćwiczenia jest wymodelowanie przebiegu reakcji chemicznej podstawienia nukleofilowego zachodzącego zgodnie z mechanizmem SN2. Wprowadzenie:
Układy wieloelektronowe
 Układy wieloelektronowe spin cząstki nierozróżnialność cząstek a symetria funkcji falowej fermiony i bozony przybliżenie jednoelektonowe wyznacznik Slatera konfiguracje elektronowe atomów ciało posiadające
Układy wieloelektronowe spin cząstki nierozróżnialność cząstek a symetria funkcji falowej fermiony i bozony przybliżenie jednoelektonowe wyznacznik Slatera konfiguracje elektronowe atomów ciało posiadające
Wyznaczanie krzywych energii potencjalnej dla wybranych cząsteczek dwuatomowych
 Wyznaczanie krzywych energii potencjalnej dla wybranych cząsteczek dwuatomowych Wstęp Krzywa energii potencjalnej 1 to wykres zależności energii potencjalnej cząsteczek od długości wiązania (czyli od wzajemnej
Wyznaczanie krzywych energii potencjalnej dla wybranych cząsteczek dwuatomowych Wstęp Krzywa energii potencjalnej 1 to wykres zależności energii potencjalnej cząsteczek od długości wiązania (czyli od wzajemnej
Różne typy wiązań mają ta sama przyczynę: energia powstającej stabilnej cząsteczki jest mniejsza niż sumaryczna energia tworzących ją, oddalonych
 Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
Wiązania atomowe Atomy wieloelektronowe, obsadzanie stanów elektronowych, układ poziomów energii. Przykładowe konfiguracje elektronów, gazy szlachetne, litowce, chlorowce, układ okresowy pierwiastków,
3. Cząsteczki i wiązania
 3. Cząsteczki i wiązania Elektrony walencyjne Wiązania jonowe i kowalencyjne Wiązanie typu σ i π Hybrydyzacja Przewidywanie kształtu cząsteczek AX n Orbitale zdelokalizowane Cząsteczki związków organicznych
3. Cząsteczki i wiązania Elektrony walencyjne Wiązania jonowe i kowalencyjne Wiązanie typu σ i π Hybrydyzacja Przewidywanie kształtu cząsteczek AX n Orbitale zdelokalizowane Cząsteczki związków organicznych
Wstęp do Optyki i Fizyki Materii Skondensowanej
 Wstęp do Optyki i Fizyki Materii Skondensowanej Część I: Optyka, wykład 9 wykład: Piotr Fita pokazy: Andrzej Wysmołek ćwiczenia: Anna Grochola, Barbara Piętka Wydział Fizyki Uniwersytet Warszawski 2014/15
Wstęp do Optyki i Fizyki Materii Skondensowanej Część I: Optyka, wykład 9 wykład: Piotr Fita pokazy: Andrzej Wysmołek ćwiczenia: Anna Grochola, Barbara Piętka Wydział Fizyki Uniwersytet Warszawski 2014/15
Instalacja i obsługa aplikacji MAC Diagnoza EP w celu wykonania Arkusza obserwacji
 Instalacja i obsługa aplikacji MAC Diagnoza EP w celu wykonania Arkusza obserwacji Uruchom plik setup.exe Pojawi się okno instalacji programu MAC Diagnoza EP. Wybierz przycisk AKCEPTUJĘ. Następnie zainstaluj
Instalacja i obsługa aplikacji MAC Diagnoza EP w celu wykonania Arkusza obserwacji Uruchom plik setup.exe Pojawi się okno instalacji programu MAC Diagnoza EP. Wybierz przycisk AKCEPTUJĘ. Następnie zainstaluj
Uniwersytet Śląski w Katowicach str. 1 Wydział Matematyki, Fizyki i Chemii
 Uniwersytet Śląski w Katowicach str. 1 Kierunek i poziom studiów: Chemia, drugi Sylabus modułu: Chemia teoretyczna (023) 1. Informacje ogólne koordynator modułu dr hab. Monika Musiał, prof. UŚ rok akademicki
Uniwersytet Śląski w Katowicach str. 1 Kierunek i poziom studiów: Chemia, drugi Sylabus modułu: Chemia teoretyczna (023) 1. Informacje ogólne koordynator modułu dr hab. Monika Musiał, prof. UŚ rok akademicki
1. Skopiować naswój komputer: (tymczasowy adres)
 Instrukcja instalacji Programu Ewangelie i pracy z nim 1. Skopiować naswój komputer: http://grant.rudolf.waw.pl/ (tymczasowy adres) a/ katalog ze skanami przekładu Nowego Testamentu b/pliki z edycjami
Instrukcja instalacji Programu Ewangelie i pracy z nim 1. Skopiować naswój komputer: http://grant.rudolf.waw.pl/ (tymczasowy adres) a/ katalog ze skanami przekładu Nowego Testamentu b/pliki z edycjami
I. Budowa atomu i model atomu wg. Bohra. 1. Atom - najmniejsza część pierwiastka zachowująca jego właściwości. Jądro atomowe - protony i neutrony
 Materiał powtórzeniowy do sprawdzianów - konfiguracja elektronowa, elektrony walencyjne, współczesny układ pierwiastków chemicznych, przykładowe zadania z rozwiązaniami. I. Budowa atomu i model atomu wg.
Materiał powtórzeniowy do sprawdzianów - konfiguracja elektronowa, elektrony walencyjne, współczesny układ pierwiastków chemicznych, przykładowe zadania z rozwiązaniami. I. Budowa atomu i model atomu wg.
1 i 2. Struktura elektronowa atomów, tworzenie wiązań chemicznych
 1 i 2. Struktura elektronowa atomów, tworzenie wiązań chemicznych 1 1.1. Struktura elektronowa atomów Rozkład elektronów na pierwszych czterech powłokach elektronowych 1. powłoka 2. powłoka 3. powłoka
1 i 2. Struktura elektronowa atomów, tworzenie wiązań chemicznych 1 1.1. Struktura elektronowa atomów Rozkład elektronów na pierwszych czterech powłokach elektronowych 1. powłoka 2. powłoka 3. powłoka
Sekretariat Optivum. Jak przygotować listę uczniów zawierającą tylko wybrane dane, np. adresy e-mail ucznia i jego opiekunów? Projektowanie listy
 Sekretariat Optivum Jak przygotować listę uczniów zawierającą tylko wybrane dane, np. adresy e-mail ucznia i jego opiekunów? Program Sekretariat Optivum ma wbudowane różne edytory, które umożliwiają przygotowywanie
Sekretariat Optivum Jak przygotować listę uczniów zawierającą tylko wybrane dane, np. adresy e-mail ucznia i jego opiekunów? Program Sekretariat Optivum ma wbudowane różne edytory, które umożliwiają przygotowywanie
Struktura elektronowa czasteczek. przybliżenie Borna-Oppenheimera. równania Schrödingera dla elektronów przy ustalonym po lożeniu jader
 Notatki do wyk ladu VII Struktura elektronowa czasteczek przybliżenie Borna-Oppenheimera rozwiazanie równania Schrödingera dla elektronów przy ustalonym po lożeniu jader przybliżenie jednoelektronowe metoda
Notatki do wyk ladu VII Struktura elektronowa czasteczek przybliżenie Borna-Oppenheimera rozwiazanie równania Schrödingera dla elektronów przy ustalonym po lożeniu jader przybliżenie jednoelektronowe metoda
Struktura elektronowa σ-kompleksu benzenu z centrum aktywnym Fe IV O cytochromu P450
 Struktura elektronowa σ-kompleksu benzenu z centrum aktywnym Fe IV O cytochromu P450 Modelowanie metodami DFT, CASSCF i CASPT2 Andrzej Niedziela 1 1 Wydział Chemii Uniwersytet Jagielloński 14.01.2009 /Seminarium
Struktura elektronowa σ-kompleksu benzenu z centrum aktywnym Fe IV O cytochromu P450 Modelowanie metodami DFT, CASSCF i CASPT2 Andrzej Niedziela 1 1 Wydział Chemii Uniwersytet Jagielloński 14.01.2009 /Seminarium
MS Excel 2007 Kurs zaawansowany Obsługa baz danych. prowadzi: Dr inż. Tomasz Bartuś. Kraków: 2008 04 25
 MS Excel 2007 Kurs zaawansowany Obsługa baz danych prowadzi: Dr inż. Tomasz Bartuś Kraków: 2008 04 25 Bazy danych Microsoft Excel 2007 udostępnia szereg funkcji i mechanizmów obsługi baz danych (zwanych
MS Excel 2007 Kurs zaawansowany Obsługa baz danych prowadzi: Dr inż. Tomasz Bartuś Kraków: 2008 04 25 Bazy danych Microsoft Excel 2007 udostępnia szereg funkcji i mechanizmów obsługi baz danych (zwanych
MATERIAŁY - udostępnianie materiałów dydaktycznych w sieci SGH
 MATERIAŁY - udostępnianie materiałów dydaktycznych w sieci SGH SPIS TREŚCI i EKRANÓW WSTĘP Ekran1: Wstęp. Logowanie Ekran2: Strona początkowa UDOSTEPNIONE MATERIAŁY Ekran3: Dostępne materiały Ekran4: Zawartość
MATERIAŁY - udostępnianie materiałów dydaktycznych w sieci SGH SPIS TREŚCI i EKRANÓW WSTĘP Ekran1: Wstęp. Logowanie Ekran2: Strona początkowa UDOSTEPNIONE MATERIAŁY Ekran3: Dostępne materiały Ekran4: Zawartość
www.plansoft.org plansoft.org Zmiany w Plansoft.org Panel wyszukiwania PLANOWANIE ZAJĘĆ, REZERWOWANIE SAL I ZASOBÓW
 Zmiany w Plansoft.org Panel wyszukiwania... 1 Uruchamianie panelu wyszukiwania... 2 Wyszukiwanie poleceń menu... 2 Wyszukiwanie rozkładów zajęć wykładowców... 3 Wyszukiwanie rozkładów zajęć grup i użycia
Zmiany w Plansoft.org Panel wyszukiwania... 1 Uruchamianie panelu wyszukiwania... 2 Wyszukiwanie poleceń menu... 2 Wyszukiwanie rozkładów zajęć wykładowców... 3 Wyszukiwanie rozkładów zajęć grup i użycia
5.3. Tabele. Tworzenie tabeli. Tworzenie tabeli z widoku projektu. Rozdział III Tworzenie i modyfikacja tabel
 5.3. Tabele Tabela jest podstawowym elementem bazy danych. To właśnie w tabelach gromadzone są w bazie rekordy danych. Projektując tabelę, definiujemy, jakie pola będzie zawierał pojedynczy rekord informacji.
5.3. Tabele Tabela jest podstawowym elementem bazy danych. To właśnie w tabelach gromadzone są w bazie rekordy danych. Projektując tabelę, definiujemy, jakie pola będzie zawierał pojedynczy rekord informacji.
Edytor materiału nauczania
 Edytor materiału nauczania I. Uruchomienie modułu zarządzania rozkładami planów nauczania... 2 II. Opuszczanie elektronicznej biblioteki rozkładów... 5 III. Wyszukiwanie rozkładu materiałów... 6 IV. Modyfikowanie
Edytor materiału nauczania I. Uruchomienie modułu zarządzania rozkładami planów nauczania... 2 II. Opuszczanie elektronicznej biblioteki rozkładów... 5 III. Wyszukiwanie rozkładu materiałów... 6 IV. Modyfikowanie
Konwersatorium 1. Zagadnienia na konwersatorium
 Konwersatorium 1 Zagadnienia na konwersatorium 1. Omów reguły zapełniania powłok elektronowych. 2. Podaj konfiguracje elektronowe dla atomów Cu, Ag, Au, Pd, Pt, Cr, Mo, W. 3. Wyjaśnij dlaczego występują
Konwersatorium 1 Zagadnienia na konwersatorium 1. Omów reguły zapełniania powłok elektronowych. 2. Podaj konfiguracje elektronowe dla atomów Cu, Ag, Au, Pd, Pt, Cr, Mo, W. 3. Wyjaśnij dlaczego występują
edycja szablonu za pomocą programu NVU
 edycja szablonu za pomocą programu NVU 2 Edycja szablonu za pomocą dodatkowego oprogramowania daje nam znacznie więcej możliwości. Zarówno posiada wiele dodatkowych opcji formatowania tekstu jak również
edycja szablonu za pomocą programu NVU 2 Edycja szablonu za pomocą dodatkowego oprogramowania daje nam znacznie więcej możliwości. Zarówno posiada wiele dodatkowych opcji formatowania tekstu jak również
Program EWIDENCJA ODZIEŻY ROBOCZEJ INSTRUKCJA UŻYTKOWNIKA Przejdź do strony producenta programu
 Program EWIDENCJA ODZIEŻY ROBOCZEJ INSTRUKCJA UŻYTKOWNIKA Przejdź do strony producenta programu http://www.jarsoft.poznan.pl/ 1. STRUKTURA PROGRAMU Program EWIDENCJA ODZIEŻY ROBOCZEJ jest aplikacją wspierającą
Program EWIDENCJA ODZIEŻY ROBOCZEJ INSTRUKCJA UŻYTKOWNIKA Przejdź do strony producenta programu http://www.jarsoft.poznan.pl/ 1. STRUKTURA PROGRAMU Program EWIDENCJA ODZIEŻY ROBOCZEJ jest aplikacją wspierającą
Notatki do wyk ladu V (z ) Metoda Hartree-Focka (Hartree ego-focka)
 Notatki do wyk ladu V (z 03.11.014) Metoda Hartree-Focka (Hartree ego-focka) Metoda wariacyjna, w której przyjmuje sie, że przybliżona funkcja falowa, opisujaca stan uk ladu n-elektronowego ma postać wyznacznika
Notatki do wyk ladu V (z 03.11.014) Metoda Hartree-Focka (Hartree ego-focka) Metoda wariacyjna, w której przyjmuje sie, że przybliżona funkcja falowa, opisujaca stan uk ladu n-elektronowego ma postać wyznacznika
5.4. Tworzymy formularze
 5.4. Tworzymy formularze Zastosowanie formularzy Formularz to obiekt bazy danych, który daje możliwość tworzenia i modyfikacji danych w tabeli lub kwerendzie. Jego wielką zaletą jest umiejętność zautomatyzowania
5.4. Tworzymy formularze Zastosowanie formularzy Formularz to obiekt bazy danych, który daje możliwość tworzenia i modyfikacji danych w tabeli lub kwerendzie. Jego wielką zaletą jest umiejętność zautomatyzowania
Wykład Budowa atomu 3
 Wykład 14. 12.2016 Budowa atomu 3 Model atomu według mechaniki kwantowej Równanie Schrödingera dla atomu wodoru i jego rozwiązania Liczby kwantowe n, l, m l : - Kwantowanie energii i liczba kwantowa n
Wykład 14. 12.2016 Budowa atomu 3 Model atomu według mechaniki kwantowej Równanie Schrödingera dla atomu wodoru i jego rozwiązania Liczby kwantowe n, l, m l : - Kwantowanie energii i liczba kwantowa n
WYKŁAD 3 CZĄSTECZKI WIELOATOMOWE ZWIĄZKI WĘGLA
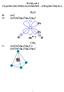 WYKŁAD 3 ZĄSTEZKI WIELOATOMOWE ZWIĄZKI WĘGLA O : (s) O: (s) (s) (p z ) (p x ) (p y ) px py s 90 o? s 4 : (s) (s) (p x ) (p y ) (s) (s) (p x ) (p y ) (p z ) s pz px py s so : (s) s s.orbital MOLEKULARNY
WYKŁAD 3 ZĄSTEZKI WIELOATOMOWE ZWIĄZKI WĘGLA O : (s) O: (s) (s) (p z ) (p x ) (p y ) px py s 90 o? s 4 : (s) (s) (p x ) (p y ) (s) (s) (p x ) (p y ) (p z ) s pz px py s so : (s) s s.orbital MOLEKULARNY
Krótki kurs obsługi środowiska programistycznego Turbo Pascal z 12 Opracował Jan T. Biernat. Wstęp
 Krótki kurs obsługi środowiska programistycznego Turbo Pascal 7.0 1 z 12 Wstęp Środowisko programistyczne Turbo Pascal, to połączenie kilku programów w jeden program. Środowisko to zawiera m.in. kompilator,
Krótki kurs obsługi środowiska programistycznego Turbo Pascal 7.0 1 z 12 Wstęp Środowisko programistyczne Turbo Pascal, to połączenie kilku programów w jeden program. Środowisko to zawiera m.in. kompilator,
Raytracer. Seminaria. Hotline. początkujący zaawansowani na miejscu
 Seminaria początkujący zaawansowani na miejscu Hotline wsparcie techniczne +420 571 894 330 zdalne sterowanie przez Team Viewer email carat@technodat.cz Zespół Spis treści Spis treści... - 2 - Informacja...
Seminaria początkujący zaawansowani na miejscu Hotline wsparcie techniczne +420 571 894 330 zdalne sterowanie przez Team Viewer email carat@technodat.cz Zespół Spis treści Spis treści... - 2 - Informacja...
Szybka instrukcja tworzenia testów dla E-SPRAWDZIAN-2 programem e_kreator_2
 Szybka instrukcja tworzenia testów dla E-SPRAWDZIAN-2 programem e_kreator_2 Spis treści: 1. Tworzenie nowego testu. str 2...5 2. Odczyt raportów z wynikami. str 6...7 3. Edycja i modyfikacja testów zapisanych
Szybka instrukcja tworzenia testów dla E-SPRAWDZIAN-2 programem e_kreator_2 Spis treści: 1. Tworzenie nowego testu. str 2...5 2. Odczyt raportów z wynikami. str 6...7 3. Edycja i modyfikacja testów zapisanych
Podstawy MATLABA, cd.
 Akademia Górniczo-Hutnicza Wydział Elektrotechniki, Automatyki, Informatyki i Elektroniki Przetwarzanie Sygnałów Studia Podyplomowe, Automatyka i Robotyka Podstawy MATLABA, cd. 1. Wielomiany 1.1. Definiowanie
Akademia Górniczo-Hutnicza Wydział Elektrotechniki, Automatyki, Informatyki i Elektroniki Przetwarzanie Sygnałów Studia Podyplomowe, Automatyka i Robotyka Podstawy MATLABA, cd. 1. Wielomiany 1.1. Definiowanie
Bazy danych kwerendy (moduł 5) 1. Przekopiuj na dysk F:\ bazę M5KW.mdb z dysku wskazanego przez prowadzącego
 Bazy danych kwerendy (moduł 5) 1. Przekopiuj na dysk F:\ bazę M5KW.mdb z dysku wskazanego przez prowadzącego 2. Otwórz bazę (F:\M5KW) 3. Zapoznaj się ze strukturą bazy (tabele, relacje) 4. Wykorzystując
Bazy danych kwerendy (moduł 5) 1. Przekopiuj na dysk F:\ bazę M5KW.mdb z dysku wskazanego przez prowadzącego 2. Otwórz bazę (F:\M5KW) 3. Zapoznaj się ze strukturą bazy (tabele, relacje) 4. Wykorzystując
CHEMIA 1. INSTYTUT MEDICUS Kurs przygotowawczy na studia medyczne kierunek lekarski, stomatologia, farmacja, analityka medyczna ATOM.
 INSTYTUT MEDICUS Kurs przygotowawczy na studia medyczne kierunek lekarski, stomatologia, farmacja, analityka medyczna tel. 0501 38 39 55 www.medicus.edu.pl CHEMIA 1 ATOM Budowa atomu - jądro, zawierające
INSTYTUT MEDICUS Kurs przygotowawczy na studia medyczne kierunek lekarski, stomatologia, farmacja, analityka medyczna tel. 0501 38 39 55 www.medicus.edu.pl CHEMIA 1 ATOM Budowa atomu - jądro, zawierające
Instrukcja obsługi programu SWWS autorstwa Michała Krzemińskiego
 Instrukcja obsługi programu SWWS autorstwa Michała Krzemińskiego Krótkie informacje o programie można znaleźć zarówno w pliku readme.txt zamieszczonym w podkatalogu DANE jak i w zakładce O programie znajdującej
Instrukcja obsługi programu SWWS autorstwa Michała Krzemińskiego Krótkie informacje o programie można znaleźć zarówno w pliku readme.txt zamieszczonym w podkatalogu DANE jak i w zakładce O programie znajdującej
ACCESS ćwiczenia (zestaw 1)
 ACCESS ćwiczenia (zestaw 1) KWERENDY Ćw. 1. Na podstawie tabeli PRACOWNICY przygotować kwerendę, która wybiera z obiektu źródłowego pola Nazwisko, Imię, KODdziału i Stawka. (- w oknie bazy danych wybrać
ACCESS ćwiczenia (zestaw 1) KWERENDY Ćw. 1. Na podstawie tabeli PRACOWNICY przygotować kwerendę, która wybiera z obiektu źródłowego pola Nazwisko, Imię, KODdziału i Stawka. (- w oknie bazy danych wybrać
Operacje na gotowych projektach.
 1 Operacje na gotowych projektach. I. Informacje wstępne. -Wiele firm udostępnia swoje produkty w postaci katalogów wykonanych w środowisku projektowania AutoCad. Podstawowym rozszerzeniem projektów stworzonych
1 Operacje na gotowych projektach. I. Informacje wstępne. -Wiele firm udostępnia swoje produkty w postaci katalogów wykonanych w środowisku projektowania AutoCad. Podstawowym rozszerzeniem projektów stworzonych
Metoda Hartree-Focka (Hartree ego-focka)
 Notatki do wyk ladu V Metoda Hartree-Focka (Hartree ego-focka) Metoda wariacyjna, w której przyjmuje sie, że przybliżona funkcja falowa, opisujaca stan uk ladu n-elektronowego ma postać wyznacznika Slatera,
Notatki do wyk ladu V Metoda Hartree-Focka (Hartree ego-focka) Metoda wariacyjna, w której przyjmuje sie, że przybliżona funkcja falowa, opisujaca stan uk ladu n-elektronowego ma postać wyznacznika Slatera,
Zakład Systemów Rozproszonych
 Zakład Systemów Rozproszonych Politechnika Rzeszowska Moduł 5: Wybrane programy użytkowe Edytor Vi Edytor Vi uruchamiany jest w oknie terminala. Przy jego pomocy możemy dokonywać następujących operacji:
Zakład Systemów Rozproszonych Politechnika Rzeszowska Moduł 5: Wybrane programy użytkowe Edytor Vi Edytor Vi uruchamiany jest w oknie terminala. Przy jego pomocy możemy dokonywać następujących operacji:
PRZEWODNIK PO ETRADER ROZDZIAŁ XII. ALERTY SPIS TREŚCI
 PRZEWODNIK PO ETRADER ROZDZIAŁ XII. ALERTY SPIS TREŚCI 1. OPIS OKNA 3 2. OTWIERANIE OKNA 3 3. ZAWARTOŚĆ OKNA 4 3.1. WIDOK AKTYWNE ALERTY 4 3.2. WIDOK HISTORIA NOWO WYGENEROWANYCH ALERTÓW 4 3.3. DEFINIOWANIE
PRZEWODNIK PO ETRADER ROZDZIAŁ XII. ALERTY SPIS TREŚCI 1. OPIS OKNA 3 2. OTWIERANIE OKNA 3 3. ZAWARTOŚĆ OKNA 4 3.1. WIDOK AKTYWNE ALERTY 4 3.2. WIDOK HISTORIA NOWO WYGENEROWANYCH ALERTÓW 4 3.3. DEFINIOWANIE
Jedną z ciekawych funkcjonalności NOLa jest możliwość dokonywania analizy technicznej na wykresach, które mogą być otwierane z poziomu okna notowań:
 Wykresy w NOLu Jedną z ciekawych funkcjonalności NOLa jest możliwość dokonywania analizy technicznej na wykresach, które mogą być otwierane z poziomu okna notowań: Po naciśnięciu F2 otwiera się nowe okno,
Wykresy w NOLu Jedną z ciekawych funkcjonalności NOLa jest możliwość dokonywania analizy technicznej na wykresach, które mogą być otwierane z poziomu okna notowań: Po naciśnięciu F2 otwiera się nowe okno,
SPIS ILUSTRACJI, BIBLIOGRAFIA
 SPIS ILUSTRACJI, BIBLIOGRAFIA Ćwiczenie 1 Automatyczne tworzenie spisu ilustracji 1. Wstaw do tekstu roboczego kilka rysunków (WSTAWIANIE OBRAZ z pliku). 2. Ustaw kursor w wersie pod zdjęciem i kliknij
SPIS ILUSTRACJI, BIBLIOGRAFIA Ćwiczenie 1 Automatyczne tworzenie spisu ilustracji 1. Wstaw do tekstu roboczego kilka rysunków (WSTAWIANIE OBRAZ z pliku). 2. Ustaw kursor w wersie pod zdjęciem i kliknij
Ćwiczenie 5 Menu programu
 Ćwiczenie 5 Menu programu Ćwiczenie ma za zadanie naukę wstawiania, edycji menu programu i procedur je obsługujących. Poznanie właściwości Items. 1. Menu Programu Należy utworzyć następujące menu programu:
Ćwiczenie 5 Menu programu Ćwiczenie ma za zadanie naukę wstawiania, edycji menu programu i procedur je obsługujących. Poznanie właściwości Items. 1. Menu Programu Należy utworzyć następujące menu programu:
Instrukcja realizacji ćwiczenia
 SIEĆ KOHONENA ROZPOZNAWANIE OBRAZÓW Cel ćwiczenia: zapoznanie się ze sposobem reprezentacji wiedzy w sieciach Kohonena i mechanizmami sąsiedztwa i sumienia neuronów. Zadanie do analizy: analizujemy sieć
SIEĆ KOHONENA ROZPOZNAWANIE OBRAZÓW Cel ćwiczenia: zapoznanie się ze sposobem reprezentacji wiedzy w sieciach Kohonena i mechanizmami sąsiedztwa i sumienia neuronów. Zadanie do analizy: analizujemy sieć
Opracowała: mgr inż. Ewelina Nowak
 Materiały dydaktyczne na zajęcia wyrównawcze z chemii dla studentów pierwszego roku kierunku zamawianego Inżynieria Środowiska w ramach projektu Era inżyniera pewna lokata na przyszłość Opracowała: mgr
Materiały dydaktyczne na zajęcia wyrównawcze z chemii dla studentów pierwszego roku kierunku zamawianego Inżynieria Środowiska w ramach projektu Era inżyniera pewna lokata na przyszłość Opracowała: mgr
Grupa Moniki Musiał. Uniwersytet Śląski Instytut Chemii Zakład Chemii Teoretycznej
 Wieloreferencyjna metoda sprzężonych klasterów w dwuwalencyjnych sektorach przestrzeni Focka oraz metoda równań ruchu w zastosowaniu do opisu stanów wzbudzonych Grupa Moniki Musiał Uniwersytet Śląski Instytut
Wieloreferencyjna metoda sprzężonych klasterów w dwuwalencyjnych sektorach przestrzeni Focka oraz metoda równań ruchu w zastosowaniu do opisu stanów wzbudzonych Grupa Moniki Musiał Uniwersytet Śląski Instytut
Notatki do wyk ladu IV (z 27.10.2014)
 Dla orbitalnego momentu p edu (L): Notatki do wyk ladu IV (z 7.10.014) ˆL ψ nlm = l(l + 1) ψ nlm (1) ˆL z ψ nlm = m ψ nlm () l + 1 możliwych wartości rzutu L z na wyróżniony kierunek w przestrzeni (l -liczba
Dla orbitalnego momentu p edu (L): Notatki do wyk ladu IV (z 7.10.014) ˆL ψ nlm = l(l + 1) ψ nlm (1) ˆL z ψ nlm = m ψ nlm () l + 1 możliwych wartości rzutu L z na wyróżniony kierunek w przestrzeni (l -liczba
Ćw. nr 31. Wahadło fizyczne o regulowanej płaszczyźnie drgań - w.2
 1 z 6 Zespół Dydaktyki Fizyki ITiE Politechniki Koszalińskiej Ćw. nr 3 Wahadło fizyczne o regulowanej płaszczyźnie drgań - w.2 Cel ćwiczenia Pomiar okresu wahań wahadła z wykorzystaniem bramki optycznej
1 z 6 Zespół Dydaktyki Fizyki ITiE Politechniki Koszalińskiej Ćw. nr 3 Wahadło fizyczne o regulowanej płaszczyźnie drgań - w.2 Cel ćwiczenia Pomiar okresu wahań wahadła z wykorzystaniem bramki optycznej
Elementy chemii obliczeniowej i bioinformatyki Zagadnienia na egzamin
 Elementy chemii obliczeniowej i bioinformatyki Zagadnienia na egzamin 1. Zapisz konfigurację elektronową dla atomu helu (dwa elektrony) i wyjaśnij, dlaczego cząsteczka wodoru jest stabilna, a cząsteczka
Elementy chemii obliczeniowej i bioinformatyki Zagadnienia na egzamin 1. Zapisz konfigurację elektronową dla atomu helu (dwa elektrony) i wyjaśnij, dlaczego cząsteczka wodoru jest stabilna, a cząsteczka
BIBLIOGRAFIA W WORD 2007
 BIBLIOGRAFIA W WORD 2007 Ćwiczenie 1 Tworzenie spisu literatury (bibliografii) Word pozwala utworzyć jedną listę główną ze źródłami (cytowanymi książkami czy artykułami), która będzie nam służyć w różnych
BIBLIOGRAFIA W WORD 2007 Ćwiczenie 1 Tworzenie spisu literatury (bibliografii) Word pozwala utworzyć jedną listę główną ze źródłami (cytowanymi książkami czy artykułami), która będzie nam służyć w różnych
Katedra Elektrotechniki Teoretycznej i Informatyki
 Katedra Elektrotechniki Teoretycznej i Informatyki Przedmiot: Technologie transmisji bezprzewodowych Numer ćwiczenia: 1 Temat: Badanie dipola półfalowego Cel ćwiczenia Celem ćwiczenia jest zapoznanie się
Katedra Elektrotechniki Teoretycznej i Informatyki Przedmiot: Technologie transmisji bezprzewodowych Numer ćwiczenia: 1 Temat: Badanie dipola półfalowego Cel ćwiczenia Celem ćwiczenia jest zapoznanie się
Spektroskopia magnetyczna
 Spektroskopia magnetyczna Literatura Zbigniew Kęcki, Podstawy spektroskopii molekularnej, PWN W- wa 1992 lub nowsze wydanie Przypomnienie 1) Mechanika ruchu obrotowego - moment bezwładności, moment pędu,
Spektroskopia magnetyczna Literatura Zbigniew Kęcki, Podstawy spektroskopii molekularnej, PWN W- wa 1992 lub nowsze wydanie Przypomnienie 1) Mechanika ruchu obrotowego - moment bezwładności, moment pędu,
Praca z widokami i nawigacja w pokazie
 Poniższe ćwiczenie ma na celu zapoznanie z ogólnymi zasadami pracy w środowisku MS PowerPoint oraz najczęściej wykorzystywanymi mechanizmami służącymi do dodawania i edycji slajdów. Należy pobrać ze wskazanej
Poniższe ćwiczenie ma na celu zapoznanie z ogólnymi zasadami pracy w środowisku MS PowerPoint oraz najczęściej wykorzystywanymi mechanizmami służącymi do dodawania i edycji slajdów. Należy pobrać ze wskazanej
znajdowały się różne instrukcje) to tak naprawdę definicja funkcji main.
 Część XVI C++ Funkcje Jeśli nasz program rozrósł się już do kilkudziesięciu linijek, warto pomyśleć o jego podziale na mniejsze części. Poznajmy więc funkcje. Szybko się przekonamy, że funkcja to bardzo
Część XVI C++ Funkcje Jeśli nasz program rozrósł się już do kilkudziesięciu linijek, warto pomyśleć o jego podziale na mniejsze części. Poznajmy więc funkcje. Szybko się przekonamy, że funkcja to bardzo
Podręcznik użytkownika programu. Ceremonia 3.1
 Podręcznik użytkownika programu Ceremonia 3.1 1 Spis treści O programie...3 Główne okno programu...4 Edytor pieśni...7 Okno ustawień programu...8 Edycja kategorii pieśni...9 Edytor schematów slajdów...10
Podręcznik użytkownika programu Ceremonia 3.1 1 Spis treści O programie...3 Główne okno programu...4 Edytor pieśni...7 Okno ustawień programu...8 Edycja kategorii pieśni...9 Edytor schematów slajdów...10
Wstęp 7 Rozdział 1. OpenOffice.ux.pl Writer środowisko pracy 9
 Wstęp 7 Rozdział 1. OpenOffice.ux.pl Writer środowisko pracy 9 Uruchamianie edytora OpenOffice.ux.pl Writer 9 Dostosowywanie środowiska pracy 11 Menu Widok 14 Ustawienia dokumentu 16 Rozdział 2. OpenOffice
Wstęp 7 Rozdział 1. OpenOffice.ux.pl Writer środowisko pracy 9 Uruchamianie edytora OpenOffice.ux.pl Writer 9 Dostosowywanie środowiska pracy 11 Menu Widok 14 Ustawienia dokumentu 16 Rozdział 2. OpenOffice
Instalacja i obsługa aplikacji MAC Diagnoza EP w celu wykonania Diagnozy rozszerzonej
 Instalacja i obsługa aplikacji MAC Diagnoza EP w celu wykonania Diagnozy rozszerzonej Uruchom plik setup.exe Pojawi się okno instalacji programu MAC Diagnoza EP. Wybierz przycisk AKCEPTUJĘ. Następnie zainstaluj
Instalacja i obsługa aplikacji MAC Diagnoza EP w celu wykonania Diagnozy rozszerzonej Uruchom plik setup.exe Pojawi się okno instalacji programu MAC Diagnoza EP. Wybierz przycisk AKCEPTUJĘ. Następnie zainstaluj
Liczby kwantowe elektronu w atomie wodoru
 Liczby kwantowe elektronu w atomie wodoru Efekt Zeemana Atom wodoru wg mechaniki kwantowej ms = magnetyczna liczba spinowa ms = -1/2, do pełnego opisu stanu elektronu potrzebna jest ta liczba własność
Liczby kwantowe elektronu w atomie wodoru Efekt Zeemana Atom wodoru wg mechaniki kwantowej ms = magnetyczna liczba spinowa ms = -1/2, do pełnego opisu stanu elektronu potrzebna jest ta liczba własność
WYŻSZA SZKOŁA PEDAGOGICZNA IM. JANUSZA KORCZAKA W WARSZAWIE Platforma E-Learning INSTRUKCJA UŻYTKOWANIA PLATFORMY E-LEARNING STUDENT
 INSTRUKCJA UŻYTKOWANIA PLATFORMY E-LEARNING STUDENT Spis treści 1. Instrukcja logowania do Platformy E-learning:... 2 2. Opis modułów Platformy E-learning... 3 3. Instrukcja uruchamiania kontentów (wykładów)
INSTRUKCJA UŻYTKOWANIA PLATFORMY E-LEARNING STUDENT Spis treści 1. Instrukcja logowania do Platformy E-learning:... 2 2. Opis modułów Platformy E-learning... 3 3. Instrukcja uruchamiania kontentów (wykładów)
Tworzenie prezentacji w MS PowerPoint
 Tworzenie prezentacji w MS PowerPoint Program PowerPoint dostarczany jest w pakiecie Office i daje nam możliwość stworzenia prezentacji oraz uatrakcyjnienia materiału, który chcemy przedstawić. Prezentacje
Tworzenie prezentacji w MS PowerPoint Program PowerPoint dostarczany jest w pakiecie Office i daje nam możliwość stworzenia prezentacji oraz uatrakcyjnienia materiału, który chcemy przedstawić. Prezentacje
Kolory elementów. Kolory elementów
 Wszystkie elementy na schematach i planach szaf są wyświetlane w kolorach. Kolory te są zawarte w samych elementach, ale w razie potrzeby można je zmienić za pomocą opcji opisanych poniżej, przy czym dotyczy
Wszystkie elementy na schematach i planach szaf są wyświetlane w kolorach. Kolory te są zawarte w samych elementach, ale w razie potrzeby można je zmienić za pomocą opcji opisanych poniżej, przy czym dotyczy
Podręcznik użytkownika. Instrukcje
 Podręcznik użytkownika W podręczniku użytkownika opisane są najważniejsze, podstawowe zasady pracy w programie. W celu zapoznania się z bardziej szczegółowym opisem, należy zapoznać się z dalszymi instrukcjami.
Podręcznik użytkownika W podręczniku użytkownika opisane są najważniejsze, podstawowe zasady pracy w programie. W celu zapoznania się z bardziej szczegółowym opisem, należy zapoznać się z dalszymi instrukcjami.
Skróty sieciowe. Krishna Tateneni Yves Arrouye Polskie tłumaczenie: Suse Polska Aktualny opiekun tłumaczenia: Marcin Kocur
 Krishna Tateneni Yves Arrouye Polskie tłumaczenie: Suse Polska Aktualny opiekun tłumaczenia: Marcin Kocur 2 Spis treści 1 Skróty sieciowe 4 1.1 Wprowadzenie....................................... 4 1.2
Krishna Tateneni Yves Arrouye Polskie tłumaczenie: Suse Polska Aktualny opiekun tłumaczenia: Marcin Kocur 2 Spis treści 1 Skróty sieciowe 4 1.1 Wprowadzenie....................................... 4 1.2
Finanse. Jak wykonać import listy płac z programu Płace Optivum do aplikacji Finanse?
 Finanse Jak wykonać import listy płac z programu Płace Optivum do aplikacji Finanse? Operacja importu list płac z programu Płace Optivum do aplikacji Finanse przebiega w następujących krokach: 1. wybór
Finanse Jak wykonać import listy płac z programu Płace Optivum do aplikacji Finanse? Operacja importu list płac z programu Płace Optivum do aplikacji Finanse przebiega w następujących krokach: 1. wybór
Konfiguracja szablonu i wystawienie pierwszej aukcji allegro
 Konfiguracja szablonu i wystawienie pierwszej aukcji allegro Metod na wystawienie aukcji na allegro jest co najmniej 2. W pierwszej przechodzimy do zakładki MOJA SPRZEDAŻ, w USTAWIENIACH SPRZEDAŻY odnajdujemy
Konfiguracja szablonu i wystawienie pierwszej aukcji allegro Metod na wystawienie aukcji na allegro jest co najmniej 2. W pierwszej przechodzimy do zakładki MOJA SPRZEDAŻ, w USTAWIENIACH SPRZEDAŻY odnajdujemy
Notatki do wyk ladu IV (z ) Metoda Hartree-Focka (Hartree ego-focka)
 Notatki do wyk ladu IV (z 1.11.01) Metoda Hartree-Focka (Hartree ego-focka) Metoda wariacyjna, w której przyjmuje sie, że przybliżona funkcja falowa opisujac a stan uk ladu n-elektronowego ma postać wyznacznika
Notatki do wyk ladu IV (z 1.11.01) Metoda Hartree-Focka (Hartree ego-focka) Metoda wariacyjna, w której przyjmuje sie, że przybliżona funkcja falowa opisujac a stan uk ladu n-elektronowego ma postać wyznacznika
System imed24 Instrukcja Moduł Analizy i raporty
 System imed24 Instrukcja Moduł Analizy i raporty Instrukcja obowiązująca do wersji 1.8.0 Spis treści 1. Moduł Analizy i Raporty... 3 1.1. Okno główne modułu Analizy i raporty... 3 1.1.1. Lista szablonów
System imed24 Instrukcja Moduł Analizy i raporty Instrukcja obowiązująca do wersji 1.8.0 Spis treści 1. Moduł Analizy i Raporty... 3 1.1. Okno główne modułu Analizy i raporty... 3 1.1.1. Lista szablonów
Cash Flow System Instrukcja
 Cash Flow System Instrukcja Wersja 1.17 Instalacja Instalacja programu Cash Flow System polega na wywołaniu programu instalatora. Następnie postępujemy zgodnie z sugestiami proponowanymi przez program
Cash Flow System Instrukcja Wersja 1.17 Instalacja Instalacja programu Cash Flow System polega na wywołaniu programu instalatora. Następnie postępujemy zgodnie z sugestiami proponowanymi przez program
Symbol termu: edu (sumy ca lkowitego orbitalnego momentu edu i ca lkowitego spinu) Przyk lad: 2 P 3. kwantowa
 Notatki do wyk ladu VI (z 18.11.2013) Symbol termu: 2S+1 L (1) L -liczba kwantowa ca lkowitego orbitalnego momentu pedu Duże litery S, P, D, F, itd. dla L=0, 1, 2, 3, itd. 2S+1 - multipletowość; S - liczba
Notatki do wyk ladu VI (z 18.11.2013) Symbol termu: 2S+1 L (1) L -liczba kwantowa ca lkowitego orbitalnego momentu pedu Duże litery S, P, D, F, itd. dla L=0, 1, 2, 3, itd. 2S+1 - multipletowość; S - liczba
Kadry Optivum, Płace Optivum
 Kadry Optivum, Płace Optivum Jak seryjnie przygotować wykazy absencji pracowników? W celu przygotowania pism zawierających wykazy nieobecności pracowników skorzystamy z mechanizmu Nowe wydruki seryjne.
Kadry Optivum, Płace Optivum Jak seryjnie przygotować wykazy absencji pracowników? W celu przygotowania pism zawierających wykazy nieobecności pracowników skorzystamy z mechanizmu Nowe wydruki seryjne.
Ćwiczenia nr 2. Edycja tekstu (Microsoft Word)
 Dostosowywanie paska zadań Ćwiczenia nr 2 Edycja tekstu (Microsoft Word) Domyślnie program Word proponuje paski narzędzi Standardowy oraz Formatowanie z zestawem opcji widocznym poniżej: Można jednak zmodyfikować
Dostosowywanie paska zadań Ćwiczenia nr 2 Edycja tekstu (Microsoft Word) Domyślnie program Word proponuje paski narzędzi Standardowy oraz Formatowanie z zestawem opcji widocznym poniżej: Można jednak zmodyfikować
Rozdział 5: Style tekstu
 5. STYLE TEKSTU Posługując się edytorem MS Word trudno nie korzystać z możliwości jaką daje szybkie formatowanie z użyciem stylów. Stylem określa się zestaw parametrów formatowych, któremu nadano określoną
5. STYLE TEKSTU Posługując się edytorem MS Word trudno nie korzystać z możliwości jaką daje szybkie formatowanie z użyciem stylów. Stylem określa się zestaw parametrów formatowych, któremu nadano określoną
Dodawanie i modyfikacja atrybutów zbioru
 Dodawanie i modyfikacja atrybutów zbioru Program Moje kolekcje wyposażony został w narzędzia pozwalające na dodawanie, edycję oraz usuwanie atrybutów przypisanych do zbioru kolekcji. Dzięki takiemu rozwiązaniu
Dodawanie i modyfikacja atrybutów zbioru Program Moje kolekcje wyposażony został w narzędzia pozwalające na dodawanie, edycję oraz usuwanie atrybutów przypisanych do zbioru kolekcji. Dzięki takiemu rozwiązaniu
Uniwersytet Śląski w Katowicach str. 1 Wydział Matematyki, Fizyki i Chemii
 Uniwersytet Śląski w Katowicach str. 1 Kierunek i poziom studiów: Chemia, pierwszy poziom Sylabus modułu: Chemia kwantowa 021 Nazwa wariantu modułu (opcjonalnie): 1. Informacje ogólne koordynator modułu
Uniwersytet Śląski w Katowicach str. 1 Kierunek i poziom studiów: Chemia, pierwszy poziom Sylabus modułu: Chemia kwantowa 021 Nazwa wariantu modułu (opcjonalnie): 1. Informacje ogólne koordynator modułu
Obsługa programu Soldis
 Obsługa programu Soldis Uruchomienie programu Po uruchomieniu, program zapyta o licencję. Można wybrać licencję studencką (trzeba założyć konto na serwerach soldisa) lub pracować bez licencji. Pliki utworzone
Obsługa programu Soldis Uruchomienie programu Po uruchomieniu, program zapyta o licencję. Można wybrać licencję studencką (trzeba założyć konto na serwerach soldisa) lub pracować bez licencji. Pliki utworzone
Modelowanie molekularne
 Modelowanie molekularne metodami chemii kwantowej Dr hab. Artur Michalak Zakład Chemii Teoretycznej Wydział Chemii UJ Wykład 4 http://www.chemia.uj.edu.pl/~michalak/mmod2007/ Podstawowe idee i metody chemii
Modelowanie molekularne metodami chemii kwantowej Dr hab. Artur Michalak Zakład Chemii Teoretycznej Wydział Chemii UJ Wykład 4 http://www.chemia.uj.edu.pl/~michalak/mmod2007/ Podstawowe idee i metody chemii
Programowanie w języku Python. Grażyna Koba
 Programowanie w języku Python Grażyna Koba Kilka definicji Program komputerowy to ciąg instrukcji języka programowania, realizujący dany algorytm. Język programowania to zbiór określonych instrukcji i
Programowanie w języku Python Grażyna Koba Kilka definicji Program komputerowy to ciąg instrukcji języka programowania, realizujący dany algorytm. Język programowania to zbiór określonych instrukcji i
5.5. Wybieranie informacji z bazy
 5.5. Wybieranie informacji z bazy Baza danych to ogromny zbiór informacji, szczególnie jeśli jest odpowiedzialna za przechowywanie danych ogromnych firm lub korporacji. Posiadając tysiące rekordów trudno
5.5. Wybieranie informacji z bazy Baza danych to ogromny zbiór informacji, szczególnie jeśli jest odpowiedzialna za przechowywanie danych ogromnych firm lub korporacji. Posiadając tysiące rekordów trudno
1. Dockbar, CMS + wyszukiwarka aplikacji Dodawanie portletów Widok zawartości stron... 3
 DODAJEMY TREŚĆ DO STRONY 1. Dockbar, CMS + wyszukiwarka aplikacji... 2 2. Dodawanie portletów... 3 Widok zawartości stron... 3 Omówienie zawartości portletu (usunięcie ramki itd.)... 4 3. Ikonki wybierz
DODAJEMY TREŚĆ DO STRONY 1. Dockbar, CMS + wyszukiwarka aplikacji... 2 2. Dodawanie portletów... 3 Widok zawartości stron... 3 Omówienie zawartości portletu (usunięcie ramki itd.)... 4 3. Ikonki wybierz
Zadaniem tego laboratorium będzie zaznajomienie się z podstawowymi możliwościami kompozycji strony i grafiki
 Zadaniem tego laboratorium będzie zaznajomienie się z podstawowymi możliwościami kompozycji strony i grafiki Edytory tekstu oferują wiele możliwości dostosowania układu (kompozycji) strony w celu uwypuklenia
Zadaniem tego laboratorium będzie zaznajomienie się z podstawowymi możliwościami kompozycji strony i grafiki Edytory tekstu oferują wiele możliwości dostosowania układu (kompozycji) strony w celu uwypuklenia
