Wpływ chlorowodorku lidokainy na odczyn rozcieńczonych rozproszeń poli(n-izopropyloakryloamidu) w temperaturze poniŝej i powyŝej LCST
|
|
|
- Karolina Sowińska
- 8 lat temu
- Przeglądów:
Transkrypt
1 Polimery w Medycynie 2009, T. XXXIX, Nr 3 Wpływ chlorowodorku lidokainy na odczyn rozcieńczonych rozproszeń poli(n-izopropyloakryloamidu) w temperaturze poniŝej i powyŝej LCST WITOLD MUSIAŁ 1,2), VANJA KOKOL 1), BOJANA VONCINA 1) 1) Uniwersytet w Mariborze, Zakład Materiałów Włókienniczych, Laboratorium Chemii Barwników i Polimerów, Słovenia 2) Akademia Medyczna we Wrocławiu, Katedra i Zakład Technologii Postaci Leku, Polska Streszczenie W niniejszym badaniu oceniano wpływ chlorowodorku lidokainy na odczyn ph zmodyfikowanych polimerów, pochodnych N-izopropyloakryloamidu, w temperaturze określanej jako temperatura powierzchni skóry, oraz w temperaturze powyŝej i poniŝej punktu przemiany fazowej. Zsyntetyzowano trzy zróŝnicowane polimery metodą SFEP (surfactant free emulsion polymerization), oraz oceniano ph rozcieńczonych rozproszeń otrzymanych polimerów, równieŝ w obecności chlorowodorku lidokainy. Zmiany odczynu wraz ze wzrostem temperatury, w obecności chlorowodorku lidokainy, przebiegały podobnie w przypadku wszystkich trzech polimerów. Wartość ph wzrastała od zakresu 5,39-5,90 do zakresu 6,22-6,55. JednakŜe zmiana odczynu była bardziej uwidoczniona w zakresie temperatury pomiędzy 25ºC i 32ºC, niŝ w zakresie pomiędzy 32ºC i 45ºC. Obecność chlorowodorku lidokainy wpływa na obserwowane wartości ph badanych układów. W przebiegu prac badawczo-rozwojowych dotyczących produktów leczniczych podawanych na skórę, w przypadku stosowania polimerów termowraŝliwych naleŝy w szczególności uwzględnić ocenę odczynu w zróŝnicowanych zakresach temperatury. 1
2 Słowa kluczowe: chlorowodorek lidokainy, mikroŝele, N-izopropyloakryloamid, termowraŝliwość WPROWADZENIE MikroŜele na bazie poli(n-izopropyloakrylamidu) są stosowane w wielu dziedzinach techniki, a atrakcyjność badań tych związków wiąŝe się z faktem, Ŝe charakteryzują się punktem przemiany fazowej - w układzie wodnym około temperatury 32ºC [1-3]. MikroŜele charakteryzuje się jako trwałe sieci polimerowe, o wymiarach rzędu nanometrów i mikrometrów. W procesie pęcznienia czynnikiem decydującym o szybkości jest dyfuzja, a stała szybkości zapadania się sieci polimerowej jest uzaleŝniona od wielkości porów w tej sieci [4]. Polimery termowraŝliwe znajdują zastosowanie w badaniach medycznych, jako termowraŝliwe nośniki substancji leczniczej, zmieniające swoje właściwości w zakresie temperatury pomiędzy 32ºC i 36ºC. Dzięki temu substancje lecznicze mogą być dostarczane do miejsca działania w sposób celowany [5]. Zastosowanie tzw. kontrolowanego dostarczania substancji czynnej, np. po podaniu na skórę, moŝe przyczynić się do zapewnienia terapeutycznych stęŝeń leku w miejscu podania, oraz zmniejszenia ryzyka wystąpienia ewentualnych działań niepoŝądanych. W tym celu oceniano między innymi wiązanie kwasu benzoesowego, diltiazemu, cyjanokobalaminy, dekstranu z podłoŝami termowraŝliwymi [6]. Chemiczna modyfikacja w tej grupie polimerów moŝe prowadzić do uzyskania efektu przedłuŝonego działania leku, lub zapewnić celowane podawanie substancji czynnej do właściwego miejsca działania. NaleŜy jednak pamiętać, Ŝe potencjalne polimerowe nośniki leków mogą takŝe wpływać na odczyn powierzchni skóry i zmieniać go w niekorzystnym kierunku. W skomplikowanych systemach wodnych, z polimerem termowraŝliwym i substancją czynną, odczyn ph powinien być oceniany w szerszym zakresie temperatury, w celu wykazania odpowiednich właściwości preparatu w miejscu jego stosowania. Jednym z częściej stosowanych lokalnych anestetyków jest chlorowodorek lidokainy, który badano pod kątem uwalniania z podłoŝa polimerowego [7, 8]. 2
3 Celem badania była ocena wpływu chlorowodorku lidokainy, leku miejscowo znieczulającego, na odczyn rozcieńczonych wodnych układów zawierających modyfikowane pochodne N-izopropyloakryloamidu. MATERIAŁ I METODY Materiały Chlorowodorek lidokainy został zakupiony w firmie Sigma-Aldrich. Wodę dejonizowaną otrzymano metodą wymiany jonowej (system TKA DI 6000, Niemcy) i stosowano we wszystkich pomiarach i badaniach. N-izopropyloakryloamid, a pozostałe odczynniki do syntezy zakupiono w sieci dystrybucyjnej Sigma-Aldrich. Jako substancje wyjściowe do sporządzenia buforów zastosowano diwodorofosforan potasu i wodorofosforan disodowy, zgodne z wymaganiami farmakopealnymi. Badane polimery W niniejszym badaniu zastosowano polimery zsyntetyzowane w poprzednich badaniach metodą SFEP. Synteza w środowisku wodnym przebiegała w temperaturze 343 K, w atmosferze gazu obojętnego. Prowadzono ją zgodnie z postępowaniem opisanym przez Peltona [9] i rozwiniętym m. in. przez Vincenta [10], oraz D'Emanuele`a i Dinarvanda [11]. Polimer PNM-I charakteryzował się anionowymi grupami terminalnymi, podczas gdy PNM-II zawierał kationowe grupy terminalne, zgodnie z zastosowanym inicjatorem procesu polimeryzacji. Przyjęto, Ŝe polimer PNM-III charakteryzuje się zwiększoną hydrofobowością, wynikającą z wykorzystania wysoce lipofilowego komonomeru. Skład badanych systemów Skład ocenianych systemów przedstawiono w tabeli 1. Odpowiednie ilości chlorowodorku lidokainy mieszano przez 24 h z wodną dyspersją zsyntetyzowanego polimeru, w temperaturze pokojowej. 3
4 Pomiary ph Pomiarów ph dokonywano za pomocą specjalistycznego pehametru SevenMulti Metler Toledo z zastosowaniem przystawki ION segment, ph/mv/orp. Wykorzystano elektrodę InLab 413, NTC, ph 0 14, 0 80ºC, a wszystkie pomiary wykonywano z uŝyciem wody dejonizowanej i powtarzano pięciokrotnie. Roztwory buforowe W celach porównawczych przygotowano roztwory buforowe o odczynie 6,87 i 7,41 - ich wartości ph były najbardziej zbliŝone do odczynu badanych preparatów [12]. Skład roztworów buforowych przedstawiono w tabeli 2. Ocena LCST metodą turbidymetryczną Badanie turbidymetryczne przeprowadzono w zakresie temperatury od 18ºC do 50 ºC. Wartość ta pozwalała na pokrycie całego obszaru temperatury przemiany fazowej. WYNIKI LCST wyznaczone dla badanych systemów wynosiło ponad 32ºC i przedstawiono je dla poszczególnych polimerów w tabeli 3. Zaobserwowane wartości układają się w następującej kolejności: PNM-I<PNM-II<PNM-III. Wartości ph badanych rozproszeń polimerów zmieniały się wraz ze wzrostem temperatury. ph PNM-I wzrastało z ok. 6,21 w temperaturze 25ºC do około 6,66 w temperaturze 32ºC. Po kolejnej zwyŝce temperatury do 45ºC zaobserwowano jednak spadek ph do wartości 6,38. Przeciwne zaleŝności zaobserwowano w przypadku polimeru PNM-II. Względnie wysokie ph ok. 6,87 w temperaturze 25ºC obniŝyło się do minimum 6,14 przy 32ºC, po czym wzrosło do 6,54 dla 45ºC. Podobne zaleŝności zaobserwowano w przypadku PNM-III, aczkolwiek bezwzględne róŝnice ph były znacznie mniejsze niŝ dla PNM-II. Dla porównania przedstawiono na załączonych wykresach takŝe ph standardowego roztworu buforowego (ph 6,87) (rycina 1). 4
5 Wraz z dodatkiem chlorowodorku lidokainy zmieniła się takŝe wartość ph systemu. Przebieg zmian był podobny w przypadku wszystkich trzech systemów. Wartość ph wzrastała od zakresu ok. 5,39-5,90 do wartości pomiędzy 6,22-6,55. JednakŜe zmiana odczynu pomiędzy temperaturą 25ºC i 32ºC była bardziej widoczna, niŝ w przypadku zmiany ph w zakresie od 32ºC do 45ºC. Dla układu zawierającego PNM-II, zmiana była niewielka z ph 6,13 do ph 6,22, odpowiednio przy wzroście temperatury z 32ºC do 45ºC. Zmierzono takŝe ph roztworów buforowych (ph 6,87 i 7,41) w badanym zakresie temperatur i zamieszczono na wspólnym wykresie z wynikami pomiarów ph systemów polimer-lidokaina. Przebieg linii ukazujących odczyn buforu w zaleŝności od temperatury jest zbliŝony do linii prostej, nie obserwowano zasadniczych minimów lub maksimów (rycina 2). DYSKUSJA Odczyn systemu wodnego, badanego w róŝnych temperaturach moŝe się róŝnić, co wynika z równania 1. Przedstawia ono zaleŝność zmierzonego potencjału od temperatury. E = E 0 2,3 (RT/nF) log a H + (1) gdzie: E - potencjał (w mv) pomiędzy elektrodą czujnika i odniesienia, E 0 - potencjał standardowy gdy a H+ = 1 mol/l, R - stała gazowa, T - temperatura, n - wartościowość jonu Aktywność jonów wodorowych moŝe podlegać w roztworze zmianom, zaleŝnym od temperatury, podobnie jak charakterystyka elektrody. Niewielki spadek odczynu bywa obserwowany w przypadku buforów zasadowych, po ich ogrzaniu. Przeciwnie, w przypadku buforów kwasowych obserwowano wzrost wartości ph. Zgodnie z pomiarami ph rozproszeń zsyntetyzowanych polimerów, oraz ich mieszanin z chlorowodorkiem lidokainy, w niektórych przypadkach wykazano minima i maksima ph w biegu wzrastającej temperatury, a róŝnice te były istotne statystycznie. Proponowane wyjaśnienie tych zmian, porównując ze standardowym buforem, opiera się na fakcie, Ŝe otrzymane polimery wykazują się tzw. 5
6 termowraŝliwością. PoniŜej temperatury punktu przemiany fazowej (LCST) cząsteczki polimeru pozostają w formie całkowicie rozwiniętej, a woda ma swobodny dostęp do makromolekuły. Pozostałości inicjatora reakcji polimeryzacji, wciąŝ obecne w makrocząsteczce, mogą przyczyniać się do aktywności jonowej dającej w efekcie odczyn bardziej kwasowy lub zasadowy, zaleŝnie od uŝytego inicjatora. Przedstawiona koncepcja znalazła potwierdzenie w wynikach badań, bowiem początkowy odczyn polimeru zsyntetyzowanego z uŝyciem inicjatora kwasowego wynosił ok. 6,87. Wraz ze wzrostem temperatury do punktu przemiany fazowej (LCST), makromolekuła zapadała się i pozostałości inicjatora zamykane były w obszarze mezoformicznym. Obecność mezostruktur badano w rozproszonych w wodzie makromolekułach białek [13], polimerów syntetycznych [14,15], a takŝe mikroŝeli [16], gdzie wykryto formowanie się sieci polimerowej o specyficznych właściwościach. W kolejnym kroku - po wyraźnym podwyŝszeniu temperatury systemu powyŝej LCST zgodnie z danymi bibliograficznymi - dochodzi do demontaŝu struktur mezo" i ostatecznego pozbycia się resztek wody lub roztworu wodnego z przestrzeni sieci polimeru. Obserwowane wartości odczynu mogą być przypisane usuniętym z przestrzeni sieciowej resztkom inicjatora, aczkolwiek część jego moŝe pozostawać związana z polimerem, w tym etapie pozostającym w formie ściśle upakowanej. Stąd odczyn polimeru nie osiąga w temperaturze powyŝej LCST wartości pierwotnych, tj. odpowiadających początkowej temperaturze. Odpowiedni schemat przedstawiono na rycinie 3. W przypadku wprowadzenia do układu polimerowego chlorowodorku lidokainy, wartości ph wzrastają wraz ze wzrostem temperatury. Nie obserwuje się tutaj, jak w przypadku pierwotnych dyspersji polimerów, minimów lub maksimów ph, a jedynie konsekwentny wzrost ph, bardziej zaznaczony w przypadku zmiany ph z 25ºC na 32ºC. Polimer PNM-III zasadniczo nie zmienia odczynu pomiędzy temperaturą 32ºC i 45ºC. Fakt ten moŝna wyjaśnić szybkim i niemal całkowitym zakończeniem procesu usuwania wodnego roztworu lidokainy z obszaru wewnątrz polimeru. Jest to prawdopodobnie związane z nasiloną lipofilowością polimeru PNM-III. ZaleŜność pomiędzy stałymi równowagi, zgodnie z ryciną 4, moŝe być wyraŝona szeregiem: KI<KII<KIII, chociaŝ KII-KI jest wyŝsza, niŝ KIII-KII. 6
7 WNIOSKI 1. Zgodnie z przedstawionymi wynikami, polimery N-izopropyloakrylamidu charakteryzują się interesującymi właściwościami zmiany odczynu w zaleŝności od temperatury. 2. Obecność chlorowodorku lidokainy wpływa w istotny sposób na zmiany odczynu badanych polimerów w zróŝnicowanej temperaturze. 3. Zakres odczynu badanych rozproszeń polimerów wynosił od 5,39 do 6,55. Porównanie tych wartości z fizjologicznym odczynem skóry ludzkiej wskazuje na korzystne właściwości tych polimerów w zakresie zgodności ph. 4. NaleŜy jednak pamiętać, Ŝe dla systemów termowraŝliwych temperatura ma szczególny wpływ na obserwowane wartości odczynu. Powinny one być szczegółowo ocenione w przypadku zamiaru stosowania tych polimerów na powierzchnie skóry lub błon śluzowych. LITERATURA [1] Graham N. B., Cameron A.: Nanogels and microgels: The new polymeric materials playground. Pure App. Chem. (1998), 70, [2] Mason T. G., Lin M. Y.: Density profiles of temperature-sensitive microgel particles. Phys. Rev. E. (2005), 71, [3] Saunders B. R., Crowther H. M., Morris G. E., Mears S. J., Cosgrove T., Vincent B., : Factors affecting the swelling of poly(n-isopropylacrylamide) microgel particles: fundamental and commercial implications. Coll. Surf. A. Physicochem. Eng. Asp. (1999), 149, [4] Bromberg L. E., Ron E. S.: Protein and peptide release from temperatureresponsive gels and thermogelling polymer matrices. Adv. Drug Delivery Revs. (1998), 31, [5] Saunders J. M., Tong T., Le Maitre C. L., Freemont T. J., Saunders B. R.: A study of ph-responsive microgel dispersions: from fluid-to-gel transitions to mechanical property restoration for load-bearing tissue. Soft Matter (2007), 3,
8 [6] Coughlan D. C., Corrigan O. I.: Drug-polymer interactions and their effect on thermoresponsive poly(n-isopropylacrylamide) drug delivery systems. (2006), 313, [7] Ganguly S., Dash A. K.: A novel in situ gel for sustained drug delivery and targeting. Int. J. Pharm. (2004), 276, [8] Ricci E. J., Lunardi L. O., Nanclares D. M. A., Marchetti J. M.: Sustained release of lidocaine from Poloxamer 407 gels. Int. J. Pharm. (2005), 288, [9] Pelton R.: Temperature-sensitive aqueous microgels. Adv. Colloid Interface Sci. (2000), 85, [10] Vincent B.,Clarke J.,Barnett K. G.: The flocculation of non-aqueous stericallystabilised latex dispersions in the presence of free polymer. Coll. Surf. (1986), 17, [11] D'Emanuele A., Dinarvan R.: Preparation, characterisation, and drug release from thermoresponsive microspheres. Int. J. Pharm. (1995), 118, [12] Polish Pharmacopoeia, Vol. I, page 112, Warszawa, Ministry of Health, [13] Manski J. M., van dr Goot A. J., Boom R. M.: Advences in structure formation of anisotropic protein-rich foods through novel processing concepts. Trends in Food Sci. Techn. (2007) 18, [14] Ba J., Polleux J., Antonietti M., Niederberger M.: Nonaqueous synthesis of tin oxide nanocrystals and their assembly into ordered porous mesostructures. Adv. Mater. (2005), 17, [15] Ma Y., Borner H. G., Hartmann J., Colfen H.: Synthesis of DL-alanine hollow tubes and core-shell mesostructures. Chem. Eur. J. (2006), 12, [16] Bischofsberger I., Trappe V.: Intriguing behaviour of gels formed by poly-nisopropylacrylamide particles. [in:] UK Polymer Colloids Forum, University of Greenwich, London, August, Abstract Book. Badanie zostało sfinansowane w ramach programu Marie Curie Transfer of Knowledge Fellowship of the European Community 6th Frame Programme, kontrakt nr MTKD-CT POLYSURF i wykonane w Uniwersytecie w Mariborze. 8
9 Adres autorów Uniwersytet w Mariborze Wydział Materiałów Włókienniczych Laboratorium Chemii Barwników i Polimerów 2000 Maribor, Smetanova 17, Słowenia Tel: ; Fax: bojana.voncina@uni-mb.si Akademia Medyczna we Wrocławiu Katedra i Zakład Technologii Postaci Leku ul. Szewska 38, Wrocław, Polska Tel: ; Fax witold@ktpl.am.wroc.pl 9
10 Tabela1. Skład badanych układów Table 1. The composition of evaluated dispersions Skład Composition PNM- I PNM- II PNM- III LD [mg] Woda Water [g] [mg] [mg] [mg] PNM-I-LD 2, ,5 30,00 PNM-II-LD - 2,5-2,5 30,00 PNM-III-LD - - 2,5 2,5 30,00 LD ,5 30,00 PNM-I, PNM-II, PNM-III - polimery/polymers, LD - chlorowodorek lidokainy/lidocaine hydrochloride Tabela 2. Skład porównawczych roztworów buforowych Table 2. Composition of buffer solutions Składniki Components Diwodorofosforan potasu Monopotassium phosphate [M] Wodorofdosforan sodu Disodium phosphate [M] Objętość roztworu wodnego Aqueous solution volume [ml] Roztwór buforowy Buffer solution ph 6,87 Roztwór buforowy Buffer solution ph 7,41 0,0125 0, ,0125 0, ,0 1000,0 10
11 Tabela 3. LCST badanych systemów Table 3. The LCST of assessed systems Polimer LCST [ºC] PNM-I 32 PNM-II 34 PNM-III 35 LCST - temperatura w punkcie przemiany fazowej /lower critical solution temperature 11
12 Ryc.1. Wpływ temperatury na odczyn badanych polimerów N-izopropyloakryloamidu Fig.1. The environmental ph of synthesized polymers at different temperatures 12
13 Ryc.2. Odczyn rozcieńczonych układów lidokaina polimer Fig. 2. The influence of lidocaine hydrochloride on the ph of diluted dispersions of synthesized polymers 13
14 Ryc.3. Schematyczne przedstawienie zmian średnicy i morfologii zsyntetyzowanych polimerów Fig. 3. Schematic representation of changes in the diameter and morphology of synthesized thermosensitive polymers 14
15 Ryc. 4. Zobrazowana równowaga dynamiczna pomiędzy cząsteczkami lidokainy pozostającymi w obrębie nośnika polimerowego, oraz w otaczającym go środowisku wodnym Fig. 4. Depicted dynamic equilibrium between lidocaine hydrochloride attached to the polymeric carrier and present in the aqueous environment 15
Zmiany odczynu rozcieńczonych rozproszeń polimerów N-izopropyloakryloamidu poniŝej i powyŝej LCST w obecności chlorheksydyny
 Polimery w Medycynie 2009, T. XXXIX, Nr 3 Zmiany odczynu rozcieńczonych rozproszeń polimerów N-izopropyloakryloamidu poniŝej i powyŝej LCST w obecności chlorheksydyny WITOLD MUSIAL 1,2), VANJA KOKOL 1),
Polimery w Medycynie 2009, T. XXXIX, Nr 3 Zmiany odczynu rozcieńczonych rozproszeń polimerów N-izopropyloakryloamidu poniŝej i powyŝej LCST w obecności chlorheksydyny WITOLD MUSIAL 1,2), VANJA KOKOL 1),
POLITECHNIKA POZNAŃSKA ZAKŁAD CHEMII FIZYCZNEJ ĆWICZENIA PRACOWNI CHEMII FIZYCZNEJ
 WARTOŚĆ ph ROZTWORÓW WODNYCH WSTĘP 1. Wartość ph wody i roztworów Woda dysocjuje na jon wodorowy i wodorotlenowy: H 2 O H + + OH (1) Stała równowagi tej reakcji, K D : wyraża się wzorem: K D = + [ Η ][
WARTOŚĆ ph ROZTWORÓW WODNYCH WSTĘP 1. Wartość ph wody i roztworów Woda dysocjuje na jon wodorowy i wodorotlenowy: H 2 O H + + OH (1) Stała równowagi tej reakcji, K D : wyraża się wzorem: K D = + [ Η ][
HYDROLIZA SOLI. ROZTWORY BUFOROWE
 Ćwiczenie 9 semestr 2 HYDROLIZA SOLI. ROZTWORY BUFOROWE Obowiązujące zagadnienia: Hydroliza soli-anionowa, kationowa, teoria jonowa Arrheniusa, moc kwasów i zasad, równania hydrolizy soli, hydroliza wieloetapowa,
Ćwiczenie 9 semestr 2 HYDROLIZA SOLI. ROZTWORY BUFOROWE Obowiązujące zagadnienia: Hydroliza soli-anionowa, kationowa, teoria jonowa Arrheniusa, moc kwasów i zasad, równania hydrolizy soli, hydroliza wieloetapowa,
POLIMERY W MEDYCYNIE 2009, T. XXXIX, Nr 3. Kwartalnik indeksowany w INDEX COPERNICUS 4.5 pkt. Punktacja KBN 4 pkt. Kwartalnik indeksowany w MEDLINE
 POLIMERY W MEDYCYNIE 2009, T. XXXIX, Nr 3 Kwartalnik indeksowany w INDEX COPERNICUS 4.5 pkt. Punktacja KBN 4 pkt. Kwartalnik indeksowany w MEDLINE POLYMERS IN MEDICINE 2009, T. XXXIX, No. 3 Spis treści
POLIMERY W MEDYCYNIE 2009, T. XXXIX, Nr 3 Kwartalnik indeksowany w INDEX COPERNICUS 4.5 pkt. Punktacja KBN 4 pkt. Kwartalnik indeksowany w MEDLINE POLYMERS IN MEDICINE 2009, T. XXXIX, No. 3 Spis treści
AUTOMATYKA I POMIARY LABORATORIUM - ĆWICZENIE NR 13 WŁAŚCIWOŚCI METROLOGICZNE POTENCJOMETRYCZNYCH CZUJNIKÓW GAZOWYCH
 AUTOMATYKA I POMIARY LABORATORIUM - ĆWICZENIE NR 13 WŁAŚCIWOŚCI METROLOGICZNE POTENCJOMETRYCZNYCH CZUJNIKÓW GAZOWYCH Występowanie dwutlenku węgla w atmosferze i powolny wzrost jego stęŝenia jest główną
AUTOMATYKA I POMIARY LABORATORIUM - ĆWICZENIE NR 13 WŁAŚCIWOŚCI METROLOGICZNE POTENCJOMETRYCZNYCH CZUJNIKÓW GAZOWYCH Występowanie dwutlenku węgla w atmosferze i powolny wzrost jego stęŝenia jest główną
Beata Mendak fakultety z chemii II tura PYTANIA Z KLASY PIERWSZEJ
 Beata Mendak fakultety z chemii II tura Test rozwiązywany na zajęciach wymaga powtórzenia stężenia procentowego i rozpuszczalności. Podaję również pytania do naszej zaplanowanej wcześniej MEGA POWTÓRKI
Beata Mendak fakultety z chemii II tura Test rozwiązywany na zajęciach wymaga powtórzenia stężenia procentowego i rozpuszczalności. Podaję również pytania do naszej zaplanowanej wcześniej MEGA POWTÓRKI
Roztwory buforowe (bufory) (opracowanie: dr Katarzyna Makyła-Juzak)
 Roztwory buforowe (bufory) (opracowanie: dr Katarzyna Makyła-Juzak) 1. Właściwości roztworów buforowych Dodatek nieznacznej ilości mocnego kwasu lub mocnej zasady do czystej wody powoduje stosunkowo dużą
Roztwory buforowe (bufory) (opracowanie: dr Katarzyna Makyła-Juzak) 1. Właściwości roztworów buforowych Dodatek nieznacznej ilości mocnego kwasu lub mocnej zasady do czystej wody powoduje stosunkowo dużą
Korozja drutów ortodontycznych typu Remanium o zróŝnicowanej średnicy w roztworze sztucznej śliny w warunkach stanu zapalnego
 Korozja drutów ortodontycznych typu Remanium o zróŝnicowanej średnicy w roztworze sztucznej śliny w warunkach stanu zapalnego Marta Rydzewska-Wojnecka WyŜsza Szkoła InŜynierii Dentystycznej w Ustroniu
Korozja drutów ortodontycznych typu Remanium o zróŝnicowanej średnicy w roztworze sztucznej śliny w warunkach stanu zapalnego Marta Rydzewska-Wojnecka WyŜsza Szkoła InŜynierii Dentystycznej w Ustroniu
WYMAGANIA EDUKACYJNE
 GIMNAZJUM NR 2 W RYCZOWIE WYMAGANIA EDUKACYJNE niezbędne do uzyskania poszczególnych śródrocznych i rocznych ocen klasyfikacyjnych z CHEMII w klasie II gimnazjum str. 1 Wymagania edukacyjne niezbędne do
GIMNAZJUM NR 2 W RYCZOWIE WYMAGANIA EDUKACYJNE niezbędne do uzyskania poszczególnych śródrocznych i rocznych ocen klasyfikacyjnych z CHEMII w klasie II gimnazjum str. 1 Wymagania edukacyjne niezbędne do
Kryteria oceniania z chemii kl VII
 Kryteria oceniania z chemii kl VII Ocena dopuszczająca -stosuje zasady BHP w pracowni -nazywa sprzęt laboratoryjny i szkło oraz określa ich przeznaczenie -opisuje właściwości substancji używanych na co
Kryteria oceniania z chemii kl VII Ocena dopuszczająca -stosuje zasady BHP w pracowni -nazywa sprzęt laboratoryjny i szkło oraz określa ich przeznaczenie -opisuje właściwości substancji używanych na co
Kopolimery statystyczne. Kopolimery blokowe. kopolimerów w blokowych. Sonochemiczna synteza -A-A-A-A-A-A-A-B-B-B-B-B-B-B-B-B-B- Typowe metody syntezy:
 1 Sonochemiczna synteza kopolimerów w blokowych Kopolimery statystyczne -A-B-A-A-B-A-B-B-A-B-A-B-A-A-B-B-A- Kopolimery blokowe -A-A-A-A-A-A-A-B-B-B-B-B-B-B-B-B-B- Typowe metody syntezy: Polimeryzacja żyjąca
1 Sonochemiczna synteza kopolimerów w blokowych Kopolimery statystyczne -A-B-A-A-B-A-B-B-A-B-A-B-A-A-B-B-A- Kopolimery blokowe -A-A-A-A-A-A-A-B-B-B-B-B-B-B-B-B-B- Typowe metody syntezy: Polimeryzacja żyjąca
Zadanie 2. (1 pkt) Uzupełnij tabelę, wpisując wzory sumaryczne tlenków w odpowiednie kolumny. CrO CO 2 Fe 2 O 3 BaO SO 3 NO Cu 2 O
 Test maturalny Chemia ogólna i nieorganiczna Zadanie 1. (1 pkt) Uzupełnij zdania. Pierwiastek chemiczny o liczbie atomowej 16 znajduje się w.... grupie i. okresie układu okresowego pierwiastków chemicznych,
Test maturalny Chemia ogólna i nieorganiczna Zadanie 1. (1 pkt) Uzupełnij zdania. Pierwiastek chemiczny o liczbie atomowej 16 znajduje się w.... grupie i. okresie układu okresowego pierwiastków chemicznych,
Badanie właściwości związków powierzchniowo czynnych
 POLITECHNIKA ŚLĄSKA WYDZIAŁ CHEMICZNY KATEDRA TECHNOLOGII CHEMICZNEJ ORGANICZNEJ I PETROCHEMII INSTRUKCJA DO ĆWICZEŃ LABORATORYJNYCH: Badanie właściwości związków powierzchniowo czynnych Laboratorium z
POLITECHNIKA ŚLĄSKA WYDZIAŁ CHEMICZNY KATEDRA TECHNOLOGII CHEMICZNEJ ORGANICZNEJ I PETROCHEMII INSTRUKCJA DO ĆWICZEŃ LABORATORYJNYCH: Badanie właściwości związków powierzchniowo czynnych Laboratorium z
Wyznaczanie stałej szybkości reakcji wymiany jonowej
 Wyznaczanie stałej szybkości reakcji wymiany jonowej Ćwiczenie laboratoryjne nr 4 Elementy termodynamiki i kinetyki procesowej Anna Ptaszek Elementy kinetyki chemicznej Pojęcie szybkości reakcji Pojęcie
Wyznaczanie stałej szybkości reakcji wymiany jonowej Ćwiczenie laboratoryjne nr 4 Elementy termodynamiki i kinetyki procesowej Anna Ptaszek Elementy kinetyki chemicznej Pojęcie szybkości reakcji Pojęcie
Roztwory elekreolitów
 Imię i nazwisko:... Roztwory elekreolitów Zadanie 1. (2pkt) W teorii Brönsteda sprzężoną parą kwas-zasada nazywa się układ złożony z kwasu oraz zasady, która powstaje z tego kwasu przez odłączenie protonu.
Imię i nazwisko:... Roztwory elekreolitów Zadanie 1. (2pkt) W teorii Brönsteda sprzężoną parą kwas-zasada nazywa się układ złożony z kwasu oraz zasady, która powstaje z tego kwasu przez odłączenie protonu.
Laboratorium Chemii Barwników i Polimerów, Slovenia. Katedra i Zakład Technologii Postaci Leku, Polska. Streszczenie
 Zastosowanie pomiarów przewodnictwa do oceny badań kontrolowanego uwalniania chloroheksydyny z termowrażliwych mikrożeli, pochodnych N-izopropyloakryloamidu Witold Musiał 1,2), Vanja Kokol 1), Bojana Voncina
Zastosowanie pomiarów przewodnictwa do oceny badań kontrolowanego uwalniania chloroheksydyny z termowrażliwych mikrożeli, pochodnych N-izopropyloakryloamidu Witold Musiał 1,2), Vanja Kokol 1), Bojana Voncina
ODPORNOŚĆ KOROZYJNA STALI 316L W PŁYNACH USTROJOWYCH CZŁOWIEKA
 WyŜsza Szkoła InŜynierii Dentystycznej im. prof. Meissnera w Ustroniu ODPORNOŚĆ KOROZYJNA STALI 316L W PŁYNACH USTROJOWYCH CZŁOWIEKA Magdalena Puda Promotor: Dr inŝ. Jacek Grzegorz Chęcmanowski Cel pracy
WyŜsza Szkoła InŜynierii Dentystycznej im. prof. Meissnera w Ustroniu ODPORNOŚĆ KOROZYJNA STALI 316L W PŁYNACH USTROJOWYCH CZŁOWIEKA Magdalena Puda Promotor: Dr inŝ. Jacek Grzegorz Chęcmanowski Cel pracy
2.1. Charakterystyka badanego sorbentu oraz ekstrahentów
 BADANIA PROCESU SORPCJI JONÓW ZŁOTA(III), PLATYNY(IV) I PALLADU(II) Z ROZTWORÓW CHLORKOWYCH ORAZ MIESZANINY JONÓW NA SORBENCIE DOWEX OPTIPORE L493 IMPREGNOWANYM CYANEXEM 31 Grzegorz Wójcik, Zbigniew Hubicki,
BADANIA PROCESU SORPCJI JONÓW ZŁOTA(III), PLATYNY(IV) I PALLADU(II) Z ROZTWORÓW CHLORKOWYCH ORAZ MIESZANINY JONÓW NA SORBENCIE DOWEX OPTIPORE L493 IMPREGNOWANYM CYANEXEM 31 Grzegorz Wójcik, Zbigniew Hubicki,
Wymagania edukacyjne niezbędne do uzyskania poszczególnych śródrocznych i rocznych ocen klasyfikacyjnych. CHEMIA klasa II.
 Wymagania edukacyjne niezbędne do uzyskania poszczególnych śródrocznych i rocznych ocen klasyfikacyjnych CHEMIA klasa II Oceny śródroczne: Ocenę dopuszczającą otrzymuje uczeń, który: -wymienia zasady bhp
Wymagania edukacyjne niezbędne do uzyskania poszczególnych śródrocznych i rocznych ocen klasyfikacyjnych CHEMIA klasa II Oceny śródroczne: Ocenę dopuszczającą otrzymuje uczeń, który: -wymienia zasady bhp
PEHAMETRIA I ROZTWORY BUFOROWE
 4. PEHAMETRIA I ROZTWORY BUFOROWE 1. Sporządzanie i oznaczanie buforu octanowego Pehametria jest analizą instrumentalną, słuŝącą do potencjometrycznego bezpośredniego pomiaru wskaźnika stęŝenia jonów H
4. PEHAMETRIA I ROZTWORY BUFOROWE 1. Sporządzanie i oznaczanie buforu octanowego Pehametria jest analizą instrumentalną, słuŝącą do potencjometrycznego bezpośredniego pomiaru wskaźnika stęŝenia jonów H
Inżynieria Środowiska
 ROZTWORY BUFOROWE Roztworami buforowymi nazywamy takie roztwory, w których stężenie jonów wodorowych nie ulega większym zmianom ani pod wpływem rozcieńczania wodą, ani pod wpływem dodatku nieznacznych
ROZTWORY BUFOROWE Roztworami buforowymi nazywamy takie roztwory, w których stężenie jonów wodorowych nie ulega większym zmianom ani pod wpływem rozcieńczania wodą, ani pod wpływem dodatku nieznacznych
EFEKT SOLNY BRÖNSTEDA
 EFEKT SLNY RÖNSTED Pojęcie eektu solnego zostało wprowadzone przez rönsteda w celu wytłumaczenia wpływu obojętnego elektrolitu na szybkość reakcji zachodzących między jonami. Założył on, że reakcja pomiędzy
EFEKT SLNY RÖNSTED Pojęcie eektu solnego zostało wprowadzone przez rönsteda w celu wytłumaczenia wpływu obojętnego elektrolitu na szybkość reakcji zachodzących między jonami. Założył on, że reakcja pomiędzy
CHEMIA. Wymagania szczegółowe. Wymagania ogólne
 CHEMIA Wymagania ogólne Wymagania szczegółowe Uczeń: zapisuje konfiguracje elektronowe atomów pierwiastków do Z = 36 i jonów o podanym ładunku, uwzględniając rozmieszczenie elektronów na podpowłokach [
CHEMIA Wymagania ogólne Wymagania szczegółowe Uczeń: zapisuje konfiguracje elektronowe atomów pierwiastków do Z = 36 i jonów o podanym ładunku, uwzględniając rozmieszczenie elektronów na podpowłokach [
Przyspieszenie separacji faz w zmiennym polu elektrycznym
 Przyspieszenie separacji faz w zmiennym polu elektrycznym Niejednorodne układy polimer / ciekły kryształ ze względu na zastosowania techniczne cieszą się niesłabnącym zainteresowaniem. Polimery są dodawane
Przyspieszenie separacji faz w zmiennym polu elektrycznym Niejednorodne układy polimer / ciekły kryształ ze względu na zastosowania techniczne cieszą się niesłabnącym zainteresowaniem. Polimery są dodawane
Wymagania programowe na poszczególne oceny. Chemia Kl.2. I. Kwasy
 Wymagania programowe na poszczególne oceny Chemia Kl.2 I. Kwasy Ocena dopuszczająca zna zasady bhp dotyczące obchodzenia się z kwasami definiuje elektrolit, nieelektrolit wyjaśnia pojęcie wskaźnika i wymienia
Wymagania programowe na poszczególne oceny Chemia Kl.2 I. Kwasy Ocena dopuszczająca zna zasady bhp dotyczące obchodzenia się z kwasami definiuje elektrolit, nieelektrolit wyjaśnia pojęcie wskaźnika i wymienia
Wymagania edukacyjne na poszczególne oceny z chemii dla klasy II gimnazjum oparte na programie nauczania Chemia Nowa Era
 Wymagania edukacyjne na poszczególne oceny z chemii dla klasy II gimnazjum oparte na programie nauczania Chemia Nowa Era IV. Kwasy Opracowała mgr Agnieszka Para Ocena dopuszczająca [1] wymienia zasady
Wymagania edukacyjne na poszczególne oceny z chemii dla klasy II gimnazjum oparte na programie nauczania Chemia Nowa Era IV. Kwasy Opracowała mgr Agnieszka Para Ocena dopuszczająca [1] wymienia zasady
Nanostrukturalne materiały hybrydowe dla potrzeb regeneracyjnej terapii ortopedycznej
 Nanostrukturalne materiały hybrydowe dla potrzeb regeneracyjnej terapii ortopedycznej Streszczenie Lidia Libowicz-Nadobny Promotorzy: Prof. dr hab. Maria Nowakowska Prof. dr hab. med. Tadeusz Niedźwiedzki
Nanostrukturalne materiały hybrydowe dla potrzeb regeneracyjnej terapii ortopedycznej Streszczenie Lidia Libowicz-Nadobny Promotorzy: Prof. dr hab. Maria Nowakowska Prof. dr hab. med. Tadeusz Niedźwiedzki
Szczegółowy opis treści programowych obowiązujących na etapie szkolnym konkursu przedmiotowego z chemii 2018/2019
 Szczegółowy opis treści programowych obowiązujących na etapie szkolnym konkursu przedmiotowego z chemii 2018/2019 I. Eliminacje szkolne (60 minut, liczba punktów: 30). Wymagania szczegółowe. Cele kształcenia
Szczegółowy opis treści programowych obowiązujących na etapie szkolnym konkursu przedmiotowego z chemii 2018/2019 I. Eliminacje szkolne (60 minut, liczba punktów: 30). Wymagania szczegółowe. Cele kształcenia
HYDROLIZA SOLI. 1. Hydroliza soli mocnej zasady i słabego kwasu. Przykładem jest octan sodu, dla którego reakcja hydrolizy przebiega następująco:
 HYDROLIZA SOLI Hydroliza to reakcja chemiczna zachodząca między jonami słabo zdysocjowanej wody i jonami dobrze zdysocjowanej soli słabego kwasu lub słabej zasady. Reakcji hydrolizy mogą ulegać następujące
HYDROLIZA SOLI Hydroliza to reakcja chemiczna zachodząca między jonami słabo zdysocjowanej wody i jonami dobrze zdysocjowanej soli słabego kwasu lub słabej zasady. Reakcji hydrolizy mogą ulegać następujące
Spis treści. Wstęp... 9
 Spis treści Wstęp... 9 1. Szkło i sprzęt laboratoryjny 1.1. Szkła laboratoryjne własności, skład chemiczny, podział, zastosowanie.. 11 1.2. Wybrane szkło laboratoryjne... 13 1.3. Szkło miarowe... 14 1.4.
Spis treści Wstęp... 9 1. Szkło i sprzęt laboratoryjny 1.1. Szkła laboratoryjne własności, skład chemiczny, podział, zastosowanie.. 11 1.2. Wybrane szkło laboratoryjne... 13 1.3. Szkło miarowe... 14 1.4.
Sporządzanie roztworów buforowych i badanie ich właściwości
 Sporządzanie roztworów buforowych i badanie ich właściwości (opracowanie: Barbara Krajewska) Celem ćwiczenia jest zbadanie właściwości roztworów buforowych. Przygotujemy dwa roztwory buforowe: octanowy
Sporządzanie roztworów buforowych i badanie ich właściwości (opracowanie: Barbara Krajewska) Celem ćwiczenia jest zbadanie właściwości roztworów buforowych. Przygotujemy dwa roztwory buforowe: octanowy
Zasady oceniania z chemii w klasie II w roku szkolnym 2015/2016. Ocena dopuszczająca Ocena dostateczna Ocena dobra Ocena bardzo dobra
 Zasady oceniania z chemii w klasie II w roku szkolnym 2015/2016 I. Kwasy wymienia zasady bhp dotyczące obchodzenia się z kwasami definiuje pojęcia: elektrolit i nieelektrolit wyjaśnia, co to jest wskaźnik
Zasady oceniania z chemii w klasie II w roku szkolnym 2015/2016 I. Kwasy wymienia zasady bhp dotyczące obchodzenia się z kwasami definiuje pojęcia: elektrolit i nieelektrolit wyjaśnia, co to jest wskaźnik
Politechnika Warszawska. Wydział Budownictwa Mechaniki i Petrochemii w Płocku Laboratorium Chemii Budowlanej
 Politechnika Warszawska Wydział Budownictwa Mechaniki i Petrochemii w Płocku Laboratorium Chemii Budowlanej Instrukcja do ćwiczenia: SZYBKOŚĆ PRZEMIAN CHEMICZNYCH Opracowała: dr inŝ. Maria Bukowska Płock,
Politechnika Warszawska Wydział Budownictwa Mechaniki i Petrochemii w Płocku Laboratorium Chemii Budowlanej Instrukcja do ćwiczenia: SZYBKOŚĆ PRZEMIAN CHEMICZNYCH Opracowała: dr inŝ. Maria Bukowska Płock,
Mechanizm działania buforów *
 Mechanizm działania buforów * UNIWERSYTET PRZYRODNICZY Z doświadczenia nabytego w laboratorium wiemy, że dodanie kropli stężonego kwasu do 10 ml wody powoduje gwałtowny spadek ph o kilka jednostek. Tymczasem
Mechanizm działania buforów * UNIWERSYTET PRZYRODNICZY Z doświadczenia nabytego w laboratorium wiemy, że dodanie kropli stężonego kwasu do 10 ml wody powoduje gwałtowny spadek ph o kilka jednostek. Tymczasem
Ćwiczenie 14. Maria Bełtowska-Brzezinska KINETYKA REAKCJI ENZYMATYCZNYCH
 Ćwiczenie 14 aria Bełtowska-Brzezinska KINETYKA REAKCJI ENZYATYCZNYCH Zagadnienia: Podstawowe pojęcia kinetyki chemicznej (szybkość reakcji, reakcje elementarne, rząd reakcji). Równania kinetyczne prostych
Ćwiczenie 14 aria Bełtowska-Brzezinska KINETYKA REAKCJI ENZYATYCZNYCH Zagadnienia: Podstawowe pojęcia kinetyki chemicznej (szybkość reakcji, reakcje elementarne, rząd reakcji). Równania kinetyczne prostych
Ćwiczenie 8 (studenci biotechnologii) Potencjometria Potencjometryczne wyznaczanie PK miareczkowania słabego kwasu
 Ćwiczenie 8 (studenci biotechnologii) Potencjometria Potencjometryczne wyznaczanie PK miareczkowania słabego kwasu Potencjometria Klasyczne miareczkowanie od miareczkowania potencjometrycznego różni się
Ćwiczenie 8 (studenci biotechnologii) Potencjometria Potencjometryczne wyznaczanie PK miareczkowania słabego kwasu Potencjometria Klasyczne miareczkowanie od miareczkowania potencjometrycznego różni się
BADANIE CIEPLNE LAMINATÓW EPOKSYDOWO-SZKLANYCH STARZONYCH W WODZIE THERMAL RESERACH OF GLASS/EPOXY LAMINATED AGING IN WATER
 Andrzej PUSZ, Łukasz WIERZBICKI, Krzysztof PAWLIK Politechnika Śląska Instytut Materiałów InŜynierskich i Biomedycznych E-mail: lukasz.wierzbicki@polsl.pl BADANIE CIEPLNE LAMINATÓW EPOKSYDOWO-SZKLANYCH
Andrzej PUSZ, Łukasz WIERZBICKI, Krzysztof PAWLIK Politechnika Śląska Instytut Materiałów InŜynierskich i Biomedycznych E-mail: lukasz.wierzbicki@polsl.pl BADANIE CIEPLNE LAMINATÓW EPOKSYDOWO-SZKLANYCH
Wpływ warunków przechowywania na fizyczną stabilność tabletek. Barbara Mikolaszek
 Wpływ warunków przechowywania na fizyczną stabilność tabletek Barbara Mikolaszek Wpływ wilgoci na tabletki Ilość wilgoci, która została zaadsorbowana przez substancję leczniczą lub nośnik wpływa na: -
Wpływ warunków przechowywania na fizyczną stabilność tabletek Barbara Mikolaszek Wpływ wilgoci na tabletki Ilość wilgoci, która została zaadsorbowana przez substancję leczniczą lub nośnik wpływa na: -
Związki nieorganiczne
 strona 1/8 Związki nieorganiczne Dorota Lewandowska, Anna Warchoł, Lidia Wasyłyszyn Treść podstawy programowej: Typy związków nieorganicznych: kwasy, zasady, wodorotlenki, dysocjacja jonowa, odczyn roztworu,
strona 1/8 Związki nieorganiczne Dorota Lewandowska, Anna Warchoł, Lidia Wasyłyszyn Treść podstawy programowej: Typy związków nieorganicznych: kwasy, zasady, wodorotlenki, dysocjacja jonowa, odczyn roztworu,
CHEMIA KLASA II I PÓŁROCZE
 CHEMIA KLASA II I PÓŁROCZE wymienia zasady bhp dotyczące obchodzenia się z kwasami definiuje pojęcia: elektrolit i nieelektrolit wyjaśnia, co to jest wskaźnik i wymienia trzy przykłady odróżnia kwasy od
CHEMIA KLASA II I PÓŁROCZE wymienia zasady bhp dotyczące obchodzenia się z kwasami definiuje pojęcia: elektrolit i nieelektrolit wyjaśnia, co to jest wskaźnik i wymienia trzy przykłady odróżnia kwasy od
Monowarstwy nanocząstek srebra charakterystyka QCM
 IKiFP im. J. Habera PAN Monowarstwy nanocząstek srebra charakterystyka QCM Katarzyna Kubiak, Zbigniew Adamczyk, Monika Wasilewska, Aneta Michna, Krzysztof Jamroży F U N A N O Cel pracy: pomiar w warunkach
IKiFP im. J. Habera PAN Monowarstwy nanocząstek srebra charakterystyka QCM Katarzyna Kubiak, Zbigniew Adamczyk, Monika Wasilewska, Aneta Michna, Krzysztof Jamroży F U N A N O Cel pracy: pomiar w warunkach
Wykład 11. Membrany ciekłe i biopodobne. Opracowała dr Elżbieta Megiel
 Wykład 11 Membrany ciekłe i biopodobne Opracowała dr Elżbieta Megiel Rodzaje membran ciekłych Faza donorowa f Faza akceptorowa s Membrany grubowarstwowe ( BLM ang. Bulk liquid membrane) Membrany ciekłe
Wykład 11 Membrany ciekłe i biopodobne Opracowała dr Elżbieta Megiel Rodzaje membran ciekłych Faza donorowa f Faza akceptorowa s Membrany grubowarstwowe ( BLM ang. Bulk liquid membrane) Membrany ciekłe
Temat 7. Równowagi jonowe w roztworach słabych elektrolitów, stała dysocjacji, ph
 Temat 7. Równowagi jonowe w roztworach słabych elektrolitów, stała dysocjacji, ph Dysocjacja elektrolitów W drugiej połowie XIX wieku szwedzki chemik S.A. Arrhenius doświadczalnie udowodnił, że substancje
Temat 7. Równowagi jonowe w roztworach słabych elektrolitów, stała dysocjacji, ph Dysocjacja elektrolitów W drugiej połowie XIX wieku szwedzki chemik S.A. Arrhenius doświadczalnie udowodnił, że substancje
KONKURS PRZEDMIOTOWY Z CHEMII
 Pieczęć KONKURS PRZEDMIOTOWY Z CHEMII dla uczniów gimnazjów województwa lubuskiego 26 stycznia 2012 r. zawody II stopnia (rejonowe) Witamy Cię na drugim etapie Konkursu Chemicznego. Przed przystąpieniem
Pieczęć KONKURS PRZEDMIOTOWY Z CHEMII dla uczniów gimnazjów województwa lubuskiego 26 stycznia 2012 r. zawody II stopnia (rejonowe) Witamy Cię na drugim etapie Konkursu Chemicznego. Przed przystąpieniem
WYMAGANIA EDUKACYJNE na poszczególne oceny śródroczne i roczne Z CHEMII W KLASIE II gimnazjum
 WYMAGANIA EDUKACYJNE na poszczególne oceny śródroczne i roczne Z CHEMII W KLASIE II gimnazjum Program nauczania chemii w gimnazjum autorzy: Teresa Kulawik, Maria Litwin Program realizowany przy pomocy
WYMAGANIA EDUKACYJNE na poszczególne oceny śródroczne i roczne Z CHEMII W KLASIE II gimnazjum Program nauczania chemii w gimnazjum autorzy: Teresa Kulawik, Maria Litwin Program realizowany przy pomocy
Chemia Nowej Ery Wymagania programowe na poszczególne oceny dla klasy II
 Chemia Nowej Ery Wymagania programowe na poszczególne oceny dla klasy II Szczegółowe kryteria oceniania po pierwszym półroczu klasy II: III. Woda i roztwory wodne charakteryzuje rodzaje wód występujących
Chemia Nowej Ery Wymagania programowe na poszczególne oceny dla klasy II Szczegółowe kryteria oceniania po pierwszym półroczu klasy II: III. Woda i roztwory wodne charakteryzuje rodzaje wód występujących
Roztwory buforowe modyfikacja wykonania ćwiczenia.
 Roztwory buforowe modyfikacja wykonania ćwiczenia. Roztwory buforowe otrzymywane będą z 0,1 M roztworów kwasu octowego i octanu sodu. Do roztworów buforowych i wód dodawane będą z biurety roztwory 0,1
Roztwory buforowe modyfikacja wykonania ćwiczenia. Roztwory buforowe otrzymywane będą z 0,1 M roztworów kwasu octowego i octanu sodu. Do roztworów buforowych i wód dodawane będą z biurety roztwory 0,1
ODCZYN WODY BADANIE ph METODĄ POTENCJOMETRYCZNĄ
 ODCZYN WODY BADANIE ph METODĄ POTENCJOMETRYCZNĄ Instrukcja do ćwiczeń opracowana w Katedrze Chemii Środowiska Uniwersytetu Łódzkiego. 1. Wprowadzenie 1.1. Odczyn wody Odczyn roztworu określa stężenie,
ODCZYN WODY BADANIE ph METODĄ POTENCJOMETRYCZNĄ Instrukcja do ćwiczeń opracowana w Katedrze Chemii Środowiska Uniwersytetu Łódzkiego. 1. Wprowadzenie 1.1. Odczyn wody Odczyn roztworu określa stężenie,
Ćwiczenie 1: Wyznaczanie warunków odporności, korozji i pasywności metali
 Ćwiczenie 1: Wyznaczanie warunków odporności, korozji i pasywności metali Wymagane wiadomości Podstawy korozji elektrochemicznej, wykresy E-pH. Wprowadzenie Główną przyczyną zniszczeń materiałów metalicznych
Ćwiczenie 1: Wyznaczanie warunków odporności, korozji i pasywności metali Wymagane wiadomości Podstawy korozji elektrochemicznej, wykresy E-pH. Wprowadzenie Główną przyczyną zniszczeń materiałów metalicznych
ĆWICZENIE 2 WSPÓŁOZNACZANIE WODOROTLENKU I WĘGLANÓW METODĄ WARDERA. DZIAŁ: Alkacymetria
 ĆWICZENIE 2 WSPÓŁOZNACZANIE WODOROTLENKU I WĘGLANÓW METODĄ WARDERA DZIAŁ: Alkacymetria ZAGADNIENIA Prawo zachowania masy i prawo działania mas. Stała równowagi reakcji. Stała dysocjacji, stopień dysocjacji
ĆWICZENIE 2 WSPÓŁOZNACZANIE WODOROTLENKU I WĘGLANÓW METODĄ WARDERA DZIAŁ: Alkacymetria ZAGADNIENIA Prawo zachowania masy i prawo działania mas. Stała równowagi reakcji. Stała dysocjacji, stopień dysocjacji
Wymagania z chemii na poszczególne oceny Klasa 2 gimnazjum. Kwasy.
 Wymagania z chemii na poszczególne oceny Klasa 2 gimnazjum Stopień celujący mogą otrzymać uczniowie, którzy spełniają kryteria na stopień bardzo dobry oraz: Omawiają przemysłową metodę otrzymywania kwasu
Wymagania z chemii na poszczególne oceny Klasa 2 gimnazjum Stopień celujący mogą otrzymać uczniowie, którzy spełniają kryteria na stopień bardzo dobry oraz: Omawiają przemysłową metodę otrzymywania kwasu
d[a] = dt gdzie: [A] - stężenie aspiryny [OH - ] - stężenie jonów hydroksylowych - ] K[A][OH
![d[a] = dt gdzie: [A] - stężenie aspiryny [OH - ] - stężenie jonów hydroksylowych - ] K[A][OH d[a] = dt gdzie: [A] - stężenie aspiryny [OH - ] - stężenie jonów hydroksylowych - ] K[A][OH](/thumbs/48/24702101.jpg) 1 Ćwiczenie 7. Wyznaczanie stałej szybkości oraz parametrów termodynamicznych reakcji hydrolizy aspiryny. Chemiczna stabilność leków jest ważnym terapeutycznym problemem W przypadku chemicznej niestabilności
1 Ćwiczenie 7. Wyznaczanie stałej szybkości oraz parametrów termodynamicznych reakcji hydrolizy aspiryny. Chemiczna stabilność leków jest ważnym terapeutycznym problemem W przypadku chemicznej niestabilności
Summary. Streszczenie. Polimery w Medycynie 2009, T. XXXIX, Nr 4. Witold Musial 1, 2, Vanja Kokol 1, 1
 Witold Musiał i inni Polimery termowrażliwe Polimery w Medycynie 2009, T. XXXIX, Nr 4 Zastosowanie pomiarów konduktometrycznych w ocenie potencjalnego pulsacyjnego uwalniania chlorowodorku lidokainy z
Witold Musiał i inni Polimery termowrażliwe Polimery w Medycynie 2009, T. XXXIX, Nr 4 Zastosowanie pomiarów konduktometrycznych w ocenie potencjalnego pulsacyjnego uwalniania chlorowodorku lidokainy z
Metody Badań Składu Chemicznego
 Metody Badań Składu Chemicznego Wydział Inżynierii Materiałowej i Ceramiki Kierunek: Inżynieria Materiałowa (NIESTACJONARNE) Ćwiczenie 5: Pomiary SEM ogniwa - miareczkowanie potencjometryczne. Pomiary
Metody Badań Składu Chemicznego Wydział Inżynierii Materiałowej i Ceramiki Kierunek: Inżynieria Materiałowa (NIESTACJONARNE) Ćwiczenie 5: Pomiary SEM ogniwa - miareczkowanie potencjometryczne. Pomiary
Wodorotlenki. n to liczba grup wodorotlenowych w cząsteczce wodorotlenku (równa wartościowości M)
 Wodorotlenki Definicja - Wodorotlenkami nazywamy związki chemiczne, zbudowane z kationu metalu (zazwyczaj) (M) i anionu wodorotlenowego (OH - ) Ogólny wzór wodorotlenków: M(OH) n M oznacza symbol metalu.
Wodorotlenki Definicja - Wodorotlenkami nazywamy związki chemiczne, zbudowane z kationu metalu (zazwyczaj) (M) i anionu wodorotlenowego (OH - ) Ogólny wzór wodorotlenków: M(OH) n M oznacza symbol metalu.
Spektroskopia molekularna. Ćwiczenie nr 1. Widma absorpcyjne błękitu tymolowego
 Spektroskopia molekularna Ćwiczenie nr 1 Widma absorpcyjne błękitu tymolowego Doświadczenie to ma na celu zaznajomienie uczestników ćwiczeń ze sposobem wykonywania pomiarów metodą spektrofotometryczną
Spektroskopia molekularna Ćwiczenie nr 1 Widma absorpcyjne błękitu tymolowego Doświadczenie to ma na celu zaznajomienie uczestników ćwiczeń ze sposobem wykonywania pomiarów metodą spektrofotometryczną
PRACOWNIA CHEMII. Wygaszanie fluorescencji (Fiz4)
 PRACOWNIA CHEMII Ćwiczenia laboratoryjne dla studentów II roku kierunku Zastosowania fizyki w biologii i medycynie Biofizyka molekularna Projektowanie molekularne i bioinformatyka Wygaszanie fluorescencji
PRACOWNIA CHEMII Ćwiczenia laboratoryjne dla studentów II roku kierunku Zastosowania fizyki w biologii i medycynie Biofizyka molekularna Projektowanie molekularne i bioinformatyka Wygaszanie fluorescencji
PRZYKŁADOWE ROZWIĄZANIA ZADAŃ
 PRZYKŁADOWE ROZWIĄZANIA ZADAŃ 1. Odważono 1.0 g mieszaniny zawierającej NaOH, Na 2 CO 3 oraz substancje obojętną i rozpuszczono w kolbie miarowej o pojemności 250 ml. Na zmiareczkowanie próbki o objętości
PRZYKŁADOWE ROZWIĄZANIA ZADAŃ 1. Odważono 1.0 g mieszaniny zawierającej NaOH, Na 2 CO 3 oraz substancje obojętną i rozpuszczono w kolbie miarowej o pojemności 250 ml. Na zmiareczkowanie próbki o objętości
Zadanie: 1 (3 pkt) Metanoamina (metyloamina) rozpuszcza się w wodzie, a także reaguje z nią.
 Zadanie: 1 (3 pkt) Metanoamina (metyloamina) rozpuszcza się w wodzie, a także reaguje z nią. Napisz, posługując się wzorami grupowymi (półstrukturalnymi) związków organicznych, równanie reakcji metanoaminy
Zadanie: 1 (3 pkt) Metanoamina (metyloamina) rozpuszcza się w wodzie, a także reaguje z nią. Napisz, posługując się wzorami grupowymi (półstrukturalnymi) związków organicznych, równanie reakcji metanoaminy
WYZNACZANIE STAŁEJ DYSOCJACJI p-nitrofenolu METODĄ SPEKTROFOTOMETRII ABSORPCYJNEJ
 Ćwiczenie nr 13 WYZNCZNIE STŁEJ DYSOCJCJI p-nitrofenolu METODĄ SPEKTROFOTOMETRII BSORPCYJNEJ I. Cel ćwiczenia Celem ćwiczenia jest wyznaczenie metodą spektrofotometryczną stałej dysocjacji słabego kwasu,
Ćwiczenie nr 13 WYZNCZNIE STŁEJ DYSOCJCJI p-nitrofenolu METODĄ SPEKTROFOTOMETRII BSORPCYJNEJ I. Cel ćwiczenia Celem ćwiczenia jest wyznaczenie metodą spektrofotometryczną stałej dysocjacji słabego kwasu,
dla której jest spełniony warunek równowagi: [H + ] [X ] / [HX] = K
![dla której jest spełniony warunek równowagi: [H + ] [X ] / [HX] = K dla której jest spełniony warunek równowagi: [H + ] [X ] / [HX] = K](/thumbs/55/36391740.jpg) RÓWNOWAGI W ROZTWORACH Szwedzki chemik Svante Arrhenius w 1887 roku jako pierwszy wykazał, że procesowi rozpuszczania wielu substancji towarzyszy dysocjacja, czyli rozpad cząsteczek na jony naładowane
RÓWNOWAGI W ROZTWORACH Szwedzki chemik Svante Arrhenius w 1887 roku jako pierwszy wykazał, że procesowi rozpuszczania wielu substancji towarzyszy dysocjacja, czyli rozpad cząsteczek na jony naładowane
1 Kinetyka reakcji chemicznych
 Podstawy obliczeń chemicznych 1 1 Kinetyka reakcji chemicznych Szybkość reakcji chemicznej definiuje się jako ubytek stężenia substratu lub wzrost stężenia produktu w jednostce czasu. ν = c [ ] 2 c 1 mol
Podstawy obliczeń chemicznych 1 1 Kinetyka reakcji chemicznych Szybkość reakcji chemicznej definiuje się jako ubytek stężenia substratu lub wzrost stężenia produktu w jednostce czasu. ν = c [ ] 2 c 1 mol
Ćwiczenie 7. Wyznaczanie stałej szybkości oraz parametrów termodynamicznych reakcji hydrolizy aspiryny.
 1 Ćwiczenie 7. Wyznaczanie stałej szybkości oraz parametrów termodynamicznych reakcji hydrolizy aspiryny. Chemiczna stabilność leków jest ważnym terapeutycznym problemem W przypadku chemicznej niestabilności
1 Ćwiczenie 7. Wyznaczanie stałej szybkości oraz parametrów termodynamicznych reakcji hydrolizy aspiryny. Chemiczna stabilność leków jest ważnym terapeutycznym problemem W przypadku chemicznej niestabilności
SPRAWOZDANIE 2. Data:... Kierunek studiów i nr grupy...
 SPRAWOZDANIE 2 Imię i nazwisko:... Data:.... Kierunek studiów i nr grupy..... Doświadczenie 1.1. Wskaźniki ph stosowane w laboratorium chemicznym. Zanotować obserwowane barwy roztworów w obecności badanych
SPRAWOZDANIE 2 Imię i nazwisko:... Data:.... Kierunek studiów i nr grupy..... Doświadczenie 1.1. Wskaźniki ph stosowane w laboratorium chemicznym. Zanotować obserwowane barwy roztworów w obecności badanych
Glicyna budowa cząsteczki i właściwości
 Waldemar Plewiński Glicyna budowa cząsteczki i właściwości Waldemar Plewiński 252 Cele ogólne lekcji Uczeń: planuje i przeprowadza eksperymenty chemiczne, planuje proces badawczy określonego problemu naukowego,
Waldemar Plewiński Glicyna budowa cząsteczki i właściwości Waldemar Plewiński 252 Cele ogólne lekcji Uczeń: planuje i przeprowadza eksperymenty chemiczne, planuje proces badawczy określonego problemu naukowego,
Spektrofotometryczne wyznaczanie stałej dysocjacji czerwieni fenolowej
 Spektrofotometryczne wyznaczanie stałej dysocjacji czerwieni fenolowej Metoda: Spektrofotometria UV-Vis Cel ćwiczenia: Celem ćwiczenia jest zapoznanie studenta z fotometryczną metodą badania stanów równowagi
Spektrofotometryczne wyznaczanie stałej dysocjacji czerwieni fenolowej Metoda: Spektrofotometria UV-Vis Cel ćwiczenia: Celem ćwiczenia jest zapoznanie studenta z fotometryczną metodą badania stanów równowagi
STAłA I STOPIEŃ DYSOCJACJI; ph MIX ZADAŃ Czytaj uważnie polecenia. Powodzenia!
 STAłA I STOPIEŃ DYSOCJACJI; ph MIX ZADAŃ Czytaj uważnie polecenia. Powodzenia! 001 Obliczyć stężenie molowe jonów Ca 2+ w roztworze zawierającym 2,22g CaCl2 w 100 ml roztworu, przyjmując a = 100%. 002
STAłA I STOPIEŃ DYSOCJACJI; ph MIX ZADAŃ Czytaj uważnie polecenia. Powodzenia! 001 Obliczyć stężenie molowe jonów Ca 2+ w roztworze zawierającym 2,22g CaCl2 w 100 ml roztworu, przyjmując a = 100%. 002
WYMAGANIA NA POSZCZEGÓLNE OCENY Z CHEMII DLA KLASY II. mgr Marta Warecka Lenart
 WYMAGANIA NA POSZCZEGÓLNE OCENY Z CHEMII DLA KLASY II mgr Marta Warecka Lenart (program nauczania chemii Chemia Nowej Ery autorstwa T.Kulawik i M.Litwin) Ocenę dopuszczający otrzymuje uczeń, który w 75%
WYMAGANIA NA POSZCZEGÓLNE OCENY Z CHEMII DLA KLASY II mgr Marta Warecka Lenart (program nauczania chemii Chemia Nowej Ery autorstwa T.Kulawik i M.Litwin) Ocenę dopuszczający otrzymuje uczeń, który w 75%
Wymagania programowe na poszczególne oceny. IV. Kwasy. Ocena bardzo dobra. Ocena dostateczna. Ocena dopuszczająca. Ocena dobra [1] [ ]
![Wymagania programowe na poszczególne oceny. IV. Kwasy. Ocena bardzo dobra. Ocena dostateczna. Ocena dopuszczająca. Ocena dobra [1] [ ] Wymagania programowe na poszczególne oceny. IV. Kwasy. Ocena bardzo dobra. Ocena dostateczna. Ocena dopuszczająca. Ocena dobra [1] [ ]](/thumbs/59/43143309.jpg) Wymagania programowe na poszczególne oceny IV. Kwasy Ocena dopuszczająca Ocena dostateczna Ocena dobra Ocena bardzo dobra [1] [1 + 2] [1 + 2 + 3] [1 + 2 + 3 + 4] wymienia zasady bhp dotyczące obchodzenia
Wymagania programowe na poszczególne oceny IV. Kwasy Ocena dopuszczająca Ocena dostateczna Ocena dobra Ocena bardzo dobra [1] [1 + 2] [1 + 2 + 3] [1 + 2 + 3 + 4] wymienia zasady bhp dotyczące obchodzenia
K02 Instrukcja wykonania ćwiczenia
 Katedra Chemii Fizycznej Uniwersytetu Łódzkiego K2 Instrukcja wykonania ćwiczenia Wyznaczanie krytycznego stężenia micelizacji (CMC) z pomiarów napięcia powierzchniowego Zakres zagadnień obowiązujących
Katedra Chemii Fizycznej Uniwersytetu Łódzkiego K2 Instrukcja wykonania ćwiczenia Wyznaczanie krytycznego stężenia micelizacji (CMC) z pomiarów napięcia powierzchniowego Zakres zagadnień obowiązujących
WPŁYW PROCESU TARCIA NA ZMIANĘ MIKROTWARDOŚCI WARSTWY WIERZCHNIEJ MATERIAŁÓW POLIMEROWYCH
 WOJCIECH WIELEBA WPŁYW PROCESU TARCIA NA ZMIANĘ MIKROTWARDOŚCI WARSTWY WIERZCHNIEJ MATERIAŁÓW POLIMEROWYCH THE INFLUENCE OF FRICTION PROCESS FOR CHANGE OF MICROHARDNESS OF SURFACE LAYER IN POLYMERIC MATERIALS
WOJCIECH WIELEBA WPŁYW PROCESU TARCIA NA ZMIANĘ MIKROTWARDOŚCI WARSTWY WIERZCHNIEJ MATERIAŁÓW POLIMEROWYCH THE INFLUENCE OF FRICTION PROCESS FOR CHANGE OF MICROHARDNESS OF SURFACE LAYER IN POLYMERIC MATERIALS
WPŁYW SUBSTANCJI TOWARZYSZĄCYCH NA ROZPUSZCZALNOŚĆ OSADÓW
 WPŁYW SUBSTANCJI TOWARZYSZĄCYCH NA ROZPUSZCZALNOŚĆ OSADÓW Wstęp Mianem rozpuszczalności określamy maksymalną ilość danej substancji (w gramach lub molach), jaką w danej temperaturze można rozpuścić w określonej
WPŁYW SUBSTANCJI TOWARZYSZĄCYCH NA ROZPUSZCZALNOŚĆ OSADÓW Wstęp Mianem rozpuszczalności określamy maksymalną ilość danej substancji (w gramach lub molach), jaką w danej temperaturze można rozpuścić w określonej
Wymagania programowe na poszczególne oceny. III. Woda i roztwory wodne. Ocena dopuszczająca [1] Uczeń: Ocena dostateczna [1 + 2]
![Wymagania programowe na poszczególne oceny. III. Woda i roztwory wodne. Ocena dopuszczająca [1] Uczeń: Ocena dostateczna [1 + 2] Wymagania programowe na poszczególne oceny. III. Woda i roztwory wodne. Ocena dopuszczająca [1] Uczeń: Ocena dostateczna [1 + 2]](/thumbs/97/134409727.jpg) Wymagania programowe na poszczególne oceny III. Woda i roztwory wodne charakteryzuje rodzaje wód występujących podaje, na czym polega obieg wody wymienia stany skupienia wody nazywa przemiany stanów skupienia
Wymagania programowe na poszczególne oceny III. Woda i roztwory wodne charakteryzuje rodzaje wód występujących podaje, na czym polega obieg wody wymienia stany skupienia wody nazywa przemiany stanów skupienia
KINETYKA INWERSJI SACHAROZY
 Dorota Warmińska, Maciej Śmiechowski Katedra Chemii Fizycznej, Wydział Chemiczny, Politechnika Gdańska KINETYKA INWERSJI SACHAROZY Wstęp teoretyczny Kataliza kwasowo-zasadowa Kataliza kwasowo-zasadowa
Dorota Warmińska, Maciej Śmiechowski Katedra Chemii Fizycznej, Wydział Chemiczny, Politechnika Gdańska KINETYKA INWERSJI SACHAROZY Wstęp teoretyczny Kataliza kwasowo-zasadowa Kataliza kwasowo-zasadowa
Zestaw pytań egzaminu inŝynierskiego przeprowadzanego w Katedrze Fizykochemii i Technologii Polimerów dla kierunku CHEMIA
 Zestaw pytań egzaminu inŝynierskiego przeprowadzanego w Katedrze Fizykochemii i Technologii Polimerów dla kierunku CHEMIA 1. Metody miareczkowania w analizie chemicznej, wyjaśnić działanie wskaźników 2.
Zestaw pytań egzaminu inŝynierskiego przeprowadzanego w Katedrze Fizykochemii i Technologii Polimerów dla kierunku CHEMIA 1. Metody miareczkowania w analizie chemicznej, wyjaśnić działanie wskaźników 2.
A B. Modelowanie reakcji chemicznych: numeryczne rozwiązywanie równań na szybkość reakcji chemicznych B: 1. da dt. A v. v t
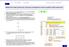 B: 1 Modelowanie reakcji chemicznych: numeryczne rozwiązywanie równań na szybkość reakcji chemicznych 1. ZałóŜmy, Ŝe zmienna A oznacza stęŝenie substratu, a zmienna B stęŝenie produktu reakcji chemicznej
B: 1 Modelowanie reakcji chemicznych: numeryczne rozwiązywanie równań na szybkość reakcji chemicznych 1. ZałóŜmy, Ŝe zmienna A oznacza stęŝenie substratu, a zmienna B stęŝenie produktu reakcji chemicznej
Zagadnienia do pracy klasowej: Kinetyka, równowaga, termochemia, chemia roztworów wodnych
 Zagadnienia do pracy klasowej: Kinetyka, równowaga, termochemia, chemia roztworów wodnych 1. Równanie kinetyczne, szybkość reakcji, rząd i cząsteczkowość reakcji. Zmiana szybkości reakcji na skutek zmiany
Zagadnienia do pracy klasowej: Kinetyka, równowaga, termochemia, chemia roztworów wodnych 1. Równanie kinetyczne, szybkość reakcji, rząd i cząsteczkowość reakcji. Zmiana szybkości reakcji na skutek zmiany
Seria 2, ćwiczenia do wykładu Od eksperymentu do poznania materii
 Seria 2, ćwiczenia do wykładu Od eksperymentu do poznania materii 8.1.21 Zad. 1. Obliczyć ciśnienie potrzebne do przemiany grafitu w diament w temperaturze 25 o C. Objętość właściwa (odwrotność gęstości)
Seria 2, ćwiczenia do wykładu Od eksperymentu do poznania materii 8.1.21 Zad. 1. Obliczyć ciśnienie potrzebne do przemiany grafitu w diament w temperaturze 25 o C. Objętość właściwa (odwrotność gęstości)
KALORYMETRYCZNA OCENA WPŁYWU POLISTYRENU NA KRYSTALIZACJĘ POLIPROPYLENU
 ARTUR KOŚCIUSZKO *, PAULINA JAKUBOWSKA, ARKADIUSZ KLOZIŃSKI **, TOMASZ STERZYŃSKI *** KALORYMETRYCZNA OCENA WPŁYWU POLISTYRENU NA KRYSTALIZACJĘ POLIPROPYLENU THE CALORIMETRIC STUDIES OF AN INFLUENCE OF
ARTUR KOŚCIUSZKO *, PAULINA JAKUBOWSKA, ARKADIUSZ KLOZIŃSKI **, TOMASZ STERZYŃSKI *** KALORYMETRYCZNA OCENA WPŁYWU POLISTYRENU NA KRYSTALIZACJĘ POLIPROPYLENU THE CALORIMETRIC STUDIES OF AN INFLUENCE OF
ANEKS 5 Ocena poprawności analiz próbek wody
 ANEKS 5 Ocena poprawności analiz próbek wody Bilans jonów Zasady ogólne Kontroli jakości danych dokonuje się wykonując bilans jonów. Bilans jonów jest podstawowym testem poprawności wyników analiz chemicznych
ANEKS 5 Ocena poprawności analiz próbek wody Bilans jonów Zasady ogólne Kontroli jakości danych dokonuje się wykonując bilans jonów. Bilans jonów jest podstawowym testem poprawności wyników analiz chemicznych
Wymagania programowe na poszczególne oceny CHEMII kl. II 2017/2018. III. Woda i roztwory wodne. Ocena dopuszczająca [1] Uczeń:
![Wymagania programowe na poszczególne oceny CHEMII kl. II 2017/2018. III. Woda i roztwory wodne. Ocena dopuszczająca [1] Uczeń: Wymagania programowe na poszczególne oceny CHEMII kl. II 2017/2018. III. Woda i roztwory wodne. Ocena dopuszczająca [1] Uczeń:](/thumbs/70/63524095.jpg) Wymagania programowe na poszczególne oceny CHEMII kl. II 2017/2018 III. Woda i roztwory wodne charakteryzuje rodzaje wód występujących w przyrodzie podaje, na czym polega obieg wody w przyrodzie wymienia
Wymagania programowe na poszczególne oceny CHEMII kl. II 2017/2018 III. Woda i roztwory wodne charakteryzuje rodzaje wód występujących w przyrodzie podaje, na czym polega obieg wody w przyrodzie wymienia
Scenariusz lekcji w technikum zakres podstawowy 2 godziny
 Scenariusz lekcji w technikum zakres podstawowy 2 godziny Temat : Hydroliza soli. Cele dydaktyczno wychowawcze: Wyjaśnienie przyczyn różnych odczynów soli Uświadomienie różnej roli wody w procesach dysocjacji
Scenariusz lekcji w technikum zakres podstawowy 2 godziny Temat : Hydroliza soli. Cele dydaktyczno wychowawcze: Wyjaśnienie przyczyn różnych odczynów soli Uświadomienie różnej roli wody w procesach dysocjacji
Kryteria oceniania z chemii dla klasy drugiej DLA UCZNIÓW Z OBOWIĄZKIEM DOSTOSOWANIA WYMAGAŃ EDUKACYJNYCH
 Kryteria oceniania z chemii dla klasy drugiej DLA UCZNIÓW Z OBOWIĄZKIEM DOSTOSOWANIA WYMAGAŃ EDUKACYJNYCH (na podstawie treści zawartych w podstawie programowej, programie nauczania oraz podręczniku dla
Kryteria oceniania z chemii dla klasy drugiej DLA UCZNIÓW Z OBOWIĄZKIEM DOSTOSOWANIA WYMAGAŃ EDUKACYJNYCH (na podstawie treści zawartych w podstawie programowej, programie nauczania oraz podręczniku dla
H2S, H2SO4, H2SO3, HNO3, H2CO3,
 Wymagania programowe z chemii dla klasy drugiej (na podstawie treści zawartych w podstawie programowej, programie nauczania oraz podręczniku dla klasy drugiej gimnazjum Chemia Nowej Ery). Wyróżnione wymagania
Wymagania programowe z chemii dla klasy drugiej (na podstawie treści zawartych w podstawie programowej, programie nauczania oraz podręczniku dla klasy drugiej gimnazjum Chemia Nowej Ery). Wyróżnione wymagania
Estry. 1. Cele lekcji. 2. Metoda i forma pracy. 3. Środki dydaktyczne. a) Wiadomości. b) Umiejętności
 Estry 1. Cele lekcji a) Wiadomości Uczeń: wie, jak zbudowane są cząsteczki estrów, wie, jakie jest zastosowanie estrów, wie, jakie są właściwości fizyczne octanu etylu zna pojęcia: stan równowagi dynamicznej,
Estry 1. Cele lekcji a) Wiadomości Uczeń: wie, jak zbudowane są cząsteczki estrów, wie, jakie jest zastosowanie estrów, wie, jakie są właściwości fizyczne octanu etylu zna pojęcia: stan równowagi dynamicznej,
Wielofunkcyjne związki organiczne poziom rozszerzony
 Wielofunkcyjne związki organiczne poziom rozszerzony Zadanie 1. (2 pkt) Źródło: KE 2010 (PR), zad. 29. Pewien dwufunkcyjny związek organiczny ma masę molową równą 90 g/mol. W jego cząsteczce stosunek liczby
Wielofunkcyjne związki organiczne poziom rozszerzony Zadanie 1. (2 pkt) Źródło: KE 2010 (PR), zad. 29. Pewien dwufunkcyjny związek organiczny ma masę molową równą 90 g/mol. W jego cząsteczce stosunek liczby
Instrukcja do ćwiczeń laboratoryjnych
 UNIWERSYTET GDAŃSKI WYDZIAŁ CHEMII Pracownia studencka Katedra Analizy Środowiska Instrukcja do ćwiczeń laboratoryjnych Ćwiczenie nr 3 OZNACZANIE CHLORKÓW METODĄ SPEKTROFOTOMETRYCZNĄ Z TIOCYJANIANEM RTĘCI(II)
UNIWERSYTET GDAŃSKI WYDZIAŁ CHEMII Pracownia studencka Katedra Analizy Środowiska Instrukcja do ćwiczeń laboratoryjnych Ćwiczenie nr 3 OZNACZANIE CHLORKÓW METODĄ SPEKTROFOTOMETRYCZNĄ Z TIOCYJANIANEM RTĘCI(II)
ĆWICZENIE 2 KONDUKTOMETRIA
 ĆWICZENIE 2 KONDUKTOMETRIA 1. Oznaczanie słabych kwasów w sokach i syropach owocowych metodą miareczkowania konduktometrycznego Celem ćwiczenia jest ilościowe oznaczenie zawartości słabych kwasów w sokach
ĆWICZENIE 2 KONDUKTOMETRIA 1. Oznaczanie słabych kwasów w sokach i syropach owocowych metodą miareczkowania konduktometrycznego Celem ćwiczenia jest ilościowe oznaczenie zawartości słabych kwasów w sokach
WYZNACZANIE STAŁEJ DYSOCJACJI SŁABEGO KWASU ORGANICZNEGO
 10 WYZNACZANIE STAŁEJ DYSOCJACJI SŁABEGO KWASU ORGANICZNEGO CEL ĆWICZENIA Poznanie podstawowych zagadnień teorii dysocjacji elektrolitycznej i problemów związanych z właściwościami kwasów i zasad oraz
10 WYZNACZANIE STAŁEJ DYSOCJACJI SŁABEGO KWASU ORGANICZNEGO CEL ĆWICZENIA Poznanie podstawowych zagadnień teorii dysocjacji elektrolitycznej i problemów związanych z właściwościami kwasów i zasad oraz
KONKURS CHEMICZNY ROK PRZED MATURĄ
 Wydział Chemii UMCS Polskie Towarzystwo Chemiczne Doradca metodyczny ds. nauczania chemii KONKURS CHEMICZNY ROK PRZED MATURĄ ROK SZKOLNY 2006/2007 ETAP SZKOLNY Numer kodowy Suma punktów Podpisy Komisji:
Wydział Chemii UMCS Polskie Towarzystwo Chemiczne Doradca metodyczny ds. nauczania chemii KONKURS CHEMICZNY ROK PRZED MATURĄ ROK SZKOLNY 2006/2007 ETAP SZKOLNY Numer kodowy Suma punktów Podpisy Komisji:
WPŁYW SUBSTANCJI TOWARZYSZĄCYCH NA ROZPUSZCZALNOŚĆ OSADÓW
 WPŁYW SUBSTANCJI TOWARZYSZĄCYCH NA ROZPUSZCZALNOŚĆ OSADÓW Wstęp W przypadku trudno rozpuszczalnej soli, mimo osiągnięcia stanu nasycenia, jej stężenie w roztworze jest bardzo małe i przyjmuje się, że ta
WPŁYW SUBSTANCJI TOWARZYSZĄCYCH NA ROZPUSZCZALNOŚĆ OSADÓW Wstęp W przypadku trudno rozpuszczalnej soli, mimo osiągnięcia stanu nasycenia, jej stężenie w roztworze jest bardzo małe i przyjmuje się, że ta
SZCZEGÓŁOWE KRYTERIA OCENIANIA Z CHEMII DLA KLASY II GIMNAZJUM Nauczyciel Katarzyna Kurczab
 SZCZEGÓŁOWE KRYTERIA OCENIANIA Z CHEMII DLA KLASY II GIMNAZJUM Nauczyciel Katarzyna Kurczab CZĄSTECZKA I RÓWNANIE REKCJI CHEMICZNEJ potrafi powiedzieć co to jest: wiązanie chemiczne, wiązanie jonowe, wiązanie
SZCZEGÓŁOWE KRYTERIA OCENIANIA Z CHEMII DLA KLASY II GIMNAZJUM Nauczyciel Katarzyna Kurczab CZĄSTECZKA I RÓWNANIE REKCJI CHEMICZNEJ potrafi powiedzieć co to jest: wiązanie chemiczne, wiązanie jonowe, wiązanie
Chemia - B udownictwo WS TiP
 Chemia - B udownictwo WS TiP dysocjacja elektrolityczna, reakcje w roztworach wodnych, ph wykład nr 2b Teoria dys ocjacji jonowej Elektrolity i nieelektrolity Wpływ polarnej budowy cząsteczki wody na proces
Chemia - B udownictwo WS TiP dysocjacja elektrolityczna, reakcje w roztworach wodnych, ph wykład nr 2b Teoria dys ocjacji jonowej Elektrolity i nieelektrolity Wpływ polarnej budowy cząsteczki wody na proces
PODSTAWY CHEMII INŻYNIERIA BIOMEDYCZNA. Wykład 2
 PODSTAWY CEMII INŻYNIERIA BIOMEDYCZNA Wykład Plan wykładu II,III Woda jako rozpuszczalnik Zjawisko dysocjacji Równowaga w roztworach elektrolitów i co z tego wynika Bufory ydroliza soli Roztwory (wodne)-
PODSTAWY CEMII INŻYNIERIA BIOMEDYCZNA Wykład Plan wykładu II,III Woda jako rozpuszczalnik Zjawisko dysocjacji Równowaga w roztworach elektrolitów i co z tego wynika Bufory ydroliza soli Roztwory (wodne)-
Propozycja planu wynikowego Chemia Nowej Ery - klasa 2 gimnazjum
 1 Propozycja planu wynikowego Chemia Nowej Ery - klasa 2 gimnazjum Tytuł rozdziału w podręczniku Temat lekcji Dział III. Woda i roztwory wodne Treści nauczania 7. Poznajemy związek chemiczny wodoru i tlenu
1 Propozycja planu wynikowego Chemia Nowej Ery - klasa 2 gimnazjum Tytuł rozdziału w podręczniku Temat lekcji Dział III. Woda i roztwory wodne Treści nauczania 7. Poznajemy związek chemiczny wodoru i tlenu
Podstawowe pojęcia 1
 Tomasz Lubera Półogniwo Podstawowe pojęcia 1 układ złożony z min. dwóch faz pozostających ze sobą w kontakcie, w którym w wyniku zachodzących procesów utleniania lub redukcji ustala się stan równowagi,
Tomasz Lubera Półogniwo Podstawowe pojęcia 1 układ złożony z min. dwóch faz pozostających ze sobą w kontakcie, w którym w wyniku zachodzących procesów utleniania lub redukcji ustala się stan równowagi,
a) 1 mol b) 0,5 mola c) 1,7 mola d) potrzebna jest znajomość objętości zbiornika, aby można było przeprowadzić obliczenia
 1. Oblicz wartość stałej równowagi reakcji: 2HI H 2 + I 2 w temperaturze 600K, jeśli wiesz, że stężenia reagentów w stanie równowagi wynosiły: [HI]=0,2 mol/dm 3 ; [H 2 ]=0,02 mol/dm 3 ; [I 2 ]=0,024 mol/dm
1. Oblicz wartość stałej równowagi reakcji: 2HI H 2 + I 2 w temperaturze 600K, jeśli wiesz, że stężenia reagentów w stanie równowagi wynosiły: [HI]=0,2 mol/dm 3 ; [H 2 ]=0,02 mol/dm 3 ; [I 2 ]=0,024 mol/dm
Komunikat. Tajemnice produktów polikrzemianowych SEMPRE.
 Komunikat Tajemnice produktów polikrzemianowych SEMPRE. Tynki polikrzemianowe produkowane przez SEMPRE Farby sp. z o.o. zawierają nanocząsteczkowe wodne dyspersje polikrzemianów. Stanowią one cząsteczki
Komunikat Tajemnice produktów polikrzemianowych SEMPRE. Tynki polikrzemianowe produkowane przez SEMPRE Farby sp. z o.o. zawierają nanocząsteczkowe wodne dyspersje polikrzemianów. Stanowią one cząsteczki
STĘŻENIE JONÓW WODOROWYCH. DYSOCJACJA JONOWA. REAKTYWNOŚĆ METALI
 Ćwiczenie 8 Semestr 2 STĘŻENIE JONÓW WODOROWYCH. DYSOCJACJA JONOWA. REAKTYWNOŚĆ METALI Obowiązujące zagadnienia: Stężenie jonów wodorowych: ph, poh, iloczyn jonowy wody, obliczenia rachunkowe, wskaźniki
Ćwiczenie 8 Semestr 2 STĘŻENIE JONÓW WODOROWYCH. DYSOCJACJA JONOWA. REAKTYWNOŚĆ METALI Obowiązujące zagadnienia: Stężenie jonów wodorowych: ph, poh, iloczyn jonowy wody, obliczenia rachunkowe, wskaźniki
1. za pomocą pomiaru SEM (siła elektromotoryczna róŝnica potencjałów dwóch elektrod) i na podstawie wzoru wyznaczenie stęŝenia,
 Potencjometria Potencjometria instrumentalna metoda analityczna, wykorzystująca zaleŝność pomiędzy potencjałem elektrody wzorcowej, a aktywnością jonów lub cząstek w badanym roztworze (elektrody wskaźnikowej).
Potencjometria Potencjometria instrumentalna metoda analityczna, wykorzystująca zaleŝność pomiędzy potencjałem elektrody wzorcowej, a aktywnością jonów lub cząstek w badanym roztworze (elektrody wskaźnikowej).
