Spis treści. Fizyka wczoraj, dziś, jutro. Z naszych lekcji. Astronomia dla każdego. Olimpiady, konkursy, zadania
|
|
|
- Stefan Grzelak
- 7 lat temu
- Przeglądów:
Transkrypt
1 Spis treści Fizyka wczoraj, dziś, jutro Modelowanie fizyczne wybranych 4 procesów biologicznych Kazimierz Mikulski Z naszych lekcji Energia elektryczna z kwiatów 29 ogniwa fotowoltaiczne wykorzystujące naturalne barwniki Katarzyna Siuzdak Tomografia komputerowa 7 Tomasz Kubiak Archeologia XXI wieku, cz. II 11 Sławomir Jędraszek Fotoniczny układ rozwiązujący 27 zagadnienie z mechaniki kwantowej Marcin Majka, Tomasz M. Majka Astronomia dla każdego Astronomia w programach 14 szkolnych Jerzy M. Kreiner Marsjańskie morze Hellas 19 Natalia Zalewska Bernoulli, Magnus i ping-pong 33 (i nie tylko) Juliusz Domański e-doświadczenia w fizyce 35 nowoczesne technologie w służbie dydaktyki, gdy tradycyjne metody są niewystarczające Paweł Syty, Patryk Jasik Niepewność pomiarowa bez 37 pochodnych Waldemar Reńda Innowacje społeczne w obszarze Edukacja 39 i szkolnictwo wyższe Dariusz Pietrzyk Wygraj kosmiczne wakacje! 42 ASTROBOT konkurs dla gimnazjalistów Nieskończoność w zadaniach 43 z fizyki Janusz Rokita Co w fizyce piszczy? 47 Zbigniew Wiśniewski Olimpiady, konkursy, zadania Turniej zadaniowy Zostań 48 Mistrzem. Seria 108 Bogusław Urwanowicz
2 Energia elektryczna z kwiatów ogniwa fotowoltaiczne wykorzystujące naturalne barwniki Katarzyna Siuzdak Wstęp Od momentu odkrycia efektu fotowoltaicznego przez Aleksandra Becquerela prowadzone są intensywne badania w obszarze ogniw fotowoltaicznych po to, aby uzyskać jak najwyższą wydajność konwersji światła słonecznego na energię elektryczną. Najczęściej badania te dotyczą wykorzystania coraz to nowych materiałów. Obok popularnego krzemu pojawił się tellurek kadmu, selenek miedzi i indu czy arsenek galu. Jednak tak naprawdę efekt fotowoltaiczny został odkryty i wykorzystany ponad 2,8 mld lat temu przez bakterie fotosyntezujące prekursory roślin. Co ciekawe, fotosynteza nie była uznawana za podstawę rozwoju ogniw słonecznych aż do lat 90. ubiegłego wieku, czyli ponad 160 lat po odkryciu efektu fotowoltaicznego przez Becquerela. W 1991 roku Michael Grätzel i Brian O Regan [1] opracowali nową technologię wytwarzania ogniw słonecznych, których działanie imituje właśnie mechanizm fotosyntezy. Nowe ogniwa słoneczne nazwano barwnikowymi ogniwami fotowoltaicznymi (DSSC, ang. dye-sensitized solar cells). Cieszą się one coraz większym zainteresowaniem ze względu na ich potencjał w niskokosztowej konwersji światła słonecznego na energię elektryczną. W porównaniu z ogniwami krzemowymi barwnikowe ogniwa fotowoltaiczne wytwarzane są z tańszych materiałów, bezpiecznych dla środowiska naturalnego, a ich czystość nie musi być tak wysoka jak w przypadku krzemu. Obecnie rekord wydajności tego typu ogniw to 13% [2], a szacowany na podstawie badań stabilności czas życia w warunkach eksploatacyjnych wynosi 10 lat. Jednakże biorąc pod uwagę wydajność, barwnikowe ogniwa słoneczne niestety nie mogą równać się z tradycyjnymi ogniwami krzemowymi, ale ich zalety zachęcają do rozpowszechnienia tych ogniw na rynku. Należą do nich: mniejsza ilość CO 2 wytwarzanego podczas produkcji; możliwość zmiany koloru i stopnia przezroczystości ogniwa w zależności od zastosowanego barwnika, warstwy tlenkowej, co umożliwia projektowanie urządzeń; produkcja odbywa się prostą techniką sitodruku; Rys. 1. Budowa barwnikowego ogniwa słonecznego krótszy czas zwrotu energii z panelu DSSC (0,3 roku) w porównaniu z innymi typami ogniw (scsi 2,2 roku, CdTe 0,7 roku) [3]. Budowa i zasada działania ogniwa barwnikowego Barwnikowe ogniwo fotowoltaiczne składa się z następujących części: fotoanody (zbudowanej z nanokrystalicznego, półprzewodzącego tlenku metalu uczulonego barwnikiem), pary redoksowej jodek/trójjodek (rozpuszczonej w odpowiednim medium stanowiącym elektrolit) oraz katody (jest nią materiał katalizujący reakcję redoksową). Schemat budowy barwnikowego ogniwa fotowoltaicznego przedstawiono na rys. 1. Sercem całego układu jest właśnie fotoanoda, którą stanowi porowata warstwa tlenkowa zbudowana z cząsteczek o rozmiarach nanometrycznych, naniesiona na półprzewodzące i półprzezroczyste podłoże. Jako podłoże stosuje się tlenek indu domieszkowany fluorem (FTO). Z kolei najczęściej wykorzystywanym materiałem tlenkowym jest ditlenek tytanu. Oprócz popularnego TiO 2 wykorzystuje się również tlenek cynku, wanadu czy niobu. Na powierzchni tlenku zaadsorbowany jest barwnik, który jest odpowiedzialny za efektywne pochłanianie promieniowania słonecznego z zakresu widzialnego. Molekuły barwnika są trwale zamocowane na powierzchni warstwy tlenku przez utworzenie Fizyka w Szkole 1/
3 wiązania między grupą hydroksylową TiO 2 a ugrupowaniem, np. karboksylowym, obecnym w strukturze barwnika. Barwniki stosowane w tego typu ogniwach powinny charakteryzować się: szerokim widmem absorpcji promieniowania słonecznego; obecnością ugrupowań umożliwiających trwałe związanie z powierzchnią tlenku ( COOH, H 2 PO 3, SO 3 H); wyższą energią wzbudzenia barwnika niż krawędź pasma przewodnictwa półprzewodnika, tak by mógł zajść efektywny proces przeniesienia elektronu między wzbudzonym barwnikiem a pasmem przewodnictwa półprzewodnika; bardziej dodatnim poziomem stanu utlenionego niż potencjał redoksowy elektrolitu, co zapewnia regenerację barwnika; odpornością na fotodegradację, stabilność termiczną i elektrochemiczną. Najczęściej wykorzystywanymi barwnikami są kompleksy rutenu, np. cis-diizotiocyjanian bis(2,2 -bipirydylo-4,4 -dikarbonylo) rutenu (II), znany powszechnie jako N3, czy jego sól tetrabutyloamoniowa oznaczana jako N719. Stosuje się również kompleksy osmu, miedzi, a także porfiryny i ftalocyjaniany. Drugą elektrodę (katodę) stanowi najczęściej warstwa platyny nałożona na przezroczyste, półprzewodzące podłoże. Jej zadaniem jest katalizowanie reakcji redukcji I 3 do I. Przestrzeń między elektrodami wypełnia elektrolit z parą redoksową I /I 3, której rolą jest regeneracja barwnika, czyli umożliwienie mu powrotu ze stanu wzbudzonego do podstawowego. Na rys. 2 przedstawiono drogę przemieszania się ładunku w barwnikowym ogniwie fotowoltaicznym. Zgodnie z oznaczeniami zasada działania jest następująca [1]: 1 cząsteczki barwnika absorbują foton, co prowadzi do przeniesienia elektronu ze stanu podstawowego S 0 do stanu wzbudzonego barwnika S*; 2 następuje wstrzyknięcie elektronu do pasma przewodnictwa półprzewodnika; Rys. 2. Schemat obrazujący zasadę działania ogniwa (opis poszczególnych etapów omówiono w treści artykułu) 3 jon I prowadzi do redukcji stanu wzbudzonego molekuł barwnika z S* do S o ; 4 transport elektronu w porowatej warstwie półprzewodnika do przewodzącej elektrody; 5 obwodem zewnętrznym elektron dociera do katody; 6 elektron jest przeniesiony z katody na I 3 i następuje redukcja do I (I 3 + 2e 3 I ). Rys. 3. Proces wytwarzania barwnikowego ogniwa słonecznego (opis poszczególnych etapów omówiono w treści artykułu) Wytwarzanie W przeciwieństwie do tradycyjnych ogniw krzemowych czy cienkowarstwowych ogniw CIGS wytwarzanie barwnikowych ogniw słonecznych nie wymaga skomplikowanej aparatury ani ściśle kontrolowanych warunków atmosfery. Proces wytwarzania został przedstawiony na rys. 3. Rozpoczyna się on od przygotowania półprzezroczystych podłoży przewodzących FTO. Poddawane są one standardowej procedurze oczyszczania (etap 1) przez zanurzenie kolejno w wodzie dejonizowanej, acetonie, etanolu i na koniec w izopropanolu. W każdym z roztworów szła FTO są przetrzymywane przez ok minut i poddane działaniu ultradźwięków, tak by dokładnie usunąć wszelkie zabrudzenia. Następnie, wykorzystując materiał tlenkowy w postaci pasty, na oczyszczone podłoże FTO nakładana jest cienka warstwa (ok. 3 µm) techniką sitodruku (etap 2). W celu otrzymania pasty miesza się tlenek metalu w formie proszku z substancjami pomocniczymi, które np. nadają odpowiednią lepkość, stabilizują dyspersję, np. glikol etylenowy, monohydrat kwasu cytrynowego. Warstwy po kolei trafiają do pieca, gdzie w temperaturze C (przez ok. 1 godzinę) dochodzi do kalcynacji, podczas której usuwane są organiczne składniki pasty (etap 3). Po ochłodzeniu do temperatury ok. 80 C podłoża z warstwą tlenku są zanurzane w roztworze barwnika i przechowywane w miejscu z dala od światła (etap 4). Roztwór barwnika sporządza się najczęściej przez rozpuszczenie proszku syntetycznego barwnika w etanolu lub uzyskuje się go w wyniku ekstrakcji ze źródeł naturalnych, np. płatków, liści czy owoców. Po ok. 24 godzinach zabarwione warstwy wyjmuje się z roztworu barwnika i delikatnie przemywa czystym etanolem, aby usunąć nadmiar barwnika, który nie zaadsorbował na powierzchni tlenku. W powyżej opisany sposób powstaje fotoanoda. 30 Fizyka w Szkole 1/2014
4 Jak już wspomniano, katodą jest najczęściej cienka warstwa Pt naniesiona na podłoże FTO. Warstwy te nakłada się różnymi sposobami, m.in. z roztworu przez naniesienie cienkiej warstwy z roztworu H 2 PtCl 6 (np. w warunkach laboratoryjnych wystarczy przetrzeć powierzchnię FTO wacikiem zanurzonym w roztworze H 2 PtCl 6 ) (etap 5) i utrwalenie w wysokiej temperaturze (etap 6), przez osadzenie elektrochemiczne czy napylenie w wyniku ablacji laserowej z blaszki platynowej. Gotowe ogniwa powstają przez połączenie anody z katodą przy użyciu folii uszczelniającej, która pełni jednocześnie funkcję separatora obu elektrod (etap 7). Przestrzeń między elektrodami wypełnia się elektrolitem. Elektrolit stanowi roztwór jodu i jodku w rozpuszczalniku organicznym (np. acetonitrylu), do którego często dodaje się substancję wspomagającą ruchliwość jonów. Jak otrzymać naturalne barwniki? Barwniki syntetyczne są stosunkowo tanie i zapewniają wysoką wydajność ogniwa słonecznego. Jednakże ich synteza jest skomplikowana, a jej wydajność niewielka. Barwniki naturalne, które znajdują się w kwiatach, liściach czy owocach, można bardzo łatwo uzyskać za pomocą powszechnie znanej metody ekstrakcji. Ze względu na ich niewielki koszt, brak toksyczności czy zdolność całkowitej biodegradacji naturalne barwniki bardzo często są wykorzystywane w badaniach naukowych [5, 6, 7]. Dotąd użyto m.in. antocyjanów, karotenu, taniny, chlorofilu jako naturalnych substancji fotouczulających. Aby uzyskać takie naturalne barwniki, wystarczy zebrać kwiaty, liście czy też owoce bogate w substancje barwne. Następnie należy je suszyć przez co najmniej 10 godzin w temperaturze ok. 65 C, aby pozbyć się wody. Otrzymany susz trzeba dokładnie rozetrzeć w moździerzu, aż powstanie bardzo drobny proszek. Następnie należy wymieszać ok. 1 g proszkowej próbki z 60 ml etanolu i zostawić na 24 godziny w temperaturze pokojowej, ale z dala od światła. W tym czasie barwnik przejdzie z proszku do alkoholu w wyniku ekstrakcji. Na koniec należy otrzymaną zawiesinę przefiltrować, tak by oddzielić zabarwiony alkohol od osadu, czyli pozostałości proszku. Przefiltrowany alkoholowy roztwór barwnika można następnie wykorzystać do zabarwienia fotoanody. Opisany proces ekstrakcji można z powodzeniem zastosować do otrzymania barwnika z kwiatów: rododendronu, petunii, begonii, róży, fiołka czy nagietka. Jednakże wiele płatków czy owoców zawiera więcej niż jedną substancję barwną, co wymaga przeprowadzenia kilkustopniowej ekstrakcji. Ciekawym przykładem wykorzystania Fot. 1. Owoc mangostanu [8] bardziej złożonego procesu uzyskiwania barwników jest ekstrakcja substancji barwnych z mangostanu (fot. 1) jednego z najsmaczniejszych owoców tropikalnych. Przypomina on pomarańczę, morelę i ananasa. Owoc ten jest uprawiany głównie w południowo-wschodniej Azji. Z tłuszczu wytłaczanego z jego nasion produkuje się mydło, a drewno jest wykorzystywane w rzeźbiarstwie. Badania opublikowane przez Zhou i współpracowników [4] pokazały, że spośród wielu naturalnych barwników to właśnie barwnik otrzymany z mangostanu pozwolił na uzyskanie najwyższej wydajności fotoogniwa (1,17%). Na rys. 4 przedstawiono kolejne etapy otrzymywania barwnika z tego owocu. W ostatnim etapie (według schematu na rys. 4a) uzyskuje się dwa ekstrakty oznaczone jako A i B. Roztwór B poddaje się dalszemu oczyszczaniu, który pokazano na schemacie na rys. 4b. Jak widać, z roztworu B otrzymuje się pięć ekstraktów: eter naftowy (I), chloroform (II), octan etylu (III), n-butanol (IV) i wodę (V). Wśród tych roztworów eter naftowy jest bezbarwny, podczas gdy pozostałe cztery są kolorowe. Na rys. 5 przedstawiono główne składniki ekstraktu w różnych rozpuszczalnikach. Wykorzystując roztwór (III) do barwienia fotoanody, uzyskuje się najwyższą wydajność fotokonwersji 1,12%, a dla pozostałych ekstraktów wydajność wynosi odpowiednio: (II) 0,92%, (IV) Rys. 4. Proces oczyszczania ekstraktów otrzymanych z owocu mangostanu Fizyka w Szkole 1/
5 0,33%, (V) 0,3%. Znaczne różnice w wydajności fotokonwersji między ekstraktami III i II a IV i V wynikają z większej ilości ugrupowań hydroksylowych obecnych w związkach (II) i (III), które biorą udział w wiązaniu z powierzchniowymi ugrupowaniami OH warstwy ditlenku tytanu. Co ciekawe, zastosowanie do barwienia mieszaniny wszystkich związków barwnych, czyli roztworu B, nie jest sumą wydajności uzyskanych dla poszczególnych roztworów (I) (V). Oznacza to, że nie obserwuje się efektu synergistycznego, co można wytłumaczyć na dwa sposoby. Po pierwsze, mimo że adsorpcja kilku substancji barwnych pozwala na pochłanianie światła z szerszego zakresu promieniowania, to jednocześnie dochodzi do hamowania procesu wstrzykiwania elektronów do pasma przewodnictwa półprzewodnika. Po drugie, silny efekt steryczny (efekt wynikający z budowy przestrzennej cząsteczki) mangostanu, rutyny, trihamnozydu mangostynu przeszkadza w efektywnym zaczepieniu się cząsteczek różnych barwników na powierzchni TiO 2. Rys. 5. Wzór strukturalny głównych składników ekstraktu owocu mangostanu z różnych roztworów: (II) chloroformu, (III) octanu etylu oraz (IV) butanolu Rys. 6. Przykłady wykorzystania barwnikowych ogniw słonecznych. Od lewej: półprzezroczyste okno, lampion, torba z wbudowanym ogniwem [9, 10] Ciekawe zastosowanie Barwnikowe ogniwo fotowoltaiczne, jak każde ogniwo słoneczne, jest źródłem energii elektrycznej uzyskanej w wyniku konwersji światła słonecznego. Jednakże dzięki zastosowaniu różnych barwników czy past tlenkowych możliwe jest wytworzenie urządzenia, które spełnia funkcje nie tylko użytkowe, ale i estetyczne (rys. 6). Przykładowo zastosowanie półprzezroczystych elektrod tlenkowych pozwala na konstrukcję ogniwa, które częściowo przepuszcza promieniowanie słoneczne i może pełnić funkcję powierzchni przyciemniającej. Wykorzystanie zaś różnego koloru barwników (naturalnych bądź syntetycznych) umożliwia kontrolę wyglądu ogniwa, co znalazło zastosowanie m.in. w konstrukcji lampionów. Ciekawym rozwiązaniem jest też wbudowanie takiego ogniwa do torby, dzięki czemu można ładować podręczny sprzęt elektroniczny, np. laptop, telefon komórkowy czy odtwarzacz mp3. Omówione tu barwnikowe ogniwo fotowoltaiczne to idealny temat na bardzo ciekawą lekcję fizyki. Odwołując się do mechanizmu fotosyntezy znanego z lekcji biologii, można w nietypowy sposób przejść do efektu fotowoltaicznego i zasady działania ogniwa DSSC. Ponadto jeśli dysponujemy dobrze wyposażonym laboratorium fizykochemicznym, możemy pokusić się o wykonanie takiego ogniwa w warunkach szkolnych. Warto wykorzystać również gotowe zestawy, które oferuje np. firma Solaronix ( Pozwalają one na sprawne złożenie całego ogniwa słonecznego i sprawdzenie jego działania przez podłączenie niewielkiego wiatraczka zasilanego energią uzyskaną z ogniwa DSSC. dr inż. Katarzyna Siuzdak Ośrodek Techniki Plazmowej i Laserowej, Instytut Maszyn Przepływowych im. Roberta Szewalskiego w Gdańsku LITERATURA [1] O Regan B., Grätzel M., A low-cost, high-efficiency solar cells based on dye-sensitized colloidal TiO 2 films, Nature 1991, Vol. 353, s [2] Yella A., Lee H.W., Tsao H.N. et al., Porphyrin-sensitized solar cells with cobalt (II/III)-based redox electrolyte exceed 12 percent efficiency, Science 2011, Vol. 334, s [3] [dostęp: ] [4] Zhou H., Wu L., Gao Y., Ma T., Dye-sensitized solar cells using 20 natural dyes as sensitizers, Journal of Photochemistry Photobiology A: Chemistry 2011, Vol. 219, s [5] Jasim K.E., Natural dye-sensitized solar cell based on nanocrystalline TiO 2, Sains Malaysiana 2012, Vol. 41, s [6] Kim H., Bin Y., Karthick S.N., Hemalatha K.V., Justin Raj C., Venkatesan S., Park S., Vijayakumar G., Natural dye extracted from Rhododendron species flowers as a photosensitized in dye-sensitized solar cell, International Journal of Electrochemcal Science 2013, Vol. 8, s [7] Taya S., El-Agez T.M., El-Ghamri H.S., Abdel-Latif M.S., Dye-sensitized solar cells using fresh and dried natural dyes, International Journal of Materials Science and Applications 2013, Vol. 2, s [8] [dostęp: ] 32 Fizyka w Szkole 1/2014
zasada działania, prawidłowy dobór wielkości instalacji, usytuowanie instalacji, produkcja energii w cyklu rocznym dr inż. Andrzej Wiszniewski
 Fotowoltaika w teorii zasada działania, prawidłowy dobór wielkości instalacji, usytuowanie instalacji, produkcja energii w cyklu rocznym dr inż. Andrzej Wiszniewski Technicznie dostępny potencjał energii
Fotowoltaika w teorii zasada działania, prawidłowy dobór wielkości instalacji, usytuowanie instalacji, produkcja energii w cyklu rocznym dr inż. Andrzej Wiszniewski Technicznie dostępny potencjał energii
Laboratorium z Konwersji Energii. Ogniwo Paliwowe PEM
 Laboratorium z Konwersji Energii Ogniwo Paliwowe PEM 1.0 WSTĘP Ogniwo paliwowe typu PEM (ang. PEM FC) Ogniwa paliwowe są urządzeniami elektro chemicznymi, stanowiącymi przełom w dziedzinie źródeł energii,
Laboratorium z Konwersji Energii Ogniwo Paliwowe PEM 1.0 WSTĘP Ogniwo paliwowe typu PEM (ang. PEM FC) Ogniwa paliwowe są urządzeniami elektro chemicznymi, stanowiącymi przełom w dziedzinie źródeł energii,
Badania i rozwój technologii ogniw PV
 Badania i rozwój technologii ogniw PV Autor: dr inż. Katarzyna Siuzdak, mgr inż. Maciej Klein, mgr inż. Mariusz Szkoda Instytut Maszyn Przepływowych PAN, Gdańsk ("Czysta Energia" - 12/2014) W ostatnich
Badania i rozwój technologii ogniw PV Autor: dr inż. Katarzyna Siuzdak, mgr inż. Maciej Klein, mgr inż. Mariusz Szkoda Instytut Maszyn Przepływowych PAN, Gdańsk ("Czysta Energia" - 12/2014) W ostatnich
Architektoniczne walory ogniw DSSC
 Architektoniczne walory ogniw DSSC Autorzy: dr inż. Jolanta Szlachta, mgr inż. Ludmiła Marszałek, mgr inż. Sławomir Chrobak - ML System, Rzeszów ("Czysta Energia" - nr 7-8/2014) Barwnikowe ogniwa słoneczne
Architektoniczne walory ogniw DSSC Autorzy: dr inż. Jolanta Szlachta, mgr inż. Ludmiła Marszałek, mgr inż. Sławomir Chrobak - ML System, Rzeszów ("Czysta Energia" - nr 7-8/2014) Barwnikowe ogniwa słoneczne
Nanokrystaliczne ogniwo słoneczne
 Nanokrystaliczne ogniwo słoneczne Wprowadzenie Ogniwa słoneczne. Celem niniejszego ćwiczenia jest zbudowanie fotoelektrochemicznego ogniwa słonecznego działającego na półprzewodniku sensybilizowanym barwnikiem
Nanokrystaliczne ogniwo słoneczne Wprowadzenie Ogniwa słoneczne. Celem niniejszego ćwiczenia jest zbudowanie fotoelektrochemicznego ogniwa słonecznego działającego na półprzewodniku sensybilizowanym barwnikiem
LABORATORIUM PRZEMIAN ENERGII
 LABORATORIUM PRZEMIAN ENERGII BADANIE OGNIWA PALIWOWEGO TYPU PEM I. Wstęp Ćwiczenie polega na badaniu ogniwa paliwowego typu PEM. Urządzenia tego typy są obecnie rozwijane i przystosowywane do takich aplikacji
LABORATORIUM PRZEMIAN ENERGII BADANIE OGNIWA PALIWOWEGO TYPU PEM I. Wstęp Ćwiczenie polega na badaniu ogniwa paliwowego typu PEM. Urządzenia tego typy są obecnie rozwijane i przystosowywane do takich aplikacji
Nanorurki w służbie fotowoltaiki
 Nanorurki w służbie fotowoltaiki Autorzy: dr inż. Kamila Żelechowska, inż. Adam Wróbel, Katedra Fizyki Zjawisk Elektronowych, Wydział Fizyki Technicznej i Matematyki Stosowanej, Politechnika Gdańska (
Nanorurki w służbie fotowoltaiki Autorzy: dr inż. Kamila Żelechowska, inż. Adam Wróbel, Katedra Fizyki Zjawisk Elektronowych, Wydział Fizyki Technicznej i Matematyki Stosowanej, Politechnika Gdańska (
OGNIWO SŁONECZNE. Rys.1 Typowe ogniwo słoneczne. Na skutek absorpcji fotonu powstają dziury i elektrony (nośniki prądu), które są
 OGNIWO SŁONECZNE Cel ćwiczenia Budowa nanokrystalicznego ogniwa słonecznego półprzewodnikowego TiO2 z zaadsorbowanym barwnikiem organicznym i pomiar jego charakterystyki napięcie - prąd Zakres wymaganych
OGNIWO SŁONECZNE Cel ćwiczenia Budowa nanokrystalicznego ogniwa słonecznego półprzewodnikowego TiO2 z zaadsorbowanym barwnikiem organicznym i pomiar jego charakterystyki napięcie - prąd Zakres wymaganych
WARSTWY KATALITYCZNE W OGNIWACH TYPU DSSC CATALYTIC LAYER IN DSSC SOLAR CELLS
 JANUSZ WALTER WARSTWY KATALITYCZNE W OGNIWACH TYPU DSSC CATALYTIC LAYER IN DSSC SOLAR CELLS Streszczenie Abstract W artykule omówiono wytwarzanie katalitycznych warstw platynowych metodą poliol, które
JANUSZ WALTER WARSTWY KATALITYCZNE W OGNIWACH TYPU DSSC CATALYTIC LAYER IN DSSC SOLAR CELLS Streszczenie Abstract W artykule omówiono wytwarzanie katalitycznych warstw platynowych metodą poliol, które
Sposób i urządzenie do odzysku materiałów krzemowych z ogniw fotowoltaicznych
 Sposób i urządzenie do odzysku materiałów krzemowych z ogniw fotowoltaicznych 5 30 Przedmiotem wynalazku jest sposób i urządzenie do kontrolowanego i automatycznego odzysku materiałów krzemowych z ogniw
Sposób i urządzenie do odzysku materiałów krzemowych z ogniw fotowoltaicznych 5 30 Przedmiotem wynalazku jest sposób i urządzenie do kontrolowanego i automatycznego odzysku materiałów krzemowych z ogniw
Cienkowarstwowe ogniwa słoneczne: przegląd materiałów, technologii i sytuacji rynkowej
 Cienkowarstwowe ogniwa słoneczne: przegląd materiałów, technologii i sytuacji rynkowej Przez ostatnie lata, rynek fotowoltaiki rozwijał się, wraz ze sprzedażą niemal zupełnie zdominowaną przez produkty
Cienkowarstwowe ogniwa słoneczne: przegląd materiałów, technologii i sytuacji rynkowej Przez ostatnie lata, rynek fotowoltaiki rozwijał się, wraz ze sprzedażą niemal zupełnie zdominowaną przez produkty
Wybrane Działy Fizyki
 Wybrane Działy Fizyki energia elektryczna i jadrowa W. D ebski 25.11.2009 Rodzaje energii energia mechaniczna energia cieplna (chemiczna) energia elektryczna energia jadrowa debski@igf.edu.pl: W5-1 WNZ
Wybrane Działy Fizyki energia elektryczna i jadrowa W. D ebski 25.11.2009 Rodzaje energii energia mechaniczna energia cieplna (chemiczna) energia elektryczna energia jadrowa debski@igf.edu.pl: W5-1 WNZ
NOWE TECHNOLOGIE w FOTOWOLTAICE
 NOWE TECHNOLOGIE w FOTOWOLTAICE Do wykorzystania mamy 46-51% energii słońca, która do nas dociera po odbiciu przez atmosferę, chmury i samą powierzchnię ziemi. W Polsce, rocznie suma energii słonecznej
NOWE TECHNOLOGIE w FOTOWOLTAICE Do wykorzystania mamy 46-51% energii słońca, która do nas dociera po odbiciu przez atmosferę, chmury i samą powierzchnię ziemi. W Polsce, rocznie suma energii słonecznej
Wykład 3 Energia słoneczna systemy PV
 WYDZIAŁ INŻYNIERII ŚRODOWISKA Odnawialne źródła energii dla budynków Wykład 3 Energia słoneczna systemy PV PV historia 1839 Edmund Becquerel odkrycie zjawiska fotowoltaicznego, pierwsze ogniwo wykonano
WYDZIAŁ INŻYNIERII ŚRODOWISKA Odnawialne źródła energii dla budynków Wykład 3 Energia słoneczna systemy PV PV historia 1839 Edmund Becquerel odkrycie zjawiska fotowoltaicznego, pierwsze ogniwo wykonano
Celem ćwiczenia jest wyznaczenie charakterystyki prądowo- napięciowej elektrolizera typu PEM,
 Ćw.2 Elektroliza wody za pomocą ogniwa paliwowego typu PEM Celem ćwiczenia jest wyznaczenie charakterystyki prądowo- napięciowej elektrolizera typu PEM, A także określenie wydajności tego urządzenia, jeśli
Ćw.2 Elektroliza wody za pomocą ogniwa paliwowego typu PEM Celem ćwiczenia jest wyznaczenie charakterystyki prądowo- napięciowej elektrolizera typu PEM, A także określenie wydajności tego urządzenia, jeśli
Elektronika Molekularna
 Elektronika Molekularna Instrukcja do ćwiczenia laboratoryjnego BARWNIKOWE OGNIWA SŁONECZNE Opracował: mgr inż. Maciej Klein Sprawdził i zatwierdził: dr hab. inż. Waldemar Stampor, prof. nadzw. PG Politechnika
Elektronika Molekularna Instrukcja do ćwiczenia laboratoryjnego BARWNIKOWE OGNIWA SŁONECZNE Opracował: mgr inż. Maciej Klein Sprawdził i zatwierdził: dr hab. inż. Waldemar Stampor, prof. nadzw. PG Politechnika
TECHNOLOGIE MATERIAŁÓW. dr inż. Anna Zielińska-Jurek Katedra Technologii Chemicznej pok. 026 Ch.A., tel
 TECHNOLOGIE MATERIAŁÓW BUDOWLANYCH dr inż. Anna Zielińska-Jurek Katedra Technologii Chemicznej pok. 026 Ch.A., tel. 58 347 29 37 e-mail: annjurek@pg.gda.pl TiO 2 właściwości i zastosowanie Ditlenek tytanu
TECHNOLOGIE MATERIAŁÓW BUDOWLANYCH dr inż. Anna Zielińska-Jurek Katedra Technologii Chemicznej pok. 026 Ch.A., tel. 58 347 29 37 e-mail: annjurek@pg.gda.pl TiO 2 właściwości i zastosowanie Ditlenek tytanu
PL 198188 B1. Instytut Chemii Przemysłowej im.prof.ignacego Mościckiego,Warszawa,PL 03.04.2006 BUP 07/06
 RZECZPOSPOLITA POLSKA (12) OPIS PATENTOWY (19) PL (11) 198188 (13) B1 (21) Numer zgłoszenia: 370289 (51) Int.Cl. C01B 33/00 (2006.01) C01B 33/18 (2006.01) Urząd Patentowy Rzeczypospolitej Polskiej (22)
RZECZPOSPOLITA POLSKA (12) OPIS PATENTOWY (19) PL (11) 198188 (13) B1 (21) Numer zgłoszenia: 370289 (51) Int.Cl. C01B 33/00 (2006.01) C01B 33/18 (2006.01) Urząd Patentowy Rzeczypospolitej Polskiej (22)
Półprzewodnikami wykorzystywanymi w fotowoltaice, w zależności od technologii, są: krzem amorficzny,
 Generacja energii elektrycznej Panele fotowoltaiczne umożliwiają produkcję energii elektrycznej dzięki tzw. efektowi fotowoltaicznemu Jest to zjawisko, które powoduje powstawanie siły elektromotorycznej
Generacja energii elektrycznej Panele fotowoltaiczne umożliwiają produkcję energii elektrycznej dzięki tzw. efektowi fotowoltaicznemu Jest to zjawisko, które powoduje powstawanie siły elektromotorycznej
wykład 6 elektorochemia
 elektorochemia Ogniwa elektrochemiczne Ogniwo elektrochemiczne składa się z dwóch elektrod będących w kontakcie z elektrolitem, który może być roztworem, cieczą lub ciałem stałym. Elektrolit wraz z zanurzona
elektorochemia Ogniwa elektrochemiczne Ogniwo elektrochemiczne składa się z dwóch elektrod będących w kontakcie z elektrolitem, który może być roztworem, cieczą lub ciałem stałym. Elektrolit wraz z zanurzona
Różne dziwne przewodniki
 Różne dziwne przewodniki czyli trzy po trzy o mechanizmach przewodzenia prądu elektrycznego Przewodniki elektronowe Metale Metale (zwane również przewodnikami) charakteryzują się tym, że elektrony ich
Różne dziwne przewodniki czyli trzy po trzy o mechanizmach przewodzenia prądu elektrycznego Przewodniki elektronowe Metale Metale (zwane również przewodnikami) charakteryzują się tym, że elektrony ich
Wykład 3 Energia słoneczna systemy PV
 WYDZIAŁ INŻYNIERII ŚRODOWISKA Odnawialne źródła energii dla budynków Wykład 3 Energia słoneczna systemy PV PV historia 1839 Edmund Becquerel odkrycie zjawiska fotowoltaicznego, pierwsze ogniwo wykonano
WYDZIAŁ INŻYNIERII ŚRODOWISKA Odnawialne źródła energii dla budynków Wykład 3 Energia słoneczna systemy PV PV historia 1839 Edmund Becquerel odkrycie zjawiska fotowoltaicznego, pierwsze ogniwo wykonano
Wykład 4 Energia słoneczna systemy PV
 WYDZIAŁ INŻYNIERII ŚRODOWISKA Odnawialne źródła energii dla budynków Wykład 4 Energia słoneczna systemy PV page 2 PV historia 1839 Edmund Becquerel odkrycie zjawiska fotowoltaicznego, pierwsze ogniwo wykonano
WYDZIAŁ INŻYNIERII ŚRODOWISKA Odnawialne źródła energii dla budynków Wykład 4 Energia słoneczna systemy PV page 2 PV historia 1839 Edmund Becquerel odkrycie zjawiska fotowoltaicznego, pierwsze ogniwo wykonano
Sposób oczyszczania wody ze ścieków fenolowych w fotokatalitycznym reaktorze przepływowym oraz wkład fotokatalityczny do reaktora przepływowego
 PL 213675 B1 RZECZPOSPOLITA POLSKA (12) OPIS PATENTOWY (19) PL (11) 213675 (13) B1 Urząd Patentowy Rzeczypospolitej Polskiej (21) Numer zgłoszenia: 382362 (22) Data zgłoszenia: 04.05.2007 (51) Int.Cl.
PL 213675 B1 RZECZPOSPOLITA POLSKA (12) OPIS PATENTOWY (19) PL (11) 213675 (13) B1 Urząd Patentowy Rzeczypospolitej Polskiej (21) Numer zgłoszenia: 382362 (22) Data zgłoszenia: 04.05.2007 (51) Int.Cl.
Podstawowe pojęcia 1
 Tomasz Lubera Półogniwo Podstawowe pojęcia 1 układ złożony z min. dwóch faz pozostających ze sobą w kontakcie, w którym w wyniku zachodzących procesów utleniania lub redukcji ustala się stan równowagi,
Tomasz Lubera Półogniwo Podstawowe pojęcia 1 układ złożony z min. dwóch faz pozostających ze sobą w kontakcie, w którym w wyniku zachodzących procesów utleniania lub redukcji ustala się stan równowagi,
Badanie ogniwa fotowoltaicznego
 Badanie ogniwa fotowoltaicznego Cel ćwiczenia Zapoznanie się z podstawowymi wiadomościami na temat ogniw fotowoltaicznych oraz wyznaczenie: zależności prądu fotoogniwa od natężenia oświetlenia, charakterystyk
Badanie ogniwa fotowoltaicznego Cel ćwiczenia Zapoznanie się z podstawowymi wiadomościami na temat ogniw fotowoltaicznych oraz wyznaczenie: zależności prądu fotoogniwa od natężenia oświetlenia, charakterystyk
BADANIA MODELOWE OGNIW SŁONECZNYCH
 POZNAN UNIVE RSITY OF TE CHNOLOGY ACADE MIC JOURNALS No 70 Electrical Engineering 2012 Bartosz CERAN* BADANIA MODELOWE OGNIW SŁONECZNYCH W artykule przedstawiono model matematyczny modułu fotowoltaicznego.
POZNAN UNIVE RSITY OF TE CHNOLOGY ACADE MIC JOURNALS No 70 Electrical Engineering 2012 Bartosz CERAN* BADANIA MODELOWE OGNIW SŁONECZNYCH W artykule przedstawiono model matematyczny modułu fotowoltaicznego.
Badanie utleniania kwasu mrówkowego na stopach trójskładnikowych Pt-Rh-Pd
 Badanie utleniania kwasu mrówkowego na stopach trójskładnikowych Pt-Rh-Pd Kamil Wróbel Pracownia Elektrochemicznych Źródeł Energii Kierownik pracy: prof. dr hab. A. Czerwiński Opiekun pracy: dr M. Chotkowski
Badanie utleniania kwasu mrówkowego na stopach trójskładnikowych Pt-Rh-Pd Kamil Wróbel Pracownia Elektrochemicznych Źródeł Energii Kierownik pracy: prof. dr hab. A. Czerwiński Opiekun pracy: dr M. Chotkowski
dr inż. Beata Brożek-Pluska SERS La boratorium La serowej
 dr inż. Beata Brożek-Pluska La boratorium La serowej Spektroskopii Molekularnej PŁ Powierzchniowo wzmocniona sp ektroskopia Ramana (Surface Enhanced Raman Spectroscopy) Cząsteczki zaadsorbowane na chropowatych
dr inż. Beata Brożek-Pluska La boratorium La serowej Spektroskopii Molekularnej PŁ Powierzchniowo wzmocniona sp ektroskopia Ramana (Surface Enhanced Raman Spectroscopy) Cząsteczki zaadsorbowane na chropowatych
Akademickie Centrum Czystej Energii. Ogniwo paliwowe
 Ogniwo paliwowe 1. Zagadnienia elektroliza, prawo Faraday a, pierwiastki galwaniczne, ogniwo paliwowe 2. Opis Główną częścią ogniwa paliwowego PEM (Proton Exchange Membrane) jest membrana złożona z katody
Ogniwo paliwowe 1. Zagadnienia elektroliza, prawo Faraday a, pierwiastki galwaniczne, ogniwo paliwowe 2. Opis Główną częścią ogniwa paliwowego PEM (Proton Exchange Membrane) jest membrana złożona z katody
Technologia ogniw paliwowych w IEn
 Technologia ogniw paliwowych w IEn Mariusz Krauz 1 Wstęp Opracowanie technologii ES-SOFC 3 Opracowanie technologii AS-SOFC 4 Podsumowanie i wnioski 1 Wstęp Rodzaje ogniw paliwowych Temperatura pracy Temperatura
Technologia ogniw paliwowych w IEn Mariusz Krauz 1 Wstęp Opracowanie technologii ES-SOFC 3 Opracowanie technologii AS-SOFC 4 Podsumowanie i wnioski 1 Wstęp Rodzaje ogniw paliwowych Temperatura pracy Temperatura
Schemat ogniwa:... Równanie reakcji:...
 Zadanie 1. Wykorzystując dane z szeregu elektrochemicznego metali napisz schemat ogniwa, w którym elektroda cynkowa pełni rolę anody. Zapisz równanie reakcji zachodzącej w półogniwie cynkowym. Schemat
Zadanie 1. Wykorzystując dane z szeregu elektrochemicznego metali napisz schemat ogniwa, w którym elektroda cynkowa pełni rolę anody. Zapisz równanie reakcji zachodzącej w półogniwie cynkowym. Schemat
LABORATORIUM FIZYKI PAŃSTWOWEJ WYŻSZEJ SZKOŁY ZAWODOWEJ W NYSIE. Ćwiczenie nr 2 Temat: Wyznaczenie współczynnika elektrochemicznego i stałej Faradaya.
 LABOATOIUM FIZYKI PAŃSTWOWEJ WYŻSZEJ SZKOŁY ZAWODOWEJ W NYSIE Ćwiczenie nr Temat: Wyznaczenie współczynnika elektrochemicznego i stałej Faradaya.. Wprowadzenie Proces rozpadu drobin związków chemicznych
LABOATOIUM FIZYKI PAŃSTWOWEJ WYŻSZEJ SZKOŁY ZAWODOWEJ W NYSIE Ćwiczenie nr Temat: Wyznaczenie współczynnika elektrochemicznego i stałej Faradaya.. Wprowadzenie Proces rozpadu drobin związków chemicznych
Ćwiczenie 2. Charakteryzacja niskotemperaturowego czujnika tlenu. (na prawach rękopisu)
 Ćwiczenie 2. Charakteryzacja niskotemperaturowego czujnika tlenu (na prawach rękopisu) W analityce procesowej istotne jest określenie stężeń rozpuszczonych w cieczach gazów. Gazy rozpuszczają się w cieczach
Ćwiczenie 2. Charakteryzacja niskotemperaturowego czujnika tlenu (na prawach rękopisu) W analityce procesowej istotne jest określenie stężeń rozpuszczonych w cieczach gazów. Gazy rozpuszczają się w cieczach
Laboratorium Ochrony przed Korozją. Ćw. 9: ANODOWE OKSYDOWANIEALUMINIUM
 Akademia Górniczo-Hutnicza im. Stanisława Staszica Wydział Inżynierii Materiałowej i Ceramiki Katedra Fizykochemii i Modelowania Procesów Laboratorium Ochrony przed Korozją Ćw. 9: ANODOWE OKSYDOWANIEALUMINIUM
Akademia Górniczo-Hutnicza im. Stanisława Staszica Wydział Inżynierii Materiałowej i Ceramiki Katedra Fizykochemii i Modelowania Procesów Laboratorium Ochrony przed Korozją Ćw. 9: ANODOWE OKSYDOWANIEALUMINIUM
Sonochemia. Schemat 1. Strefy reakcji. Rodzaje efektów sonochemicznych. Oscylujący pęcherzyk gazu. Woda w stanie nadkrytycznym?
 Schemat 1 Strefy reakcji Rodzaje efektów sonochemicznych Oscylujący pęcherzyk gazu Woda w stanie nadkrytycznym? Roztwór Znaczne gradienty ciśnienia Duże siły hydrodynamiczne Efekty mechanochemiczne Reakcje
Schemat 1 Strefy reakcji Rodzaje efektów sonochemicznych Oscylujący pęcherzyk gazu Woda w stanie nadkrytycznym? Roztwór Znaczne gradienty ciśnienia Duże siły hydrodynamiczne Efekty mechanochemiczne Reakcje
Sprawozdanie z laboratorium proekologicznych źródeł energii
 P O L I T E C H N I K A G D A Ń S K A Sprawozdanie z laboratorium proekologicznych źródeł energii Temat: Wyznaczanie charakterystyk prądowo-napięciowych modułu ogniw fotowoltaicznych i sprawności konwersji
P O L I T E C H N I K A G D A Ń S K A Sprawozdanie z laboratorium proekologicznych źródeł energii Temat: Wyznaczanie charakterystyk prądowo-napięciowych modułu ogniw fotowoltaicznych i sprawności konwersji
Badanie baterii słonecznych w zależności od natężenia światła
 POLITECHNIKA WARSZAWSKA Instytut Elektroenergetyki, Zakład Elektrowni i Gospodarki Elektroenergetycznej Przemiany energii laboratorium Ćwiczenie Badanie baterii słonecznych w zależności od natężenia światła
POLITECHNIKA WARSZAWSKA Instytut Elektroenergetyki, Zakład Elektrowni i Gospodarki Elektroenergetycznej Przemiany energii laboratorium Ćwiczenie Badanie baterii słonecznych w zależności od natężenia światła
CHP z ogniwem paliwowym Przegląd rynku
 Piotr Stawski IASE CHP z ogniwem paliwowym Przegląd rynku ENERGYREGION - Efektywny rozwój rozproszonej energetyki odnawialnej w połączeniu z konwencjonalną w regionach. Zalety gospodarki skojarzonej K.Sroka,
Piotr Stawski IASE CHP z ogniwem paliwowym Przegląd rynku ENERGYREGION - Efektywny rozwój rozproszonej energetyki odnawialnej w połączeniu z konwencjonalną w regionach. Zalety gospodarki skojarzonej K.Sroka,
Wyciskamy z cytryny... prąd elektryczny. Wpisany przez Administrator środa, 04 lipca :26 -
 Jak nazwa działu wskazuje będę tu umieszczał różne rozwiązania umożliwiające pozyskiwanie energii elektrycznej z niekonwencjonalnych źródeł. Zaczniemy od eksperymentu, który każdy może wykonać sobie w
Jak nazwa działu wskazuje będę tu umieszczał różne rozwiązania umożliwiające pozyskiwanie energii elektrycznej z niekonwencjonalnych źródeł. Zaczniemy od eksperymentu, który każdy może wykonać sobie w
Współczesne metody chromatograficzne: Chromatografia cienkowarstwowa
 Ćwiczenie 2: Chromatografia dwuwymiarowa (TLC 2D) 1. Celem ćwiczenia jest zaobserwowanie rozdziału mieszaniny aminokwasów w dwóch układach rozwijających. Aminokwasy: Asp, Cys, His, Leu, Ala, Val (1% roztwory
Ćwiczenie 2: Chromatografia dwuwymiarowa (TLC 2D) 1. Celem ćwiczenia jest zaobserwowanie rozdziału mieszaniny aminokwasów w dwóch układach rozwijających. Aminokwasy: Asp, Cys, His, Leu, Ala, Val (1% roztwory
Wrocław dn. 22 listopada 2005 roku. Temat lekcji: Elektroliza roztworów wodnych.
 Piotr Chojnacki IV rok, informatyka chemiczna Liceum Ogólnokształcące Nr I we Wrocławiu Wrocław dn. 22 listopada 2005 roku Temat lekcji: Elektroliza roztworów wodnych. Cel ogólny lekcji: Wprowadzenie pojęcia
Piotr Chojnacki IV rok, informatyka chemiczna Liceum Ogólnokształcące Nr I we Wrocławiu Wrocław dn. 22 listopada 2005 roku Temat lekcji: Elektroliza roztworów wodnych. Cel ogólny lekcji: Wprowadzenie pojęcia
INSTYTUT INŻYNIERII MATERIAŁOWEJ PŁ LABORATORIUM TECHNOLOGII POWŁOK OCHRONNYCH ĆWICZENIE 1 POWŁOKI KONWERSYJNE-TECHNOLOGIE NANOSZENIA
 INSTYTUT INŻYNIERII MATERIAŁOWEJ PŁ LABORATORIUM TECHNOLOGII POWŁOK OCHRONNYCH ĆWICZENIE 1 POWŁOKI KONWERSYJNE-TECHNOLOGIE NANOSZENIA WSTĘP TEORETYCZNY Powłoki konwersyjne tworzą się na powierzchni metalu
INSTYTUT INŻYNIERII MATERIAŁOWEJ PŁ LABORATORIUM TECHNOLOGII POWŁOK OCHRONNYCH ĆWICZENIE 1 POWŁOKI KONWERSYJNE-TECHNOLOGIE NANOSZENIA WSTĘP TEORETYCZNY Powłoki konwersyjne tworzą się na powierzchni metalu
Badanie zależności energii generowanej w panelach fotowoltaicznych od natężenia promieniowania słonecznego
 POLITECHNIKA BIAŁOSTOCKA Wydział Budownictwa i Inżynierii Środowiska Instrukcja do zajęć laboratoryjnych fotowoltaicznych od natężenia promieniowania słonecznego Ćwiczenie nr 10 Laboratorium z przedmiotu
POLITECHNIKA BIAŁOSTOCKA Wydział Budownictwa i Inżynierii Środowiska Instrukcja do zajęć laboratoryjnych fotowoltaicznych od natężenia promieniowania słonecznego Ćwiczenie nr 10 Laboratorium z przedmiotu
Fotowoltaika i sensory w proekologicznym rozwoju Małopolski
 Fotowoltaika i sensory w proekologicznym rozwoju Małopolski Photovoltaic and Sensors in Environmental Development of Malopolska Region ZWIĘKSZANIE WYDAJNOŚCI SYSTEMÓW FOTOWOLTAICZNYCH Plan prezentacji
Fotowoltaika i sensory w proekologicznym rozwoju Małopolski Photovoltaic and Sensors in Environmental Development of Malopolska Region ZWIĘKSZANIE WYDAJNOŚCI SYSTEMÓW FOTOWOLTAICZNYCH Plan prezentacji
Karta pracy III/1a Elektrochemia: ogniwa galwaniczne
 Karta pracy III/1a Elektrochemia: ogniwa galwaniczne I. Elektroda, półogniwo, ogniowo Elektroda przewodnik elektryczny (blaszka metalowa lub pręcik grafitowy) który ma być zanurzony w roztworze elektrolitu
Karta pracy III/1a Elektrochemia: ogniwa galwaniczne I. Elektroda, półogniwo, ogniowo Elektroda przewodnik elektryczny (blaszka metalowa lub pręcik grafitowy) który ma być zanurzony w roztworze elektrolitu
Ogniwa fotowoltaiczne wykorzystanie w OZE
 Ogniwa fotowoltaiczne wykorzystanie w OZE Fizyka IV Michał Trojgo, gr 1.3 Energia Słońca Do górnych warstw atmosfery Ziemi dociera promieniowanie słoneczne o natężeniu napromieniowania 1366,1 W/m². Oznacza
Ogniwa fotowoltaiczne wykorzystanie w OZE Fizyka IV Michał Trojgo, gr 1.3 Energia Słońca Do górnych warstw atmosfery Ziemi dociera promieniowanie słoneczne o natężeniu napromieniowania 1366,1 W/m². Oznacza
Ogniwo paliwowe typu PEM (ang. PEM-FC)
 OPRACOWALI: MGR INŻ. JAKUB DŁUGOSZ MGR INŻ. MARCIN MICHALSKI OGNIWA PALIWOWE I PRODUKCJA WODORU LABORATORIUM I- ZASADA DZIAŁANIA SYSTEMU OGNIW PALIWOWYCH TYPU PEM NA PRZYKŁADZIE SYSTEMU NEXA 1,2 kw II-
OPRACOWALI: MGR INŻ. JAKUB DŁUGOSZ MGR INŻ. MARCIN MICHALSKI OGNIWA PALIWOWE I PRODUKCJA WODORU LABORATORIUM I- ZASADA DZIAŁANIA SYSTEMU OGNIW PALIWOWYCH TYPU PEM NA PRZYKŁADZIE SYSTEMU NEXA 1,2 kw II-
K, Na, Ca, Mg, Al, Zn, Fe, Sn, Pb, H, Cu, Ag, Hg, Pt, Au
 WSTĘP DO ELEKTROCHEMII (opracowanie dr Katarzyna Makyła-Juzak Elektrochemia jest działem chemii fizycznej, który zajmuje się zarówno reakcjami chemicznymi stanowiącymi źródło prądu elektrycznego (ogniwa
WSTĘP DO ELEKTROCHEMII (opracowanie dr Katarzyna Makyła-Juzak Elektrochemia jest działem chemii fizycznej, który zajmuje się zarówno reakcjami chemicznymi stanowiącymi źródło prądu elektrycznego (ogniwa
PL B1. Akademia Górniczo-Hutnicza im. Stanisława Staszica,Kraków,PL BUP 14/02. Irena Harańczyk,Kraków,PL Stanisława Gacek,Kraków,PL
 RZECZPOSPOLITA POLSKA (12) OPIS PATENTOWY (19)PL (11)195686 (13) B1 Urząd Patentowy Rzeczypospolitej Polskiej (21) Numer zgłoszenia: 344720 (22) Data zgłoszenia: 19.12.2000 (51) Int.Cl. B22F 9/18 (2006.01)
RZECZPOSPOLITA POLSKA (12) OPIS PATENTOWY (19)PL (11)195686 (13) B1 Urząd Patentowy Rzeczypospolitej Polskiej (21) Numer zgłoszenia: 344720 (22) Data zgłoszenia: 19.12.2000 (51) Int.Cl. B22F 9/18 (2006.01)
Powstawanie żelazianu(vi) sodu przebiega zgodnie z równaniem: Ponieważ termiczny rozkład kwasu borowego(iii) zachodzi zgodnie z równaniem:
 Zad. 1 Ponieważ reakcja jest egzoenergetyczna (ujemne ciepło reakcji) to wzrost temperatury spowoduje przesunięcie równowagi w lewo, zatem mieszanina przyjmie intensywniejszą barwę. Układ będzie przeciwdziałał
Zad. 1 Ponieważ reakcja jest egzoenergetyczna (ujemne ciepło reakcji) to wzrost temperatury spowoduje przesunięcie równowagi w lewo, zatem mieszanina przyjmie intensywniejszą barwę. Układ będzie przeciwdziałał
ZASTOSOWANIE WYBRANYCH BARWNIKÓW ORGANICZNYCH W BARWNIKOWYCH OGNIWACH SŁONECZNYCH
 CZASOPISMO INŻYNIERII LĄDOWEJ, ŚRODOWISKA I ARCHITEKTURY JOURNAL OF CIVIL ENGINEERING, ENVIRONMENT AND ARCHITECTURE JCEEA, t. XXXIII, z. 63 (3/16), lipiec-wrzesień 2016, s. 413-420 Karolina SIEDLISKA 1
CZASOPISMO INŻYNIERII LĄDOWEJ, ŚRODOWISKA I ARCHITEKTURY JOURNAL OF CIVIL ENGINEERING, ENVIRONMENT AND ARCHITECTURE JCEEA, t. XXXIII, z. 63 (3/16), lipiec-wrzesień 2016, s. 413-420 Karolina SIEDLISKA 1
Recykling surowcowy odpadowego PET (politereftalanu etylenu)
 Laboratorium: Powstawanie i utylizacja zanieczyszczeń i odpadów Makrokierunek Zarządzanie Środowiskiem INSTRUKCJA DO ĆWICZENIA 24 Recykling surowcowy odpadowego PET (politereftalanu etylenu) 1 I. Cel ćwiczenia
Laboratorium: Powstawanie i utylizacja zanieczyszczeń i odpadów Makrokierunek Zarządzanie Środowiskiem INSTRUKCJA DO ĆWICZENIA 24 Recykling surowcowy odpadowego PET (politereftalanu etylenu) 1 I. Cel ćwiczenia
Program Wydziałowej Konferencji Sprawozdawczej w dniach lutego 2013r. 11 lutego 2013 r.
 Wydział Chemii UMCS Program Wydziałowej Konferencji Sprawozdawczej w dniach 11-12 lutego 2013r. 9 00 9 10 Otwarcie 11 lutego 2013 r. Sesja I Przewodniczący prof. dr hab. Mieczysław Korolczuk 9 10-9 30
Wydział Chemii UMCS Program Wydziałowej Konferencji Sprawozdawczej w dniach 11-12 lutego 2013r. 9 00 9 10 Otwarcie 11 lutego 2013 r. Sesja I Przewodniczący prof. dr hab. Mieczysław Korolczuk 9 10-9 30
Zadanie 2. (0 1) Uzupełnij schemat reakcji estryfikacji. Wybierz spośród podanych wzór kwasu karboksylowego A albo B oraz wzór alkoholu 1 albo 2.
 Zadanie 1. (0 1) W celu odróżnienia kwasu oleinowego od stopionego kwasu palmitynowego wykonano doświadczenie, którego przebieg przedstawiono na schemacie. W probówce I wybrany odczynnik zmienił zabarwienie.
Zadanie 1. (0 1) W celu odróżnienia kwasu oleinowego od stopionego kwasu palmitynowego wykonano doświadczenie, którego przebieg przedstawiono na schemacie. W probówce I wybrany odczynnik zmienił zabarwienie.
PL B1 AKADEMIA GÓRNICZO-HUTNICZA IM. STANISŁAWA STASZICA, KRAKÓW, PL BUP 08/07
 RZECZPOSPOLITA POLSKA (12) OPIS PATENTOWY (19) PL (11) 205765 (13) B1 (21) Numer zgłoszenia: 377546 (51) Int.Cl. C25B 1/00 (2006.01) C01G 5/00 (2006.01) Urząd Patentowy Rzeczypospolitej Polskiej (22) Data
RZECZPOSPOLITA POLSKA (12) OPIS PATENTOWY (19) PL (11) 205765 (13) B1 (21) Numer zgłoszenia: 377546 (51) Int.Cl. C25B 1/00 (2006.01) C01G 5/00 (2006.01) Urząd Patentowy Rzeczypospolitej Polskiej (22) Data
Obwody prądu stałego. Materiały dydaktyczne dla kierunku Technik Optyk (W12)Kwalifikacyjnego kursu zawodowego.
 Obwody prądu stałego Materiały dydaktyczne dla kierunku Technik Optyk (W12)Kwalifikacyjnego kursu zawodowego. Podstawowe prawa elektrotechniki w zastosowaniu do obwodów elektrycznych: Obwód elektryczny
Obwody prądu stałego Materiały dydaktyczne dla kierunku Technik Optyk (W12)Kwalifikacyjnego kursu zawodowego. Podstawowe prawa elektrotechniki w zastosowaniu do obwodów elektrycznych: Obwód elektryczny
Laboratorium Ochrony przed Korozją. GALWANOTECHNIKA II Ćw. 6: ANODOWE OKSYDOWANIE ALUMINIUM
 Akademia Górniczo-Hutnicza im. Stanisława Staszica Wydział Inżynierii Materiałowej i Ceramiki Katedra Fizykochemii i Modelowania Procesów Laboratorium Ochrony przed Korozją GALWANOTECHNIKA II Ćw. 6: ANODOWE
Akademia Górniczo-Hutnicza im. Stanisława Staszica Wydział Inżynierii Materiałowej i Ceramiki Katedra Fizykochemii i Modelowania Procesów Laboratorium Ochrony przed Korozją GALWANOTECHNIKA II Ćw. 6: ANODOWE
Rekapitulacja. Detekcja światła. Rekapitulacja. Rekapitulacja
 Rekapitulacja Detekcja światła Sebastian Maćkowski Instytut Fizyki Uniwersytet Mikołaja Kopernika Adres poczty elektronicznej: mackowski@fizyka.umk.pl Biuro: 365, telefon: 611-3250 Konsultacje: czwartek
Rekapitulacja Detekcja światła Sebastian Maćkowski Instytut Fizyki Uniwersytet Mikołaja Kopernika Adres poczty elektronicznej: mackowski@fizyka.umk.pl Biuro: 365, telefon: 611-3250 Konsultacje: czwartek
Grafen perspektywy zastosowań
 Grafen perspektywy zastosowań Paweł Szroeder 3 czerwca 2014 Spis treści 1 Wprowadzenie 1 2 Właściwości grafenu 2 3 Perspektywy zastosowań 2 3.1 Procesory... 2 3.2 Analogoweelementy... 3 3.3 Czujniki...
Grafen perspektywy zastosowań Paweł Szroeder 3 czerwca 2014 Spis treści 1 Wprowadzenie 1 2 Właściwości grafenu 2 3 Perspektywy zastosowań 2 3.1 Procesory... 2 3.2 Analogoweelementy... 3 3.3 Czujniki...
Elektrochemia - szereg elektrochemiczny metali. Zadania
 Elektrochemia - szereg elektrochemiczny metali Zadania Czym jest szereg elektrochemiczny metali? Szereg elektrochemiczny metali jest to zestawienie metali według wzrastających potencjałów normalnych. Wartości
Elektrochemia - szereg elektrochemiczny metali Zadania Czym jest szereg elektrochemiczny metali? Szereg elektrochemiczny metali jest to zestawienie metali według wzrastających potencjałów normalnych. Wartości
ARKUSZ 1 POWTÓRZENIE DO EGZAMINU Z CHEMII
 ARKUSZ 1 POWTÓRZENIE DO EGZAMINU Z CHEMII Zadanie 1. Na rysunku przedstawiono fragment układu okresowego pierwiastków. Dokoocz zdania tak aby były prawdziwe. Wiązanie jonowe występuje w związku chemicznym
ARKUSZ 1 POWTÓRZENIE DO EGZAMINU Z CHEMII Zadanie 1. Na rysunku przedstawiono fragment układu okresowego pierwiastków. Dokoocz zdania tak aby były prawdziwe. Wiązanie jonowe występuje w związku chemicznym
Dioda półprzewodnikowa OPRACOWANIE: MGR INŻ. EWA LOREK
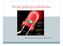 Dioda półprzewodnikowa OPRACOWANIE: MGR INŻ. EWA LOREK Budowa diody Dioda zbudowana jest z dwóch warstw półprzewodników: półprzewodnika typu n (nośnikami prądu elektrycznego są elektrony) i półprzewodnika
Dioda półprzewodnikowa OPRACOWANIE: MGR INŻ. EWA LOREK Budowa diody Dioda zbudowana jest z dwóch warstw półprzewodników: półprzewodnika typu n (nośnikami prądu elektrycznego są elektrony) i półprzewodnika
DYREKTYWA KOMISJI 2011/3/UE
 18.1.2011 Dziennik Urzędowy Unii Europejskiej L 13/59 DYREKTYWY DYREKTYWA KOMISJI 2011/3/UE z dnia 17 stycznia 2011 r. zmieniająca dyrektywę 2008/128/WE ustanawiającą szczególne kryteria czystości dotyczące
18.1.2011 Dziennik Urzędowy Unii Europejskiej L 13/59 DYREKTYWY DYREKTYWA KOMISJI 2011/3/UE z dnia 17 stycznia 2011 r. zmieniająca dyrektywę 2008/128/WE ustanawiającą szczególne kryteria czystości dotyczące
Ogniwa fotowoltaiczne
 Ogniwa fotowoltaiczne Efekt fotowoltaiczny: Ogniwo słoneczne Symulacja http://www.redarc.com.au/solar/about/solarpanels/ Historia 1839: Odkrycie efektu fotowoltaicznego przez francuza Alexandre-Edmond
Ogniwa fotowoltaiczne Efekt fotowoltaiczny: Ogniwo słoneczne Symulacja http://www.redarc.com.au/solar/about/solarpanels/ Historia 1839: Odkrycie efektu fotowoltaicznego przez francuza Alexandre-Edmond
X / \ Y Y Y Z / \ W W ... imię i nazwisko,nazwa szkoły, miasto
 Zadanie 1. (3 pkt) Nadtlenek litu (Li 2 O 2 ) jest ciałem stałym, występującym w temperaturze pokojowej w postaci białych kryształów. Stosowany jest w oczyszczaczach powietrza, gdzie ważna jest waga użytego
Zadanie 1. (3 pkt) Nadtlenek litu (Li 2 O 2 ) jest ciałem stałym, występującym w temperaturze pokojowej w postaci białych kryształów. Stosowany jest w oczyszczaczach powietrza, gdzie ważna jest waga użytego
Materiały w bateriach litowych.
 Materiały w bateriach litowych. Dlaczego lit? 1. Pierwiastek najbardziej elektrododatni ( pot. 3.04V wobec standardowej elektrody wodorowej ). 2. Najlżejszy metal ( d = 0.53 g/cm 3 ). 3. Gwarantuje wysoką
Materiały w bateriach litowych. Dlaczego lit? 1. Pierwiastek najbardziej elektrododatni ( pot. 3.04V wobec standardowej elektrody wodorowej ). 2. Najlżejszy metal ( d = 0.53 g/cm 3 ). 3. Gwarantuje wysoką
Najbardziej rozpowszechniony pierwiastek we Wszechświecie, Stanowi główny składnik budujący gwiazdy,
 Położenie pierwiastka w UKŁADZIE OKRESOWYM Nazwa Nazwa łacińska Symbol Liczba atomowa 1 Wodór Hydrogenium Masa atomowa 1,00794 Temperatura topnienia -259,2 C Temperatura wrzenia -252,2 C Gęstość H 0,08988
Położenie pierwiastka w UKŁADZIE OKRESOWYM Nazwa Nazwa łacińska Symbol Liczba atomowa 1 Wodór Hydrogenium Masa atomowa 1,00794 Temperatura topnienia -259,2 C Temperatura wrzenia -252,2 C Gęstość H 0,08988
Chemia jesienią. Profil chemiczny spotkanie II. mgr Ewelina Zielińska
 Chemia jesienią Profil chemiczny spotkanie II mgr Ewelina Zielińska Barwniki roślinne Do barwienia tkanin i innych przedmiotów codziennego użytku stosowane były już około 4000 lat p.n.e. w Chinach, Indiach
Chemia jesienią Profil chemiczny spotkanie II mgr Ewelina Zielińska Barwniki roślinne Do barwienia tkanin i innych przedmiotów codziennego użytku stosowane były już około 4000 lat p.n.e. w Chinach, Indiach
Laboratorium z Elektrochemii Ciała Stałego
 Laboratorium z Elektrochemii Ciała Stałego Ćwiczenie nr 1 Nanokrystaliczne ogniwa słoneczne Spis treści 1. Cel ćwiczenia... 2 2. Widmo elektromagnetyczne... 2 3. Odziaływanie materii ze światłem... 3 4.
Laboratorium z Elektrochemii Ciała Stałego Ćwiczenie nr 1 Nanokrystaliczne ogniwa słoneczne Spis treści 1. Cel ćwiczenia... 2 2. Widmo elektromagnetyczne... 2 3. Odziaływanie materii ze światłem... 3 4.
Organiczne ogniwa słonecznes. Ogniwa półprzewodnikowe. p przewodnikowe zasada ania. Charakterystyki fotoogniwa
 j Elektronika plastikowa i organiczna Organiczne ogniwa słonecznes Ogniwa półprzewodnikowe p przewodnikowe zasada działania ania Charakterystyki fotoogniwa współczynnik wypełnienia, wydajność Moc w obwodzie
j Elektronika plastikowa i organiczna Organiczne ogniwa słonecznes Ogniwa półprzewodnikowe p przewodnikowe zasada działania ania Charakterystyki fotoogniwa współczynnik wypełnienia, wydajność Moc w obwodzie
Test kompetencji z chemii do liceum. Grupa A.
 Test kompetencji z chemii do liceum. Grupa A. 1. Atomy to: A- niepodzielne cząstki pierwiastka B- ujemne cząstki materii C- dodatnie cząstki materii D- najmniejsze cząstki pierwiastka, zachowujące jego
Test kompetencji z chemii do liceum. Grupa A. 1. Atomy to: A- niepodzielne cząstki pierwiastka B- ujemne cząstki materii C- dodatnie cząstki materii D- najmniejsze cząstki pierwiastka, zachowujące jego
Wykład 5 Fotodetektory, ogniwa słoneczne
 Wykład 5 Fotodetektory, ogniwa słoneczne 1 Generacja optyczna swobodnych nośników Fotoprzewodnictwo σ=e(µ e n+µ h p) Fotodioda optyczna generacja par elektron-dziura pole elektryczne złącza rozdziela parę
Wykład 5 Fotodetektory, ogniwa słoneczne 1 Generacja optyczna swobodnych nośników Fotoprzewodnictwo σ=e(µ e n+µ h p) Fotodioda optyczna generacja par elektron-dziura pole elektryczne złącza rozdziela parę
WPŁYW POSTĘPU TECHNICZNEGO NA WYDAJNOŚĆ SYSTEMÓW FOTOWOLTAICZNYCH ML SYSTEM S.A.
 WPŁYW POSTĘPU TECHNICZNEGO NA WYDAJNOŚĆ SYSTEMÓW FOTOWOLTAICZNYCH ML SYSTEM S.A. Anna Warzybok Z-ca Dyrektora ds. Badań i Rozwoju ML SYSTEM S. A. Rzeszów, 25.04.2017 ML SYSTEM S.A. ML SYSTEM S.A. ZAPOTRZEBOWANIE
WPŁYW POSTĘPU TECHNICZNEGO NA WYDAJNOŚĆ SYSTEMÓW FOTOWOLTAICZNYCH ML SYSTEM S.A. Anna Warzybok Z-ca Dyrektora ds. Badań i Rozwoju ML SYSTEM S. A. Rzeszów, 25.04.2017 ML SYSTEM S.A. ML SYSTEM S.A. ZAPOTRZEBOWANIE
ĆWICZENIE I - BIAŁKA. Celem ćwiczenia jest zapoznanie się z właściwościami fizykochemicznymi białek i ich reakcjami charakterystycznymi.
 ĆWICZENIE I - BIAŁKA Celem ćwiczenia jest zapoznanie się z właściwościami fizykochemicznymi białek i ich reakcjami charakterystycznymi. Odczynniki: - wodny 1% roztwór siarczanu(vi) miedzi(ii), - 10% wodny
ĆWICZENIE I - BIAŁKA Celem ćwiczenia jest zapoznanie się z właściwościami fizykochemicznymi białek i ich reakcjami charakterystycznymi. Odczynniki: - wodny 1% roztwór siarczanu(vi) miedzi(ii), - 10% wodny
Fascynujący świat chemii
 Opracowanie pochodzi ze strony www.materiaienergia.pisz.pl Zeskakuj telefonem kod QR i odwiedź nas w Internecie Fascynujący świat chemii Szybkość reakcji chemicznych i katalizatory Wstęp Celem prowadzenia
Opracowanie pochodzi ze strony www.materiaienergia.pisz.pl Zeskakuj telefonem kod QR i odwiedź nas w Internecie Fascynujący świat chemii Szybkość reakcji chemicznych i katalizatory Wstęp Celem prowadzenia
Materiały elektrodowe
 Materiały elektrodowe Potencjał (względem drugiej elektrody): różnica potencjałów pomiędzy elektrodami określa napięcie możliwe do uzyskania w ogniwie. Wpływa na ilość energii zgromadzonej w ogniwie. Pojemność
Materiały elektrodowe Potencjał (względem drugiej elektrody): różnica potencjałów pomiędzy elektrodami określa napięcie możliwe do uzyskania w ogniwie. Wpływa na ilość energii zgromadzonej w ogniwie. Pojemność
BARWNIKOWE OGNIWA SŁONECZNE
 BARWNIKOWE OGNIWA SŁONECZNE Dye-sensitized solar cell (DSSC, DSC) Katarzyna Anna Bialecka Fraunhofer-Institut für Solare Energiesysteme ISE II Warsztaty Organicznej Drukowanej i Elastycznej Elektroniki
BARWNIKOWE OGNIWA SŁONECZNE Dye-sensitized solar cell (DSSC, DSC) Katarzyna Anna Bialecka Fraunhofer-Institut für Solare Energiesysteme ISE II Warsztaty Organicznej Drukowanej i Elastycznej Elektroniki
PL 215770 B1. POLITECHNIKA GDAŃSKA, Gdańsk, PL 23.05.2011 BUP 11/11
 PL 215770 B1 RZECZPOSPOLITA POLSKA (12) OPIS PATENTOWY (19) PL (11) 215770 (13) B1 Urząd Patentowy Rzeczypospolitej Polskiej (21) Numer zgłoszenia: 389528 (22) Data zgłoszenia: 10.11.2009 (51) Int.Cl.
PL 215770 B1 RZECZPOSPOLITA POLSKA (12) OPIS PATENTOWY (19) PL (11) 215770 (13) B1 Urząd Patentowy Rzeczypospolitej Polskiej (21) Numer zgłoszenia: 389528 (22) Data zgłoszenia: 10.11.2009 (51) Int.Cl.
PL B1. Symetryczne czwartorzędowe sole imidazoliowe, pochodne achiralnego alkoholu monoterpenowego oraz sposób ich wytwarzania
 PL 215465 B1 RZECZPOSPOLITA POLSKA (12) OPIS PATENTOWY (19) PL (11) 215465 (13) B1 (21) Numer zgłoszenia: 398943 (51) Int.Cl. C07D 233/60 (2006.01) C07C 31/135 (2006.01) Urząd Patentowy Rzeczypospolitej
PL 215465 B1 RZECZPOSPOLITA POLSKA (12) OPIS PATENTOWY (19) PL (11) 215465 (13) B1 (21) Numer zgłoszenia: 398943 (51) Int.Cl. C07D 233/60 (2006.01) C07C 31/135 (2006.01) Urząd Patentowy Rzeczypospolitej
Szanowne koleżanki i koledzy nauczyciele chemii!
 Szanowne koleżanki i koledzy nauczyciele chemii! Chciałabym podzielić się z Wami moimi spostrzeżeniami dotyczącymi poziomu wiedzy z chemii uczniów rozpoczynających naukę w Liceum Ogólnokształcącym. Co
Szanowne koleżanki i koledzy nauczyciele chemii! Chciałabym podzielić się z Wami moimi spostrzeżeniami dotyczącymi poziomu wiedzy z chemii uczniów rozpoczynających naukę w Liceum Ogólnokształcącym. Co
POLITECHNIKA WARSZAWSKA WYDZIAŁ ELEKTRYCZNY. PRACOWNIA MATERIAŁOZNAWSTWA ELEKTROTECHNICZNEGO KWNiAE
 POLITECHNIK WRSZWSK WYDZIŁ ELEKTRYCZNY PRCOWNI MTERIŁOZNWSTW ELEKTROTECHNICZNEGO KWNiE ĆWICZENIE 11 WYZNCZNIE ELEKTROCHEMICZNEGO RÓWNOWśNIK MIEDZI ORZ STŁEJ FRDY 1. Elektrolity i przewodnictwo jonowe Ogólnie
POLITECHNIK WRSZWSK WYDZIŁ ELEKTRYCZNY PRCOWNI MTERIŁOZNWSTW ELEKTROTECHNICZNEGO KWNiE ĆWICZENIE 11 WYZNCZNIE ELEKTROCHEMICZNEGO RÓWNOWśNIK MIEDZI ORZ STŁEJ FRDY 1. Elektrolity i przewodnictwo jonowe Ogólnie
Wykład 5 Fotodetektory, ogniwa słoneczne
 Wykład 5 Fotodetektory, ogniwa słoneczne 1 Generacja optyczna swobodnych nośników Fotoprzewodnictwo σ=e(µ e n+µ h p) Fotodioda optyczna generacja par elektron-dziura pole elektryczne złącza rozdziela parę
Wykład 5 Fotodetektory, ogniwa słoneczne 1 Generacja optyczna swobodnych nośników Fotoprzewodnictwo σ=e(µ e n+µ h p) Fotodioda optyczna generacja par elektron-dziura pole elektryczne złącza rozdziela parę
Przetwarzanie energii: kondensatory
 Przetwarzanie energii: kondensatory Ładując kondensator wykonujemy pracę nad ładunkiem. Przetwarzanie energii: ogniwa paliwowe W ogniwach paliwowych następuje elektrochemiczne spalanie paliwa. Energia
Przetwarzanie energii: kondensatory Ładując kondensator wykonujemy pracę nad ładunkiem. Przetwarzanie energii: ogniwa paliwowe W ogniwach paliwowych następuje elektrochemiczne spalanie paliwa. Energia
ZWIĄZKI WĘGLA Z WODOREM 1) Uzupełnij i uzgodnij równania reakcji spalania całkowitego alkanów, alkenów i alkinów.
 Nauczanie domowe WIEM, CO TRZEBA Klasa VIII Chemia od listopada do czerwca aktualizacja 05.10.2018 ZWIĄZKI WĘGLA Z WODOREM 1) Uzupełnij i uzgodnij równania reakcji spalania całkowitego alkanów, alkenów
Nauczanie domowe WIEM, CO TRZEBA Klasa VIII Chemia od listopada do czerwca aktualizacja 05.10.2018 ZWIĄZKI WĘGLA Z WODOREM 1) Uzupełnij i uzgodnij równania reakcji spalania całkowitego alkanów, alkenów
Materiały katodowe dla ogniw Li-ion wybrane zagadnienia
 Materiały katodowe dla ogniw Li-ion wybrane zagadnienia Szeroki zakres interkalacji y, a więc duża dopuszczalna zmiana zawartości litu w materiale, która powinna zachodzić przy minimalnych zaburzeniach
Materiały katodowe dla ogniw Li-ion wybrane zagadnienia Szeroki zakres interkalacji y, a więc duża dopuszczalna zmiana zawartości litu w materiale, która powinna zachodzić przy minimalnych zaburzeniach
PODSTAWY KOROZJI ELEKTROCHEMICZNEJ
 PODSTAWY KOROZJI ELEKTROCHEMICZNEJ PODZIAŁ KOROZJI ZE WZGLĘDU NA MECHANIZM Korozja elektrochemiczna zachodzi w środowiskach wilgotnych, w wodzie i roztworach wodnych, w glebie, w wilgotnej atmosferze oraz
PODSTAWY KOROZJI ELEKTROCHEMICZNEJ PODZIAŁ KOROZJI ZE WZGLĘDU NA MECHANIZM Korozja elektrochemiczna zachodzi w środowiskach wilgotnych, w wodzie i roztworach wodnych, w glebie, w wilgotnej atmosferze oraz
Repetytorium z wybranych zagadnień z chemii
 Repetytorium z wybranych zagadnień z chemii Mol jest to liczebność materii występująca, gdy liczba cząstek (elementów) układu jest równa liczbie atomów zawartych w masie 12 g węgla 12 C (równa liczbie
Repetytorium z wybranych zagadnień z chemii Mol jest to liczebność materii występująca, gdy liczba cząstek (elementów) układu jest równa liczbie atomów zawartych w masie 12 g węgla 12 C (równa liczbie
EUROPEJSKIE SŁONECZNE DNI ENERGIA SŁOŃCA FOTOWOLTAIKA TECHNOLOGIE, OPŁACALNOSĆ, REALIZACJE Olsztyn 9 MAJA 2013 R.
 EUROPEJSKIE SŁONECZNE DNI ENERGIA SŁOŃCA FOTOWOLTAIKA TECHNOLOGIE, OPŁACALNOSĆ, REALIZACJE Olsztyn 9 MAJA 2013 R. Fotowoltaika - stan obecny oraz kierunki rozwoju w Polsce oraz UE Adam Cenian IMP PAN Słońce
EUROPEJSKIE SŁONECZNE DNI ENERGIA SŁOŃCA FOTOWOLTAIKA TECHNOLOGIE, OPŁACALNOSĆ, REALIZACJE Olsztyn 9 MAJA 2013 R. Fotowoltaika - stan obecny oraz kierunki rozwoju w Polsce oraz UE Adam Cenian IMP PAN Słońce
Budowa i zasada działania akumulatora
 Budowa i zasada działania akumulatora Źródło https://neomax.pl/akumulator-world-batt-12v44ah-wbs02-03.html Źródło https://www.tayna.co.uk/industrial-batteries/sonnenschein/a602-1000/ 1 Akumulator elektryczny
Budowa i zasada działania akumulatora Źródło https://neomax.pl/akumulator-world-batt-12v44ah-wbs02-03.html Źródło https://www.tayna.co.uk/industrial-batteries/sonnenschein/a602-1000/ 1 Akumulator elektryczny
L E D light emitting diode
 Elektrotechnika Studia niestacjonarne L E D light emitting diode Wg PN-90/E-01005. Technika świetlna. Terminologia. (845-04-40) Dioda elektroluminescencyjna; dioda świecąca; LED element półprzewodnikowy
Elektrotechnika Studia niestacjonarne L E D light emitting diode Wg PN-90/E-01005. Technika świetlna. Terminologia. (845-04-40) Dioda elektroluminescencyjna; dioda świecąca; LED element półprzewodnikowy
E12. Wyznaczanie parametrów użytkowych fotoogniwa
 1/5 E12. Wyznaczanie parametrów użytkowych fotoogniwa Celem ćwiczenia jest poznanie podstaw zjawiska konwersji energii świetlnej na elektryczną, zasad działania fotoogniwa oraz wyznaczenie jego podstawowych
1/5 E12. Wyznaczanie parametrów użytkowych fotoogniwa Celem ćwiczenia jest poznanie podstaw zjawiska konwersji energii świetlnej na elektryczną, zasad działania fotoogniwa oraz wyznaczenie jego podstawowych
Fotoelementy. Symbole graficzne półprzewodnikowych elementów optoelektronicznych: a) fotoogniwo b) fotorezystor
 Fotoelementy Wstęp W wielu dziedzinach techniki zachodzi potrzeba rejestracji, wykrywania i pomiaru natężenia promieniowania elektromagnetycznego o różnych długościach fal, w tym i promieniowania widzialnego,
Fotoelementy Wstęp W wielu dziedzinach techniki zachodzi potrzeba rejestracji, wykrywania i pomiaru natężenia promieniowania elektromagnetycznego o różnych długościach fal, w tym i promieniowania widzialnego,
Przetwarzanie energii: kondensatory
 Przetwarzanie energii: kondensatory Ładując kondensator wykonujemy pracę nad ładunkiem. Przetwarzanie energii: ogniwa paliwowe W ogniwach paliwowych następuje elektrochemiczne spalanie paliwa. Energia
Przetwarzanie energii: kondensatory Ładując kondensator wykonujemy pracę nad ładunkiem. Przetwarzanie energii: ogniwa paliwowe W ogniwach paliwowych następuje elektrochemiczne spalanie paliwa. Energia
metody nanoszenia katalizatorów na struktury Metalowe
 metody nanoszenia katalizatorów na struktury Metalowe mgr inż. Ewelina Piwowarczyk Uniwersytet Jagielloński Wydział Chemii 1 Metody nanoszenia katalizatorów na struktury Metalowe Katalizatory na nośniku
metody nanoszenia katalizatorów na struktury Metalowe mgr inż. Ewelina Piwowarczyk Uniwersytet Jagielloński Wydział Chemii 1 Metody nanoszenia katalizatorów na struktury Metalowe Katalizatory na nośniku
1. za pomocą pomiaru SEM (siła elektromotoryczna róŝnica potencjałów dwóch elektrod) i na podstawie wzoru wyznaczenie stęŝenia,
 Potencjometria Potencjometria instrumentalna metoda analityczna, wykorzystująca zaleŝność pomiędzy potencjałem elektrody wzorcowej, a aktywnością jonów lub cząstek w badanym roztworze (elektrody wskaźnikowej).
Potencjometria Potencjometria instrumentalna metoda analityczna, wykorzystująca zaleŝność pomiędzy potencjałem elektrody wzorcowej, a aktywnością jonów lub cząstek w badanym roztworze (elektrody wskaźnikowej).
wodny roztwór chlorku cyny (SnCl 2 ) stężony kwas solny (HCl), dwie elektrody: pręcik cynowy i gwóźdź stalowy, źródło prądu stałego (zasilacz).
 21.03.2018 Do doświadczenia użyto: wodny roztwór chlorku cyny (SnCl 2 ) stężony kwas solny (HCl), dwie elektrody: pręcik cynowy i gwóźdź stalowy, źródło prądu stałego (zasilacz). Do naczynia wlano roztwór
21.03.2018 Do doświadczenia użyto: wodny roztwór chlorku cyny (SnCl 2 ) stężony kwas solny (HCl), dwie elektrody: pręcik cynowy i gwóźdź stalowy, źródło prądu stałego (zasilacz). Do naczynia wlano roztwór
XX KONKURS CHEMICZNY KLAS TRZECICH GIMNAZJALNYCH ROK SZKOLNY 2012/2013
 IMIĘ I NAZWISKO PUNKTACJA SZKOŁA KLASA NAZWISKO NAUCZYCIELA CHEMII I LICEUM OGÓLNOKSZTAŁCĄCE Inowrocław 25 maja 2013 Im. Jana Kasprowicza INOWROCŁAW XX KONKURS CHEMICZNY KLAS TRZECICH GIMNAZJALNYCH ROK
IMIĘ I NAZWISKO PUNKTACJA SZKOŁA KLASA NAZWISKO NAUCZYCIELA CHEMII I LICEUM OGÓLNOKSZTAŁCĄCE Inowrocław 25 maja 2013 Im. Jana Kasprowicza INOWROCŁAW XX KONKURS CHEMICZNY KLAS TRZECICH GIMNAZJALNYCH ROK
Scenariusz lekcji w technikum z działu Jednofunkcyjne pochodne węglowodorów ( 1 godz.) Temat: Estry pachnąca chemia.
 Scenariusz lekcji w technikum z działu Jednofunkcyjne pochodne węglowodorów ( 1 godz.) Temat: Estry pachnąca chemia. Cele dydaktyczno- wychowawcze: Wyjaśnienie mechanizmu reakcji estryfikacji Poznanie
Scenariusz lekcji w technikum z działu Jednofunkcyjne pochodne węglowodorów ( 1 godz.) Temat: Estry pachnąca chemia. Cele dydaktyczno- wychowawcze: Wyjaśnienie mechanizmu reakcji estryfikacji Poznanie
2.1. Charakterystyka badanego sorbentu oraz ekstrahentów
 BADANIA PROCESU SORPCJI JONÓW ZŁOTA(III), PLATYNY(IV) I PALLADU(II) Z ROZTWORÓW CHLORKOWYCH ORAZ MIESZANINY JONÓW NA SORBENCIE DOWEX OPTIPORE L493 IMPREGNOWANYM CYANEXEM 31 Grzegorz Wójcik, Zbigniew Hubicki,
BADANIA PROCESU SORPCJI JONÓW ZŁOTA(III), PLATYNY(IV) I PALLADU(II) Z ROZTWORÓW CHLORKOWYCH ORAZ MIESZANINY JONÓW NA SORBENCIE DOWEX OPTIPORE L493 IMPREGNOWANYM CYANEXEM 31 Grzegorz Wójcik, Zbigniew Hubicki,
