Kinetyka koagulacji hydrozolu jodku srebra
|
|
|
- Kajetan Wójcik
- 7 lat temu
- Przeglądów:
Transkrypt
1 Waldemar Nowicki ĆWCZENE Kinetyka koagulacji hydrozolu jodku srebra Podstawowe pojęcia: koagulacja, koagulacja szybka, koagulacja powolna, próg koagulacji, połowiczny czas koagulacji t /, zmętnienie, absorbancja pozorna Wstęp Koloidy liofobowe są z reguły układami termodynamicznie nietrwałymi. Stabilność układu koloidalnego zaleŝy od wielu czynników. W przypadku układów dyspersyjnych, w których materiał rozproszony jest ciałem stałym, a ośrodek rozpraszający - cieczą, jednym z najwaŝniejszych czynników wpływających na stabilność koloidalną układu jest siła jonowa ośrodka,. Celem ćwiczenia jest zbadanie zaleŝności pomiędzy szybkością koagulacji hydrozolu jodku srebra (Ag rozproszonego w wodzie) a stęŝeniem azotanu potasu w ośrodku dyspersyjnym. Miarą szybkości procesu koagulacji jest tzw. połowiczny czas koagulacji t /, czyli czas, w którym liczba cząstek hydrozolu zmniejszy się do połowy początkowej wartości. Teoria Oddziaływania pomiędzy cząstkami koloidalnymi WyróŜnia się dwa podstawowe mechanizmy zmniejszania się stopnia dyspersji układu koloidalnego: - koagulacja, tj. łączenie się cząstek koloidalnych na skutek zderzeń spowodowanych ruchami Browna, - migracja pojedynczych molekuł poprzez ośrodek dyspersyjny od mniejszych cząstek koloidalnych do cząstek większych - jako rezultat zaleŝności rozpuszczalności materiału rozproszonego od wielkości cząstek. Występowanie sił odpychania między cząstkami obniŝa szybkość procesu koagulacji. Źródłem sił odpychania jest ładunek elektryczny powstały, na przykład, w wyniku specyficznego zaadsorbowania się na powierzchni cząstek
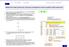
2 KNETYKA KOAGULACJ HYDOZOLU JODKU SEBA 73 części jonów elektrolitu znajdującego się w ośrodku dyspersyjnym. Zaadsorbowane specyficznie, jednoimienne jony są przyczyną gromadzenia się w ich sąsiedztwie jonów o znaku przeciwnym. W rezultacie, w pobliŝu powierzchni cząstek koloidalnych powstaje specyficzna struktura - podwójna warstwa elektryczna. Jej obecność sprawia, Ŝe gdy cząstki zbliŝają się do siebie, pojawia się pomiędzy nimi odpychanie elektrostatyczne. Odpychaniu elektrostatycznemu przeciwdziała przyciąganie, którego źródłem są głównie oddziaływania dyspersyjne. Wypadkowa energia oddziaływania pomiędzy cząstkami (V T ) jest superpozycją energii elektrostatycznego odpychania (V ) oraz przyciągania wynikającego z oddziaływań dyspersyjnych (V A ). Postulat ten jest podstawą teorii DLVO (od nazwisk: Derjaguin, Landau, Vervey i Overbeek), wyjaśniającej trwałość koloidów liofobowych. Energia potencjalna/kt 4 3 c E = mmol/dm 3 c E = mmol/dm 3 - c E = mmol/dm 3 5 Odległość między cząstkami, nm ys.. ZaleŜność energii potencjalnej oddziaływania pomiędzy dwiema cząstkami o potencjale Sterna Ψ δ =,9 V i stałej Hamakera A=,4 J, zanurzonymi w ośrodku dyspersyjnym zawierającym elektrolit typu : o stęŝeniu c E od odległości między nimi. Zarówno oddziaływania dyspersyjne, jak i elektrostatyczne są funkcją odległości d pomiędzy cząstkami. W rezultacie, jak pokazano na rys., na zaleŝności V T od d pojawia się - przy pewnej odległości pomiędzy cząstkami - bariera potencjalna. JeŜeli bariera ta ma na tyle duŝą wysokość, Ŝe energia kinetyczna cząstek jest niewystarczająca dla jej pokonania, wtedy układ koloidalny jest stabilny (niezaleŝnie jednak od wysokości bariery, zawsze istnieje moŝliwość uzyskania przez cząstki koloidalne, w wyniku fluktuacji, energii kinetycznej wystarczającej do pokonania tej bariery).
3 74 ĆWCZENE Stabilność koloidu zaleŝy od siły jonowej ośrodka dyspersyjnego. W zakresie stosunkowo niskich stęŝeń elektrolitu, wpływ wartości na wielkość oddziaływań dyspersyjnych jest niewielki i moŝna go zaniedbać. Natomiast wartość V moŝe ulegać duŝym zmianom wskutek wzrostu. Zmiany te mogą być wywołane przez dwa efekty: zmianę ładunku powierzchniowego cząstek w wyniku specyficznej adsorpcji jonów, zmniejszenie grubości podwójnej warstwy elektrycznej. Jak wynika z rys., na którym przedstawiono przykładową zaleŝność V T = f(d) przy róŝnych stęŝeniach c E elektrolitu w układzie, wraz ze zmniejszaniem się grubości podwójnej warstwy elektrycznej - spowodowanym wprowadzeniem elektrolitu - obniŝa się wysokość bariery potencjału. W wyniku tego obniŝenia rośnie liczba zderzeń pomiędzy cząstkami, których skutkiem jest agregacja, a więc - rośnie szybkość koagulacji. Przy pewnym stęŝeniu elektrolitu wysokość bariery potencjału staje się na tyle mała, Ŝe praktycznie kaŝde zbliŝenie cząstek na odległość promienia działania sił dyspersyjnych prowadzi do ich agregacji. Mówimy wtedy, Ŝe w układzie zachodzi koagulacja szybka; najmniejsze stęŝenie elektrolitu, przy którym zachodzi koagulacja szybka nazywamy progiem koagulacji. Dla odróŝnienia, proces agregacji zachodzący przy występowaniu bariery potencjału, gdy nie kaŝde zderzenie cząstek prowadzi do agregacji, nazywamy koagulacją powolną. Kinetyka koagulacji Matematyczny model kinetyki procesu koagulacji został opracowany przez Smoluchowskiego. Model ten opisuje układ koloidalny zawierający jednakowe kuliste cząstki, które poruszają się ruchami Browna. JeŜeli odległość między cząstkami (a dokładniej - pomiędzy ich środkami geometrycznymi) stanie się równa sumie promieni cząstek, to dochodzi do ich nieodwracalnego połączenia. Łączyć się mogą zarówno pojedyncze cząstki, jak i ich agregaty złoŝone z dwu lub więcej cząstek pierwotnych. Szybkość procesu koagulacji opisana jest wzorem r = k N N () xy xy x y gdzie r xy oznacza szybkość łączenia się agregatów składających się z x oraz y pierwotnych cząstek koloidalnych, N x, N y oznaczają, odpowiednio, stęŝenia liczbowe tych agregatów, natomiast k xy jest stałą szybkości procesu, zaleŝną od współczynników dyfuzji agregatów. Dla koagulacji szybkiej Smoluchowski załoŝył dodatkowo, Ŝe stała szybkości reakcji nie zaleŝy od wielkości agregatów, tzn. od wartości x i y
4 KNETYKA KOAGULACJ HYDOZOLU JODKU SEBA 75 k = k xy () ZałoŜenie to jest dość dobrze spełnione w początkowym okresie koagulacji. Smoluchowski wyprowadził równanie opisujące zaleŝność liczby N i agregatów znajdujących się w jednostce objętości i składających się z i cząstek koloidalnych od czasu trwania koagulacji t i t N t/ N i = i+ (3) t + t/ gdzie N - początkowa liczba cząstek w jednostce objętości układu, t / - połowiczny czas koagulacji, w którym liczba wszystkich cząstek koloidalnych w układzie zmniejszy się dwukrotnie w stosunku do wartości początkowej. Parametr t / jest związany ze współczynnikiem dyfuzji cząstek, D, oraz stałą szybkości koagulacji szybkiej, k, zaleŝnością t / = = (4) 4 π DN kn gdzie - podwojony promień cząstki. W przypadku koagulacji powolnej, gdy nie wszystkie zderzenia cząstek prowadzą do ich agregacji (prowadzi do niej tylko ułamek α zderzeń), wyraŝenie na czas połowicznej koagulacji moŝna wyrazić równaniem t / = (5) 4πDN α ozpraszanie światła w układach koloidalnych Fala elektromagnetyczna oddziaływując z cząstką koloidalną indukuje w niej drgający dipol elektryczny, który staje się źródłem światła rozproszonego o tej samej długości fali światła, λ, co światło wzbudzające. Jedną z pierwszych teorii opisujących zjawisko rozpraszania światła opracował J. ayleigh. Teoria ta opiera się na następujących załoŝeniach: cząstki koloidalne nie absorbują promieniowania, cząstki są małe w porównaniu z długością fali λ,
5 76 ĆWCZENE cząstki są kuliste i mają identyczne promienie, układ koloidalny jest rozcieńczony nie występuje zjawisko rozpraszania wtórnego. Całkowite natęŝenie światła rozproszonego przez jednostkową objętość układu koloidalnego, zawierającego N cząstek, kaŝda o objętości V, dane jest równaniem = KV N (6) gdzie jest natęŝeniem wiązki padającej, a K jest stałą, charakterystyczną dla danego układu i zaleŝną od długości fali światła rozpraszanego. NatęŜenie wiązki światła przechodzącego przez warstwę rozpraszającego układu, p, maleje wykładniczo wraz z grubością l tej warstwy ( τl) P = exp (7) gdzie τ jest współczynnikiem charakterystycznym dla danego układu, zwanym zmętnieniem. JeŜeli zmniejszenie natęŝenia wiązki padającej, spowodowane rozpraszaniem, jest małe, to P ~ τ (8) óŝnica P określa osłabienie natęŝenia wiązki przechodzącej przez ośrodek rozpraszający, a zatem odpowiada natęŝeniu światła rozproszonego we wszystkich kierunkach. Stąd τ ~ (9) Wpływ procesu koagulacji na natęŝenie światła rozproszonego przez układ koloidalny Niech jednostkowa objętość układu zawiera N cząstek, z których kaŝda ma objętość V. NatęŜenie światła rozproszonego przez ten układ we wszystkich kierunkach przedstawia równanie (6). JeŜeli w wyniku koagulacji w układzie powstaną agregaty złoŝone z róŝnych liczb cząstek pierwotnych, natęŝenie światła rozproszonego będzie wyraŝone równaniem i= = K N i V i ()
6 KNETYKA KOAGULACJ HYDOZOLU JODKU SEBA 77 gdzie N i oznacza liczbę agregatów zbudowanych z i pierwotnych cząstek, natomiast V i - objętość tych agregatów. Łącząc równania (3) i () otrzymujemy następujący związek pomiędzy natęŝeniem światła rozproszonego, i czasem koagulacji, t = t + K N V () t/ Wraz ze wzrostem czasu trwania procesu koagulacji właściwości układu coraz bardziej odbiegają od właściwości modeli, dla których zostały wyprowadzone równania (3) i (). Dlatego teŝ stosowalność równania () do opisu przebiegu koagulacji ogranicza się jedynie do początkowego etapu procesu. Pomiar natęŝenia światła rozproszonego moŝna zastąpić przez pomiar absorbancji pozornej, A A log =,43τ l =,43 l () p Podstawiając za wyraŝenie wynikające z równania (), otrzymujemy gdzie t A = ' K N V + l t (3) / ' K jest stałą charakterystyczną dla danego układu koloidalnego. Część praktyczna Metoda Badanie kinetyki procesu koagulacji polega na określeniu zaleŝności pomiędzy liczbą niezaleŝnych kinetycznie obiektów w jednostce objętości, a czasem trwania koagulacji. W ćwiczeniu wykorzystuje się w tym celu zjawisko rozpraszania światła []. Koagulację jodku srebra śledzi się mierząc zaleŝność absorbancji pozornej od czasu, A eksp = f(t). Procedura opracowania wyników polega na dopasowaniu paraboli do punktów doświadczalnych, w celu wyznaczenia nachylenia krzywej A eksp = f(t) w punkcie t =. Połowiczny czasu koagulacji, t / wyznacza się w oparciu o wzór (3), który opisuje styczną do danych eksperymentalnych w t =.
7 78 ĆWCZENE Odczynniki i aparatura - wodny roztwór K o stęŝeniu,88 3 mol/dm 3 - wodny roztwór AgNO 3 o stęŝeniu,8 3 mol/dm 3 - azotan potasu, cz.d.a. (stały) - spektrofotometr CECL (instrukcja obsługi znajduje się przy przyrządzie) - mieszadło magnetyczne oraz -3 elementy mieszające - stoper - waga analityczna, szpachtułka, naczynie słuŝące do przygotowania nawaŝki - pipeta automatyczna wielomiarowa o pojemności 5 cm 3 - biureta o pojemności 5 cm 3 - zlewka o pojemności 5- cm 3-5 zlewek o pojemności 5 cm 3 - kolba miarowa o pojemności 5 cm 3 - lejek - tryskawka Wykonanie ćwiczenia Preparatyka hydrozolu jodku srebra Do zlewki o pojemności 5- cm 3 wlać 5 cm 3 roztworu K o stęŝeniu,88 3 mol/dm 3. Do roztworu wkroplić powoli z biurety 5 cm 3 roztworu AgNO 3 o stęŝeniu,8 3 mol/dm 3 ; roztwór w zlewce powinien być intensywnie mieszany przy uŝyciu mieszadła magnetycznego. Spreparowany zol pozostawić na około 3 min. Zastosowana metoda prowadzi do tworzenia się cząstek naładowanych ujemnie. Jony jodkowe, które są w nadmiarze, ulegają specyficznej adsorpcji na powierzchni cząstek - ze względu na powinowactwo do sieci krystalicznej - gromadząc na niej ładunek ujemny. Jony K + oraz NO 3 nie adsorbują się na powierzchni cząstek Ag. Wyznaczanie zaleŝności pomiędzy absorbancją pozorną a czasem koagulacji. Zmieszać 5 cm 3 hydrozolu Ag z 5 cm 3 wodnego roztworu KNO 3 o znanym stęŝeniu. Mieszaniną napełnić kuwetę spektrofotometru, a następnie zmierzyć absorbancję tej mieszaniny względem wody przy λ = 4 nm. Pomiaru dokonać dokładnie po upływie minuty od momentu zmieszania zolu z roztworem elektrolitu. Pomiar powtórzyć 9-krotnie w odstępach (dokładnie) jednominutowych.. Pomiary przeprowadzić dla róŝnych stęŝeń roztworów KNO 3. Zaleca się przygotowanie roztworów o następujących stęŝeniach:,;,4;,8;,3;,36;,4 oraz,44 mol/dm 3. Ponadto naleŝy przeprowadzić pomiar absorbancji
8 KNETYKA KOAGULACJ HYDOZOLU JODKU SEBA 79 próbki uzyskanej przez zmieszanie zolu z wodą destylowaną; absorbancja tej próby będzie dalej oznaczana jako A. 3. Po kaŝdej zakończonej serii pomiarów, kuwety naleŝy przemyć wodnym roztworem jodku potasu, wypłukać wodą destylowaną, następnie metanolem i wysuszyć. Obliczenia Zgodnie z równaniem (3), zaleŝność A = f(t) jest prostoliniowa. Badany układ koloidalny nie spełnia jednak wszystkich załoŝeń poczynionych przy wyprowadzaniu tego wzoru - przede wszystkim hydrozol Ag jest polidyspersyjny. Ponadto, wraz ze wzrostem czasu koagulacji, właściwości układu - ze względu na ciągły wzrost agregatów - coraz bardziej odbiegają od załoŝeń modelowych. Wzór (3) opisuje dane eksperymentalne dla małych wartości czasu t i jest równaniem prostej, stycznej do krzywej eksperymentalnej A eksp = f(t) w punkcie t =. ZaleŜność doświadczalną A eksp = f(t) dobrze opisuje parabola A + eksp = c + bt at (4) przy czym dla t = mamy A = A. Pochodna absorbancji A eksp względem czasu jest dana równaniem da eksp = b + at (5) dt Wartość pochodnej da eksp /dt w punkcie t =, a więc takŝe wartość współczynnika kierunkowego prostej stycznej do paraboli w tym punkcie, wynosi b. zędna początkowa tej stycznej, podobnie jak rzędna początkowa pararaboli, ma wartość A. Wynika stąd, Ŝe równanie prostej, stycznej do paraboli w punkcie t =, ma postać A = A + bt = c + bt (6) Z przyjętych załoŝeń wynika, Ŝe równania (3) i (6) opisują tą samą prostą, zatem ' K N V l = c K N V l = b t ' / (7) (8)
9 8 ĆWCZENE Czas połowicznej przemiany, t /, wyznaczamy z równania c t / = (9) b Dla uzyskanych wartości parametrów t / wyliczamy przedziały ufności. Sporządzamy wykres zaleŝności t / od stęŝenia elektrolitu. Dyskusja. Przedstaw interpretację otrzymanej zaleŝności t / od stęŝenia elektrolitu.. Uzasadnij, dlaczego zmętnienie τ jest w przybliŝeniu równe względnemu osłabieniu wiązki przechodzącej przez ośrodek rozpraszający (zaleŝność (8)). 3. WykaŜ, Ŝe natęŝenie światła rozproszonego jest funkcją czasu trwania koagulacji (równanie ()). Literatura cytowana [] W. Nowicki, G. Nowicka, J. Chem. Educ., 68 (99) 53. Literatura uzupełniająca [] H. Sonntag, Koloidy, PWN, Warszawa, 98. Zagadnienia dodatkowe Definicja pojęcia układu koloidalnego. Klasyfikacja układów koloidalnych. Dyfuzja w układach koloidalnych. uchy Browna.
WYZNACZANIE STAŁEJ DYSOCJACJI p-nitrofenolu METODĄ SPEKTROFOTOMETRII ABSORPCYJNEJ
 Ćwiczenie nr 13 WYZNCZNIE STŁEJ DYSOCJCJI p-nitrofenolu METODĄ SPEKTROFOTOMETRII BSORPCYJNEJ I. Cel ćwiczenia Celem ćwiczenia jest wyznaczenie metodą spektrofotometryczną stałej dysocjacji słabego kwasu,
Ćwiczenie nr 13 WYZNCZNIE STŁEJ DYSOCJCJI p-nitrofenolu METODĄ SPEKTROFOTOMETRII BSORPCYJNEJ I. Cel ćwiczenia Celem ćwiczenia jest wyznaczenie metodą spektrofotometryczną stałej dysocjacji słabego kwasu,
PRACOWNIA CHEMII. Wygaszanie fluorescencji (Fiz4)
 PRACOWNIA CHEMII Ćwiczenia laboratoryjne dla studentów II roku kierunku Zastosowania fizyki w biologii i medycynie Biofizyka molekularna Projektowanie molekularne i bioinformatyka Wygaszanie fluorescencji
PRACOWNIA CHEMII Ćwiczenia laboratoryjne dla studentów II roku kierunku Zastosowania fizyki w biologii i medycynie Biofizyka molekularna Projektowanie molekularne i bioinformatyka Wygaszanie fluorescencji
Ćwiczenie 8. Waldemar Nowicki i Grażyna Nowicka KOAGULACJA KOLOIDÓW LIOFOBOWYCH
 Ćwiczenie 8 Waldemar Nowicki i Grażyna Nowicka KOAGULACJA KOLOIDÓW LIOFOBOWYCH Zagadnienia: Definicja pojęcia stan koloidalny. Klasyfikacja układów koloidalnych. Dyfuzja w układach koloidalnych; ruchy
Ćwiczenie 8 Waldemar Nowicki i Grażyna Nowicka KOAGULACJA KOLOIDÓW LIOFOBOWYCH Zagadnienia: Definicja pojęcia stan koloidalny. Klasyfikacja układów koloidalnych. Dyfuzja w układach koloidalnych; ruchy
EFEKT SOLNY BRÖNSTEDA
 EFEKT SLNY RÖNSTED Pojęcie eektu solnego zostało wprowadzone przez rönsteda w celu wytłumaczenia wpływu obojętnego elektrolitu na szybkość reakcji zachodzących między jonami. Założył on, że reakcja pomiędzy
EFEKT SLNY RÖNSTED Pojęcie eektu solnego zostało wprowadzone przez rönsteda w celu wytłumaczenia wpływu obojętnego elektrolitu na szybkość reakcji zachodzących między jonami. Założył on, że reakcja pomiędzy
Ćwiczenie 14. Maria Bełtowska-Brzezinska KINETYKA REAKCJI ENZYMATYCZNYCH
 Ćwiczenie 14 aria Bełtowska-Brzezinska KINETYKA REAKCJI ENZYATYCZNYCH Zagadnienia: Podstawowe pojęcia kinetyki chemicznej (szybkość reakcji, reakcje elementarne, rząd reakcji). Równania kinetyczne prostych
Ćwiczenie 14 aria Bełtowska-Brzezinska KINETYKA REAKCJI ENZYATYCZNYCH Zagadnienia: Podstawowe pojęcia kinetyki chemicznej (szybkość reakcji, reakcje elementarne, rząd reakcji). Równania kinetyczne prostych
Ćwiczenie 8 Wyznaczanie stałej szybkości reakcji utleniania jonów tiosiarczanowych
 CHEMI FIZYCZN Ćwiczenie 8 Wyznaczanie stałej szybkości reakcji utleniania jonów tiosiarczanowych W ćwiczeniu przeprowadzana jest reakcja utleniania jonów tiosiarczanowych za pomocą jonów żelaza(iii). Przebieg
CHEMI FIZYCZN Ćwiczenie 8 Wyznaczanie stałej szybkości reakcji utleniania jonów tiosiarczanowych W ćwiczeniu przeprowadzana jest reakcja utleniania jonów tiosiarczanowych za pomocą jonów żelaza(iii). Przebieg
Przedmiot: Chemia budowlana Zakład Materiałoznawstwa i Technologii Betonu
 Przedmiot: Chemia budowlana Zakład Materiałoznawstwa i Technologii Betonu Ćw. 4 Kinetyka reakcji chemicznych Zagadnienia do przygotowania: Szybkość reakcji chemicznej, zależność szybkości reakcji chemicznej
Przedmiot: Chemia budowlana Zakład Materiałoznawstwa i Technologii Betonu Ćw. 4 Kinetyka reakcji chemicznych Zagadnienia do przygotowania: Szybkość reakcji chemicznej, zależność szybkości reakcji chemicznej
SZYBKOŚĆ REAKCJI JONOWYCH W ZALEŻNOŚCI OD SIŁY JONOWEJ ROZTWORU
 POLITECHNIKA ŚLĄSKA WYDZIAŁ CHEMICZNY KATEDRA FIZYKOCHEMII I TECHNOLOGII POLIMERÓW SZYBKOŚĆ REAKCI ONOWYCH W ZALEŻNOŚCI OD SIŁY ONOWE ROZTWORU Opiekun: Krzysztof Kozieł Miejsce ćwiczenia: Czerwona Chemia,
POLITECHNIKA ŚLĄSKA WYDZIAŁ CHEMICZNY KATEDRA FIZYKOCHEMII I TECHNOLOGII POLIMERÓW SZYBKOŚĆ REAKCI ONOWYCH W ZALEŻNOŚCI OD SIŁY ONOWE ROZTWORU Opiekun: Krzysztof Kozieł Miejsce ćwiczenia: Czerwona Chemia,
Politechnika Warszawska. Wydział Budownictwa Mechaniki i Petrochemii w Płocku Laboratorium Chemii Budowlanej
 Politechnika Warszawska Wydział Budownictwa Mechaniki i Petrochemii w Płocku Laboratorium Chemii Budowlanej Instrukcja do ćwiczenia: SZYBKOŚĆ PRZEMIAN CHEMICZNYCH Opracowała: dr inŝ. Maria Bukowska Płock,
Politechnika Warszawska Wydział Budownictwa Mechaniki i Petrochemii w Płocku Laboratorium Chemii Budowlanej Instrukcja do ćwiczenia: SZYBKOŚĆ PRZEMIAN CHEMICZNYCH Opracowała: dr inŝ. Maria Bukowska Płock,
Wyznaczanie stałej dysocjacji pk a słabego kwasu metodą konduktometryczną CZĘŚĆ DOŚWIADCZALNA. Tabela wyników pomiaru
 Wyznaczanie stałej dysocjacji pk a słabego kwasu metodą konduktometryczną Cel ćwiczenia Celem ćwiczenia jest wyznaczenie stałej dysocjacji pk a słabego kwasu metodą konduktometryczną. Zakres wymaganych
Wyznaczanie stałej dysocjacji pk a słabego kwasu metodą konduktometryczną Cel ćwiczenia Celem ćwiczenia jest wyznaczenie stałej dysocjacji pk a słabego kwasu metodą konduktometryczną. Zakres wymaganych
ĆWICZENIE 2 KONDUKTOMETRIA
 ĆWICZENIE 2 KONDUKTOMETRIA 1. Oznaczanie słabych kwasów w sokach i syropach owocowych metodą miareczkowania konduktometrycznego Celem ćwiczenia jest ilościowe oznaczenie zawartości słabych kwasów w sokach
ĆWICZENIE 2 KONDUKTOMETRIA 1. Oznaczanie słabych kwasów w sokach i syropach owocowych metodą miareczkowania konduktometrycznego Celem ćwiczenia jest ilościowe oznaczenie zawartości słabych kwasów w sokach
TRANSPORT NIEELEKTROLITÓW PRZEZ BŁONY WYZNACZANIE WSPÓŁCZYNNIKA PRZEPUSZCZALNOŚCI
 Ćwiczenie nr 7 TRANSPORT NIEELEKTROLITÓW PRZEZ BŁONY WYZNACZANIE WSPÓŁCZYNNIKA PRZEPUSZCZALNOŚCI Celem ćwiczenia jest zapoznanie się z podstawami teorii procesów transportu nieelektrolitów przez błony.
Ćwiczenie nr 7 TRANSPORT NIEELEKTROLITÓW PRZEZ BŁONY WYZNACZANIE WSPÓŁCZYNNIKA PRZEPUSZCZALNOŚCI Celem ćwiczenia jest zapoznanie się z podstawami teorii procesów transportu nieelektrolitów przez błony.
Ćwiczenie IX KATALITYCZNY ROZKŁAD WODY UTLENIONEJ
 Wprowadzenie Ćwiczenie IX KATALITYCZNY ROZKŁAD WODY UTLENIONEJ opracowanie: Barbara Stypuła Celem ćwiczenia jest poznanie roli katalizatora w procesach chemicznych oraz prostego sposobu wyznaczenia wpływu
Wprowadzenie Ćwiczenie IX KATALITYCZNY ROZKŁAD WODY UTLENIONEJ opracowanie: Barbara Stypuła Celem ćwiczenia jest poznanie roli katalizatora w procesach chemicznych oraz prostego sposobu wyznaczenia wpływu
WYZNACZANIE STAŁEJ DYSOCJACJI SŁABEGO KWASU ORGANICZNEGO
 10 WYZNACZANIE STAŁEJ DYSOCJACJI SŁABEGO KWASU ORGANICZNEGO CEL ĆWICZENIA Poznanie podstawowych zagadnień teorii dysocjacji elektrolitycznej i problemów związanych z właściwościami kwasów i zasad oraz
10 WYZNACZANIE STAŁEJ DYSOCJACJI SŁABEGO KWASU ORGANICZNEGO CEL ĆWICZENIA Poznanie podstawowych zagadnień teorii dysocjacji elektrolitycznej i problemów związanych z właściwościami kwasów i zasad oraz
Ć W I C Z E N I E 5. Kinetyka cementacji metali
 Ć W I C Z E N I E Kinetyka cementacji metali WPROWADZENIE Proces cementacji jest jednym ze sposobów wydzielania metali z roztworów wodnych. Polega on na wytrącaniu jonów metalu bardziej szlachetnego przez
Ć W I C Z E N I E Kinetyka cementacji metali WPROWADZENIE Proces cementacji jest jednym ze sposobów wydzielania metali z roztworów wodnych. Polega on na wytrącaniu jonów metalu bardziej szlachetnego przez
Katedra Chemii Fizycznej Uniwersytetu Łódzkiego. Wyznaczanie stałej szybkości i rzędu reakcji metodą graficzną. opiekun mgr K.
 Katedra Chemii Fizycznej Uniwersytetu Łódzkiego Wyznaczanie stałej szybkości i rzędu reakcji metodą graficzną opiekun mgr K. Łudzik ćwiczenie nr 27 Zakres zagadnień obowiązujących do ćwiczenia 1. Zastosowanie
Katedra Chemii Fizycznej Uniwersytetu Łódzkiego Wyznaczanie stałej szybkości i rzędu reakcji metodą graficzną opiekun mgr K. Łudzik ćwiczenie nr 27 Zakres zagadnień obowiązujących do ćwiczenia 1. Zastosowanie
RÓWNOWAGI REAKCJI KOMPLEKSOWANIA
 POLITECHNIK POZNŃSK ZKŁD CHEMII FIZYCZNEJ ĆWICZENI PRCOWNI CHEMII FIZYCZNEJ RÓWNOWGI REKCJI KOMPLEKSOWNI WSTĘP Ważną grupę reakcji chemicznych wykorzystywanych w chemii fizycznej i analitycznej stanowią
POLITECHNIK POZNŃSK ZKŁD CHEMII FIZYCZNEJ ĆWICZENI PRCOWNI CHEMII FIZYCZNEJ RÓWNOWGI REKCJI KOMPLEKSOWNI WSTĘP Ważną grupę reakcji chemicznych wykorzystywanych w chemii fizycznej i analitycznej stanowią
Laboratorium Podstaw Biofizyki
 CEL ĆWICZENIA Celem ćwiczenia jest zbadanie procesu adsorpcji barwnika z roztworu oraz wyznaczenie równania izotermy Freundlicha. ZAKRES WYMAGANYCH WIADOMOŚCI I UMIEJĘTNOŚCI: widmo absorpcyjne, prawo Lamberta-Beera,
CEL ĆWICZENIA Celem ćwiczenia jest zbadanie procesu adsorpcji barwnika z roztworu oraz wyznaczenie równania izotermy Freundlicha. ZAKRES WYMAGANYCH WIADOMOŚCI I UMIEJĘTNOŚCI: widmo absorpcyjne, prawo Lamberta-Beera,
Spektroskopia molekularna. Ćwiczenie nr 1. Widma absorpcyjne błękitu tymolowego
 Spektroskopia molekularna Ćwiczenie nr 1 Widma absorpcyjne błękitu tymolowego Doświadczenie to ma na celu zaznajomienie uczestników ćwiczeń ze sposobem wykonywania pomiarów metodą spektrofotometryczną
Spektroskopia molekularna Ćwiczenie nr 1 Widma absorpcyjne błękitu tymolowego Doświadczenie to ma na celu zaznajomienie uczestników ćwiczeń ze sposobem wykonywania pomiarów metodą spektrofotometryczną
Wyznaczanie stałej szybkości reakcji wymiany jonowej
 Wyznaczanie stałej szybkości reakcji wymiany jonowej Ćwiczenie laboratoryjne nr 4 Elementy termodynamiki i kinetyki procesowej Anna Ptaszek Elementy kinetyki chemicznej Pojęcie szybkości reakcji Pojęcie
Wyznaczanie stałej szybkości reakcji wymiany jonowej Ćwiczenie laboratoryjne nr 4 Elementy termodynamiki i kinetyki procesowej Anna Ptaszek Elementy kinetyki chemicznej Pojęcie szybkości reakcji Pojęcie
LABORATORIUM Z KATALIZY HOMOGENICZNEJ I HETEROGENICZNEJ WYZNACZANIE STAŁEJ SZYBKOŚCI REAKCJI UTLENIANIA POLITECHNIKA ŚLĄSKA WYDZIAŁ CHEMICZNY
 POLITECHNIKA ŚLĄSKA WYDZIAŁ CHEMICZNY KATEDRA FIZYKOCHEMII I TECHNOLOGII POLIMERÓW WYZNACZANIE STAŁEJ SZYBKOŚCI REAKCJI UTLENIANIA JONÓW TIOSIARCZANOWYCH Miejsce ćwiczenia: Zakład Chemii Fizycznej, sala
POLITECHNIKA ŚLĄSKA WYDZIAŁ CHEMICZNY KATEDRA FIZYKOCHEMII I TECHNOLOGII POLIMERÓW WYZNACZANIE STAŁEJ SZYBKOŚCI REAKCJI UTLENIANIA JONÓW TIOSIARCZANOWYCH Miejsce ćwiczenia: Zakład Chemii Fizycznej, sala
Katedra Chemii Fizycznej Uniwersytetu Łódzkiego. Wpływ stężenia kwasu na szybkość hydrolizy estru
 Katedra Chemii Fizycznej Uniwersytetu Łódzkiego Wpływ stężenia kwasu na szybkość hydrolizy estru ćwiczenie nr 25 opracowała dr B. Nowicka, aktualizacja D. Waliszewski Zakres zagadnień obowiązujących do
Katedra Chemii Fizycznej Uniwersytetu Łódzkiego Wpływ stężenia kwasu na szybkość hydrolizy estru ćwiczenie nr 25 opracowała dr B. Nowicka, aktualizacja D. Waliszewski Zakres zagadnień obowiązujących do
A4.05 Instrukcja wykonania ćwiczenia
 Katedra Chemii Fizycznej Uniwersytetu Łódzkiego A4.05 nstrukcja wykonania ćwiczenia Wyznaczanie współczynników aktywności soli trudno rozpuszczalnej metodą pomiaru rozpuszczalności Zakres zagadnień obowiązujących
Katedra Chemii Fizycznej Uniwersytetu Łódzkiego A4.05 nstrukcja wykonania ćwiczenia Wyznaczanie współczynników aktywności soli trudno rozpuszczalnej metodą pomiaru rozpuszczalności Zakres zagadnień obowiązujących
Kinetyka chemiczna jest działem fizykochemii zajmującym się szybkością i mechanizmem reakcji chemicznych w różnych warunkach. a RT.
 Ćwiczenie 12, 13. Kinetyka chemiczna. Kinetyka chemiczna jest działem fizykochemii zajmującym się szybkością i mechanizmem reakcji chemicznych w różnych warunkach. Szybkość reakcji chemicznej jest związana
Ćwiczenie 12, 13. Kinetyka chemiczna. Kinetyka chemiczna jest działem fizykochemii zajmującym się szybkością i mechanizmem reakcji chemicznych w różnych warunkach. Szybkość reakcji chemicznej jest związana
OZNACZANIE ŻELAZA METODĄ SPEKTROFOTOMETRII UV/VIS
 OZNACZANIE ŻELAZA METODĄ SPEKTROFOTOMETRII UV/VIS Zagadnienia teoretyczne. Spektrofotometria jest techniką instrumentalną, w której do celów analitycznych wykorzystuje się przejścia energetyczne zachodzące
OZNACZANIE ŻELAZA METODĄ SPEKTROFOTOMETRII UV/VIS Zagadnienia teoretyczne. Spektrofotometria jest techniką instrumentalną, w której do celów analitycznych wykorzystuje się przejścia energetyczne zachodzące
Optyczna spektroskopia oscylacyjna. w badaniach powierzchni
 Optyczna spektroskopia oscylacyjna w badaniach powierzchni Zalety oscylacyjnej spektroskopii optycznej uŝycie fotonów jako cząsteczek wzbudzających i rejestrowanych nie wymaga uŝycia próŝni (moŝliwość
Optyczna spektroskopia oscylacyjna w badaniach powierzchni Zalety oscylacyjnej spektroskopii optycznej uŝycie fotonów jako cząsteczek wzbudzających i rejestrowanych nie wymaga uŝycia próŝni (moŝliwość
PROFIL PRĘDKOŚCI W RURZE PROSTOLINIOWEJ
 LABORATORIUM MECHANIKI PŁYNÓW Ćwiczenie N 7 PROFIL PRĘDKOŚCI W RURZE PROSTOLINIOWEJ . Cel ćwiczenia Doświadczalne i teoretyczne wyznaczenie profilu prędkości w rurze prostoosiowej 2. Podstawy teoretyczne:
LABORATORIUM MECHANIKI PŁYNÓW Ćwiczenie N 7 PROFIL PRĘDKOŚCI W RURZE PROSTOLINIOWEJ . Cel ćwiczenia Doświadczalne i teoretyczne wyznaczenie profilu prędkości w rurze prostoosiowej 2. Podstawy teoretyczne:
Laboratorium 5. Wpływ temperatury na aktywność enzymów. Inaktywacja termiczna
 Laboratorium 5 Wpływ temperatury na aktywność enzymów. Inaktywacja termiczna Prowadzący: dr inż. Karolina Labus 1. CZĘŚĆ TEORETYCZNA Szybkość reakcji enzymatycznej zależy przede wszystkim od stężenia substratu
Laboratorium 5 Wpływ temperatury na aktywność enzymów. Inaktywacja termiczna Prowadzący: dr inż. Karolina Labus 1. CZĘŚĆ TEORETYCZNA Szybkość reakcji enzymatycznej zależy przede wszystkim od stężenia substratu
I ,11-1, 1, C, , 1, C
 Materiał powtórzeniowy - budowa atomu - cząstki elementarne, izotopy, promieniotwórczość naturalna, okres półtrwania, średnia masa atomowa z przykładowymi zadaniami I. Cząstki elementarne atomu 1. Elektrony
Materiał powtórzeniowy - budowa atomu - cząstki elementarne, izotopy, promieniotwórczość naturalna, okres półtrwania, średnia masa atomowa z przykładowymi zadaniami I. Cząstki elementarne atomu 1. Elektrony
Wyznaczanie krzywej ładowania kondensatora
 Ćwiczenie E10 Wyznaczanie krzywej ładowania kondensatora E10.1. Cel ćwiczenia Celem ćwiczenia jest zbadanie przebiegu procesu ładowania kondensatora oraz wyznaczenie stałej czasowej szeregowego układu.
Ćwiczenie E10 Wyznaczanie krzywej ładowania kondensatora E10.1. Cel ćwiczenia Celem ćwiczenia jest zbadanie przebiegu procesu ładowania kondensatora oraz wyznaczenie stałej czasowej szeregowego układu.
Podstawowe prawa opisujące właściwości gazów zostały wyprowadzone dla gazu modelowego, nazywanego gazem doskonałym (idealnym).
 Spis treści 1 Stan gazowy 2 Gaz doskonały 21 Definicja mikroskopowa 22 Definicja makroskopowa (termodynamiczna) 3 Prawa gazowe 31 Prawo Boyle a-mariotte a 32 Prawo Gay-Lussaca 33 Prawo Charlesa 34 Prawo
Spis treści 1 Stan gazowy 2 Gaz doskonały 21 Definicja mikroskopowa 22 Definicja makroskopowa (termodynamiczna) 3 Prawa gazowe 31 Prawo Boyle a-mariotte a 32 Prawo Gay-Lussaca 33 Prawo Charlesa 34 Prawo
Instrukcja do ćwiczeń laboratoryjnych
 UNIWERSYTET GDAŃSKI WYDZIAŁ CHEMII Pracownia studencka Katedra Analizy Środowiska Instrukcja do ćwiczeń laboratoryjnych Ćwiczenie nr 3 OZNACZANIE CHLORKÓW METODĄ SPEKTROFOTOMETRYCZNĄ Z TIOCYJANIANEM RTĘCI(II)
UNIWERSYTET GDAŃSKI WYDZIAŁ CHEMII Pracownia studencka Katedra Analizy Środowiska Instrukcja do ćwiczeń laboratoryjnych Ćwiczenie nr 3 OZNACZANIE CHLORKÓW METODĄ SPEKTROFOTOMETRYCZNĄ Z TIOCYJANIANEM RTĘCI(II)
Instrukcja do ćwiczeń laboratoryjnych
 UNIWERSYTET GDAŃSKI WYDZIAŁ CHEMII Pracownia studencka Katedry Analizy Środowiska Instrukcja do ćwiczeń laboratoryjnych Ćwiczenie nr 3 Oznaczanie chlorków metodą spektrofotometryczną z tiocyjanianem rtęci(ii)
UNIWERSYTET GDAŃSKI WYDZIAŁ CHEMII Pracownia studencka Katedry Analizy Środowiska Instrukcja do ćwiczeń laboratoryjnych Ćwiczenie nr 3 Oznaczanie chlorków metodą spektrofotometryczną z tiocyjanianem rtęci(ii)
Ćw. 5 Absorpcjometria I
 Ćw. 5 Absorpcjometria I Absorpcja promieniowania elektromagnetycznego z obszaru widzialnego i nadfioletowego przez atomy i cząsteczki powoduje zmianę ich stanu elektronowego. Zjawiska te moŝna badać za
Ćw. 5 Absorpcjometria I Absorpcja promieniowania elektromagnetycznego z obszaru widzialnego i nadfioletowego przez atomy i cząsteczki powoduje zmianę ich stanu elektronowego. Zjawiska te moŝna badać za
CHEMIA ŚRODKÓW BIOAKTYWNYCH I KOSMETYKÓW PRACOWNIA CHEMII ANALITYCZNEJ. Ćwiczenie 9
 CHEMIA ŚRODKÓW BIOAKTYWNYCH I KOSMETYKÓW PRACOWNIA CHEMII ANALITYCZNEJ Ćwiczenie 9 Zastosowanie metod miareczkowania strąceniowego do oznaczania chlorków w mydłach metodą Volharda. Ćwiczenie obejmuje:
CHEMIA ŚRODKÓW BIOAKTYWNYCH I KOSMETYKÓW PRACOWNIA CHEMII ANALITYCZNEJ Ćwiczenie 9 Zastosowanie metod miareczkowania strąceniowego do oznaczania chlorków w mydłach metodą Volharda. Ćwiczenie obejmuje:
PRACOWNIA CHEMII. Reakcje fotochemiczne (Fiz3)
 PRACOWNIA CHEMII Ćwiczenia laboratoryjne dla studentów II roku kierunku Zastosowania fizyki w biologii i medycynie Biofizyka molekularna Projektowanie molekularne i bioinformatyka Reakcje fotochemiczne
PRACOWNIA CHEMII Ćwiczenia laboratoryjne dla studentów II roku kierunku Zastosowania fizyki w biologii i medycynie Biofizyka molekularna Projektowanie molekularne i bioinformatyka Reakcje fotochemiczne
POLITECHNIKA POZNAŃSKA ZAKŁAD CHEMII FIZYCZNEJ ĆWICZENIA PRACOWNI CHEMII FIZYCZNEJ
 ZALEŻNOŚĆ STAŁEJ SZYBKOŚCI REAKCJI OD TEMPERATURY WSTĘP Szybkość reakcji drugiego rzędu: A + B C (1) zależy od stężenia substratów A oraz B v = k [A][B] (2) Gdy jednym z reagentów jest rozpuszczalnik (np.
ZALEŻNOŚĆ STAŁEJ SZYBKOŚCI REAKCJI OD TEMPERATURY WSTĘP Szybkość reakcji drugiego rzędu: A + B C (1) zależy od stężenia substratów A oraz B v = k [A][B] (2) Gdy jednym z reagentów jest rozpuszczalnik (np.
Polarymetr. Ćwiczenie 74. Cel ćwiczenia Pomiar kąta skręcenia płaszczyzny polaryzacji w roztworach cukru. Wprowadzenie
 Ćwiczenie 74 Polarymetr Cel ćwiczenia Pomiar kąta skręcenia płaszczyzny polaryzacji w roztworach cukru. Wprowadzenie Światło liniowo spolaryzowane* rozchodzi się bez zmiany płaszczyzny polaryzacji w próŝni
Ćwiczenie 74 Polarymetr Cel ćwiczenia Pomiar kąta skręcenia płaszczyzny polaryzacji w roztworach cukru. Wprowadzenie Światło liniowo spolaryzowane* rozchodzi się bez zmiany płaszczyzny polaryzacji w próŝni
Seria 2, ćwiczenia do wykładu Od eksperymentu do poznania materii
 Seria 2, ćwiczenia do wykładu Od eksperymentu do poznania materii 8.1.21 Zad. 1. Obliczyć ciśnienie potrzebne do przemiany grafitu w diament w temperaturze 25 o C. Objętość właściwa (odwrotność gęstości)
Seria 2, ćwiczenia do wykładu Od eksperymentu do poznania materii 8.1.21 Zad. 1. Obliczyć ciśnienie potrzebne do przemiany grafitu w diament w temperaturze 25 o C. Objętość właściwa (odwrotność gęstości)
A B. Modelowanie reakcji chemicznych: numeryczne rozwiązywanie równań na szybkość reakcji chemicznych B: 1. da dt. A v. v t
 B: 1 Modelowanie reakcji chemicznych: numeryczne rozwiązywanie równań na szybkość reakcji chemicznych 1. ZałóŜmy, Ŝe zmienna A oznacza stęŝenie substratu, a zmienna B stęŝenie produktu reakcji chemicznej
B: 1 Modelowanie reakcji chemicznych: numeryczne rozwiązywanie równań na szybkość reakcji chemicznych 1. ZałóŜmy, Ŝe zmienna A oznacza stęŝenie substratu, a zmienna B stęŝenie produktu reakcji chemicznej
Katedra Chemii Fizycznej Uniwersytetu Łódzkiego. Wyznaczanie lepkości wodnych roztworów sacharozy. opracowała dr A. Kacperska
 Katedra Chemii Fizycznej Uniwersytetu Łódzkiego Wyznaczanie lepkości wodnych roztworów sacharozy opracowała dr A. Kacperska ćwiczenie nr 20 Zakres zagadnień obowiązujących do ćwiczenia 1. Oddziaływania
Katedra Chemii Fizycznej Uniwersytetu Łódzkiego Wyznaczanie lepkości wodnych roztworów sacharozy opracowała dr A. Kacperska ćwiczenie nr 20 Zakres zagadnień obowiązujących do ćwiczenia 1. Oddziaływania
Katedra Chemii Fizycznej Uniwersytetu Łódzkiego. Lepkościowo średnia masa cząsteczkowa polimeru. opiekun ćwiczenia: dr A.
 Katedra Chemii Fizycznej Uniwersytetu Łódzkiego Lepkościowo średnia masa cząsteczkowa polimeru ćwiczenie nr 21 opiekun ćwiczenia: dr A. Kacperska Zakres zagadnień obowiązujących do ćwiczenia 1. Związki
Katedra Chemii Fizycznej Uniwersytetu Łódzkiego Lepkościowo średnia masa cząsteczkowa polimeru ćwiczenie nr 21 opiekun ćwiczenia: dr A. Kacperska Zakres zagadnień obowiązujących do ćwiczenia 1. Związki
KINETYKA INWERSJI SACHAROZY
 Dorota Warmińska, Maciej Śmiechowski Katedra Chemii Fizycznej, Wydział Chemiczny, Politechnika Gdańska KINETYKA INWERSJI SACHAROZY Wstęp teoretyczny Kataliza kwasowo-zasadowa Kataliza kwasowo-zasadowa
Dorota Warmińska, Maciej Śmiechowski Katedra Chemii Fizycznej, Wydział Chemiczny, Politechnika Gdańska KINETYKA INWERSJI SACHAROZY Wstęp teoretyczny Kataliza kwasowo-zasadowa Kataliza kwasowo-zasadowa
KOROZJA. Korozja kontaktowa z depolaryzacja tlenową 1
 KOROZJA Słowa kluczowe do ćwiczeń laboratoryjnych z korozji: korozja kontaktowa depolaryzacja tlenowa depolaryzacja wodorowa gęstość prądu korozyjnego natęŝenie prądu korozyjnego prawo Faradaya równowaŝnik
KOROZJA Słowa kluczowe do ćwiczeń laboratoryjnych z korozji: korozja kontaktowa depolaryzacja tlenowa depolaryzacja wodorowa gęstość prądu korozyjnego natęŝenie prądu korozyjnego prawo Faradaya równowaŝnik
Badanie kinetyki katalitycznego rozkładu H 2 O 2
 Badanie kinetyki katalitycznego rozkładu H 2 O 2 (opracowanie: Barbara Krajewska) Celem ćwiczenia jest zapoznanie się z prawami kinetyki chemicznej, sposobem wyznaczenia stałej szybkości i rzędu reakcji
Badanie kinetyki katalitycznego rozkładu H 2 O 2 (opracowanie: Barbara Krajewska) Celem ćwiczenia jest zapoznanie się z prawami kinetyki chemicznej, sposobem wyznaczenia stałej szybkości i rzędu reakcji
CHEMIA ŚRODKÓW BIOAKTYWNYCH I KOSMETYKÓW PRACOWNIA CHEMII ANALITYCZNEJ. Ćwiczenie 8. Argentometryczne oznaczanie chlorków metodą Fajansa
 CHEMIA ŚRODKÓW BIOAKTYWNYCH I KOSMETYKÓW PRACOWNIA CHEMII ANALITYCZNEJ Ćwiczenie 8 Argentometryczne oznaczanie chlorków metodą Fajansa Ćwiczenie obejmuje: 1. Oznaczenie miana roztworu AgNO 3 2. Oznaczenie
CHEMIA ŚRODKÓW BIOAKTYWNYCH I KOSMETYKÓW PRACOWNIA CHEMII ANALITYCZNEJ Ćwiczenie 8 Argentometryczne oznaczanie chlorków metodą Fajansa Ćwiczenie obejmuje: 1. Oznaczenie miana roztworu AgNO 3 2. Oznaczenie
Układy zdyspergowane. Wykład 6
 Układy zdyspergowane Wykład 6 Treśd Podwójna warstwa elektryczna Zjawiska elektrokinetyczne Potencjał zeta Nowoczesne metody oznaczania Stabilnośd dyspersji Stabilnośd dyspersji koloidalnej jest wypadkową
Układy zdyspergowane Wykład 6 Treśd Podwójna warstwa elektryczna Zjawiska elektrokinetyczne Potencjał zeta Nowoczesne metody oznaczania Stabilnośd dyspersji Stabilnośd dyspersji koloidalnej jest wypadkową
Ćwiczenie 1. Technika ważenia oraz wyznaczanie błędów pomiarowych. Ćwiczenie 2. Sprawdzanie pojemności pipety
 II. Wagi i ważenie. Roztwory. Emulsje i koloidy Zagadnienia Rodzaje wag laboratoryjnych i technika ważenia Niepewność pomiarowa. Błąd względny i bezwzględny Roztwory właściwe Stężenie procentowe i molowe.
II. Wagi i ważenie. Roztwory. Emulsje i koloidy Zagadnienia Rodzaje wag laboratoryjnych i technika ważenia Niepewność pomiarowa. Błąd względny i bezwzględny Roztwory właściwe Stężenie procentowe i molowe.
K02 Instrukcja wykonania ćwiczenia
 Katedra Chemii Fizycznej Uniwersytetu Łódzkiego K2 Instrukcja wykonania ćwiczenia Wyznaczanie krytycznego stężenia micelizacji (CMC) z pomiarów napięcia powierzchniowego Zakres zagadnień obowiązujących
Katedra Chemii Fizycznej Uniwersytetu Łódzkiego K2 Instrukcja wykonania ćwiczenia Wyznaczanie krytycznego stężenia micelizacji (CMC) z pomiarów napięcia powierzchniowego Zakres zagadnień obowiązujących
Opracował dr inż. Tadeusz Janiak
 Opracował dr inż. Tadeusz Janiak 1 Uwagi dla wykonujących ilościowe oznaczanie metodami spektrofotometrycznymi 3. 3.1. Ilościowe oznaczanie w metodach spektrofotometrycznych Ilościowe określenie zawartości
Opracował dr inż. Tadeusz Janiak 1 Uwagi dla wykonujących ilościowe oznaczanie metodami spektrofotometrycznymi 3. 3.1. Ilościowe oznaczanie w metodach spektrofotometrycznych Ilościowe określenie zawartości
Adsorpcja błękitu metylenowego na węglu aktywnym w obecności acetonu
 Adsorpcja błękitu metylenowego na węglu aktywnym w obecności acetonu Cel ćwiczenia Celem ćwiczenia jest zbadanie procesu adsorpcji barwnika z roztworu, wyznaczenie równania izotermy Freundlicha oraz wpływu
Adsorpcja błękitu metylenowego na węglu aktywnym w obecności acetonu Cel ćwiczenia Celem ćwiczenia jest zbadanie procesu adsorpcji barwnika z roztworu, wyznaczenie równania izotermy Freundlicha oraz wpływu
1. PRZYGOTOWANIE ROZTWORÓW KOMPLEKSUJĄCYCH
 1. PRZYGOTOWANIE ROZTWORÓW KOMPLEKSUJĄCYCH 1.1. przygotowanie 20 g 20% roztworu KSCN w wodzie destylowanej 1.1.1. odważenie 4 g stałego KSCN w stożkowej kolbie ze szlifem 1.1.2. odważenie 16 g wody destylowanej
1. PRZYGOTOWANIE ROZTWORÓW KOMPLEKSUJĄCYCH 1.1. przygotowanie 20 g 20% roztworu KSCN w wodzie destylowanej 1.1.1. odważenie 4 g stałego KSCN w stożkowej kolbie ze szlifem 1.1.2. odważenie 16 g wody destylowanej
Ćwiczenie 25. Piotr Skołuda OGNIWA STĘŻENIOWE
 Ćwiczenie 25 Piotr Skołuda OGNIWA STĘŻENIOWE Zagadnienia: Ogniwa stężeniowe z przenoszeniem i bez przenoszenia jonów. Ogniwa chemiczne, ze szczególnym uwzględnieniem ogniw wykorzystywanych w praktyce jako
Ćwiczenie 25 Piotr Skołuda OGNIWA STĘŻENIOWE Zagadnienia: Ogniwa stężeniowe z przenoszeniem i bez przenoszenia jonów. Ogniwa chemiczne, ze szczególnym uwzględnieniem ogniw wykorzystywanych w praktyce jako
KATALIZA I KINETYKA CHEMICZNA
 9 KATALIZA I KINETYKA CHEMICZNA CEL ĆWICZENIA Zapoznanie studenta z procesami katalitycznymi oraz wpływem stężenia, temperatury i obecności katalizatora na szybkość reakcji chemicznej. Zakres obowiązującego
9 KATALIZA I KINETYKA CHEMICZNA CEL ĆWICZENIA Zapoznanie studenta z procesami katalitycznymi oraz wpływem stężenia, temperatury i obecności katalizatora na szybkość reakcji chemicznej. Zakres obowiązującego
1.UKŁADY RÓWNAŃ LINIOWYCH
 UKŁADY RÓWNAŃ 1.UKŁADY RÓWNAŃ LINIOWYCH Układ: a1x + b1y = c1 a x + by = c nazywamy układem równań liniowych. Rozwiązaniem układu jest kaŝda para liczb spełniająca kaŝde z równań. Przy rozwiązywaniu układów
UKŁADY RÓWNAŃ 1.UKŁADY RÓWNAŃ LINIOWYCH Układ: a1x + b1y = c1 a x + by = c nazywamy układem równań liniowych. Rozwiązaniem układu jest kaŝda para liczb spełniająca kaŝde z równań. Przy rozwiązywaniu układów
KONDUKTOMETRIA. Konduktometria. Przewodnictwo elektrolityczne. Przewodnictwo elektrolityczne zaleŝy od:
 KONDUKTOMETRIA Konduktometria Metoda elektroanalityczna oparta na pomiarze przewodnictwa elektrolitycznego, którego wartość ulega zmianie wraz ze zmianą stęŝenia jonów zawartych w roztworze. Przewodnictwo
KONDUKTOMETRIA Konduktometria Metoda elektroanalityczna oparta na pomiarze przewodnictwa elektrolitycznego, którego wartość ulega zmianie wraz ze zmianą stęŝenia jonów zawartych w roztworze. Przewodnictwo
ĆWICZENIE 2. Usuwanie chromu (VI) z zastosowaniem wymieniaczy jonowych
 ĆWICZENIE 2 Usuwanie chromu (VI) z zastosowaniem wymieniaczy jonowych Część doświadczalna 1. Metody jonowymienne Do usuwania chromu (VI) można stosować między innymi wymieniacze jonowe. W wyniku przepuszczania
ĆWICZENIE 2 Usuwanie chromu (VI) z zastosowaniem wymieniaczy jonowych Część doświadczalna 1. Metody jonowymienne Do usuwania chromu (VI) można stosować między innymi wymieniacze jonowe. W wyniku przepuszczania
Sławomir Wysocki* wiertnictwo nafta gaz TOM 27 ZESZYT
 wiertnictwo nafta gaz TOM 27 ZESZYT 4 2010 Sławomir Wysocki* Flokulacja suspensji ilastych i Zasolonych płuczek wiertniczych z zastosowaniem nowo opracowanych flokulantów kationowych (PT-floc-201107)**
wiertnictwo nafta gaz TOM 27 ZESZYT 4 2010 Sławomir Wysocki* Flokulacja suspensji ilastych i Zasolonych płuczek wiertniczych z zastosowaniem nowo opracowanych flokulantów kationowych (PT-floc-201107)**
Katedra Chemii Fizycznej Uniwersytetu Łódzkiego. Wyznaczanie przewodnictwa granicznego mocnego elektrolitu
 Katedra Chemii Fizycznej Uniwersytetu Łódzkiego Wyznaczanie przewodnictwa granicznego mocnego elektrolitu Wyznaczanie stałej dysocjacji kwasu octowego poprzez pomiar przewodnictwa ćwiczenie nr 14 Opiekun
Katedra Chemii Fizycznej Uniwersytetu Łódzkiego Wyznaczanie przewodnictwa granicznego mocnego elektrolitu Wyznaczanie stałej dysocjacji kwasu octowego poprzez pomiar przewodnictwa ćwiczenie nr 14 Opiekun
Ćwiczenie M-2 Pomiar przyśpieszenia ziemskiego za pomocą wahadła rewersyjnego Cel ćwiczenia: II. Przyrządy: III. Literatura: IV. Wstęp. l Rys.
 Ćwiczenie M- Pomiar przyśpieszenia ziemskiego za pomocą wahadła rewersyjnego. Cel ćwiczenia: pomiar przyśpieszenia ziemskiego przy pomocy wahadła fizycznego.. Przyrządy: wahadło rewersyjne, elektroniczny
Ćwiczenie M- Pomiar przyśpieszenia ziemskiego za pomocą wahadła rewersyjnego. Cel ćwiczenia: pomiar przyśpieszenia ziemskiego przy pomocy wahadła fizycznego.. Przyrządy: wahadło rewersyjne, elektroniczny
Pracownia analizy ilościowej dla studentów II roku Chemii specjalność Chemia podstawowa i stosowana. Argentometryczne oznaczanie chlorków w mydłach
 Pracownia analizy ilościowej dla studentów II roku Chemii specjalność Chemia podstawowa i stosowana Argentometryczne oznaczanie chlorków w mydłach Ćwiczenie obejmuje: 1. Oznaczenie miana roztworu AgNO
Pracownia analizy ilościowej dla studentów II roku Chemii specjalność Chemia podstawowa i stosowana Argentometryczne oznaczanie chlorków w mydłach Ćwiczenie obejmuje: 1. Oznaczenie miana roztworu AgNO
VII. Elementy teorii stabilności. Funkcja Lapunowa. 1. Stabilność w sensie Lapunowa.
 VII. Elementy teorii stabilności. Funkcja Lapunowa. 1. Stabilność w sensie Lapunowa. W rozdziale tym zajmiemy się dokładniej badaniem stabilności rozwiązań równania różniczkowego. Pojęcie stabilności w
VII. Elementy teorii stabilności. Funkcja Lapunowa. 1. Stabilność w sensie Lapunowa. W rozdziale tym zajmiemy się dokładniej badaniem stabilności rozwiązań równania różniczkowego. Pojęcie stabilności w
CZAS I PRZESTRZEŃ EINSTEINA. Szczególna teoria względności. Spotkanie II ( marzec/kwiecień, 2013)
 CZAS I PRZESTRZEŃ EINSTEINA Szczególna teoria względności Spotkanie II ( marzec/kwiecień, 013) u Masa w szczególnej teorii względności u Określenie relatywistycznego pędu u Wyprowadzenie wzoru Einsteina
CZAS I PRZESTRZEŃ EINSTEINA Szczególna teoria względności Spotkanie II ( marzec/kwiecień, 013) u Masa w szczególnej teorii względności u Określenie relatywistycznego pędu u Wyprowadzenie wzoru Einsteina
Katedra Chemii Fizycznej Uniwersytetu Łódzkiego. Adsorpcja kwasu octowego na węglu aktywnym. opracowała dr hab. Małgorzata Jóźwiak
 Katedra Chemii Fizycznej Uniwersytetu Łódzkiego Adsorpcja kwasu octowego na węglu aktywnym opracowała dr hab. Małgorzata Jóźwiak ćwiczenie nr Zakres zagadnień obowiązujących do ćwiczenia 1. Charakterystyka
Katedra Chemii Fizycznej Uniwersytetu Łódzkiego Adsorpcja kwasu octowego na węglu aktywnym opracowała dr hab. Małgorzata Jóźwiak ćwiczenie nr Zakres zagadnień obowiązujących do ćwiczenia 1. Charakterystyka
PEHAMETRIA I ROZTWORY BUFOROWE
 4. PEHAMETRIA I ROZTWORY BUFOROWE 1. Sporządzanie i oznaczanie buforu octanowego Pehametria jest analizą instrumentalną, słuŝącą do potencjometrycznego bezpośredniego pomiaru wskaźnika stęŝenia jonów H
4. PEHAMETRIA I ROZTWORY BUFOROWE 1. Sporządzanie i oznaczanie buforu octanowego Pehametria jest analizą instrumentalną, słuŝącą do potencjometrycznego bezpośredniego pomiaru wskaźnika stęŝenia jonów H
K05 Instrukcja wykonania ćwiczenia
 Katedra Chemii Fizycznej Uniwersytetu Łódzkiego K05 Instrukcja wykonania ćwiczenia Wyznaczanie punktu izoelektrycznego żelatyny metodą wiskozymetryczną Zakres zagadnień obowiązujących do ćwiczenia 1. Układy
Katedra Chemii Fizycznej Uniwersytetu Łódzkiego K05 Instrukcja wykonania ćwiczenia Wyznaczanie punktu izoelektrycznego żelatyny metodą wiskozymetryczną Zakres zagadnień obowiązujących do ćwiczenia 1. Układy
cyklicznej woltamperometrii
 17. Badanie właściwości oksydacyjno-redukcyjnych kompleksów żelaza metodą cyklicznej woltamperometrii Jedną z częściej stosowanych w badaniach związków kompleksowych technik jest cykliczna woltamperometria.
17. Badanie właściwości oksydacyjno-redukcyjnych kompleksów żelaza metodą cyklicznej woltamperometrii Jedną z częściej stosowanych w badaniach związków kompleksowych technik jest cykliczna woltamperometria.
W zaleŝności od charakteru i ilości cząstek wyróŝniamy: a. opadanie cząstek ziarnistych, b. opadanie cząstek kłaczkowatych.
 BADANIE PROCESU SEDYMENTACJI Wstęp teoretyczny. Sedymentacja, to proces opadania cząstek ciała stałego w cieczy, w wyniku działania siły grawitacji lub sił bezwładności. Zaistnienie róŝnicy gęstości ciała
BADANIE PROCESU SEDYMENTACJI Wstęp teoretyczny. Sedymentacja, to proces opadania cząstek ciała stałego w cieczy, w wyniku działania siły grawitacji lub sił bezwładności. Zaistnienie róŝnicy gęstości ciała
KATALITYCZNE OZNACZANIE ŚLADÓW MIEDZI
 6 KATALITYCZNE OZNACZANIE ŚLADÓW MIEDZI CEL ĆWICZENIA Zapoznanie studenta z zagadnieniami katalizy homogenicznej i wykorzystanie reakcji tego typu do oznaczania śladowych ilości jonów Cu 2+. Zakres obowiązującego
6 KATALITYCZNE OZNACZANIE ŚLADÓW MIEDZI CEL ĆWICZENIA Zapoznanie studenta z zagadnieniami katalizy homogenicznej i wykorzystanie reakcji tego typu do oznaczania śladowych ilości jonów Cu 2+. Zakres obowiązującego
OZNACZANIE ZAWARTOŚCI MANGANU W GLEBIE
 OZNACZANIE ZAWARTOŚCI MANGANU W GLEBIE WPROWADZENIE Przyswajalność pierwiastków przez rośliny zależy od procesów zachodzących między fazą stałą i ciekłą gleby oraz korzeniami roślin. Pod względem stopnia
OZNACZANIE ZAWARTOŚCI MANGANU W GLEBIE WPROWADZENIE Przyswajalność pierwiastków przez rośliny zależy od procesów zachodzących między fazą stałą i ciekłą gleby oraz korzeniami roślin. Pod względem stopnia
Podstawy fizyki wykład 7
 Podstawy fizyki wykład 7 Dr Piotr Sitarek Katedra Fizyki Doświadczalnej, W11, PWr Drgania Drgania i fale Drgania harmoniczne Siła sprężysta Energia drgań Składanie drgań Drgania tłumione i wymuszone Fale
Podstawy fizyki wykład 7 Dr Piotr Sitarek Katedra Fizyki Doświadczalnej, W11, PWr Drgania Drgania i fale Drgania harmoniczne Siła sprężysta Energia drgań Składanie drgań Drgania tłumione i wymuszone Fale
WYZNACZANIE STAŁEJ SZYBKOŚCI REAKCJI I ENERGII AKTYWACJI
 Ćwiczenie nr 4 WYZNACZANIE STAŁEJ SZYBKOŚCI REAKCJI I ENERGII AKTYWACJI I. Cel ćwiczenia Celem ćwiczenia jest wyznaczenie stałej szybkości reakcji zmydlania estru etylowego w dwóch różnych temperaturach,
Ćwiczenie nr 4 WYZNACZANIE STAŁEJ SZYBKOŚCI REAKCJI I ENERGII AKTYWACJI I. Cel ćwiczenia Celem ćwiczenia jest wyznaczenie stałej szybkości reakcji zmydlania estru etylowego w dwóch różnych temperaturach,
Ćw. 2 Miareczkowanie potencjometryczne
 Ćw. 2 Miareczkowanie potencjometryczne Podstawy teoretyczne Miareczkowanie jest w analizie ilościowej jedną z najwaŝniejszych metod oznaczania stęŝenia związków chemicznych. Metoda ta polega na dodawaniu
Ćw. 2 Miareczkowanie potencjometryczne Podstawy teoretyczne Miareczkowanie jest w analizie ilościowej jedną z najwaŝniejszych metod oznaczania stęŝenia związków chemicznych. Metoda ta polega na dodawaniu
BADANIE PROMIENIOWANIA CIAŁA DOSKONALE CZARNEGO
 ZADANIE 9 BADANIE PROMIENIOWANIA CIAŁA DOSKONALE CZARNEGO Wstęp KaŜde ciało o temperaturze wyŝszej niŝ K promieniuje energię w postaci fal elektromagnetycznych. Widmowa zdolność emisyjną ciała o temperaturze
ZADANIE 9 BADANIE PROMIENIOWANIA CIAŁA DOSKONALE CZARNEGO Wstęp KaŜde ciało o temperaturze wyŝszej niŝ K promieniuje energię w postaci fal elektromagnetycznych. Widmowa zdolność emisyjną ciała o temperaturze
Pochodna i różniczka funkcji oraz jej zastosowanie do obliczania niepewności pomiarowych
 Pochodna i różniczka unkcji oraz jej zastosowanie do obliczania niepewności pomiarowych Krzyszto Rębilas DEFINICJA POCHODNEJ Pochodna unkcji () w punkcie określona jest jako granica: lim 0 Oznaczamy ją
Pochodna i różniczka unkcji oraz jej zastosowanie do obliczania niepewności pomiarowych Krzyszto Rębilas DEFINICJA POCHODNEJ Pochodna unkcji () w punkcie określona jest jako granica: lim 0 Oznaczamy ją
Kinetyka reakcji hydrolizy sacharozy katalizowanej przez inwertazę
 Kinetyka reakcji hydrolizy sacharozy katalizowanej przez inwertazę Prowadzący: dr hab. inż. Ilona WANDZIK mgr inż. Sebastian BUDNIOK mgr inż. Marta GREC mgr inż. Jadwiga PASZKOWSKA Miejsce ćwiczenia: sala
Kinetyka reakcji hydrolizy sacharozy katalizowanej przez inwertazę Prowadzący: dr hab. inż. Ilona WANDZIK mgr inż. Sebastian BUDNIOK mgr inż. Marta GREC mgr inż. Jadwiga PASZKOWSKA Miejsce ćwiczenia: sala
Ćwiczenie 5. Potencjał zeta, wyznaczanie punktu IEP. mgr Jacek Patkowski. Zakład Radiochemii i Chemii Koloidów UMCS
 Ćwiczenie 5 Potencjał zeta, wyznaczanie punktu IEP ćwiczenie opracowali: dr Małgorzata Paszkiewicz mgr Jacek Patkowski Zakład Radiochemii i Chemii Koloidów UMCS STRUKTURA PWE NA GRANICY FAZ TLENEK METALU/WODNY
Ćwiczenie 5 Potencjał zeta, wyznaczanie punktu IEP ćwiczenie opracowali: dr Małgorzata Paszkiewicz mgr Jacek Patkowski Zakład Radiochemii i Chemii Koloidów UMCS STRUKTURA PWE NA GRANICY FAZ TLENEK METALU/WODNY
Kinetyka. Kinetyka. Stawia dwa pytania: 1)Jak szybko biegną reakcje? 2) W jaki sposób przebiegają reakcje? energia swobodna, G. postęp reakcji.
 Kinetyka energia swobodna, G termodynamika stan 1 kinetyka termodynamika stan 2 postęp reakcji 1 Kinetyka Stawia dwa pytania: 1)Jak szybko biegną reakcje? 2) W jaki sposób przebiegają reakcje? 2 Jak szybko
Kinetyka energia swobodna, G termodynamika stan 1 kinetyka termodynamika stan 2 postęp reakcji 1 Kinetyka Stawia dwa pytania: 1)Jak szybko biegną reakcje? 2) W jaki sposób przebiegają reakcje? 2 Jak szybko
Ćwiczenie 7. Wyznaczanie stałej szybkości oraz parametrów termodynamicznych reakcji hydrolizy aspiryny.
 1 Ćwiczenie 7. Wyznaczanie stałej szybkości oraz parametrów termodynamicznych reakcji hydrolizy aspiryny. Chemiczna stabilność leków jest ważnym terapeutycznym problemem W przypadku chemicznej niestabilności
1 Ćwiczenie 7. Wyznaczanie stałej szybkości oraz parametrów termodynamicznych reakcji hydrolizy aspiryny. Chemiczna stabilność leków jest ważnym terapeutycznym problemem W przypadku chemicznej niestabilności
Ćwiczenie 42 WYZNACZANIE OGNISKOWEJ SOCZEWKI CIENKIEJ. Wprowadzenie teoretyczne.
 Ćwiczenie 4 WYZNACZANIE OGNISKOWEJ SOCZEWKI CIENKIEJ Wprowadzenie teoretyczne. Soczewka jest obiektem izycznym wykonanym z materiału przezroczystego o zadanym kształcie i symetrii obrotowej. Interesować
Ćwiczenie 4 WYZNACZANIE OGNISKOWEJ SOCZEWKI CIENKIEJ Wprowadzenie teoretyczne. Soczewka jest obiektem izycznym wykonanym z materiału przezroczystego o zadanym kształcie i symetrii obrotowej. Interesować
Kinetyka. energia swobodna, G. postęp reakcji. stan 1 stan 2. kinetyka
 Kinetyka postęp reakcji energia swobodna, G termodynamika kinetyka termodynamika stan 1 stan 2 Kinetyka Stawia dwa pytania: 1) Jak szybko biegną reakcje? 2) W jaki sposób przebiegają reakcje? 1) Jak szybko
Kinetyka postęp reakcji energia swobodna, G termodynamika kinetyka termodynamika stan 1 stan 2 Kinetyka Stawia dwa pytania: 1) Jak szybko biegną reakcje? 2) W jaki sposób przebiegają reakcje? 1) Jak szybko
ĆWICZENIE 13 TEORIA BŁĘDÓW POMIAROWYCH
 ĆWICZENIE 13 TEORIA BŁĘDÓW POMIAROWYCH Pomiary (definicja, skale pomiarowe, pomiary proste, złożone, zliczenia). Błędy ( definicja, rodzaje błędów, błąd maksymalny i przypadkowy,). Rachunek błędów Sposoby
ĆWICZENIE 13 TEORIA BŁĘDÓW POMIAROWYCH Pomiary (definicja, skale pomiarowe, pomiary proste, złożone, zliczenia). Błędy ( definicja, rodzaje błędów, błąd maksymalny i przypadkowy,). Rachunek błędów Sposoby
1. za pomocą pomiaru SEM (siła elektromotoryczna róŝnica potencjałów dwóch elektrod) i na podstawie wzoru wyznaczenie stęŝenia,
 Potencjometria Potencjometria instrumentalna metoda analityczna, wykorzystująca zaleŝność pomiędzy potencjałem elektrody wzorcowej, a aktywnością jonów lub cząstek w badanym roztworze (elektrody wskaźnikowej).
Potencjometria Potencjometria instrumentalna metoda analityczna, wykorzystująca zaleŝność pomiędzy potencjałem elektrody wzorcowej, a aktywnością jonów lub cząstek w badanym roztworze (elektrody wskaźnikowej).
Skręcenie wektora polaryzacji w ośrodku optycznie czynnym
 WFiIS PRACOWNIA FIZYCZNA I i II Imię i nazwisko: 1.. TEMAT: ROK GRUPA ZESPÓŁ NR ĆWICZENIA ata wykonania: ata oddania: Zwrot do poprawy: ata oddania: ata zliczenia: OCENA Cel ćwiczenia: Celem ćwiczenia
WFiIS PRACOWNIA FIZYCZNA I i II Imię i nazwisko: 1.. TEMAT: ROK GRUPA ZESPÓŁ NR ĆWICZENIA ata wykonania: ata oddania: Zwrot do poprawy: ata oddania: ata zliczenia: OCENA Cel ćwiczenia: Celem ćwiczenia
Elektrostatyka ŁADUNEK. Ładunek elektryczny. Dr PPotera wyklady fizyka dosw st podypl. n p. Cząstka α
 Elektrostatyka ŁADUNEK elektron: -e = -1.610-19 C proton: e = 1.610-19 C neutron: 0 C n p p n Cząstka α Ładunek elektryczny Ładunek jest skwantowany: Jednostką ładunku elektrycznego w układzie SI jest
Elektrostatyka ŁADUNEK elektron: -e = -1.610-19 C proton: e = 1.610-19 C neutron: 0 C n p p n Cząstka α Ładunek elektryczny Ładunek jest skwantowany: Jednostką ładunku elektrycznego w układzie SI jest
UKŁADY KONDENSATOROWE
 UKŁADY KONDENSATOROWE 3.1. Wyprowadzić wzory na: a) pojemność kondensatora sferycznego z izolacją jednorodną (ε), b) pojemność kondensatora sferycznego z izolacją warstwową (ε 1, ε 2 ) c) pojemność odosobnionej
UKŁADY KONDENSATOROWE 3.1. Wyprowadzić wzory na: a) pojemność kondensatora sferycznego z izolacją jednorodną (ε), b) pojemność kondensatora sferycznego z izolacją warstwową (ε 1, ε 2 ) c) pojemność odosobnionej
HYDROLIZA SOLI. ROZTWORY BUFOROWE
 Ćwiczenie 9 semestr 2 HYDROLIZA SOLI. ROZTWORY BUFOROWE Obowiązujące zagadnienia: Hydroliza soli-anionowa, kationowa, teoria jonowa Arrheniusa, moc kwasów i zasad, równania hydrolizy soli, hydroliza wieloetapowa,
Ćwiczenie 9 semestr 2 HYDROLIZA SOLI. ROZTWORY BUFOROWE Obowiązujące zagadnienia: Hydroliza soli-anionowa, kationowa, teoria jonowa Arrheniusa, moc kwasów i zasad, równania hydrolizy soli, hydroliza wieloetapowa,
A4.04 Instrukcja wykonania ćwiczenia
 Katedra Chemii Fizycznej Uniwersytetu Łódzkiego A4.04 Instrukcja wykonania ćwiczenia Wyznaczanie cząstkowych molowych objętości wody i alkoholu Zakres zagadnień obowiązujących do ćwiczenia 1. Znajomość
Katedra Chemii Fizycznej Uniwersytetu Łódzkiego A4.04 Instrukcja wykonania ćwiczenia Wyznaczanie cząstkowych molowych objętości wody i alkoholu Zakres zagadnień obowiązujących do ćwiczenia 1. Znajomość
Wyznaczanie modułu sztywności metodą Gaussa
 Ćwiczenie M13 Wyznaczanie modułu sztywności metodą Gaussa M13.1. Cel ćwiczenia Celem ćwiczenia jest wyznaczenie wartości modułu sztywności stali metodą dynamiczną Gaussa. M13.2. Zagadnienia związane z
Ćwiczenie M13 Wyznaczanie modułu sztywności metodą Gaussa M13.1. Cel ćwiczenia Celem ćwiczenia jest wyznaczenie wartości modułu sztywności stali metodą dynamiczną Gaussa. M13.2. Zagadnienia związane z
Definicja pochodnej cząstkowej
 1 z 8 gdzie punkt wewnętrzny Definicja pochodnej cząstkowej JeŜeli iloraz ma granicę dla to granicę tę nazywamy pochodną cząstkową funkcji względem w punkcie. Oznaczenia: Pochodną cząstkową funkcji względem
1 z 8 gdzie punkt wewnętrzny Definicja pochodnej cząstkowej JeŜeli iloraz ma granicę dla to granicę tę nazywamy pochodną cząstkową funkcji względem w punkcie. Oznaczenia: Pochodną cząstkową funkcji względem
POLITECHNIKA WARSZAWSKA WYDZIAŁ ELEKTRYCZNY. PRACOWNIA MATERIAŁOZNAWSTWA ELEKTROTECHNICZNEGO KWNiAE
 POLITECHNIK WRSZWSK WYDZIŁ ELEKTRYCZNY PRCOWNI MTERIŁOZNWSTW ELEKTROTECHNICZNEGO KWNiE ĆWICZENIE 11 WYZNCZNIE ELEKTROCHEMICZNEGO RÓWNOWśNIK MIEDZI ORZ STŁEJ FRDY 1. Elektrolity i przewodnictwo jonowe Ogólnie
POLITECHNIK WRSZWSK WYDZIŁ ELEKTRYCZNY PRCOWNI MTERIŁOZNWSTW ELEKTROTECHNICZNEGO KWNiE ĆWICZENIE 11 WYZNCZNIE ELEKTROCHEMICZNEGO RÓWNOWśNIK MIEDZI ORZ STŁEJ FRDY 1. Elektrolity i przewodnictwo jonowe Ogólnie
CZYNNIKI WPŁYWAJĄCE NA SZYBKOŚĆ REAKCJI CHEMICZNYCH. ILOŚCIOWE ZBADANIE SZYBKOŚCI ROZPADU NADTLENKU WODORU.
 CZYNNIKI WPŁYWAJĄCE NA SZYBKOŚĆ REAKCJI CHEMICZNYCH. ILOŚCIOWE ZBADANIE SZYBKOŚCI ROZPADU NADTLENKU WODORU. Projekt zrealizowany w ramach Mazowieckiego programu stypendialnego dla uczniów szczególnie uzdolnionych
CZYNNIKI WPŁYWAJĄCE NA SZYBKOŚĆ REAKCJI CHEMICZNYCH. ILOŚCIOWE ZBADANIE SZYBKOŚCI ROZPADU NADTLENKU WODORU. Projekt zrealizowany w ramach Mazowieckiego programu stypendialnego dla uczniów szczególnie uzdolnionych
LABORATORIUM Z PODSTAW BIOFIZYKI ĆWICZENIE NR 4 1. CEL ĆWICZENIA
 1. CEL ĆWICZENIA Pomiar potencjału dyfuzyjnego roztworów o różnych stężeniach jonów oddzielonych membranami: półprzepuszczalną i jonoselektywną w funkcji ich stężenia. Wykorzystanie równania Nernsta do
1. CEL ĆWICZENIA Pomiar potencjału dyfuzyjnego roztworów o różnych stężeniach jonów oddzielonych membranami: półprzepuszczalną i jonoselektywną w funkcji ich stężenia. Wykorzystanie równania Nernsta do
Spektrofotometryczne wyznaczanie stałej dysocjacji czerwieni fenolowej
 Spektrofotometryczne wyznaczanie stałej dysocjacji czerwieni fenolowej Metoda: Spektrofotometria UV-Vis Cel ćwiczenia: Celem ćwiczenia jest zapoznanie studenta z fotometryczną metodą badania stanów równowagi
Spektrofotometryczne wyznaczanie stałej dysocjacji czerwieni fenolowej Metoda: Spektrofotometria UV-Vis Cel ćwiczenia: Celem ćwiczenia jest zapoznanie studenta z fotometryczną metodą badania stanów równowagi
Wyznaczanie współczynnika sprężystości sprężyn i ich układów
 Ćwiczenie 63 Wyznaczanie współczynnika sprężystości sprężyn i ich układów 63.1. Zasada ćwiczenia W ćwiczeniu określa się współczynnik sprężystości pojedynczych sprężyn i ich układów, mierząc wydłużenie
Ćwiczenie 63 Wyznaczanie współczynnika sprężystości sprężyn i ich układów 63.1. Zasada ćwiczenia W ćwiczeniu określa się współczynnik sprężystości pojedynczych sprężyn i ich układów, mierząc wydłużenie
GRAWITACYJNE ZAGĘSZCZANIE OSADÓW
 GRAWITACYJNE ZAGĘSZCZANIE OSADÓW Ćwiczenie nr 4 1. CHARAKTERYSTYKA PROCESU Ze względu na wysokie uwodnienie oraz niewielką ilość suchej masy, osady powstające w oczyszczalni ścieków należy poddawać procesowi
GRAWITACYJNE ZAGĘSZCZANIE OSADÓW Ćwiczenie nr 4 1. CHARAKTERYSTYKA PROCESU Ze względu na wysokie uwodnienie oraz niewielką ilość suchej masy, osady powstające w oczyszczalni ścieków należy poddawać procesowi
3. Badanie kinetyki enzymów
 3. Badanie kinetyki enzymów Przy stałym stężeniu enzymu, a przy zmieniającym się początkowym stężeniu substratu, zmiany szybkości reakcji katalizy, wyrażonej jako liczba moli substratu przetworzonego w
3. Badanie kinetyki enzymów Przy stałym stężeniu enzymu, a przy zmieniającym się początkowym stężeniu substratu, zmiany szybkości reakcji katalizy, wyrażonej jako liczba moli substratu przetworzonego w
KINETYKA REAKCJI ENZYMATYCZNYCH
 ĆWICZENIE 8 KINETYKA REAKCJI ENZYMATYCZNYCH Wyznaczanie stałej Michaelisa i szybkości maksymalnej reakcji utleniania gwajakolu przez H 2 2, katalizowanej przez peroksydazę chrzanową. Badanie wpływu siarczanu
ĆWICZENIE 8 KINETYKA REAKCJI ENZYMATYCZNYCH Wyznaczanie stałej Michaelisa i szybkości maksymalnej reakcji utleniania gwajakolu przez H 2 2, katalizowanej przez peroksydazę chrzanową. Badanie wpływu siarczanu
Podstawy i ogólne zasady pracy w laboratorium. Analiza miareczkowa.
 Podstawy i ogólne zasady pracy w laboratorium. Analiza miareczkowa. Celem ćwiczenia jest: - zapoznanie się z zasadami BHP obowiązującymi w laboratorium chemicznym - zapoznanie się z wyposaŝeniem i sposobami
Podstawy i ogólne zasady pracy w laboratorium. Analiza miareczkowa. Celem ćwiczenia jest: - zapoznanie się z zasadami BHP obowiązującymi w laboratorium chemicznym - zapoznanie się z wyposaŝeniem i sposobami
Doświadczenie nr 7. Określenie średniego czasu życia mionu.
 Doświadczenie nr 7 Określenie średniego czasu życia mionu. Teleskop licznikowy Układ elektroniczny 1. Student winien wykazać się znajomością następujących zagadnień: 1. Promieniowanie kosmiczne wpływ ziemskiego
Doświadczenie nr 7 Określenie średniego czasu życia mionu. Teleskop licznikowy Układ elektroniczny 1. Student winien wykazać się znajomością następujących zagadnień: 1. Promieniowanie kosmiczne wpływ ziemskiego
