Test immunofluorescencji pośredniej dla bakterii patogenicznych dla roślin
|
|
|
- Piotr Krawczyk
- 7 lat temu
- Przeglądów:
Transkrypt
1 Europejska i Śródziemnomorska Organizacja Ochrony Roślin PM 7/97(1) Organisation Européenne et Méditerranéenne pour la Protection des Plantem Diagnostyka Diagnostics Test immunofluorescencji pośredniej dla bakterii patogenicznych dla roślin Zakres Standard ten opisuje w jaki sposób wykonać test immunofluorescencji pośredniej (IF) dla bakterii patogenicznych dla roślin 1. Zatwierdzenie i nowelizacja Zatwierdzono jako Standard EPPO W Załączniku 1 zawarto instrukcję wykonania testu IF. Do wykonania testu należy użyć zwalidowanych przeciwciał lub surowicy przeciw poszukiwanemu organizmowi. Laboratorium zobowiązane jest do wykonania walidacji w przypadku gdy dane dotyczące walidacji nie zostały dostarczone przez dostawcę odczynnika. Miano surowicy/przeciwciał należy określić dla każdej partii odczynnika. Zgodnie z zaleceniami producenta miano określa się jako najwyższe rozcieńczenie przy którym występuje optymalna reakcja podczas badania zawiesiny szczepu referencyjnego poszukiwanego organizmu zawierającej komórek bakterii na mililitr przy użyciu odpowiedniego rozcieńczenia koniugatu znakowanego barwnikiem fluorescencyjnym (np. fluoresceiną lub rodaminą). Zalecany szczep referencyjny powinien być homologiczny ze szczepem wykorzystanym do produkcji surowicy/przeciwciał. Nie rozcieńczone surowice poliklonalne powinny, jeśli to jest możliwe, mieć minimalne miano o wartości Do testów rutynowych należy używać rozcieńczeń roboczych surowicy/przeciwciał (RR), które osiągają wartość bliską lub równą wartości miana. W celu wykrycia poszukiwanego organizmu należy zastosować test IF na świeżo przygotowanym ekstrakcie próbki. W celu dokonania identyfikacji bakterii test IF należy przeprowadzić na zawiesinie wyizolowanej czystej kultury. W razie konieczności test IF można w zadawalający sposób wykonać na ekstrakcie z dodatkiem glicerolu (10 25% obj./obj.) przechowywanym w temperaturze poniżej -68 C. Glicerol można usunąć z ekstraktu poprzez dodanie i wymieszanie z taką samą ilością buforu do zawieszania osadu w stosunku do ilości ekstraktu (Załącznik 2), a następnie odwirowanie przez 15 minut z przyśpieszeniem 7000 g i zawieszenie osadu w takiej samej ilości buforu do zawieszania osadu jaką stanowił początkowo uzyskany ekstrakt. Szkiełka mikroskopowe zawierające kontrole należy przygotować oddzielnie, zgodnie z Załącznikiem 3. Kontrolę surowicy/przeciwciał (= kontrola pozytywna) należy przygotować z wykorzystaniem izolatu homologicznego lub innego izolatu referencyjnego poszukiwanego organizmu zawieszonego w ekstrakcie próbki, która wcześniej została uznana za wolną od poszukiwanego organizmu. Opcjonalnie można przygotować zgodnie z Załącznikiem 3 zawiesinę komórek w buforze do zawieszania osadu. W tym celu należy 1 Użycie w tym standardzie EPPO nazw firm produkujących odczynniki lub wyposażenie nie sugeruje wyłączności ich zastosowania, gdyż inne odczynniki również mogą zostać zastosowane OEPP/EPP0,Bulletin OEPP/EPP0 Bulletin 39,
2 użyć zamrożone lub zliofilizowane ekstrakty skontaminowane wybranym izolatem. Jeśli to jest możliwe należy użyć na tym samym szkiełku mikroskopowym jako dodatkową kontrolę pozytywną zliofilizowany lub zamrożony w temperaturze -16 C ekstrakt pochodzący z naturalnie zainfekowanej tkanki. Pozwoli to na obserwację w ekstrakcie porażonym w sposób naturalny morfologii komórek bakterii, która może różnić się znacznie od morfologii komórek pochodzących z podłoża hodowlanego, które zostały wykorzystane do sztucznej kontaminacji. Zawiesinę ekstraktu próbki, w której nie stwierdzono obecności poszukiwanego organizmu należy użyć jako kontroli dla testu IF (= kontrola negatywna) (Załącznik 3). Test IF można zastosować także w celu dokonania identyfikacji czystych kultur podejrzanych izolatów bakterii. W tym celu należy przygotować i użyć zawiesinę bakterii o gęstości 10 6 komórek na mililitr buforu do testu IF (Załącznik 2). Podziękowanie Opis testu IF został opracowany przez P. Muller (JKI, DE), J. Janse (Dutch General Inspection Service, NL) na podstawie Dyrektywy Rady UE dotyczącej zwalczania Ralstonia solanacearum (UE, 1998) oraz Dyrektywy Komisji 2006/63/WE z 14 lipca 2006 zmieniającej Załączniki II do VII do Dyrektywy Rady 98/57/WE dotyczącej zwalczania Ralstonia solanacearum (Smith) Yabuuchi et al.; Dziennik Urzędowy Wspólnoty Europejskiej (UE, 2006). Materiały źródłowe UE (1998) Derektywa Rady 98/57/WE z 20 lipca 1998 dotycząca zwalczania Ralstonia solanacearum Załącznik II schemat badania diagnostycznego, wykrywania oraz identyfikacji Ralstonia solanacearum (Smith) Yabuuchi et al.; Dziennik Urzędowy Wspólnoty Europejskiej nr L235, UE (2006) Dyrektywa Komisji 2006/63/WE z 14 lipca 2006 zmieniająca Załączniki II do VII do Dyrektywy Rady 98/57/WE dotyczącej zwalczania Ralstonia solanacearum (Smith) Yabuuchi et al.; Dziennik Urzędowy Wspólnoty Europejskiej nr L206, Załącznik 1 Instrukcja wykonania testu IF Do testów IF należy użyć wielopunktowych szkiełek mikroskopowych najlepiej z 10 okienkami o średnicy co najmniej 6 mm. Materiał kontrolny należy traktować w taki sam sposób jak próbkę (próbki). 1. Przygotowanie szkiełek Przygotować szkiełka testowe według jednej z następujących procedur. 1.1 Dla ekstraktów roślinnych uzyskanych z próbek zawierających stosunkowo małą ilość osadu skrobi/ zanieczyszczeń: Za pomocą pipety nanieść standardową objętość (objętość 15 µl jest odpowiednia dla szkiełka o średnicy okienka 6 mm należy zwiększyć objętość dla szkiełek o większej średnicy okienek) rozcieńczenia ekstraktu próbki w stosunku 1:100 na pierwsze okienko szkiełka do IF. Następnie na pozostałe okienka w tym samym rzędzie nanieść za pomocą pipety taką samą objętość nie rozcieńczonego ekstraktu próbki (1:1). Drugi rząd może zostać wykorzystany dla powtórzenia próbki lub dla innej próbki 2 jak to przedstawiono na rys. 1A. 2 Należy zwrócić uwagę aby nie doszło do kontaminacji próbek 2009 OEPP/EPP0,Bulletin OEPP/EPP0 Bulletin 39,
3 1.2 Dla innych ekstraktów próbek: Należy przygotować dziesięciokrotne rozcieńczenia (1:10, 1:100) ekstraktu roślinnego w buforze do zawieszania osadu. Za pomocą pipety nanieść standardową objętość (objętość 15 µl jest odpowiednia dla szkiełka o średnicy okienka 6 mm należy zwiększyć objętość dla szkiełek o większej średnicy okienek) ekstraktu próbki oraz każdego z rozcieńczeń na poszczególne okienka w rzędzie szkiełka mikroskopowego. Drugi rząd może zostać wykorzystany dla powtórzenia próbki lub dla innej próbki jak to przedstawiono na rys. 1B. 2. Utrwalanie komórek bakterii Wysuszyć krople w temperaturze otoczenia lub poprzez ogrzewanie (temperatura maksymalna 45 C). Utrwalić komórki bakterii na szkiełku przez opalenie szkiełek albo ogrzewanie preparatów (15 minut w temperaturze maksimum 60 C) lub przez pokrycie okienek szkiełka etanolem (>95%) przez 3 minuty lub zgodnie ze szczegółową instrukcją dołączoną przez dostawcę przeciwciał. Szkiełka należy poddać dalszemu badaniu tak szybko jak to możliwe lub jeśli to konieczne utrwalone szkiełka można przechowywać w suchym pojemniku w stanie zamrożonym (maksymalnie do 3 miesięcy) przed dalszym badaniem. A B Rys. 1 (A) Rozcieńczenia ekstraktu próbki, naniesione na szkiełko testowe zgodnie z punktem 1.1 i 3.1. (B) Rozcieńczenie robocze surowicy/przeciwciał naniesione na szkiełko testowe zgodnie z punktem 1.2 i Procedura IF 3.1 W zależności od sposobu przygotowania szkiełek testowych punkt 1.1 Przygotować zestaw dwukrotnych rozcieńczeń przeciwciał w buforze do testu IF (Załącznik 2). Pierwsze rozcieńczenie powinno mieć wartość ½ miana (T/2), a pozostałe odpowiednio: ¼ miana (T/4), ½ miana (T/2), miano (T) i podwójna wartość miana (2T) (T=miano) OEPP/EPP0,Bulletin OEPP/EPP0 Bulletin 39,
4 3.2 Przygotowanie szkiełek testowych zgodnie z punktem 1.2: Przygotować rozcieńczenie robocze (RR) przeciwciał (bliskie lub równe mianu) w buforze do IF (Załącznik 2). 3.3 Umieścić szkiełka na wilgotnej bibule. Pokryć całkowicie wszystkie okienka szkiełka testowego rozcieńczonymi przeciwciałami. Objętość przeciwciał naniesiona na każde z okienek szkiełka powinna odpowiadać co najmniej objętości naniesionego ekstraktu. Etap ten należy przeprowadzić w przypadku braku szczegółowej instrukcji od dostawcy przeciwciał. 3.4 Inkubować szkiełka na wilgotnej bibule pod przykryciem przez 30 minut (±10 min) w temperaturze otoczenia (18-25 C). 3.5 Strzepnąć krople z każdego szkiełka i płukać ostrożnie w buforze do IF. Płukać szkiełka poprzez zanurzenie przez około 5 minut w buforze do IF z dodatkiem Tween (Załącznik 2), a następnie w buforze do IF bez dodatku Tween. Unikać powstawania aerozolu lub przeniesienia kropli, co może spowodować kontaminację. Usunąć delikatnie nadmiar wilgoci za pomocą bibuły. 3.6 Umieścić szkiełka na wilgotnej bibule. Przykryć okienka szkiełka rozcieńczonym koniugatem FITC wykorzystywanym do określenia miana. Objętość koniugatu naniesiona na okienka szkiełka powinna odpowiadać co najmniej objętości naniesionych przeciwciał. 3.7 Inkubować szkiełka na wilgotnej bibule pod przykryciem przez 30 minut (±10 min) w temperaturze otoczenia (18-25 C). 3.8 Strzepnąć ze szkiełka krople koniugatu. Zanurzyć szkiełka i płukać jak poprzednio (3.5). Usunąć delikatnie nadmiar wilgoci za pomocą bibuły. 3.9 Za pomocą pipety nanieść na każde okienko szkiełka 5 µl 10 µl 0,1 M buforu fosforanowo-glicerynowego (Załącznik 2) lub innego dostępnego w handlu utrwalacza albo nanieść odpowiednią ilość w poprzek szkiełka i przykryć je szkiełkiem nakrywkowym unikając nadmiernej ekspozycji szkiełka na świetle. 4. Odczytywanie testu IF 4.1 Sprawdzić szkiełka pod mikroskopem epifluorescencyjnym z filtrem i źródłem światła właściwym dla wzbudzenia FITC, pod olejem, glicerolem lub wodą immersyjną przy powiększeniu razy. Okienka przeglądać wzdłuż dwóch średnic i dookoła obwodu okienka. Sprawdzić przynajmniej 40 pól mikroskopowych w przypadku próbek nie zawierających komórek lub zawierających ich małą ilość. Sprawdzić najpierw szkiełko z kontrolą pozytywną. Komórki muszą fluoryzować jasno, a ściany komórkowe muszą być całkowicie wybarwione przy określonym mianie przeciwciał lub rozcieńczeniu roboczym. Test IF należy powtórzyć jeśli wybarwienie nie jest właściwe OEPP/EPP0,Bulletin OEPP/EPP0 Bulletin 39,
5 4.2 Poszukiwać w okienkach szkiełek testowych jaskrawo fluoryzujących komórek o charakterystycznej morfologii dla poszukiwanego organizmu. Intensywność fluorescencji przy tym samym rozcieńczeniu surowicy musi być równoważna intensywności wykazywanej przez szczep wykorzystany w kontroli pozytywnej. Komórki niecałkowicie wybarwione lub komórki o słabej fluorescencji należy odrzucić. W przypadku podejrzenia wystąpienia kontaminacji test należy powtórzyć. W przypadku gdy wszystkie szkiełka w badanej partii wykazują obecność pozytywnych komórek lub gdy pozytywne komórki znajdują się na szkiełku nakrywkowym (na zewnątrz okienek szkiełka mikroskopowego) można podejrzewać kontaminację buforu. 4.3 Istnieje kilka problemów wynikających ze specyfiki testu immunofluorescencji. W przypadku próbek roślinnych oraz próbek nasion można obserwować w tle obecność fluoryzujących komórek o nietypowej morfologii, jak również krzyżowo reagujące bakterie saprofityczne posiadające wymiary i morfologię podobne do wymiarów i morfologii poszukiwanego organizmu. 4.4 Uwzględnić wyłącznie fluoryzujące komórki o typowym rozmiarze i morfologii przy określonym mianie surowicy/przeciwciał lub rozcieńczeniu roboczym. 5. Interpretacja wyników testu IF Test IF należy uznać za pozytywny jeśli w zawiesinie osadu lub w ekstrakcie próbki zostaną wykryte fluoryzujące komórki o typowej morfologii. Jednakże w przypadku próbki porażonej w sposób utajony w żadnym wypadku nie można wydać miarodajnego wyniku na podstawie jedynie pozytywnego wyniku testu IF. Pozytywny wynik testu IF jedynie sugeruje podejrzenie wystąpienia poszukiwanego organizmu w próbce. W celu potwierdzenia lub odrzucenia wyników testu IF zawiesina osadu lub ekstrakt próbki wymagają dalszych badań z wykorzystaniem innych testów. Próg wykrywalności dla testu IF mieści się zwykle pomiędzy komórek na mililitr zawiesiny osadu lub ekstraktu próbki. Zwykle pozytywne wyniki testu IF dla progu wykrywalności są powodowane przez reakcje krzyżowe komórek bakterii. W przypadku porażenia utajonego należy najpierw starannie obliczyć poziom porażenia dla progu wykrywalności. W przypadku gdy test IF jest na poziomie progu wykrywalności może on zostać uznany za pozytywny i jest wówczas wymagana ocena eksperta w celu podjęcia decyzji jakie dalsze analizy należy wykonać. Należy podkreślić że określenie liczby komórek bakterii jest wymagane w przypadku wykrycia obecności poszukiwanego organizmu w próbkach porażonych w formie utajonej, natomiast nie jest wymagane w przypadku zastosowania testu IF dla zawiesiny czystych kultur lub ekstraktów zainfekowanej tkanki rośliny żywicielskiej (jako próbki lub jako kontrole) OEPP/EPP0,Bulletin OEPP/EPP0 Bulletin 39,
6 6. Określenie poziomu porażenia w teście IF 6.1 Obliczyć średnią ilość typowych, fluoryzujących komórek przypadających na jedno pole widzenia (c). 6.2 Obliczyć ilość typowych fluoryzujących komórek przypadających na jedno okienko szkiełka mikroskopowego (C). Gdzie S= powierzchnia okienka szkiełka wielopunktowego, a s = powierzchnia pola obiektywu. Gdzie i = współczynnik pola (wahający się od 8 do 24 w zależności od typu okularu), K = współczynnik tubusu (1 lub 1,25), G = powiększenie obiektywu (100x, 40x itd.). 6.3 Obliczyć ilość typowych fluoryzujących komórek przypadających na mililitr zawieszonego osadu (N) Gdzie y = objętość zawieszonego osadu umieszczonego na każdym okienku, a F = współczynnik rozcieńczenia zawieszonego osadu. Załącznik 2 Bufory Bufor do zawieszania (10 mm bufor fosforanowy, ph 7,2) Bufor ten wykorzystywany jest zarówno do zawieszania skoncentrowanego poprzez wcześniejsze odwirowanie osadu ekstraktu próbki jaki i do wykonania dalszych rozcieńczeń próbki. Na 2 HPO 4 x12h 2 O NaH 2 PO 4 x2h 2 O Woda destylowana 2,7 g 0,4 g 1,0 l Składniki rozpuścić, sprawdzić ph i wysterylizować poprzez autoklawowanie w temp. 121 C przez 15 min. Bufor do IF [10 mm bufor fosforanowy z dodatkiem soli (PBS), ph 7,2] Bufor ten wykorzystywany jest do rozcieńczania przeciwciał Na 2 HPO 4 x12h 2 O 2,7 g 2009 OEPP/EPP0,Bulletin OEPP/EPP0 Bulletin 39,
7 NaH 2 PO 4 x2h 2 O NaCl Woda destylowana 0,4 g 8,0 g 1,0 l Składniki rozpuścić, sprawdzić ph i wysterylizować poprzez autoklawowanie w temp. 121 C przez 15 min. Bufor do IF z dodatkiem Tween Bufor ten wykorzystywany jest do płukania szkiełek mikroskopowych. Dodać 0,1% Tween 20 do buforu do IF. Bufor fosforanowo -glicerynowy, ph 7,6 Bufor ten wykorzystywany jest jako utrwalacz, który po naniesieniu na okienka szkiełek do IF wzmacnia fluorescencję. Na 2 HPO 4 x12h 2 O NaH 2 PO 4 x2h 2 O Glicerol Woda destylowana 3,2 g 0,15 g 50 ml 100 ml Roztwór utrwalacza przeciwdziałający wyświecaniu się fluorescencji jest dostępny w handlu pod nazwą Vectashield (Vector Laboratories, Peterborough, Wielka Brytania) lub Citifluor (Leica, Karlsruhe, Niemcy). Załącznik 3 Przygotowanie ekstraktów i szkiełek kontroli pozytywnej i negatywnej. Przygotować osobno szkiełka kontroli pozytywnej przy użyciu szczepu homologicznego lub innego szczepu referencyjnego poszukiwanego organizmu zawieszając go w ekstrakcie roślinnym, jak to przedstawiono poniżej lub opcjonalnie w buforze. Jeśli to jest możliwe należy na tym samym szkiełku użyć jako kontroli pozytywnej naturalnie zainfekowanej tkanki (przechowywanej w formie zliofilizoawnej lub zamrożonej w temperaturze poniżej 16 C). Jako kontrolę negatywną użyć należy ekstraktu próbki, która wcześniej w badaniach została uznana za wolną od poszukiwanego organizmu. Zaleca się używania szczepów referencyjnych jako kontroli pozytywnej lub podczas optymalizacji testów, w celu uniknięcia błędnej interpretacji z powodu reakcji krzyżowych. Szczepy referencyjne są dostępne w handlu z następujących kolekcji: a. National Collection of Plant Pathogenic Bacteria (NCPPB), Central Science Laboratory, York (Wielka Brytania) 2009 OEPP/EPP0,Bulletin OEPP/EPP0 Bulletin 39,
8 b. Culture Collection of the Plant Protection Service (PD), Wageningen (Holandia). c.collection Française de Bactéries Phytopathogènes (CFBP), INRA Station Phytobactériologie, Angers (Francja). 1. W celu otrzymania zawiesiny komórek bakterii w buforze do zawieszania o gęstości około 10 8 komórek na mililitr należy przeprowadzić hodowlę wirulentnego szczepu poszukiwanego organizmu poprzez inkubację szczepu przez określony czas (najczęściej 48 godzin) na Agarze Odżywczym (NA) lub innym odpowiednim podłożu (Załącznik 2). Można to otrzymać przygotowując słabo gęstą zawiesinę odpowiadającą optycznej gęstości około 0,15 przy długości fali 600 nm. Przygotować materiał roślinny, uznany za wolny od poszukiwanego organizmu w wyniku przeprowadzonych wcześniej testów i zawiesić osad w 10 ml buforu do zawieszania osadu (Załącznik2). 2. Przygotować 10 sterylnych mikroprobówek o pojemności 1,5 ml zawierających po 900 µl zawieszonego osadu (po odwirowaniu lub ekstraktu roślinnego) lub nie rozcieńczonego ekstraktu tkanki roślinnej. Do pierwszej mikroprobówki przenieść 100 µl zawiesiny poszukiwanego organizmu. Wstrząsnąć za pomocą vorteksu. Ustalić dziesięciokrotne poziomy kontaminacji poprzez dalsze rozcieńczenia w następnych czterech mikroprobówkach. Przenieść 100 µl buforu do zawieszania osadu do pięciu nie skontaminowanych mikroprobówek. Pierwsze pięć skontaminowanych mikroprobówek należy używać jako kontrole pozytywne. Następne pięć nie kontaminowanych mikroprobówek należy użyć jako kontrole negatywne. Mikroprobówki odpowiednio oznaczyć za pomocą etykiet. 3. Najpierw należy za pomocą testu IF potwierdzić czy jest obecny i w jakiej ilości poszukiwany organizm. 4. Do sterylnych mikroprobówek przenieść po 100 µl każdego rozcieńczenia, tak by uzyskać dziewięć powtórzeń każdej próbki kontrolnej. Mikroprobówki odpowiednio oznaczyć za pomocą etykiet. Do chwili użycia przechowywać w temperaturze poniżej 16 C. 5. Kontrolne szkiełka mikroskopowe do testu IF przygotować w następujący sposób: Wykonać rozcieńczenie skontaminowanej zawiesiny tak by otrzymać następujące poziomy porażenia: około , około i około komórek na mililitr. Nanieść standardową objętość każdego rozcieńczenia i kontrolę negatywną na szkiełko kontrolne (15 µl jest odpowiednią ilością dla okienek o średnicy około 6 mm w przypadku większych okienek należy odpowiednio dostosować nanoszoną objętość; ale należy pamiętać aby nanieść taką samą objętość jak w przypadku próbki która będzie badana). Dodatkowo (jeśli to możliwe) należy na szkiełko nanieść ekstrakt próbki naturalnie porażonej oraz jej dwa 10-krotne rozcieńczenia. Jako kontrolę negatywną koniugatu (KN) należy użyć rozcieńczenie oraz ekstrakt naturalnie porażonej próbki. Kontrole nanieść na szkiełka najlepiej w sposób pokazany na rysunku 2. Kontrolę pozytywną i negatywną należy przygotowywać dla każdej serii badanych próbek. Poszukiwany organizm musi być wykryty w kontroli pozytywnej i nie może być wykryty w żadnej z kontroli negatywnych OEPP/EPP0,Bulletin OEPP/EPP0 Bulletin 39,
9 Szkiełko kontroln e KN 1x10 6 1x10 6 1x10 4 5x10 3 negatywna KN naturalnie zainfekowa na Naturalnie zainfekowa na naturalnie zainfekowana 1:10 naturalnie zainfekowana 1:100 pusta KN: kontrole negatywne koniugatu Rysunek 2. Sposób naniesienia kontroli pozytywnej i negatywnej na szkiełko kontrolne. Tłumaczenie z jęz. angielskiego: Sprawdził: Zatwierdził: Anna Kołodziejska (GIORiN CL) Monika Kordyla-Bronka (GIORiN CL) Janina Butrymowicz (GIORiN CL) 2009 OEPP/EPP0,Bulletin OEPP/EPP0 Bulletin 39,
Test ELISA dla bakterii patogenicznych dla roślin
 Europejska i Śródziemnomorska Organizacja Ochrony Roślin PM 7/101 (1) Organisation Européenne et Méditerranéenne pour la Protection des Plantem Diagnostyka Diagnostics Test ELISA dla bakterii patogenicznych
Europejska i Śródziemnomorska Organizacja Ochrony Roślin PM 7/101 (1) Organisation Européenne et Méditerranéenne pour la Protection des Plantem Diagnostyka Diagnostics Test ELISA dla bakterii patogenicznych
Zestaw do wykrywania Chlamydia trachomatis w moczu lub w kulturach komórkowych
 Nr kat. PK15 Wersja zestawu: 1.2016 Zestaw do wykrywania w moczu lub w kulturach komórkowych na 50 reakcji PCR (50µl), włączając w to kontrole Detekcja oparta jest na amplifikacji fragmentu genu crp (cysteine
Nr kat. PK15 Wersja zestawu: 1.2016 Zestaw do wykrywania w moczu lub w kulturach komórkowych na 50 reakcji PCR (50µl), włączając w to kontrole Detekcja oparta jest na amplifikacji fragmentu genu crp (cysteine
BIOLOGIA KOMÓRKI KOMÓRKI EUKARIOTYCZNE W MIKROSKOPIE ŚWIETLNYM JASNEGO POLA I KONTRASTOWO- FAZOWYM; BARWIENIA CYTOCHEMICZNE KOMÓREK
 BIOLOGIA KOMÓRKI KOMÓRKI EUKARIOTYCZNE W MIKROSKOPIE ŚWIETLNYM JASNEGO POLA I KONTRASTOWO- FAZOWYM; BARWIENIA CYTOCHEMICZNE KOMÓREK KOMÓRKI EUKARIOTYCZNE W MIKROSKOPIE ŚWIETLNYM JASNEGO POLA I KONTRASTOWO-FAZOWYM;
BIOLOGIA KOMÓRKI KOMÓRKI EUKARIOTYCZNE W MIKROSKOPIE ŚWIETLNYM JASNEGO POLA I KONTRASTOWO- FAZOWYM; BARWIENIA CYTOCHEMICZNE KOMÓREK KOMÓRKI EUKARIOTYCZNE W MIKROSKOPIE ŚWIETLNYM JASNEGO POLA I KONTRASTOWO-FAZOWYM;
XXV. Grzyby cz I. Ćwiczenie 1. Wykonanie i obserwacja preparatów mikroskopowych. a. Candida albicans preparat z hodowli barwiony metoda Grama
 XXV. Grzyby cz I. Ćwiczenie 1. Wykonanie i obserwacja preparatów mikroskopowych a. Candida albicans preparat z hodowli barwiony metoda Grama Opis preparatu: b. Saccharomyces cerevisiae preparat z hodowli
XXV. Grzyby cz I. Ćwiczenie 1. Wykonanie i obserwacja preparatów mikroskopowych a. Candida albicans preparat z hodowli barwiony metoda Grama Opis preparatu: b. Saccharomyces cerevisiae preparat z hodowli
fix RNA Roztwór do przechowywania i ochrony przed degradacją próbek przeznaczonych do izolacji RNA kat. nr. E0280 Sierpień 2018
 Sierpień 2018 fix RNA Roztwór do przechowywania i ochrony przed degradacją próbek przeznaczonych do izolacji RNA kat. nr. E0280 EURx Ltd. 80-297 Gdansk Poland ul. Przyrodnikow 3, NIP 957-07-05-191 KRS
Sierpień 2018 fix RNA Roztwór do przechowywania i ochrony przed degradacją próbek przeznaczonych do izolacji RNA kat. nr. E0280 EURx Ltd. 80-297 Gdansk Poland ul. Przyrodnikow 3, NIP 957-07-05-191 KRS
ALGALTOXKIT F Procedura testu
 ALGALTOXKIT F Procedura testu 1 PRZYGOTOWANIE STANDARDOWEJ POŻYWKI A B C D - KOLBKA MIAROWA (1 litr) - FIOLKI Z ROZTWORAMI POŻYWEK A (2 fiolki), B, C, D - DESTYLOWANA (lub dejonizowana) WODA 2 A PRZENIEŚĆ
ALGALTOXKIT F Procedura testu 1 PRZYGOTOWANIE STANDARDOWEJ POŻYWKI A B C D - KOLBKA MIAROWA (1 litr) - FIOLKI Z ROZTWORAMI POŻYWEK A (2 fiolki), B, C, D - DESTYLOWANA (lub dejonizowana) WODA 2 A PRZENIEŚĆ
E.coli Transformer Zestaw do przygotowywania i transformacji komórek kompetentnych Escherichia coli
 E.coli Transformer Zestaw do przygotowywania i transformacji komórek kompetentnych Escherichia coli Wersja 0211 6x40 transformacji Nr kat. 4020-240 Zestaw zawiera komplet odczynników do przygotowania sześciu
E.coli Transformer Zestaw do przygotowywania i transformacji komórek kompetentnych Escherichia coli Wersja 0211 6x40 transformacji Nr kat. 4020-240 Zestaw zawiera komplet odczynników do przygotowania sześciu
ĆWICZENIE 5 Barwniki roślinne. Ekstrakcja barwników asymilacyjnych. Rozpuszczalność chlorofilu
 ĆWICZENIE 5 Barwniki roślinne Ekstrakcja barwników asymilacyjnych 400 mg - zhomogenizowany w ciekłym azocie proszek z natki pietruszki 6 ml - etanol 96% 2x probówki plastikowe typu Falcon na 15 ml 5x probówki
ĆWICZENIE 5 Barwniki roślinne Ekstrakcja barwników asymilacyjnych 400 mg - zhomogenizowany w ciekłym azocie proszek z natki pietruszki 6 ml - etanol 96% 2x probówki plastikowe typu Falcon na 15 ml 5x probówki
II. Badanie lekowrażliwości drobnoustrojów ćwiczenia praktyczne. Ćwiczenie 1. Oznaczanie lekowrażliwości metodą dyfuzyjno-krążkową
 II. Badanie lekowrażliwości drobnoustrojów ćwiczenia praktyczne Ćwiczenie 1. Oznaczanie lekowrażliwości metodą dyfuzyjno-krążkową Zasada metody: Krążki bibułowe nasycone odpowiednimi ilościami antybiotyków
II. Badanie lekowrażliwości drobnoustrojów ćwiczenia praktyczne Ćwiczenie 1. Oznaczanie lekowrażliwości metodą dyfuzyjno-krążkową Zasada metody: Krążki bibułowe nasycone odpowiednimi ilościami antybiotyków
MATERIAŁY SZKOLENIOWE DLA ZAKŁADÓW HIGIENY WETERYNARYJNEJ W ZAKRESIE LABORATORYJNEJ DIAGNOSTYKI AFRYKAŃSKIEGO POMORU ŚWIŃ
 MATERIAŁY SZKOLENIOWE DLA ZAKŁADÓW HIGIENY WETERYNARYJNEJ W ZAKRESIE LABORATORYJNEJ DIAGNOSTYKI AFRYKAŃSKIEGO POMORU ŚWIŃ Puławy 2013 Opracowanie: Prof. dr hab. Iwona Markowska-Daniel, mgr inż. Kinga Urbaniak,
MATERIAŁY SZKOLENIOWE DLA ZAKŁADÓW HIGIENY WETERYNARYJNEJ W ZAKRESIE LABORATORYJNEJ DIAGNOSTYKI AFRYKAŃSKIEGO POMORU ŚWIŃ Puławy 2013 Opracowanie: Prof. dr hab. Iwona Markowska-Daniel, mgr inż. Kinga Urbaniak,
Saccharomyces Transformer Kit zestaw do przygotowywania i transformacji komórek kompetentnych Saccharomyces cerevisiae. Metoda chemiczna.
 Saccharomyces Transformer Kit zestaw do przygotowywania i transformacji komórek kompetentnych Saccharomyces cerevisiae. Metoda chemiczna. wersja 0916 6 x 20 transformacji Nr kat. 4010-120 Zestaw zawiera
Saccharomyces Transformer Kit zestaw do przygotowywania i transformacji komórek kompetentnych Saccharomyces cerevisiae. Metoda chemiczna. wersja 0916 6 x 20 transformacji Nr kat. 4010-120 Zestaw zawiera
ĆWICZENIE 5 MECHANIZMY PROMUJĄCE WZROST ROŚLIN
 ĆWICZENIE 5 MECHANIZMY PROMUJĄCE WZROST ROŚLIN CZĘŚĆ TEORETYCZNA Mechanizmy promujące wzrost rośli (PGP) Metody badań PGP CZĘŚĆ PRAKTYCZNA 1. Mechanizmy promujące wzrost roślin. Odczyt. a) Wytwarzanie
ĆWICZENIE 5 MECHANIZMY PROMUJĄCE WZROST ROŚLIN CZĘŚĆ TEORETYCZNA Mechanizmy promujące wzrost rośli (PGP) Metody badań PGP CZĘŚĆ PRAKTYCZNA 1. Mechanizmy promujące wzrost roślin. Odczyt. a) Wytwarzanie
E.coli Transformer Kit
 E.coli Transformer Kit zestaw do przygotowywania i transformacji komórek kompetentnych Escherichia coli. Metoda chemiczna. wersja 1117 6 x 40 transformacji Nr kat. 4020-240 Zestaw zawiera komplet odczynników
E.coli Transformer Kit zestaw do przygotowywania i transformacji komórek kompetentnych Escherichia coli. Metoda chemiczna. wersja 1117 6 x 40 transformacji Nr kat. 4020-240 Zestaw zawiera komplet odczynników
woda do 1000 ml ph=6,9-7,1. Po sterylizacji dodać nystatynę (końcowe stężenie ok. 50 μg/ml). Agar z wyciągiem glebowym i ekstraktem drożdżowym (YS)
 Ćwiczenie 1, 2, 3, 4 Skrining ze środowiska naturalnego: selekcja promieniowców zdolnych do produkcji antybiotyków. Testowanie zdolności do syntezy antybiotyków przez wyselekcjonowane szczepy promieniowców
Ćwiczenie 1, 2, 3, 4 Skrining ze środowiska naturalnego: selekcja promieniowców zdolnych do produkcji antybiotyków. Testowanie zdolności do syntezy antybiotyków przez wyselekcjonowane szczepy promieniowców
RAPORT Z BADAŃ 164/Z/20110825/D/JOGA. Dostarczony materiał: próbki tworzyw sztucznych. Ilość próbek: 1. Rodzaj próbek: tworzywo
 Blirt S.A. 80-172 Gdańsk, ul. Trzy Lipy 3/1.38 RAPORT Z BADAŃ Dział DNA-Gdańsk Nr zlecenia 164/Z/20110825/D/JOGA NAZWA I ADRES KLIENTA GROUND-Therm spółka z o.o. ul. Stepowa 30 44-105 Gliwice Tytuł zlecenia:
Blirt S.A. 80-172 Gdańsk, ul. Trzy Lipy 3/1.38 RAPORT Z BADAŃ Dział DNA-Gdańsk Nr zlecenia 164/Z/20110825/D/JOGA NAZWA I ADRES KLIENTA GROUND-Therm spółka z o.o. ul. Stepowa 30 44-105 Gliwice Tytuł zlecenia:
Zestaw do wykrywania Babesia spp. i Theileria spp. w kleszczach, krwi i hodowlach komórkowych
 Nr kat. PK25N Wersja zestawu: 1.2012 Zestaw do wykrywania spp. i Theileria spp. w kleszczach, krwi i hodowlach komórkowych dwie oddzielne reakcje PCR 2x50 reakcji PCR (50 µl), włączając w to kontrole Zestaw
Nr kat. PK25N Wersja zestawu: 1.2012 Zestaw do wykrywania spp. i Theileria spp. w kleszczach, krwi i hodowlach komórkowych dwie oddzielne reakcje PCR 2x50 reakcji PCR (50 µl), włączając w to kontrole Zestaw
CEL ĆWICZENIA: Zapoznanie się z przykładową procedurą odsalania oczyszczanych preparatów enzymatycznych w procesie klasycznej filtracji żelowej.
 LABORATORIUM 3 Filtracja żelowa preparatu oksydazy polifenolowej (PPO) oczyszczanego w procesie wysalania siarczanem amonu z wykorzystaniem złoża Sephadex G-50 CEL ĆWICZENIA: Zapoznanie się z przykładową
LABORATORIUM 3 Filtracja żelowa preparatu oksydazy polifenolowej (PPO) oczyszczanego w procesie wysalania siarczanem amonu z wykorzystaniem złoża Sephadex G-50 CEL ĆWICZENIA: Zapoznanie się z przykładową
OSTRACODTOXKIT F Procedura testu
 OSTRACODTOXKIT F Procedura testu 1 PRZYGOTOWANIE STANDARDOWEJ POŻYWKI - KOLBKA MIAROWA (1 litr) - FIOLKI Z ROZTWORAMI SKONCENTROWANYCH SOLI - DESTYLOWANA (lub dejonizowana) WODA 2 PRZELAĆ ZAWARTOŚĆ 5 FIOLEK
OSTRACODTOXKIT F Procedura testu 1 PRZYGOTOWANIE STANDARDOWEJ POŻYWKI - KOLBKA MIAROWA (1 litr) - FIOLKI Z ROZTWORAMI SKONCENTROWANYCH SOLI - DESTYLOWANA (lub dejonizowana) WODA 2 PRZELAĆ ZAWARTOŚĆ 5 FIOLEK
Technika hodowli komórek leukemicznych
 Fizjologiczne Techniki Badań Technika hodowli komórek leukemicznych Zasady prowadzenia hodowli komórek leukemicznych, pasażowania, mrożenia, rozmrażania i przechowywania komórek leukemicznych Warunki wstępne:
Fizjologiczne Techniki Badań Technika hodowli komórek leukemicznych Zasady prowadzenia hodowli komórek leukemicznych, pasażowania, mrożenia, rozmrażania i przechowywania komórek leukemicznych Warunki wstępne:
Genomic Maxi AX zestaw do izolacji genomowego DNA wersja 0616
 Genomic Maxi AX zestaw do izolacji genomowego DNA wersja 0616 10 izolacji Nr kat. 995-10 Pojemność kolumny do oczyszczania DNA wynosi 500 µg 1 Skład zestawu Składnik Ilość Temp. Przechowywania Kolumny
Genomic Maxi AX zestaw do izolacji genomowego DNA wersja 0616 10 izolacji Nr kat. 995-10 Pojemność kolumny do oczyszczania DNA wynosi 500 µg 1 Skład zestawu Składnik Ilość Temp. Przechowywania Kolumny
Genomic Mini AX Plant Spin
 Genomic Mini AX Plant Spin Zestaw o zwiększonej wydajności do izolacji genomowego DNA z materiału roślinnego. wersja 1017 100 izolacji Nr kat. 050-100S Pojemność kolumny do oczyszczania DNA wynosi 15 μg.
Genomic Mini AX Plant Spin Zestaw o zwiększonej wydajności do izolacji genomowego DNA z materiału roślinnego. wersja 1017 100 izolacji Nr kat. 050-100S Pojemność kolumny do oczyszczania DNA wynosi 15 μg.
OPIS PRZEDMIOTU ZAMÓWIENIA DLA CZĘŚCI NR 8
 OPIS PRZEDMIOTU ZAMÓWIENIA DLA CZĘŚCI NR 8 1. IIFT: Mozaika: Hep-2/Wątroba(Małpa) - zestaw testowy do badania in vitro autoprzeciwciał przeciwko: jądra komórkowe(ana) w ludzkiej surowicy lub plazmie 10
OPIS PRZEDMIOTU ZAMÓWIENIA DLA CZĘŚCI NR 8 1. IIFT: Mozaika: Hep-2/Wątroba(Małpa) - zestaw testowy do badania in vitro autoprzeciwciał przeciwko: jądra komórkowe(ana) w ludzkiej surowicy lub plazmie 10
ĆWICZENIA Z MECHANIZMÓW DZIAŁANIA WYBRANYCH GRUP LEKÓW
 UNIWERSYTET MARII CURIE-SKŁODOWSKIEJ WYDZIAŁ BIOLOGII I BIOTECHNOLOGII ZAKŁAD BIOLOGII MOLEKULARNEJ ĆWICZENIA Z MECHANIZMÓW DZIAŁANIA WYBRANYCH GRUP LEKÓW dla studentów I roku II 0 biotechnologii medycznej
UNIWERSYTET MARII CURIE-SKŁODOWSKIEJ WYDZIAŁ BIOLOGII I BIOTECHNOLOGII ZAKŁAD BIOLOGII MOLEKULARNEJ ĆWICZENIA Z MECHANIZMÓW DZIAŁANIA WYBRANYCH GRUP LEKÓW dla studentów I roku II 0 biotechnologii medycznej
RAPORT Z BADAŃ 01369/2015/D/AGST. Blirt S.A Gdańsk, ul. Trzy Lipy 3/1.38. Dział DNA-Gdańsk. Nr zlecenia
 Strona1/7 Blirt S.A. 80-172 Gdańsk, ul. Trzy Lipy 3/1.38 RAPORT Z BADAŃ Dział DNA-Gdańsk Nr zlecenia 01369/2015/D/AGST NAZWA I ADRES KLIENTA Zenon Koszorz Ground-Therm Sp z o.o. Ul. Stepowa 30 44-105 Gliwice
Strona1/7 Blirt S.A. 80-172 Gdańsk, ul. Trzy Lipy 3/1.38 RAPORT Z BADAŃ Dział DNA-Gdańsk Nr zlecenia 01369/2015/D/AGST NAZWA I ADRES KLIENTA Zenon Koszorz Ground-Therm Sp z o.o. Ul. Stepowa 30 44-105 Gliwice
badanie moczu Zwierzę Typ cewnika moczowego Rozmiar (jedn. francuskie) * gumy lub dla kocurów polietylenowy Elastyczny winylowy, z czerwonej
 badanie moczu Rozmiary cewników... 139 Rutynowe postępowanie przy badaniu moczu... 140 Ogólne badanie moczu... 141 Badanie osadu moczu... 142 Tabela ph moczu dla kryształów moczu 142 Komórki i wałeczki...
badanie moczu Rozmiary cewników... 139 Rutynowe postępowanie przy badaniu moczu... 140 Ogólne badanie moczu... 141 Badanie osadu moczu... 142 Tabela ph moczu dla kryształów moczu 142 Komórki i wałeczki...
Załącznik nr 4 Metodyka pobrania materiału przedstawiona jest w osobnym Instrukcja PZH
 Załącznik nr 4 Metodyka pobrania materiału przedstawiona jest w osobnym Instrukcja PZH 1. Rodzaj materiału klinicznego w zależności od kierunku i metodyki badań wykonywanych przez PZH Poz. Badanie Rodzaj
Załącznik nr 4 Metodyka pobrania materiału przedstawiona jest w osobnym Instrukcja PZH 1. Rodzaj materiału klinicznego w zależności od kierunku i metodyki badań wykonywanych przez PZH Poz. Badanie Rodzaj
StayRNA bufor zabezpieczający RNA przed degradacją wersja 0215
 StayRNA bufor zabezpieczający RNA przed degradacją wersja 0215 100 ml, 250 ml, 500 ml Nr kat. 038-100, 038-250, 038-500 Nietosyczny roztwór wodny do przechowywania i zabezpieczania różnego rodzaju tkanek
StayRNA bufor zabezpieczający RNA przed degradacją wersja 0215 100 ml, 250 ml, 500 ml Nr kat. 038-100, 038-250, 038-500 Nietosyczny roztwór wodny do przechowywania i zabezpieczania różnego rodzaju tkanek
Genomic Midi AX. 20 izolacji
 Genomic Midi AX Uniwersalny zestaw o zwiększonej wydajności do izolacji genomowego DNA z różnych materiałów. Procedura z precypitacją DNA. wersja 0517 20 izolacji Nr kat. 895-20 Pojemność kolumny do oczyszczania
Genomic Midi AX Uniwersalny zestaw o zwiększonej wydajności do izolacji genomowego DNA z różnych materiałów. Procedura z precypitacją DNA. wersja 0517 20 izolacji Nr kat. 895-20 Pojemność kolumny do oczyszczania
Zestaw do wykrywania Anaplasma phagocytophilum w kleszczach, krwi i hodowlach komórkowych
 Nr kat. PK24N Wersja zestawu: 1.2016 Zestaw do wykrywania phagocytophilum w kleszczach, krwi i hodowlach komórkowych dwie oddzielne reakcje PCR 2x50 reakcji PCR (50 µl), włączając w to kontrole Detekcja
Nr kat. PK24N Wersja zestawu: 1.2016 Zestaw do wykrywania phagocytophilum w kleszczach, krwi i hodowlach komórkowych dwie oddzielne reakcje PCR 2x50 reakcji PCR (50 µl), włączając w to kontrole Detekcja
Oznaczanie mocznika w płynach ustrojowych metodą hydrolizy enzymatycznej
 Oznaczanie mocznika w płynach ustrojowych metodą hydrolizy enzymatycznej Wprowadzenie: Większość lądowych organizmów kręgowych część jonów amonowych NH + 4, produktu rozpadu białek, wykorzystuje w biosyntezie
Oznaczanie mocznika w płynach ustrojowych metodą hydrolizy enzymatycznej Wprowadzenie: Większość lądowych organizmów kręgowych część jonów amonowych NH + 4, produktu rozpadu białek, wykorzystuje w biosyntezie
Do jednego litra medium dodać 10,0 g skrobi ziemniaczanej lub kukurydzianej i mieszać do uzyskania zawiesiny. Sterylizować w autoklawie.
 Ćwiczenie 3. Izolacja laseczek przetrwalnikujących z gleby Cel ćwiczenia: Izolacja i testowanie przydatności biotechnologicznej laseczek z rodzaju Bacillus występujących w glebie. Odczynniki i podłoża:
Ćwiczenie 3. Izolacja laseczek przetrwalnikujących z gleby Cel ćwiczenia: Izolacja i testowanie przydatności biotechnologicznej laseczek z rodzaju Bacillus występujących w glebie. Odczynniki i podłoża:
Gel-Out. 50 izolacji, 250 izolacji. Nr kat , Zestaw do izolacji DNA z żelu agarozowego. wersja 0617
 Gel-Out Zestaw do izolacji DNA z żelu agarozowego. wersja 0617 50 izolacji, 250 izolacji Nr kat. 023-50, 023-250 Pojemność kolumny do izolacji DNA - do 20 µg DNA, minimalna pojemność - 2 µg DNA (przy zawartości
Gel-Out Zestaw do izolacji DNA z żelu agarozowego. wersja 0617 50 izolacji, 250 izolacji Nr kat. 023-50, 023-250 Pojemność kolumny do izolacji DNA - do 20 µg DNA, minimalna pojemność - 2 µg DNA (przy zawartości
data ĆWICZENIE 12 BIOCHEMIA MOCZU Doświadczenie 1
 Imię i nazwisko Uzyskane punkty Nr albumu data /3 podpis asystenta ĆWICZENIE 12 BIOCHEMIA MOCZU Doświadczenie 1 Cel: Wyznaczanie klirensu endogennej kreatyniny. Miarą zdolności nerek do usuwania i wydalania
Imię i nazwisko Uzyskane punkty Nr albumu data /3 podpis asystenta ĆWICZENIE 12 BIOCHEMIA MOCZU Doświadczenie 1 Cel: Wyznaczanie klirensu endogennej kreatyniny. Miarą zdolności nerek do usuwania i wydalania
Zestaw do izolacji genomowego DNA z bakterii
 Nr kat. EM02 Wersja: 1.2018 Zestaw do izolacji genomowego DNA z bakterii EXTRACTME jest zarejestrowanym znakiem towarowym BLIRT S.A. www.blirt.eu Nr kat. EM02 I. PRZEZNACZENIE ZESTAWU Zestaw EXTRACTME
Nr kat. EM02 Wersja: 1.2018 Zestaw do izolacji genomowego DNA z bakterii EXTRACTME jest zarejestrowanym znakiem towarowym BLIRT S.A. www.blirt.eu Nr kat. EM02 I. PRZEZNACZENIE ZESTAWU Zestaw EXTRACTME
Laboratorium 3 Toksykologia żywności
 Laboratorium 3 Toksykologia żywności Literatura zalecana: Orzeł D., Biernat J. (red.) 2012. Wybrane zagadnienia z toksykologii żywności. Wydawnictwo Uniwersytetu Przyrodniczego we Wrocławiu. Wrocław. Str.:
Laboratorium 3 Toksykologia żywności Literatura zalecana: Orzeł D., Biernat J. (red.) 2012. Wybrane zagadnienia z toksykologii żywności. Wydawnictwo Uniwersytetu Przyrodniczego we Wrocławiu. Wrocław. Str.:
Genomic Maxi AX Direct
 Genomic Maxi AX Direct Uniwersalny zestaw o zwiększonej wydajności do izolacji genomowego DNA z różnych materiałów. Procedura bez etapu precypitacji. wersja 0517 10 izolacji Nr kat. 995-10D Pojemność kolumny
Genomic Maxi AX Direct Uniwersalny zestaw o zwiększonej wydajności do izolacji genomowego DNA z różnych materiałów. Procedura bez etapu precypitacji. wersja 0517 10 izolacji Nr kat. 995-10D Pojemność kolumny
Genomic Midi AX Direct zestaw do izolacji genomowego DNA (procedura bez precypitacji) wersja 1215
 Genomic Midi AX Direct zestaw do izolacji genomowego DNA (procedura bez precypitacji) wersja 1215 20 izolacji Nr kat. 895-20D Pojemność kolumny do oczyszczania DNA wynosi 100 µg 1 Skład zestawu Składnik
Genomic Midi AX Direct zestaw do izolacji genomowego DNA (procedura bez precypitacji) wersja 1215 20 izolacji Nr kat. 895-20D Pojemność kolumny do oczyszczania DNA wynosi 100 µg 1 Skład zestawu Składnik
Novabeads Food DNA Kit
 Novabeads Food DNA Kit Novabeads Food DNA Kit jest nowej generacji narzędziem w technikach biologii molekularnej, umożliwiającym izolację DNA z produktów spożywczych wysoko przetworzonych. Metoda oparta
Novabeads Food DNA Kit Novabeads Food DNA Kit jest nowej generacji narzędziem w technikach biologii molekularnej, umożliwiającym izolację DNA z produktów spożywczych wysoko przetworzonych. Metoda oparta
Izolowanie DNA i RNA z komórek hodowlanych. Ocena jakości uzyskanego materiału
 II ROK KIERUNEK WETERYNARIA UJCM INSTRUKCJA DO ĆWICZEŃ LABORATORYJNYCH VIII Izolowanie DNA i RNA z komórek hodowlanych. Ocena jakości uzyskanego materiału 2013/2014 2 ĆWICZENIE VIII Preparatyka całkowitego
II ROK KIERUNEK WETERYNARIA UJCM INSTRUKCJA DO ĆWICZEŃ LABORATORYJNYCH VIII Izolowanie DNA i RNA z komórek hodowlanych. Ocena jakości uzyskanego materiału 2013/2014 2 ĆWICZENIE VIII Preparatyka całkowitego
Genomic Mini AX Bacteria+ Spin
 Genomic Mini AX Bacteria+ Spin Zestaw o zwiększonej wydajności do izolacji genomowego DNA z bakterii Gram-dodatnich. wersja 1017 100 izolacji Nr kat. 060-100MS Pojemność kolumny do oczyszczania DNA wynosi
Genomic Mini AX Bacteria+ Spin Zestaw o zwiększonej wydajności do izolacji genomowego DNA z bakterii Gram-dodatnich. wersja 1017 100 izolacji Nr kat. 060-100MS Pojemność kolumny do oczyszczania DNA wynosi
TaqNova-RED. Polimeraza DNA RP20R, RP100R
 TaqNova-RED Polimeraza DNA RP20R, RP100R RP20R, RP100R TaqNova-RED Polimeraza DNA Rekombinowana termostabilna polimeraza DNA Taq zawierająca czerwony barwnik, izolowana z Thermus aquaticus, o przybliżonej
TaqNova-RED Polimeraza DNA RP20R, RP100R RP20R, RP100R TaqNova-RED Polimeraza DNA Rekombinowana termostabilna polimeraza DNA Taq zawierająca czerwony barwnik, izolowana z Thermus aquaticus, o przybliżonej
Zestaw do izolacji genomowego DNA z drożdży
 Nr kat. EM10 Wersja: 1.2018 Zestaw do izolacji genomowego DNA z drożdży EXTRACTME jest zastrzeżonym znakiem towarowym firmy BLIRT S.A. www.blirt.eu 2 Nr kat. EM10 I. PRZEZNACZENIE ZESTAWU Zestaw EXTRACTME
Nr kat. EM10 Wersja: 1.2018 Zestaw do izolacji genomowego DNA z drożdży EXTRACTME jest zastrzeżonym znakiem towarowym firmy BLIRT S.A. www.blirt.eu 2 Nr kat. EM10 I. PRZEZNACZENIE ZESTAWU Zestaw EXTRACTME
Laboratorium 5. Wpływ temperatury na aktywność enzymów. Inaktywacja termiczna
 Laboratorium 5 Wpływ temperatury na aktywność enzymów. Inaktywacja termiczna Prowadzący: dr inż. Karolina Labus 1. CZĘŚĆ TEORETYCZNA Szybkość reakcji enzymatycznej zależy przede wszystkim od stężenia substratu
Laboratorium 5 Wpływ temperatury na aktywność enzymów. Inaktywacja termiczna Prowadzący: dr inż. Karolina Labus 1. CZĘŚĆ TEORETYCZNA Szybkość reakcji enzymatycznej zależy przede wszystkim od stężenia substratu
AmpliTest Salmonella spp. (Real Time PCR)
 AmpliTest Salmonella spp. (Real Time PCR) Zestaw do wykrywania sekwencji DNA specyficznych dla bakterii z rodzaju Salmonella techniką Real Time PCR Nr kat.: BAC01-50 Wielkość zestawu: 50 oznaczeń Objętość
AmpliTest Salmonella spp. (Real Time PCR) Zestaw do wykrywania sekwencji DNA specyficznych dla bakterii z rodzaju Salmonella techniką Real Time PCR Nr kat.: BAC01-50 Wielkość zestawu: 50 oznaczeń Objętość
Metody immunocytochemiczne. Barwienie fluorescencyjne komórek prawidłowych i nowotworowych PRAKTIKUM Z BIOLOGII KOMÓRKI (BT 206, BT 231)
 Metody immunocytochemiczne. Barwienie fluorescencyjne komórek prawidłowych i nowotworowych PRAKTIKUM Z BIOLOGII KOMÓRKI () Metody immunocytochemiczne... Metody immunocytochemiczne. Barwienie fluorescencyjne
Metody immunocytochemiczne. Barwienie fluorescencyjne komórek prawidłowych i nowotworowych PRAKTIKUM Z BIOLOGII KOMÓRKI () Metody immunocytochemiczne... Metody immunocytochemiczne. Barwienie fluorescencyjne
1. Oznaczanie aktywności lipazy trzustkowej i jej zależności od stężenia enzymu oraz żółci jako modulatora reakcji enzymatycznej.
 ĆWICZENIE OZNACZANIE AKTYWNOŚCI LIPAZY TRZUSTKOWEJ I JEJ ZALEŻNOŚCI OD STĘŻENIA ENZYMU ORAZ ŻÓŁCI JAKO MODULATORA REAKCJI ENZYMATYCZNEJ. INHIBICJA KOMPETYCYJNA DEHYDROGENAZY BURSZTYNIANOWEJ. 1. Oznaczanie
ĆWICZENIE OZNACZANIE AKTYWNOŚCI LIPAZY TRZUSTKOWEJ I JEJ ZALEŻNOŚCI OD STĘŻENIA ENZYMU ORAZ ŻÓŁCI JAKO MODULATORA REAKCJI ENZYMATYCZNEJ. INHIBICJA KOMPETYCYJNA DEHYDROGENAZY BURSZTYNIANOWEJ. 1. Oznaczanie
Metody immunocytochemiczne. Barwienie fluorescencyjne komórek prawidłowych i nowotworowych PRAKTIKUM Z BIOLOGII KOMÓRKI (BT 106)
 Metody immunocytochemiczne. Barwienie fluorescencyjne komórek prawidłowych i nowotworowych PRAKTIKUM Z BIOLOGII KOMÓRKI (BT 106) Metody immunocytochemiczne. Barwienie fluorescencyjne komórek prawidłowych
Metody immunocytochemiczne. Barwienie fluorescencyjne komórek prawidłowych i nowotworowych PRAKTIKUM Z BIOLOGII KOMÓRKI (BT 106) Metody immunocytochemiczne. Barwienie fluorescencyjne komórek prawidłowych
SPRAWOZDANIE Z ĆWICZEŃ Z HIGIENY, TOKSYKOLOGII I BEZPIECZEŃSTWA ŻYWNOŚCI
 Data.. Imię, nazwisko, kierunek, grupa SPRAWOZDANIE Z ĆWICZEŃ Z HIGIENY, TOKSYKOLOGII I BEZPIECZEŃSTWA ŻYWNOŚCI OCENA JAKOŚCI WODY DO PICIA Ćwiczenie 1. Badanie właściwości fizykochemicznych wody Ćwiczenie
Data.. Imię, nazwisko, kierunek, grupa SPRAWOZDANIE Z ĆWICZEŃ Z HIGIENY, TOKSYKOLOGII I BEZPIECZEŃSTWA ŻYWNOŚCI OCENA JAKOŚCI WODY DO PICIA Ćwiczenie 1. Badanie właściwości fizykochemicznych wody Ćwiczenie
RT31-020, RT , MgCl 2. , random heksamerów X 6
 RT31-020, RT31-100 RT31-020, RT31-100 Zestaw TRANSCRIPTME RNA zawiera wszystkie niezbędne składniki do przeprowadzenia syntezy pierwszej nici cdna na matrycy mrna lub całkowitego RNA. Uzyskany jednoniciowy
RT31-020, RT31-100 RT31-020, RT31-100 Zestaw TRANSCRIPTME RNA zawiera wszystkie niezbędne składniki do przeprowadzenia syntezy pierwszej nici cdna na matrycy mrna lub całkowitego RNA. Uzyskany jednoniciowy
AmpliTest GMO screening-nos (Real Time PCR)
 AmpliTest GMO screening-nos (Real Time PCR) Zestaw do wykrywania sekwencji DNA terminatora NOS techniką Real Time PCR Nr kat.: GMO03-50 GMO03-100 Wielkość zestawu: 50 reakcji 100 reakcji Objętość pojedynczej
AmpliTest GMO screening-nos (Real Time PCR) Zestaw do wykrywania sekwencji DNA terminatora NOS techniką Real Time PCR Nr kat.: GMO03-50 GMO03-100 Wielkość zestawu: 50 reakcji 100 reakcji Objętość pojedynczej
Genomic Mini AX Milk Spin
 Genomic Mini AX Milk Spin Zestaw o zwiększonej wydajności do izolacji genomowego DNA z próbek mleka. wersja 1017 100 izolacji Nr kat. 059-100S Pojemność kolumny do oczyszczania DNA wynosi 15 μg. Produkt
Genomic Mini AX Milk Spin Zestaw o zwiększonej wydajności do izolacji genomowego DNA z próbek mleka. wersja 1017 100 izolacji Nr kat. 059-100S Pojemność kolumny do oczyszczania DNA wynosi 15 μg. Produkt
Ćwiczenie 1. Technika ważenia oraz wyznaczanie błędów pomiarowych. Ćwiczenie 2. Sprawdzanie pojemności pipety
 II. Wagi i ważenie. Roztwory. Emulsje i koloidy Zagadnienia Rodzaje wag laboratoryjnych i technika ważenia Niepewność pomiarowa. Błąd względny i bezwzględny Roztwory właściwe Stężenie procentowe i molowe.
II. Wagi i ważenie. Roztwory. Emulsje i koloidy Zagadnienia Rodzaje wag laboratoryjnych i technika ważenia Niepewność pomiarowa. Błąd względny i bezwzględny Roztwory właściwe Stężenie procentowe i molowe.
Otrzymany w pkt. 8 osad, zawieszony w 2 ml wody destylowanej rozpipetować do 4 szklanych probówek po ok. 0.5 ml do każdej.
 Kwasy nukleinowe izolacja DNA, wykrywanie składników. Wymagane zagadnienia teoretyczne 1. Struktura, synteza i degradacja nukleotydów purynowych i pirymidynowych. 2. Regulacja syntezy nukleotydów. Podstawowe
Kwasy nukleinowe izolacja DNA, wykrywanie składników. Wymagane zagadnienia teoretyczne 1. Struktura, synteza i degradacja nukleotydów purynowych i pirymidynowych. 2. Regulacja syntezy nukleotydów. Podstawowe
VIII. Diagnostyka mikrobiologiczna głównych drobnoustrojów odpowiedzialnych za zakażenia przewodu pokarmowego i zapalenie otrzewnej
 VIII. Diagnostyka mikrobiologiczna głównych drobnoustrojów odpowiedzialnych za zakażenia przewodu pokarmowego i zapalenie otrzewnej Pałeczki Gram-ujemne niefermentujące Ćwiczenie 1. Wykonanie i ocena preparatu
VIII. Diagnostyka mikrobiologiczna głównych drobnoustrojów odpowiedzialnych za zakażenia przewodu pokarmowego i zapalenie otrzewnej Pałeczki Gram-ujemne niefermentujące Ćwiczenie 1. Wykonanie i ocena preparatu
Zakład Biologii Molekularnej Materiały do ćwiczeń z przedmiotu: BIOLOGIA MOLEKULARNA
 Zakład Biologii Molekularnej Materiały do ćwiczeń z przedmiotu: BIOLOGIA MOLEKULARNA Zakład Biologii Molekularnej Wydział Farmaceutyczny, WUM ul. Banacha 1, 02-097 Warszawa tel. 22 572 0735, 606448502
Zakład Biologii Molekularnej Materiały do ćwiczeń z przedmiotu: BIOLOGIA MOLEKULARNA Zakład Biologii Molekularnej Wydział Farmaceutyczny, WUM ul. Banacha 1, 02-097 Warszawa tel. 22 572 0735, 606448502
Mikroskopia fluorescencyjna
 Mikroskopia fluorescencyjna Mikroskop fluorescencyjny to mikroskop świetlny, wykorzystujący zjawisko fluorescencji większość z nich to mikroskopy tzw. epi-fluorescencyjne zjawisko fotoluminescencji: fluorescencja
Mikroskopia fluorescencyjna Mikroskop fluorescencyjny to mikroskop świetlny, wykorzystujący zjawisko fluorescencji większość z nich to mikroskopy tzw. epi-fluorescencyjne zjawisko fotoluminescencji: fluorescencja
1276:1997 13368 (ATCC
 Działanie bakteriobójcze Środka biobójczego Clinell GAMA Healthcare Ltd. zbadane za pomocą Europejskiego Standardowego Testu według normy BS EN 1276:1997 wobec: Klebsiella pneumoniae NCTC 13368 (ATCC 700603).
Działanie bakteriobójcze Środka biobójczego Clinell GAMA Healthcare Ltd. zbadane za pomocą Europejskiego Standardowego Testu według normy BS EN 1276:1997 wobec: Klebsiella pneumoniae NCTC 13368 (ATCC 700603).
Identyfikacja mikroorganizmów systemem firmy Biolog
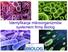 Identyfikacja mikroorganizmów systemem firmy Biolog Główne zalety systemu Ilość mikroorganizmów w bazie danych : Biolog ponad 2500 Vitek 2 ponad 330 Bez barwienia metodą Grama ( Vitek wymaga wstępnego
Identyfikacja mikroorganizmów systemem firmy Biolog Główne zalety systemu Ilość mikroorganizmów w bazie danych : Biolog ponad 2500 Vitek 2 ponad 330 Bez barwienia metodą Grama ( Vitek wymaga wstępnego
ROZPORZĄDZENIA. (4) Środki przewidziane w niniejszym rozporządzeniu są zgodne z opinią Komitetu ds. Wspólnej Organizacji Rynków Rolnych, Artykuł 1
 8.10.2016 L 273/5 ROZPORZĄDZENIA ROZPORZĄDZENIE WYKONAWCZE KOMISJI (UE) 2016/1784 z dnia 30 września 2016 r. zmieniające rozporządzenie (EWG) nr 2568/91 w sprawie właściwości oliwy z oliwek i oliwy z wytłoczyn
8.10.2016 L 273/5 ROZPORZĄDZENIA ROZPORZĄDZENIE WYKONAWCZE KOMISJI (UE) 2016/1784 z dnia 30 września 2016 r. zmieniające rozporządzenie (EWG) nr 2568/91 w sprawie właściwości oliwy z oliwek i oliwy z wytłoczyn
Reakcje utleniania i redukcji Reakcje metali z wodorotlenkiem sodu (6 mol/dm 3 )
 Imię i nazwisko.. data.. Reakcje utleniania i redukcji 7.1 Reaktywność metali 7.1.1 Reakcje metali z wodą Lp Metal Warunki oczyszczania metalu Warunki reakcji Obserwacje 7.1.2 Reakcje metali z wodorotlenkiem
Imię i nazwisko.. data.. Reakcje utleniania i redukcji 7.1 Reaktywność metali 7.1.1 Reakcje metali z wodą Lp Metal Warunki oczyszczania metalu Warunki reakcji Obserwacje 7.1.2 Reakcje metali z wodorotlenkiem
XIII. Staphylococcus, Micrococcus ćwiczenia praktyczne
 XIII. Staphylococcus, Micrococcus ćwiczenia praktyczne Ćwiczenie 1. Ocena wzrostu szczepów gronkowców na: a. agarze z dodatkiem 5% odwłóknionej krwi baraniej (AK) typ hemolizy morfologia kolonii.. b. podłożu
XIII. Staphylococcus, Micrococcus ćwiczenia praktyczne Ćwiczenie 1. Ocena wzrostu szczepów gronkowców na: a. agarze z dodatkiem 5% odwłóknionej krwi baraniej (AK) typ hemolizy morfologia kolonii.. b. podłożu
Zestaw do oczyszczania DNA po reakcjach enzymatycznych
 Cat. No. EM07.1 Wersja: 1.2017 NOWA WERSJA Zestaw do oczyszczania DNA po reakcjach enzymatycznych EXTRACTME jest zarejestrowanym znakiem towarowym BLIRT S.A. www.blirt.eu Nr kat. EM07.1 I. PRZEZNACZENIE
Cat. No. EM07.1 Wersja: 1.2017 NOWA WERSJA Zestaw do oczyszczania DNA po reakcjach enzymatycznych EXTRACTME jest zarejestrowanym znakiem towarowym BLIRT S.A. www.blirt.eu Nr kat. EM07.1 I. PRZEZNACZENIE
PathogenFree DNA Isolation Kit Zestaw do izolacji DNA Instrukcja użytkownika
 PathogenFree DNA Isolation Kit Zestaw do izolacji DNA Instrukcja użytkownika Spis treści 1. Zawartość 2 1.1 Składniki zestawu 2 2. Opis produktu 2 2.1 Założenia metody 2 2.2 Instrukcja 2 2.3 Specyfikacja
PathogenFree DNA Isolation Kit Zestaw do izolacji DNA Instrukcja użytkownika Spis treści 1. Zawartość 2 1.1 Składniki zestawu 2 2. Opis produktu 2 2.1 Założenia metody 2 2.2 Instrukcja 2 2.3 Specyfikacja
CHEMIA ŚRODKÓW BIOAKTYWNYCH I KOSMETYKÓW PRACOWNIA CHEMII ANALITYCZNEJ. Ćwiczenie 8. Argentometryczne oznaczanie chlorków metodą Fajansa
 CHEMIA ŚRODKÓW BIOAKTYWNYCH I KOSMETYKÓW PRACOWNIA CHEMII ANALITYCZNEJ Ćwiczenie 8 Argentometryczne oznaczanie chlorków metodą Fajansa Ćwiczenie obejmuje: 1. Oznaczenie miana roztworu AgNO 3 2. Oznaczenie
CHEMIA ŚRODKÓW BIOAKTYWNYCH I KOSMETYKÓW PRACOWNIA CHEMII ANALITYCZNEJ Ćwiczenie 8 Argentometryczne oznaczanie chlorków metodą Fajansa Ćwiczenie obejmuje: 1. Oznaczenie miana roztworu AgNO 3 2. Oznaczenie
Odporność na zagrzybienie płyt z krzemianu wapnia
 Gregersensvej DK-2630 Taastrup Tel. +45 72 20 20 00 Fax +45 72 20 20 19 info@teknologisk.dk www.teknologisk.dk Odporność na zagrzybienie płyt z krzemianu wapnia 22-10-2015 Sporządzono przez Trine Østergaard
Gregersensvej DK-2630 Taastrup Tel. +45 72 20 20 00 Fax +45 72 20 20 19 info@teknologisk.dk www.teknologisk.dk Odporność na zagrzybienie płyt z krzemianu wapnia 22-10-2015 Sporządzono przez Trine Østergaard
Zestaw SIT InHaVi Szybki Identyfikacyjny Test Szczepów Salmonella Infantis, Hadar oraz Virchow
 Zestaw SIT InHaVi Szybki Identyfikacyjny Test Szczepów Salmonella Infantis, Hadar oraz Virchow W związku z wprowadzeniem w 2011 roku przez Komisję UE zmian w rozporządzeniach nr 2160/3003 i 200/2010 w
Zestaw SIT InHaVi Szybki Identyfikacyjny Test Szczepów Salmonella Infantis, Hadar oraz Virchow W związku z wprowadzeniem w 2011 roku przez Komisję UE zmian w rozporządzeniach nr 2160/3003 i 200/2010 w
ROZPORZĄDZENIE MINISTRA ŚRODOWISKA 1)
 ROZPORZĄDZENIE MINISTRA ŚRODOWISKA 1) z dnia 6 listopada 2002 r. w sprawie metodyk referencyjnych badania stopnia biodegradacji substancji powierzchniowoczynnych zawartych w produktach, których stosowanie
ROZPORZĄDZENIE MINISTRA ŚRODOWISKA 1) z dnia 6 listopada 2002 r. w sprawie metodyk referencyjnych badania stopnia biodegradacji substancji powierzchniowoczynnych zawartych w produktach, których stosowanie
Raport z badania Działanie wirusobójcze środka dezynfekującego wobec Feline calicivirus. 25 października 2006
 Raport z badania Działanie wirusobójcze środka dezynfekującego wobec Feline calicivirus 25 października 2006 Dr Tobias J. Tuthill Wydział Nauk Biologicznych Uniwersytet Leeds Leeds LS2 9JT www.fbs.leeds.ac.uk
Raport z badania Działanie wirusobójcze środka dezynfekującego wobec Feline calicivirus 25 października 2006 Dr Tobias J. Tuthill Wydział Nauk Biologicznych Uniwersytet Leeds Leeds LS2 9JT www.fbs.leeds.ac.uk
Dotyczy: przetargu nieograniczonego na dostawa odczynników, krwinek wzorcowych do serologii grup krwi- metody probówkowe/szkiełkowe
 Numer sprawy: DTZ.382.10.2018 Golub-Dobrzyń, dn. 23.03.2018r. Dotyczy: przetargu nieograniczonego na dostawa odczynników, krwinek wzorcowych do serologii grup krwi- metody probówkowe/szkiełkowe W związku
Numer sprawy: DTZ.382.10.2018 Golub-Dobrzyń, dn. 23.03.2018r. Dotyczy: przetargu nieograniczonego na dostawa odczynników, krwinek wzorcowych do serologii grup krwi- metody probówkowe/szkiełkowe W związku
Laboratorium 8. Badanie stresu oksydacyjnego jako efektu działania czynników toksycznych
 Laboratorium 8 Badanie stresu oksydacyjnego jako efektu działania czynników toksycznych Literatura zalecana: Jakubowska A., Ocena toksyczności wybranych cieczy jonowych. Rozprawa doktorska, str. 28 31.
Laboratorium 8 Badanie stresu oksydacyjnego jako efektu działania czynników toksycznych Literatura zalecana: Jakubowska A., Ocena toksyczności wybranych cieczy jonowych. Rozprawa doktorska, str. 28 31.
TaqNovaHS. Polimeraza DNA RP902A, RP905A, RP910A, RP925A RP902, RP905, RP910, RP925
 TaqNovaHS RP902A, RP905A, RP910A, RP925A RP902, RP905, RP910, RP925 RP902A, RP905A, RP910A, RP925A RP902, RP905, RP910, RP925 TaqNovaHS Polimeraza TaqNovaHS jest mieszaniną termostabilnej polimerazy DNA
TaqNovaHS RP902A, RP905A, RP910A, RP925A RP902, RP905, RP910, RP925 RP902A, RP905A, RP910A, RP925A RP902, RP905, RP910, RP925 TaqNovaHS Polimeraza TaqNovaHS jest mieszaniną termostabilnej polimerazy DNA
SPRAWOZDANIE Z BADAŃ MIKROBIOLOGICZNYCH Nr 20006/11859/09
 SPRAWOZDANIE MOŻE BYĆ POWIELANE TYLKO W CAŁOŚCI. INNA FORMA KOPIOWANIA WYMAGA PISEMNEJ ZGODY LABORATORIUM. SPRAWOZDANIE Z BADAŃ MIKROBIOLOGICZNYCH Nr 20006/11859/09 BADANIA WŁASNOŚCI PRZECIWDROBNOUSTROJOWYCH
SPRAWOZDANIE MOŻE BYĆ POWIELANE TYLKO W CAŁOŚCI. INNA FORMA KOPIOWANIA WYMAGA PISEMNEJ ZGODY LABORATORIUM. SPRAWOZDANIE Z BADAŃ MIKROBIOLOGICZNYCH Nr 20006/11859/09 BADANIA WŁASNOŚCI PRZECIWDROBNOUSTROJOWYCH
PRZYGOTOWANIE PRÓBEK DO MIKROSKOPI SKANINGOWEJ
 Ewa Teper PRZYGOTOWANIE PRÓBEK DO MIKROSKOPI SKANINGOWEJ WIELKOŚĆ I RODZAJE PRÓBEK Maksymalne wymiary próbki, którą można umieścić na stoliku mikroskopu skaningowego są następujące: Próbka powinna się
Ewa Teper PRZYGOTOWANIE PRÓBEK DO MIKROSKOPI SKANINGOWEJ WIELKOŚĆ I RODZAJE PRÓBEK Maksymalne wymiary próbki, którą można umieścić na stoliku mikroskopu skaningowego są następujące: Próbka powinna się
OZNACZANIE ZAWARTOŚCI MANGANU W GLEBIE
 OZNACZANIE ZAWARTOŚCI MANGANU W GLEBIE WPROWADZENIE Przyswajalność pierwiastków przez rośliny zależy od procesów zachodzących między fazą stałą i ciekłą gleby oraz korzeniami roślin. Pod względem stopnia
OZNACZANIE ZAWARTOŚCI MANGANU W GLEBIE WPROWADZENIE Przyswajalność pierwiastków przez rośliny zależy od procesów zachodzących między fazą stałą i ciekłą gleby oraz korzeniami roślin. Pod względem stopnia
Załącznik nr 1A do siwz Część I - Zestaw testowy do szybkiej identyfikacji Escherichia coli
 Część I - Zestaw testowy do szybkiej identyfikacji Escherichia coli 1. Zestaw testowy do szybkiej identyfikacji Escherichia coli zestaw zawiera: - 50 pasków testowych, - 50 pojemników z tworzywa sztucznego,
Część I - Zestaw testowy do szybkiej identyfikacji Escherichia coli 1. Zestaw testowy do szybkiej identyfikacji Escherichia coli zestaw zawiera: - 50 pasków testowych, - 50 pojemników z tworzywa sztucznego,
POLITECHNIKA ŁÓDZKA INSTRUKCJA Z LABORATORIUM W ZAKŁADZIE BIOFIZYKI. Ćwiczenie 3 ANALIZA TRANSPORTU SUBSTANCJI NISKOCZĄSTECZKOWYCH PRZEZ
 POLITECHNIKA ŁÓDZKA INSTRUKCJA Z LABORATORIUM W ZAKŁADZIE BIOFIZYKI Ćwiczenie 3 ANALIZA TRANSPORTU SUBSTANCJI NISKOCZĄSTECZKOWYCH PRZEZ BŁONĘ KOMÓRKOWĄ I. WSTĘP TEORETYCZNY Każda komórka, zarówno roślinna,
POLITECHNIKA ŁÓDZKA INSTRUKCJA Z LABORATORIUM W ZAKŁADZIE BIOFIZYKI Ćwiczenie 3 ANALIZA TRANSPORTU SUBSTANCJI NISKOCZĄSTECZKOWYCH PRZEZ BŁONĘ KOMÓRKOWĄ I. WSTĘP TEORETYCZNY Każda komórka, zarówno roślinna,
WPŁYW SUBSTANCJI TOWARZYSZĄCYCH NA ROZPUSZCZALNOŚĆ OSADÓW
 WPŁYW SUBSTANCJI TOWARZYSZĄCYCH NA ROZPUSZCZALNOŚĆ OSADÓW Wstęp Mianem rozpuszczalności określamy maksymalną ilość danej substancji (w gramach lub molach), jaką w danej temperaturze można rozpuścić w określonej
WPŁYW SUBSTANCJI TOWARZYSZĄCYCH NA ROZPUSZCZALNOŚĆ OSADÓW Wstęp Mianem rozpuszczalności określamy maksymalną ilość danej substancji (w gramach lub molach), jaką w danej temperaturze można rozpuścić w określonej
AmpliTest Chlamydia/Chlamydophila (Real Time PCR)
 AmpliTest Chlamydia/Chlamydophila (Real Time PCR) Zestaw do wykrywania sekwencji DNA specyficznych dla bakterii z rodzajów Chlamydia i Chlamydophila techniką Real Time PCR Nr kat.: BAC18-50 BAC18-100 Wielkość
AmpliTest Chlamydia/Chlamydophila (Real Time PCR) Zestaw do wykrywania sekwencji DNA specyficznych dla bakterii z rodzajów Chlamydia i Chlamydophila techniką Real Time PCR Nr kat.: BAC18-50 BAC18-100 Wielkość
Metoda analityczna oznaczania chlorku winylu uwalnianego z materiałów i wyrobów do żywności
 Załącznik nr 4 Metoda analityczna oznaczania chlorku winylu uwalnianego z materiałów i wyrobów do żywności 1. Zakres i obszar stosowania Metoda służy do urzędowej kontroli zawartości chlorku winylu uwalnianego
Załącznik nr 4 Metoda analityczna oznaczania chlorku winylu uwalnianego z materiałów i wyrobów do żywności 1. Zakres i obszar stosowania Metoda służy do urzędowej kontroli zawartości chlorku winylu uwalnianego
KINETYKA HYDROLIZY SACHAROZY
 Ćwiczenie nr 2 KINETYKA HYDROLIZY SACHAROZY I. Kinetyka hydrolizy sacharozy reakcja chemiczna Zasada: Sacharoza w środowisku kwaśnym ulega hydrolizie z wytworzeniem -D-glukozy i -D-fruktozy. Jest to reakcja
Ćwiczenie nr 2 KINETYKA HYDROLIZY SACHAROZY I. Kinetyka hydrolizy sacharozy reakcja chemiczna Zasada: Sacharoza w środowisku kwaśnym ulega hydrolizie z wytworzeniem -D-glukozy i -D-fruktozy. Jest to reakcja
Komórki macierzyste zastosowania w biotechnologii i medycynie BT Metody identyfikacji i fenotypowania populacji komórek macierzystych
 Metody identyfikacji i fenotypowania populacji komórek macierzystych 1 Wstęp Szpik kostny zawiera hematopoetyczne (HSC) oraz niehematopoetyczne komórki macierzyste (KM). Do niehematopoetycznych KM należą:
Metody identyfikacji i fenotypowania populacji komórek macierzystych 1 Wstęp Szpik kostny zawiera hematopoetyczne (HSC) oraz niehematopoetyczne komórki macierzyste (KM). Do niehematopoetycznych KM należą:
HYDROLIZA SOLI. ROZTWORY BUFOROWE
 Ćwiczenie 9 semestr 2 HYDROLIZA SOLI. ROZTWORY BUFOROWE Obowiązujące zagadnienia: Hydroliza soli-anionowa, kationowa, teoria jonowa Arrheniusa, moc kwasów i zasad, równania hydrolizy soli, hydroliza wieloetapowa,
Ćwiczenie 9 semestr 2 HYDROLIZA SOLI. ROZTWORY BUFOROWE Obowiązujące zagadnienia: Hydroliza soli-anionowa, kationowa, teoria jonowa Arrheniusa, moc kwasów i zasad, równania hydrolizy soli, hydroliza wieloetapowa,
II. OZNACZANIE LICZBY BAKTERII Z GRUPY COLI I BAKTERII Z GRUPY COLI TYP FEKALNY METODĄ PŁYTKOWĄ W ŻYWNOŚCI I INNYCH PRODUKTACH wg PN-ISO 4832: 2007
 Katedra i Zakład Mikrobiologii i Wirusologii Wydział Farmaceutyczny z Oddziałem Medycyny Laboratoryjnej Mikrobiologia ogólna Biotechnologia medyczna II rok / I o Temat: Żywność jako środowisko życia mikroorganizmów.
Katedra i Zakład Mikrobiologii i Wirusologii Wydział Farmaceutyczny z Oddziałem Medycyny Laboratoryjnej Mikrobiologia ogólna Biotechnologia medyczna II rok / I o Temat: Żywność jako środowisko życia mikroorganizmów.
Badania mikrobiologiczne wg PN-EN ISO 11737
 Badania mikrobiologiczne wg PN-EN ISO 11737 mgr Agnieszka Wąsowska Specjalistyczne Laboratorium Badawcze ITA-TEST Z-ca Dyrektora ds. Badań Kierownik Zespołu Badań Mikrobiologicznych i Chemicznych Tel.022
Badania mikrobiologiczne wg PN-EN ISO 11737 mgr Agnieszka Wąsowska Specjalistyczne Laboratorium Badawcze ITA-TEST Z-ca Dyrektora ds. Badań Kierownik Zespołu Badań Mikrobiologicznych i Chemicznych Tel.022
X. Diagnostyka mikrobiologiczna bakterii chorobotwórczych z rodzaju: Corynebacterium, Mycobacterium, Borrelia, Treponema, Neisseria
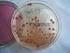 X. Diagnostyka mikrobiologiczna bakterii chorobotwórczych z rodzaju: Corynebacterium, Mycobacterium, Borrelia, Treponema, Neisseria Maczugowce (rodzaj Corynebacterium) Ćwiczenie 1. Wykonanie preparatu
X. Diagnostyka mikrobiologiczna bakterii chorobotwórczych z rodzaju: Corynebacterium, Mycobacterium, Borrelia, Treponema, Neisseria Maczugowce (rodzaj Corynebacterium) Ćwiczenie 1. Wykonanie preparatu
Plasmid Mini AX Gravity
 !"# Plasmid Mini AX Gravity zestaw do izolacji ultraczystego plazmidowego DNA (plazmidy wysokokopijne) wersja 0515/I 100 izolacji Nr kat. 015-100 1 Skład zestawu Składnik Ilość Temp. Przechowywania Kolumny
!"# Plasmid Mini AX Gravity zestaw do izolacji ultraczystego plazmidowego DNA (plazmidy wysokokopijne) wersja 0515/I 100 izolacji Nr kat. 015-100 1 Skład zestawu Składnik Ilość Temp. Przechowywania Kolumny
BIOLOGIA KOMÓRKI BANKOWANIE KOMÓREK
 BIOLOGIA KOMÓRKI BANKOWANIE KOMÓREK WSTĘP Jedną z rutynowych metod laboratoryjnych stosowanych we współczesnej biologii jest długotrwałe przechowywanie żywych komórek w obniżonej temperaturze. Metoda ta
BIOLOGIA KOMÓRKI BANKOWANIE KOMÓREK WSTĘP Jedną z rutynowych metod laboratoryjnych stosowanych we współczesnej biologii jest długotrwałe przechowywanie żywych komórek w obniżonej temperaturze. Metoda ta
Ćwiczenie II Roztwory Buforowe
 Ćwiczenie wykonać w parach lub trójkach. Ćwiczenie II Roztwory Buforowe A. Sporządzić roztwór buforu octanowego lub amonowego o określonym ph (podaje prowadzący ćwiczenia) Bufor Octanowy 1. Do zlewki wlej
Ćwiczenie wykonać w parach lub trójkach. Ćwiczenie II Roztwory Buforowe A. Sporządzić roztwór buforu octanowego lub amonowego o określonym ph (podaje prowadzący ćwiczenia) Bufor Octanowy 1. Do zlewki wlej
Zestaw SIT Szybki Identyfikacyjny Test Szczepów Salmonella Enteritidis i Typhimurium
 Zestaw SIT Szybki Identyfikacyjny Test Szczepów Salmonella Enteritidis i Typhimurium W związku z wprowadzeniem w 2011 roku przez Komisję UE zmian w rozporządzeniach nr 2160/3003 i 2073/2005 w odniesieniu
Zestaw SIT Szybki Identyfikacyjny Test Szczepów Salmonella Enteritidis i Typhimurium W związku z wprowadzeniem w 2011 roku przez Komisję UE zmian w rozporządzeniach nr 2160/3003 i 2073/2005 w odniesieniu
Genomic Micro AX Swab Gravity Plus
 Genomic Micro AX Swab Gravity Plus Zestaw do izolacji genomowego DNA z wymazów metodą grawitacyjną. W skład zestawu wchodzą wymazówki. wersja 0517 100 izolacji Nr kat. 105-100P Pojemność kolumny do oczyszczania
Genomic Micro AX Swab Gravity Plus Zestaw do izolacji genomowego DNA z wymazów metodą grawitacyjną. W skład zestawu wchodzą wymazówki. wersja 0517 100 izolacji Nr kat. 105-100P Pojemność kolumny do oczyszczania
SPIRODELA DUCKWEED TOXKIT Procedura testu
 SPIRODELA DUCKWEED TOXKIT Procedura testu 1 PRZYGOTOWANIE POŻYWKI WZROSTOWEJ I DO ROZCIEŃCZEŃ - KOLBKA MIAROWA (500 ml) - FIOLKI ZE STĘŻONYMI ROZTWORAMI POŻYWKI STEINBERG - CZYSTA WODA (dejonizowana lub
SPIRODELA DUCKWEED TOXKIT Procedura testu 1 PRZYGOTOWANIE POŻYWKI WZROSTOWEJ I DO ROZCIEŃCZEŃ - KOLBKA MIAROWA (500 ml) - FIOLKI ZE STĘŻONYMI ROZTWORAMI POŻYWKI STEINBERG - CZYSTA WODA (dejonizowana lub
Plan badania biegłości wersja uczestników strona 1/6
 strona 1/6 Spis treści 1. Informacje o Organizatorze badania biegłości 2. Charakter i cel programu badania biegłości 3. Uczestnictwo w programie i koszty udziału w badaniu 4. Rodzaj wybranego obiektu badań
strona 1/6 Spis treści 1. Informacje o Organizatorze badania biegłości 2. Charakter i cel programu badania biegłości 3. Uczestnictwo w programie i koszty udziału w badaniu 4. Rodzaj wybranego obiektu badań
Zakład Biologii Molekularnej, Wydział Farmaceutyczny, WUM.
 Zakład Biologii Molekularnej Materiały do ćwiczeń z przedmiotu: TERAPIA GENOWA Plan ćwiczeń Ćwiczenie 1: Przygotowanie warsztatu terapii genowej 1. Kontrola jakościowa preparatów plazmidowych paav/lacz,
Zakład Biologii Molekularnej Materiały do ćwiczeń z przedmiotu: TERAPIA GENOWA Plan ćwiczeń Ćwiczenie 1: Przygotowanie warsztatu terapii genowej 1. Kontrola jakościowa preparatów plazmidowych paav/lacz,
WPŁYW SUBSTANCJI TOWARZYSZĄCYCH NA ROZPUSZCZALNOŚĆ OSADÓW
 WPŁYW SUBSTANCJI TOWARZYSZĄCYCH NA ROZPUSZCZALNOŚĆ OSADÓW Wstęp W przypadku trudno rozpuszczalnej soli, mimo osiągnięcia stanu nasycenia, jej stężenie w roztworze jest bardzo małe i przyjmuje się, że ta
WPŁYW SUBSTANCJI TOWARZYSZĄCYCH NA ROZPUSZCZALNOŚĆ OSADÓW Wstęp W przypadku trudno rozpuszczalnej soli, mimo osiągnięcia stanu nasycenia, jej stężenie w roztworze jest bardzo małe i przyjmuje się, że ta
INSTRUKCJA UŻYTKOWANIA
 INSTRUKCJA UŻYTKOWANIA Certyfikowany materiał referencyjny Epower PRZEZNACZENIE Certyfikowany materiał referencyjny Epower zawiera liofilizowane, standaryzowane ilościowo preparaty mikroorganizmów, które
INSTRUKCJA UŻYTKOWANIA Certyfikowany materiał referencyjny Epower PRZEZNACZENIE Certyfikowany materiał referencyjny Epower zawiera liofilizowane, standaryzowane ilościowo preparaty mikroorganizmów, które
SNAP* BVD. Bovine Virus Diarrhea Antigen Test Kit. Zestaw diagnostyczny do wykrywania antygenu wirusa biegunki i choroby błon śluzowych bydła (BVD-MD)
 SNAP* BVD Bovine Virus Diarrhea Antigen Test Kit Zestaw diagnostyczny do wykrywania antygenu wirusa biegunki i choroby błon śluzowych bydła (BVD-MD) 06-20814-01 Bovine Virus Diarrhea Antigen Test Kit
SNAP* BVD Bovine Virus Diarrhea Antigen Test Kit Zestaw diagnostyczny do wykrywania antygenu wirusa biegunki i choroby błon śluzowych bydła (BVD-MD) 06-20814-01 Bovine Virus Diarrhea Antigen Test Kit
Total RNA Zol-Out. 25 izolacji, 100 izolacji
 Total RNA Zol-Out Zestaw do szybkiej izolacji ultraczystego, całkowitego RNA z odczynników opartych na mieszaninie fenolu oraz rodanku lub chlorowodorku guanidyny (TRIzol, TRI Reagent, RNAzol, QIAzol,
Total RNA Zol-Out Zestaw do szybkiej izolacji ultraczystego, całkowitego RNA z odczynników opartych na mieszaninie fenolu oraz rodanku lub chlorowodorku guanidyny (TRIzol, TRI Reagent, RNAzol, QIAzol,
AmpliTest Babesia spp. (PCR)
 AmpliTest Babesia spp. (PCR) Zestaw do wykrywania sekwencji DNA specyficznych dla pierwotniaków z rodzaju Babesia techniką PCR Nr kat.: BAC21-100 Wielkość zestawu: 100 oznaczeń Objętość pojedynczej reakcji:
AmpliTest Babesia spp. (PCR) Zestaw do wykrywania sekwencji DNA specyficznych dla pierwotniaków z rodzaju Babesia techniką PCR Nr kat.: BAC21-100 Wielkość zestawu: 100 oznaczeń Objętość pojedynczej reakcji:
Zestaw przeznaczony jest do całkowitej izolacji RNA z bakterii, drożdży, hodowli komórkowych, tkanek oraz krwi świeżej (nie mrożonej).
 Total RNA Mini Plus Zestaw do izolacji całkowitego RNA. Procedura izolacji nie wymaga użycia chloroformu wersja 0517 25 izolacji, 100 izolacji Nr kat. 036-25, 036-100 Zestaw przeznaczony jest do całkowitej
Total RNA Mini Plus Zestaw do izolacji całkowitego RNA. Procedura izolacji nie wymaga użycia chloroformu wersja 0517 25 izolacji, 100 izolacji Nr kat. 036-25, 036-100 Zestaw przeznaczony jest do całkowitej
BIOCHEM-ART ; ul. Elfów 75, 80-180 Gdańsk tel./fax (0-58) 304-80-77
 Delvo-X-Press ßL-II Delvo-X-Press ßL-II jest jakościowym niekompetencyjnym testem immunoenzymatycznym przeznaczonym do badania pozostałości antybiotyków ß-laktamowych w surowym i pasteryzowanym mleku krowim.
Delvo-X-Press ßL-II Delvo-X-Press ßL-II jest jakościowym niekompetencyjnym testem immunoenzymatycznym przeznaczonym do badania pozostałości antybiotyków ß-laktamowych w surowym i pasteryzowanym mleku krowim.
