Węglowodory aromatyczne Węglowodory aromatyczne, podobnie jak karbokation allilowy, posiadają zdelokalizowane orbitale typu π.
|
|
|
- Kamil Sosnowski
- 7 lat temu
- Przeglądów:
Transkrypt
1 Węglowodory aromatyczne Węglowodory aromatyczne, podobnie jak karbokation allilowy, posiadają zdelokalizowane orbitale typu π. Wykład 7 1
2 Związki aromatyczne spełniają regułę ückla: liczba elektronów w sprzężonym układzie wiązań podwójnych, spełnia zależność 4n2. A więc aromatyczne są układy z 2, 6, 10, elektronami π. C 3 C 3 C 3 Benzen Toluen o-ksylen Naftalen Liczba elektronów π Wykład 7 2
3 Charakter aromatyczny mogą również posiadać jony, jak np. posiadające po 6 elektronów π, podczas gdy te same obojętne związki nie wykazują właściwości aromatycznych. Wykład 7 3
4 Aromatyczne związki heterocykliczne Związki heterocykliczne zawierają w pierścieniu oprócz atomów węgla, atomy innych pierwiastków (heteroatomy). Jeżeli te atomy dysponują elektronami π, takie związki również mogą być aromatyczne. Jednak różnice w elektroujemnościach węgla i heteroatomów, powodują, że wiązania pomiędzy nimi nie są równocenne. N N N N N pirol furan pirydyna pirymidyna chinolina Wykład 7 4
5 Stabilność cząsteczek związków aromatycznych jest większa niż węglowodorów nienasyconych. W reakcji uwodornienia należy zastosować bardziej drastyczne warunki: 2 Pt 25 0 C, 10 3 hpa 3 2 Ni C, 10 5 hpa Natomiast reakcja z fluorowcami zachodzi w mechaniźmie substytucji elektrofilowej, a nie addycji jak dla alkenów: Fe 3 2 Wykład 7 5
6 Nomenklatura związków aromatycznych. C 3 C 3 C 3 C 3 C 2 5 benzen toluen (metylobenzen) C 3 o-ksylen (1,2-dimetylobenzen) C 3 3 C m-ksylen (1,3-dimetylobenzen) p-ksylen (1,4-dimetylobenzen) etylobenzen N 2 3 C C 3 C C C 3 C N 2 1,2,4-tribromobenzen 1,3-dinitrobenzen (m-dinitrobenzen) 2-fenylo-3-metylobutan trifenylometan Wykład 7 6 naftalen antracen fenantren
7 trzymywanie węglowodorów aromatycznych 1. Ekstrakcja ze smoły pogazowej, pozostałej po pirolizie węgla kamiennego. 2. W niewielkim stopniu destylacja ropy naftowej 3. Katalityczny reforming frakcji C 6 C 10 z ropy naftowej: 2 C 2 C C 3 C 3 C 2 C 2 katalizator C 4. Trimeryzacja etinu otrzymanie benzenu: C C C C C C C Wykład 7 7
8 Reakcje związków aromatycznych substytucja elektrofilowa N 3 2 S 4 N 2 2 nitrowanie S 3 2 S 4 S 3 2 sulfonowanie Cl 2 FeCl 3 Cl Cl chlorowanie C 3 C 3 Cl AlCl 3 Cl alkilowanie C 3 CCl AlCl 3 CC 3 Cl acylowanie Wykład 7 8
9 Mechanizm substytucji elektrofilowej Czynnikiem nitrującym jest kation nitroniowy N 2 : który zabiera parę elektronów z sekstetu elektronów aromatycznych i przyłącza się do jednego atomu węgla. Karbokation jest stabilizowany przez rezonans. Wykład 7 9
10 Mechanizm chlorowania arenów Wytworzenie kationu chlorowego pod wpływem katalizatora: Przyłączenie elektrofila do pierścienia i stabilizacja karbokationu przez struktury rezonansowe. Następnie po odejściu protonu odnowienie pierścienia aromatycznego: Wykład 7 10
11 Substytucja elektrofilowa pochodnych benzenu, efekt kierujący podstawników. 1.Podstawniki 1-go rodzaju, aktywujące: -, -N 2, -R 2.Podstawniki 1-go rodzaju, dezaktywujące: -Cl, -, -I 3.Podstawniki 2-go rodzaju, dezaktywujące: -N 2, -C, -C Podstawniki 1-go rodzaju aktywują pierścień na atak elektrofilowy na węglach orto i para. Podstawniki 2-go rodzaju dezaktywują pierścień i kierują podstawniki w położenia meta. Podstawniki 1-go rodzaju dezaktywujące, dezaktywują pierścień i kierują podstawniki w położenia orto i para. Wykład 7 11
12 Mechanizm substytucji elektrofilowej fenolu - bromowanie fenol 2 Fe 3 o-bromofenol p-bromofenol Wykład 7 12
13 Mechanizm substytucji elektrofilowej nitrobenzenu - chlorowanie N 2 N 2 nitrobenzen Cl 2 AlCl 3 Cl m-chloronitrobenzen N 2 N 2 N 2 N 2 N 2 X Cl N 2 N 2 Cl N 2 Cl Cl Cl Cl Wykład 7 13 niekorzystna struktura Cl
14 Planowanie syntezy podstawionych związków aromatycznych Aby otrzymać wszystkie możliwe izomery bromonitrobenzenu należy przeprowadzić najpierw bromowanie, a potem nitrowanie dla izomerów orto i para; a dla izomeru meta kolejność reakcji jest odwrotna. 2 Fe 3 N 3 2 S 4 2 N p-bromonitrobenzen N 2 o-bromonitrobenzen N 3 2 S 4 N 2 N 2 2 Fe 3 Wykład 7 14 m-bromonitrobenzen
15 Węglowodory alifatyczno-aromatyczne Właściwości chemiczne węglowodorów alifatyczno-aromatycznych są podobne dla obu typów związków. Reakcje charakterystyczne dla arenów będą zachodzić na pierścieniu, reakcje charakterystyczne dla alifatów, będą zachodzić na łańcuchu bocznym. C 2 C 2 C 3 C 3 2 hν 2 2 hν hν bromek benzylu dibromofenylo metan tribromofenylometan 2 C 3 C 3 C 3 Fe Fe 3 Fe 3 2-bromotoluen 2,4-dibromotoluen 2,4,6-tribromotoluen Wykład 7 15
16 Utlenianie łańcucha bocznego związków alifatyczno-aromatycznych, bez względu na długość łańcucha i podstawniki zachodzi zawsze na pierwszym atomie węgla z utworzeniem kwasu benzoesowego. C 2 C 3 3 C C 3 C KMn 4 KMn C C C 3 C C 2 C 3 KMn C KMn C KMn C C 2 C 2 N 2 Wykład 7 16
17 trzymywanie węglowodorów alifatyczno-aromatycznych 1. Alkilowanie Friedla-Craftsa: C 3 Cl C 3 AlCl 3 2. Acylowanie Friedla-Craftsa i redukcja powstałego ketonu: C 3 7 C Cl C C3 7 Zn(g) C 2 C 3 7 AlCl 3 Cl Wykład 7 17
18 Alkohole Alkohole to związki organiczne, posiadające w cząsteczce przynajmniej jedną hydroksylową grupę funkcyjną ( ). Jeżeli grupa ta jest połączona bezpośrednio z pierścieniem aromatycznym, to taki związek należy do fenoli. Duża różnica elektroujemności między węglem a tlenem, oraz hybrydyzacja sp 3 na atomie tlenu wraz z obecnością niewiążących par elektronów, powoduje polarność cząsteczki. Grupa hydroksylowa jest hydrofilowa, a część węglowodorowa jest hydrofobowa (lipofilowa). Alkohole są dobrymi rozpuszczalnikami zarówno dla związków polarnych, jak i niepolarnych. Wyższa temperatura wrzenia dzięki obecności wiązań wodorowych. Wykład 7 18
19 Nomenklatura alkoholi Nazwy alkoholi tworzy się dodając do nazwy odpowiedniego węglowodoru końcówkę ol, poprzedzoną numerem węgla, przy którym występuje. Dla alkoholi wielowodorotlenowych dodaje się końcówkę: -diol, -triol, itd. C 3 C C C 2 C 2 3 C C C 3 metanol etanol propan-1-ol propan-2-ol 2 C C 2 2 C C C 2 etano-1,2-diol (glikol etylenowy) propano-1,2,3-triol (gliceryna, glicerol) cykloheksanol fenol Wykład 7 19
20 Rząd zerowy C 3 metanol Rzędowość alkoholi Alkohole 1-rzędowe C C C 2 C 2 etanol Alkohole 2-rzędowe 3 C C C 3 propan-2-ol Alkohole 3-rzędowe propan-1-ol 3 C C 2 C C 3 butan-2-ol (sec-butanol) 3 C C 2 C 2 C 2 butan-1-ol cykloheksanol 3 C 3 C C C 2 2-metylopropan-1-ol (izobutanol) 3 C C 3 C C 3 2-metylopropan-2-ol (tert-butanol) Wykład 7 20
21 Reakcje otrzymywania alkoholi 1. Addycja wody do wiązania podwójnego węgiel-węgiel 2. Redukcja związków karbonylowych i karboksylowych NaB 3 R C R C 2 R C R alkohol 1-rzędowy keton aldehyd R C R' Wykład 7 21 ester LiAl 4 R C 2 R' alkohol 1-rzędowy NaB 3 R C R alkohol 2-rzędowy
22 3. Synteza Grignarda otrzymywanie alkoholi ze związków magnezoorganicznych i związków karbonylowych eter δ δ R Cl Mg R Mg Cl R' δ C δ R'' δ δ 1) R MgCl 2) 2 R' R C R'' 4. ydroliza halogenków alkilowych Na R Cl R NaCl 2 Wykład 7 22
23 Reakcje alkoholi 1. Reakcje z rozerwaniem wiązania -. W obecności silnych zasad, alkohole mogą zachowywać się jak kwasy. W roztworach wodnych jednak nie ulegają dysocjacji. R N 2 - R N 3 Bezwodne alkohole reagują z metalami alkalicznymi w wydzielaniem gazowego wodoru i tworzeniem alkoholanów. R Na RNa 2 Wykład 7 23
24 Reakcja estryfikacji. Z kwasami karboksylowymi i ich pochodnymi (chlorkami, bezwodnikami) alkohole tworzą estry: R C kwas karboksylowy R' R C R' ester 2 R C Cl R' R C R' Cl chlorek kwasowy ester Estry mogą tworzyć również kwasy nieorganiczne: C 2 5 P C 2 5 C 2 5 fosforan (V) trietylu Wykład 7 24
25 2. Reakcje z rozerwaniem wiązania C-. Reakcje podstawienia nukleofilowego. Często przebiegają poprzez karbokationy: protonowanie grupy hydroksylowej i oderwanie cząsteczki wody. Karbokationy mogą ulegać przegrupowaniom do trwalszych, o większej rzędowości. Wykład 7 25
26 Mechanizm substytucji nukleofilowej S N 1i S N 2 W związku z różnicami trwałości karbokationów, reakcja podstawienia nukleofilowego może przebiegać wg dwóch mechanizmów: dwucząsteczkowego S N 2 (metanol i 1-rzędowe): C C 2 - C 2-2 C lub jednocząsteczkowego S N 1 (3-rzędowe): 3 C 3 C C 3 C 3 C 3 C C 3 C C C 3 C C 3-3 C 3 C C 3 C 2-rzędowe reagują wg mechanizmu mieszanego. Wykład 7 26
27 Reakcje z halogenowodorami przebiega wg mechanizmu substytucji nukleofilowej. Do tej reakcji konkurencyjna jest reakcja eliminacji wody. Eliminacja również może przebiegać wg mechanizmu jednocząsteczkowego E1, jak i dwucząsteczkowego E2. Na etapie karbokationu może nastąpić przegrupowanie. C C 2 S 4 Δ C C 2 Mechanizm C C C C C C 2 C C Wykład 7 27
28 Utlenianie alkoholi 1-rzędowych prowadzi do aldehydów i kwasów karboksylowych: C 3 C 2 C 2 C 2 butanol Cr 3 C 3 C 2 C 2 butanal C Cr 3 aldehyd butylowy Alkohole 2-rzędowe utleniają się do ketonów: K 2 Cr 2 7 C 3 C 2 CC 3 C 3 C 2 CC 3 butan-2-ol butanon keton metylowoetylowy C 3 C 2 C 2 C kwas butanowy kwas masłowy Alkohole 3-rzędowe można utlenić jedynie z rozpadem cząsteczki. Wykład 7 28
29 Związki, które posiadają grupę hydroksylową połączoną bezpośrednio do pierścienia aromatycznego, to fenole. Fenole mają charakter słabo kwaśny. W wodzie dysocjują na jony, a z zasadami tworzą sole fenolany. Właściwości te nadają wolne pary elektronowe na atomie tlenu, które wchodzą w rezonans z elektronami pierścienia: Z tego też powodu fenole są bardziej aktywne w reakcji substytucji elektrofilowej. Wykład 7 29
30 W fenolach występują wiązania wodorowe. Mogą one być pomiędzy cząsteczkami, lub wewnątrzcząsteczkowe. Związki z wiązaniami wodorowymi wewnątrz cząsteczki charakteryzują się mniejszą polarnością i niższą lotnością. N N Wykład 7 30
31 Nazewnictwo fenoli. C 3 Cl fenol 2-metylofenol (o-krezol) 3-chlorofenol (m-chlorofenol) N 2 4-aminofenol (p-aminofenol) C Benzeno-1,4-diol (ydrochinon) Benzeno-1,3-diol (Rezorcynol) Benzeno-1,2-diol (Pirokatechol) Kwas o-hydroksybenzoesowy (Kwas salicylowy) 2 N N 2 Wykład 7 31 N 2 1-naftol 2-naftol 2,4,6-trinitrofenol (kwas pikrynowy)
32 trzymywanie fenoli 1. Na przemysłową skalę fenol otrzymuje się z chlorobenzenu w wysokiej temperaturze i pod dużym ciśnieniem. Cl Na Δ / p 2. W laboratorium fenole otrzymuje się z sulfonianów lub soli diazoniowych. S 3 K K 2 / Δ N 2 Cl 2 2 S 4 Wykład 7 32 C 3 C 3
33 1. Dysocjacja elektrolityczna. Reakcje fenoli Anion jest stabilizowany przez rezonans: Jeszcze lepsza stabilizacja jest dla fenolanów z podstawnikami wyciągającymi elektrony. Wykład 7 33
34 2. Tworzenie estrów C C 2 5 C 2 5 C Cl Cl propionian fenylu C 3 C 3 C C C C 2 5 C 3 C octan fenylu Wykład 7 34
35 3. Substytucja elektrofilowa omowanie ,4,6-tribromofenol 2 N N 2 N 3 stęż. N 2 Nitrowanie N 3 rozc. 2,4,6-trinitrofenol N 2 N 2 p-nitrofenol Wykład 7 35 o-nitrofenol
36 4. Utlenianie Na 2 Cr 2 7 hydrochinon Na 2 Cr 2 7 pirokatechina Wykład 7 36
37 Etery związki o wzorze ogólnym R--R. R i R mogą być pochodnymi alifatycznymi lub aromatycznymi. C 2 5 C 2 5 C 3 C 3 C C 3 C 3 eter dietylowy eter izopropylowo-metylowy eter fenylowo-metylowy (metoksybenzen) eter fenylowo-1-naftylowy Wykład 7 37
38 trzymywanie eterów Synteza Williamsona: C 3 C 2 5 Na C 3 C 2 5 Na C 2 5 Cl 3 C 3 C C Na 3 C 3 C C C 2 5 NaCl Etery aromatyczno-alifatyczne: C 5 11 Cl C 5 11 NaCl 2 Wykład 7 38
Chemia organiczna to chemia związków węgla.
 Chemia organiczna to chemia związków węgla. Do tej pory wyizolowano lub zsyntetyzowano kilkanaście milionów związków organicznych. Na dużą różnorodność chemii organicznej mają wpływ: średnia elektroujemność
Chemia organiczna to chemia związków węgla. Do tej pory wyizolowano lub zsyntetyzowano kilkanaście milionów związków organicznych. Na dużą różnorodność chemii organicznej mają wpływ: średnia elektroujemność
Chemia organiczna to chemia związków węgla.
 Chemia organiczna to chemia związków węgla. Do tej pory wyizolowano lub zsyntetyzowano kilkanaście milionów związków organicznych. Na dużą różnorodność chemii organicznej mają wpływ: średnia elektroujemność
Chemia organiczna to chemia związków węgla. Do tej pory wyizolowano lub zsyntetyzowano kilkanaście milionów związków organicznych. Na dużą różnorodność chemii organicznej mają wpływ: średnia elektroujemność
CH 3 OH C 2 H 5 OH H 3 C CH 2 CH 2 OH H 3 C CH CH 3 OH metanol etanol propan-1-ol propan-2-ol H 2 C CH 2 OH OH H 2 C CH CH 2 OH OH OH
 Alkohole Alkohole to związki organiczne, posiadające w cząsteczce przynajmniej jedną hydroksylową grupę funkcyjną ( ). Jeżeli grupa ta jest połączona bezpośrednio z pierścieniem aromatycznym, to taki związek
Alkohole Alkohole to związki organiczne, posiadające w cząsteczce przynajmniej jedną hydroksylową grupę funkcyjną ( ). Jeżeli grupa ta jest połączona bezpośrednio z pierścieniem aromatycznym, to taki związek
Związki aromatyczne CH 3 NH 2 OH CN. toluen anilina fenol benzonitryl O CHO CCH 3 COOH CH CH 2. kwas benzoesowy. acetofenon. benzaldehyd.
 Związki aromatyczne Cl NO 2 C 2 C 3 benzen chlorobenzen nitrobenzen etylobenzen C 3 N 2 O CN toluen anilina fenol benzonitryl O CO CC 3 COO C C 2 benzaldehyd acetofenon kwas benzoesowy styren 1 C 3 C 3
Związki aromatyczne Cl NO 2 C 2 C 3 benzen chlorobenzen nitrobenzen etylobenzen C 3 N 2 O CN toluen anilina fenol benzonitryl O CO CC 3 COO C C 2 benzaldehyd acetofenon kwas benzoesowy styren 1 C 3 C 3
Aleksander Kołodziejczyk Krystyna Dzierzbicka CHEMII. organicznej Tom 1
 Aleksander Kołodziejczyk Krystyna Dzierzbicka CHEMII organicznej Tom 1 Gdansk 2014 PRZEWODNICZĄCY KOMITETU REDAKCYJNEGO WYDAWNICTWA POLITECHNIKI GDAŃSKIEJ Janusz T. Cieśliński RECENZENT Elżbieta Luboch
Aleksander Kołodziejczyk Krystyna Dzierzbicka CHEMII organicznej Tom 1 Gdansk 2014 PRZEWODNICZĄCY KOMITETU REDAKCYJNEGO WYDAWNICTWA POLITECHNIKI GDAŃSKIEJ Janusz T. Cieśliński RECENZENT Elżbieta Luboch
METODY OTRZYMYWANIA ESTRÓW I AMIDÓW. SYNTEZA KWASU ACETYLOSALICYLOWEGO.
 hemia organiczna METDY TRZYMYWAIA ESTRÓW I AMIDÓW. SYTEZA KWASU AETYLSALIYLWEG. Kwas acetylosalicylowy, znany jako aspiryna albo polopiryna, należy do grupy niesteroidowych leków przeciwzapalnych (LPZ)
hemia organiczna METDY TRZYMYWAIA ESTRÓW I AMIDÓW. SYTEZA KWASU AETYLSALIYLWEG. Kwas acetylosalicylowy, znany jako aspiryna albo polopiryna, należy do grupy niesteroidowych leków przeciwzapalnych (LPZ)
Slajd 1. Związki aromatyczne
 Slajd 1 Związki aromatyczne Slajd 2 Reguły aromatyczności 1. Związek musi posiadać cykliczną chmurę elektronową ponad i pod płaszczyzną cząsteczki 2. Chmura elektronów π musi zawierać nieparzystą liczbę
Slajd 1 Związki aromatyczne Slajd 2 Reguły aromatyczności 1. Związek musi posiadać cykliczną chmurę elektronową ponad i pod płaszczyzną cząsteczki 2. Chmura elektronów π musi zawierać nieparzystą liczbę
Węglowodory aromatyczne (areny) to płaskie cykliczne związki węgla i wodoru. Areny. skondensowane liniowo. skondensowane kątowo
 Spis treści Podstawowe pojęcia Właściwości chemiczne benzenu Wielopierścieniowe węglowodory aromatyczne Homologi benzenu Nazewnictwo związków aromatycznych Występowanie i otrzymywanie arenów Węglowodory
Spis treści Podstawowe pojęcia Właściwości chemiczne benzenu Wielopierścieniowe węglowodory aromatyczne Homologi benzenu Nazewnictwo związków aromatycznych Występowanie i otrzymywanie arenów Węglowodory
Pochodne węglowodorów, w cząsteczkach których jeden atom H jest zastąpiony grupą hydroksylową (- OH ).
 Cz. XXII - Alkohole monohydroksylowe Pochodne węglowodorów, w cząsteczkach których jeden atom jest zastąpiony grupą hydroksylową (- ). 1. Klasyfikacja alkoholi monohydroksylowych i rodzaje izomerii, rzędowość
Cz. XXII - Alkohole monohydroksylowe Pochodne węglowodorów, w cząsteczkach których jeden atom jest zastąpiony grupą hydroksylową (- ). 1. Klasyfikacja alkoholi monohydroksylowych i rodzaje izomerii, rzędowość
Informacje uzyskiwane dzięki spektrometrii mas
 Slajd 1 Spektrometria mas i sektroskopia w podczerwieni Slajd 2 Informacje uzyskiwane dzięki spektrometrii mas Masa cząsteczkowa Wzór związku Niektóre informacje dotyczące wzoru strukturalnego związku
Slajd 1 Spektrometria mas i sektroskopia w podczerwieni Slajd 2 Informacje uzyskiwane dzięki spektrometrii mas Masa cząsteczkowa Wzór związku Niektóre informacje dotyczące wzoru strukturalnego związku
spektroskopia UV Vis (cz. 2)
 spektroskopia UV Vis (cz. 2) spektroskopia UV-Vis dlaczego? wiele związków organicznych posiada chromofory, które absorbują w zakresie UV duża czułość: zastosowanie w badaniach kinetyki reakcji spektroskop
spektroskopia UV Vis (cz. 2) spektroskopia UV-Vis dlaczego? wiele związków organicznych posiada chromofory, które absorbują w zakresie UV duża czułość: zastosowanie w badaniach kinetyki reakcji spektroskop
Związki aromatyczne (by Aleksandra Kołodziejczyk, UG)
 Związki aromatyczne (by Aleksandra Kołodziejczyk, UG) 4 stopnie nienasycenia. ak reakcji A Źródła: - piroliza węgla smoła pogazowa; - reforming ropy naftowej Nazewnictwo przedrostek nazwa podstawnika C
Związki aromatyczne (by Aleksandra Kołodziejczyk, UG) 4 stopnie nienasycenia. ak reakcji A Źródła: - piroliza węgla smoła pogazowa; - reforming ropy naftowej Nazewnictwo przedrostek nazwa podstawnika C
Chemia organiczna. Alkohole Fenole. Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny
 Chemia organiczna Alkohole Fenole Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny 1 Związki zawierające grupę OH alkohole enole fenol sp 3 sp 2 alkohole nienasycone, aromatyczne sp 2 pochodne alkanów
Chemia organiczna Alkohole Fenole Zakład Chemii Medycznej Pomorski Uniwersytet Medyczny 1 Związki zawierające grupę OH alkohole enole fenol sp 3 sp 2 alkohole nienasycone, aromatyczne sp 2 pochodne alkanów
Kwasy karboksylowe grupa funkcyjna: -COOH. Wykład 8 1
 Kwasy karboksylowe grupa funkcyjna: -CH Wykład 8 1 1. Reakcje utleniania a) utlenianie alkoholi pierwszorzędowych trzymywanie kwasów CH 3 H 3 C C CH 2 H CH 3 alkohol pierwszorzędowy CH K 2 Cr 2 3 7 H 3
Kwasy karboksylowe grupa funkcyjna: -CH Wykład 8 1 1. Reakcje utleniania a) utlenianie alkoholi pierwszorzędowych trzymywanie kwasów CH 3 H 3 C C CH 2 H CH 3 alkohol pierwszorzędowy CH K 2 Cr 2 3 7 H 3
Slajd 1. Alkohole i fenole. Cholesterol. Slajd 2. Budowa alkoholi. metanol. metanol. Grupą funkcyjną jest (OH) Tlen posiada hybrydyzacjęsp 3
 Slajd 1 Alkohole i fenole Cholesterol Slajd 2 Budowa alkoholi woda woda metanol metanol Grupą funkcyjną jest () Tlen posiada hybrydyzacjęsp 3 Slajd 3 Podział alkoholi Pierwszorzędowe: grupa połączona jest
Slajd 1 Alkohole i fenole Cholesterol Slajd 2 Budowa alkoholi woda woda metanol metanol Grupą funkcyjną jest () Tlen posiada hybrydyzacjęsp 3 Slajd 3 Podział alkoholi Pierwszorzędowe: grupa połączona jest
TEORIE KWASÓW I ZASAD.
 TERIE KWASÓW I ZASAD. Teoria Arrheniusa (nagroda Nobla 1903 r). Kwas kaŝda substancja, która dostarcza jony + do roztworu. A + + A Zasada kaŝda substancja, która dostarcza jony do roztworu. M M + + Reakcja
TERIE KWASÓW I ZASAD. Teoria Arrheniusa (nagroda Nobla 1903 r). Kwas kaŝda substancja, która dostarcza jony + do roztworu. A + + A Zasada kaŝda substancja, która dostarcza jony do roztworu. M M + + Reakcja
Spis treści 1. Struktura elektronowa związków organicznych 2. Budowa przestrzenna cząsteczek związków organicznych
 Spis treści 1. Struktura elektronowa związków organicznych 13 2. Budowa przestrzenna cząsteczek związków organicznych 19 2.1. Zadania... 28 3. Zastosowanie metod spektroskopowych do ustalania struktury
Spis treści 1. Struktura elektronowa związków organicznych 13 2. Budowa przestrzenna cząsteczek związków organicznych 19 2.1. Zadania... 28 3. Zastosowanie metod spektroskopowych do ustalania struktury
Wymagania edukacyjne na poszczególne oceny
 Wymagania edukacyjne na poszczególne oceny VII. Węgiel i jego związki z wodorem podaje kryteria podziału chemii na organiczną i nieorganiczną określa, czym zajmuje się chemia organiczna definiuje pojęcie
Wymagania edukacyjne na poszczególne oceny VII. Węgiel i jego związki z wodorem podaje kryteria podziału chemii na organiczną i nieorganiczną określa, czym zajmuje się chemia organiczna definiuje pojęcie
Oznaczanie właściwości tłuszczów
 znaczanie właściwości tłuszczów Prowadzący: mgr inż. Maciej Chrubasik Wstęp teoretyczny Lipidy Lipidy ( tłuszcze ) są estrami kwasów tłuszczowych : - gdy alkoholem jest gliceryna ( 1,2,3-trihydroksy propan;
znaczanie właściwości tłuszczów Prowadzący: mgr inż. Maciej Chrubasik Wstęp teoretyczny Lipidy Lipidy ( tłuszcze ) są estrami kwasów tłuszczowych : - gdy alkoholem jest gliceryna ( 1,2,3-trihydroksy propan;
Lekcja 15. Temat: Prąd elektryczny w róŝnych środowiskach.
 Lekcja 15 Temat: Prąd elektryczny w róŝnych środowiskach. Pod wpływem pola elektrycznego (przyłoŝonego napięcia) w materiałach, w których istnieją ruchliwe nośniki ładunku dochodzi do zjawiska przewodzenia
Lekcja 15 Temat: Prąd elektryczny w róŝnych środowiskach. Pod wpływem pola elektrycznego (przyłoŝonego napięcia) w materiałach, w których istnieją ruchliwe nośniki ładunku dochodzi do zjawiska przewodzenia
Atom poziom podstawowy
 Atom poziom podstawowy Zadanie 1. (1 pkt) Źródło: CKE 2010 (PP), zad. 1. Atomy pewnego pierwiastka w stanie podstawowym maj nast puj c konfiguracj elektronów walencyjnych: 2s 2 2p 3 (L 5 ) Okre l po o
Atom poziom podstawowy Zadanie 1. (1 pkt) Źródło: CKE 2010 (PP), zad. 1. Atomy pewnego pierwiastka w stanie podstawowym maj nast puj c konfiguracj elektronów walencyjnych: 2s 2 2p 3 (L 5 ) Okre l po o
Podstawowe oddziaływania w Naturze
 Podstawowe oddziaływania w Naturze Wszystkie w zjawiska w Naturze są określone przez cztery podstawowe oddziaływania Silne Grawitacja Newton Elektromagnetyczne Słabe n = p + e - + ν neutron = proton +
Podstawowe oddziaływania w Naturze Wszystkie w zjawiska w Naturze są określone przez cztery podstawowe oddziaływania Silne Grawitacja Newton Elektromagnetyczne Słabe n = p + e - + ν neutron = proton +
C OH ALKOHOLE ETERY R OH R O R R' O FENOLE. Ar OH NOMENKLATURA ALKOHOLE ZWIĄZKI ORGANICZNE ZAWIERAJĄCE W STRUKTURZE ATOMY TLENU C O C OH CH 3 OH
 ZWIĄZKI GANIZNE ZAWIEAJĄE W STUKTUZE ATMY TLENU 8 1s2 2s 2 2p 4 okres 2; grupa VI w związkach jest dwuwiążący, z dwoma niewiążącymi parami elektronów drugi w skali elektroujemności Paulinga 3.5 (za fluorem)
ZWIĄZKI GANIZNE ZAWIEAJĄE W STUKTUZE ATMY TLENU 8 1s2 2s 2 2p 4 okres 2; grupa VI w związkach jest dwuwiążący, z dwoma niewiążącymi parami elektronów drugi w skali elektroujemności Paulinga 3.5 (za fluorem)
Podział związków organicznych
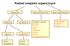 Podział związków organicznych węglowodory związki jednofunkcyjne związki wielofunkcyjne alifatyczne nasycone aromatyczne nienasycone halogenki alkilowe alkohole fenole etery aldehydy ketony aminy kwasy
Podział związków organicznych węglowodory związki jednofunkcyjne związki wielofunkcyjne alifatyczne nasycone aromatyczne nienasycone halogenki alkilowe alkohole fenole etery aldehydy ketony aminy kwasy
RJC. 1 Kwasy i Zasady. Kwasy i zasady Brønsteda Stabilizacja Rezonansowa Kwasy i Zasady Lewisa HA + B: A - + BH + Slides 1 to 35
 1 Kwasy i Zasady Kwasy i zasady Brønsteda Stabilizacja Rezonansowa Kwasy i Zasady Lewisa HA + B: A - + BH + Slides 1 to 35 2 Kwas : Definicja Brønsteda Kwasem jest taki związek zek chemiczny, który moŝe
1 Kwasy i Zasady Kwasy i zasady Brønsteda Stabilizacja Rezonansowa Kwasy i Zasady Lewisa HA + B: A - + BH + Slides 1 to 35 2 Kwas : Definicja Brønsteda Kwasem jest taki związek zek chemiczny, który moŝe
wykład: Alkohole, Etery i Fenole
 wykład: Alkohole, Etery i Fenole Alkohole Alkohole związki organiczne o wzorze ogólnym R- w których grupa hydroksylowa połączona jest z atomem węgla z łańcucha węglowego. Alkohole nasycone Alkohole nienasycone
wykład: Alkohole, Etery i Fenole Alkohole Alkohole związki organiczne o wzorze ogólnym R- w których grupa hydroksylowa połączona jest z atomem węgla z łańcucha węglowego. Alkohole nasycone Alkohole nienasycone
WĘGLOWODORY AROMATYCZNE
 WĘGLOWODORY AROMATYCZNE cykliczne węglowodory spełniające warunki aromatyczności: Ale: związki niearomatyczne 1 ZWIĄZKI AROMATYCZNE - przykłady 2 NOMENKLATURA Monocykliczne węglowodory aromatyczne są nazywane
WĘGLOWODORY AROMATYCZNE cykliczne węglowodory spełniające warunki aromatyczności: Ale: związki niearomatyczne 1 ZWIĄZKI AROMATYCZNE - przykłady 2 NOMENKLATURA Monocykliczne węglowodory aromatyczne są nazywane
RJC E + E H. Slides 1 to 41
 Aromatyczne Substytucje Elektrofilowe E + E H -H E Slides 1 to 41 Aromatyczne Addycje Elektrofilowe...do pierścienia aromatycznego przerywa sprzęŝenie elektronów π i powoduje utratę stabilizacji poprzez
Aromatyczne Substytucje Elektrofilowe E + E H -H E Slides 1 to 41 Aromatyczne Addycje Elektrofilowe...do pierścienia aromatycznego przerywa sprzęŝenie elektronów π i powoduje utratę stabilizacji poprzez
Elementy chemii organicznej
 Elementy chemii organicznej węglowodory alifatyczne węglowodory aromatyczne halogenopochodne węglowodorów alkohole etery aldehydy i ketony kwasy karboksylowe estry aminy Alkany C n H 2n+2 struktura Kekulégo
Elementy chemii organicznej węglowodory alifatyczne węglowodory aromatyczne halogenopochodne węglowodorów alkohole etery aldehydy i ketony kwasy karboksylowe estry aminy Alkany C n H 2n+2 struktura Kekulégo
Stechiometria równań reakcji chemicznych, objętość gazów w warunkach odmiennych od warunków normalnych (0 o C 273K, 273hPa)
 Karta pracy I/2a Stechiometria równań reakcji chemicznych, objętość gazów w warunkach odmiennych od warunków normalnych (0 o C 273K, 273hPa) I. Stechiometria równań reakcji chemicznych interpretacja równań
Karta pracy I/2a Stechiometria równań reakcji chemicznych, objętość gazów w warunkach odmiennych od warunków normalnych (0 o C 273K, 273hPa) I. Stechiometria równań reakcji chemicznych interpretacja równań
PODSTAWY OBLICZEŃ CHEMICZNYCH DLA MECHANIKÓW
 PODSTAWY OBLICZEŃ CHEMICZNYCH DLA MECHANIKÓW Opracowanie: dr inż. Krystyna Moskwa, dr Wojciech Solarski 1. Termochemia. Każda reakcja chemiczna związana jest z wydzieleniem lub pochłonięciem energii, najczęściej
PODSTAWY OBLICZEŃ CHEMICZNYCH DLA MECHANIKÓW Opracowanie: dr inż. Krystyna Moskwa, dr Wojciech Solarski 1. Termochemia. Każda reakcja chemiczna związana jest z wydzieleniem lub pochłonięciem energii, najczęściej
Wykład 8. Korzystałem z : R. Morrison, R. Boyd: Chemia organiczna (wyd. ang.)
 Wykład 8 Korzystałem z : R. Morrison, R. Boyd: Chemia organiczna (wyd. ang.) ALKOHOLE I FENOLE Związki o wzorze ogólnym R-OH. W fenolach grupa OH jest bezpośrednio związana z pierścieniem aromatycznum.
Wykład 8 Korzystałem z : R. Morrison, R. Boyd: Chemia organiczna (wyd. ang.) ALKOHOLE I FENOLE Związki o wzorze ogólnym R-OH. W fenolach grupa OH jest bezpośrednio związana z pierścieniem aromatycznum.
Materiały dodatkowe alkohole, fenole, etery
 Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe alkohole, fenole, etery Alkohole i fenole 1 Własności kwasowo-zasadowe alkoholi i fenoli becność grupy H, posiadającej
Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe alkohole, fenole, etery Alkohole i fenole 1 Własności kwasowo-zasadowe alkoholi i fenoli becność grupy H, posiadającej
Zapisz wzory form kwasu asparaginowego i lizyny występujących w roztworze: a) silnie kwasowym b) silnie zasadowym
 Zadanie: 1 (4pkt) Podane są wzory dwóch aminokwasów: lizyny i kwasu asparaginowego Zapisz wzory form kwasu asparaginowego i lizyny występujących w roztworze: a) silnie kwasowym b) silnie zasadowym Zadanie:
Zadanie: 1 (4pkt) Podane są wzory dwóch aminokwasów: lizyny i kwasu asparaginowego Zapisz wzory form kwasu asparaginowego i lizyny występujących w roztworze: a) silnie kwasowym b) silnie zasadowym Zadanie:
Def. Kwasy karboksylowe to związki, których cząsteczki zawierają jedną lub więcej grup
 Cz. XXV - Kwasy karboksylowe Def. Kwasy karboksylowe to związki, których cząsteczki zawierają jedną lub więcej grup karboksylowych - CH ( - C - H ), atom C w grupie funkcyjnej jest na hybrydyzacji sp 2,
Cz. XXV - Kwasy karboksylowe Def. Kwasy karboksylowe to związki, których cząsteczki zawierają jedną lub więcej grup karboksylowych - CH ( - C - H ), atom C w grupie funkcyjnej jest na hybrydyzacji sp 2,
Olej rzepakowy, jako paliwo do silników z zapłonem samoczynnym
 Coraz częściej jako paliwo stosuje się biokomponenty powstałe z roślin oleistych. Nie mniej jednak właściwości fizykochemiczne oleju napędowego i oleju powstałego z roślin znacząco różnią się miedzy sobą.
Coraz częściej jako paliwo stosuje się biokomponenty powstałe z roślin oleistych. Nie mniej jednak właściwości fizykochemiczne oleju napędowego i oleju powstałego z roślin znacząco różnią się miedzy sobą.
Techniczne nauki М.М.Zheplinska, A.S.Bessarab Narodowy uniwersytet spożywczych technologii, Кijow STOSOWANIE PARY WODNEJ SKRAPLANIA KAWITACJI
 Techniczne nauki М.М.Zheplinska, A.S.Bessarab Narodowy uniwersytet spożywczych technologii, Кijow STOSOWANIE PARY WODNEJ SKRAPLANIA KAWITACJI SKLAROWANEGO SOKU JABŁKOWEGO Skutecznym sposobem leczenia soku
Techniczne nauki М.М.Zheplinska, A.S.Bessarab Narodowy uniwersytet spożywczych technologii, Кijow STOSOWANIE PARY WODNEJ SKRAPLANIA KAWITACJI SKLAROWANEGO SOKU JABŁKOWEGO Skutecznym sposobem leczenia soku
Spektroskopia UV-VIS zagadnienia
 Spektroskopia absorbcyjna to dziedzina, która obejmuje metody badania materii przy użyciu promieniowania elektromagnetycznego, które może z tą materią oddziaływać. Spektroskopia UV-VS zagadnienia promieniowanie
Spektroskopia absorbcyjna to dziedzina, która obejmuje metody badania materii przy użyciu promieniowania elektromagnetycznego, które może z tą materią oddziaływać. Spektroskopia UV-VS zagadnienia promieniowanie
Nagroda Nobla z fizjologii i medycyny w 2004 r.
 Nagroda Nobla z fizjologii i medycyny w 2004 r. Receptory zapachu i organizacja systemu węchowego Takao Ishikawa, M.Sc. Zakład Biologii Molekularnej Instytut Biochemii Uniwersytetu Warszawskiego 10 mln
Nagroda Nobla z fizjologii i medycyny w 2004 r. Receptory zapachu i organizacja systemu węchowego Takao Ishikawa, M.Sc. Zakład Biologii Molekularnej Instytut Biochemii Uniwersytetu Warszawskiego 10 mln
18. Reakcje benzenu i jego pochodnych
 18. Reakcje benzenu i jego pochodnych 1 18.1. Nazewnictwo mono-podstawionych benzenów nazwa podstawnika - przedrostek przed słowem benzen wiele nazw zwyczajowych (pokazane wybrane związki) pierścień benzenowy
18. Reakcje benzenu i jego pochodnych 1 18.1. Nazewnictwo mono-podstawionych benzenów nazwa podstawnika - przedrostek przed słowem benzen wiele nazw zwyczajowych (pokazane wybrane związki) pierścień benzenowy
Wykład 6. Korzystałem z : R. Morrison, R. Boyd: Chemia organiczna (wyd. ang.)
 Wykład 6 Korzystałem z : R. Morrison, R. Boyd: Chemia organiczna (wyd. ang.) Dieny Dieny są alkenami, których cząsteczki zawierają 2 podwójne wiązania C=C. Zasadnicze właściwości dienów są takie jak alkenów.
Wykład 6 Korzystałem z : R. Morrison, R. Boyd: Chemia organiczna (wyd. ang.) Dieny Dieny są alkenami, których cząsteczki zawierają 2 podwójne wiązania C=C. Zasadnicze właściwości dienów są takie jak alkenów.
Jądrowy rezonans magnetyczny i elektronowy rezonans paramagnetyczny
 Jądrowy rezonans magnetyczny i elektronowy rezonans paramagnetyczny Jądrowy rezonans magnetyczny -badanie struktury małych cząsteczek -obrazowanie w medycynie Ekranowanie jądra w atomie Zewnętrzne pole
Jądrowy rezonans magnetyczny i elektronowy rezonans paramagnetyczny Jądrowy rezonans magnetyczny -badanie struktury małych cząsteczek -obrazowanie w medycynie Ekranowanie jądra w atomie Zewnętrzne pole
CHEMIA 10. Oznaczenia: R - podstawnik węglowodorowy, zwykle alifatyczny (łańcuchowy) X, X 2 - atom lub cząsteczka fluorowca
 INSTYTUT MEDICUS Kurs przygotowawczy na studia medyczne kierunek lekarski, stomatologia, farmacja, analityka medyczna tel. 0501 38 39 55 www.medicus.edu.pl CHEMIA 10 WĘGLOWODORY I ICH FLUOROWCOPOCHODNE.
INSTYTUT MEDICUS Kurs przygotowawczy na studia medyczne kierunek lekarski, stomatologia, farmacja, analityka medyczna tel. 0501 38 39 55 www.medicus.edu.pl CHEMIA 10 WĘGLOWODORY I ICH FLUOROWCOPOCHODNE.
Spis treści. Budowa i nazewnictwo fenoli
 Spis treści 1 Budowa i nazewnictwo fenoli 2 Kwasowość fenoli 2.1 Kwasowość atomów wodoru 2.2 Fenole jako kwasy organiczne. 3 Reakcje fenoli. 3.1 Zastosowanie fenolu Budowa i nazewnictwo fenoli Fenolami
Spis treści 1 Budowa i nazewnictwo fenoli 2 Kwasowość fenoli 2.1 Kwasowość atomów wodoru 2.2 Fenole jako kwasy organiczne. 3 Reakcje fenoli. 3.1 Zastosowanie fenolu Budowa i nazewnictwo fenoli Fenolami
Reakcje benzenu i jego pochodnych
 39-42. Reakcje benzenu i jego pochodnych 1 18.1. Nazewnictwo mono-podstawionych benzenów nazwa podstawnika - przedrostek przed słowem benzen wiele nazw zwyczajowych (pokazane wybrane związki) pierścień
39-42. Reakcje benzenu i jego pochodnych 1 18.1. Nazewnictwo mono-podstawionych benzenów nazwa podstawnika - przedrostek przed słowem benzen wiele nazw zwyczajowych (pokazane wybrane związki) pierścień
Alkohole i fenole. Opracowanie: Bartłomiej SIEPSIAK klasa 3d Opiekun: p. Teresa Gębicka
 Alkohole i fenole Opracowanie: Bartłomiej SIEPSIAK klasa d Opiekun: p. Teresa Gębicka Budowa alkoholi i fenoli Szereg homologiczny alkoholi Nazewnictwo Podział alkoholi Otrzymywanie alkoholi Właściwości
Alkohole i fenole Opracowanie: Bartłomiej SIEPSIAK klasa d Opiekun: p. Teresa Gębicka Budowa alkoholi i fenoli Szereg homologiczny alkoholi Nazewnictwo Podział alkoholi Otrzymywanie alkoholi Właściwości
Rozdział 6. Odpowiedzi i rozwiązania zadań. Chemia organiczna. Zdzisław Głowacki. Zakres podstawowy i rozszerzony
 Zdzisław Głowacki Chemia organiczna Zakres podstawowy i rozszerzony 2b Odpowiedzi i rozwiązania zadań Rozdział 6 Oficyna Wydawnicza TUTOR Wydanie I. Toruń 2013 r. Podpowiedzi Aldehydy i ketony Zadanie
Zdzisław Głowacki Chemia organiczna Zakres podstawowy i rozszerzony 2b Odpowiedzi i rozwiązania zadań Rozdział 6 Oficyna Wydawnicza TUTOR Wydanie I. Toruń 2013 r. Podpowiedzi Aldehydy i ketony Zadanie
CHEMIA 10 WĘGLOWODORY I ICH FLUOROWCOPOCHODNE. ALKOHOLE I FENOLE. IZOMERIA. POLIMERYZACJA.
 INSTYTUT MEDICUS Kurs przygotowawczy do matury i rekrutacji na studia medyczne Rok 2017/2018 www.medicus.edu.pl tel. 501 38 39 55 CHEMIA 10 WĘGLOWODORY I ICH FLUOROWCOPOCHODNE. ALKOHOLE I FENOLE. IZOMERIA.
INSTYTUT MEDICUS Kurs przygotowawczy do matury i rekrutacji na studia medyczne Rok 2017/2018 www.medicus.edu.pl tel. 501 38 39 55 CHEMIA 10 WĘGLOWODORY I ICH FLUOROWCOPOCHODNE. ALKOHOLE I FENOLE. IZOMERIA.
Chemia i technologia materiałów barwnych BADANIE WŁAŚCIWOŚCI ZWIĄZKÓW BARWNYCH WYKORZYSTANIEM SPEKTROFOTOMETRII UV-VIS.
 Chemia i technologia materiałów barwnych Ćwiczenia laboratoryjne BADANIE WŁAŚCIWOŚCI ZWIĄZKÓW BARWNYCH WYKORZYSTANIEM SPEKTROFOTOMETRII UV-VIS. Z Opracowanie: dr inŝ. Ewa Wagner-Wysiecka Politechnika Gdańska
Chemia i technologia materiałów barwnych Ćwiczenia laboratoryjne BADANIE WŁAŚCIWOŚCI ZWIĄZKÓW BARWNYCH WYKORZYSTANIEM SPEKTROFOTOMETRII UV-VIS. Z Opracowanie: dr inŝ. Ewa Wagner-Wysiecka Politechnika Gdańska
PRZEWODNIK PO PRZEDMIOCIE
 Nazwa przedmiotu: Kierunek: Inżynieria Biomedyczna Rodzaj przedmiotu: obowiązkowy moduł kierunkowy ogólny Rodzaj zajęć: wykład, ćwiczenia, laboratorium CHEMIA Chemistry Forma studiów: studia stacjonarne
Nazwa przedmiotu: Kierunek: Inżynieria Biomedyczna Rodzaj przedmiotu: obowiązkowy moduł kierunkowy ogólny Rodzaj zajęć: wykład, ćwiczenia, laboratorium CHEMIA Chemistry Forma studiów: studia stacjonarne
Zagadnienia z chemii na egzamin wstępny kierunek Technik Farmaceutyczny Szkoła Policealna im. J. Romanowskiej
 Zagadnienia z chemii na egzamin wstępny kierunek Technik Farmaceutyczny Szkoła Policealna im. J. Romanowskiej 1) Podstawowe prawa i pojęcia chemiczne 2) Roztwory (zadania rachunkowe zbiór zadań Pazdro
Zagadnienia z chemii na egzamin wstępny kierunek Technik Farmaceutyczny Szkoła Policealna im. J. Romanowskiej 1) Podstawowe prawa i pojęcia chemiczne 2) Roztwory (zadania rachunkowe zbiór zadań Pazdro
SCENARIUSZ ZAJĘĆ SZKOLNEGO KOŁA NAUKOWEGO Z PRZEDMIOTU CHEMIA PROWADZONEGO W RAMACH PROJEKTU AKADEMIA UCZNIOWSKA
 SCENARIUSZ ZAJĘĆ SZKOLNEGO KOŁA NAUKOWEGO Z PRZEDMIOTU CHEMIA PROWADZONEGO W RAMACH PROJEKTU AKADEMIA UCZNIOWSKA Temat lekcji Jak dowieść, że woda ma wzór H 2 O? Na podstawie pracy uczniów pod opieką Tomasza
SCENARIUSZ ZAJĘĆ SZKOLNEGO KOŁA NAUKOWEGO Z PRZEDMIOTU CHEMIA PROWADZONEGO W RAMACH PROJEKTU AKADEMIA UCZNIOWSKA Temat lekcji Jak dowieść, że woda ma wzór H 2 O? Na podstawie pracy uczniów pod opieką Tomasza
Kierunki chemicznejprzeróbki frakcji ropy naftowej. Destylacja ropy naftowej. Proces oligomeryzacji. Proces alkilowania. Proces oligomeryzacji
 Destylacja ropy naftowej Kierunki chemicznejprzeróbki frakcji ropy naftowej frakcja proces Gazowe Benzyna lekka Benzyna cięŝka Nafta napędowy mazut lekki średni gudron cięŝki izomeryzacja Reformowanie
Destylacja ropy naftowej Kierunki chemicznejprzeróbki frakcji ropy naftowej frakcja proces Gazowe Benzyna lekka Benzyna cięŝka Nafta napędowy mazut lekki średni gudron cięŝki izomeryzacja Reformowanie
Przykłady wybranych fragmentów prac egzaminacyjnych z komentarzami Technik ochrony fizycznej osób i mienia 515[01]
![Przykłady wybranych fragmentów prac egzaminacyjnych z komentarzami Technik ochrony fizycznej osób i mienia 515[01] Przykłady wybranych fragmentów prac egzaminacyjnych z komentarzami Technik ochrony fizycznej osób i mienia 515[01]](/thumbs/39/20450565.jpg) Przykłady wybranych fragmentów prac egzaminacyjnych z komentarzami Technik ochrony fizycznej osób i mienia 515[01] 1 2 3 4 5 6 Efektem rozwiązania zadania egzaminacyjnego przez zdającego była praca 7 egzaminacyjna,
Przykłady wybranych fragmentów prac egzaminacyjnych z komentarzami Technik ochrony fizycznej osób i mienia 515[01] 1 2 3 4 5 6 Efektem rozwiązania zadania egzaminacyjnego przez zdającego była praca 7 egzaminacyjna,
Kuratorium Oświaty w Lublinie
 Kuratorium Oświaty w Lublinie ZESTAW ZADAŃ KONKURSOWYCH Z CHEMII DLA UCZNIÓW GIMNAZJÓW ROK SZKOLNY 2014/2015 KOD UCZNIA ETAP OKRĘGOWY Instrukcja dla ucznia 1. Zestaw konkursowy zawiera 12 zadań. 2. Przed
Kuratorium Oświaty w Lublinie ZESTAW ZADAŃ KONKURSOWYCH Z CHEMII DLA UCZNIÓW GIMNAZJÓW ROK SZKOLNY 2014/2015 KOD UCZNIA ETAP OKRĘGOWY Instrukcja dla ucznia 1. Zestaw konkursowy zawiera 12 zadań. 2. Przed
KLAUZULE ARBITRAŻOWE
 KLAUZULE ARBITRAŻOWE KLAUZULE arbitrażowe ICC Zalecane jest, aby strony chcące w swych kontraktach zawrzeć odniesienie do arbitrażu ICC, skorzystały ze standardowych klauzul, wskazanych poniżej. Standardowa
KLAUZULE ARBITRAŻOWE KLAUZULE arbitrażowe ICC Zalecane jest, aby strony chcące w swych kontraktach zawrzeć odniesienie do arbitrażu ICC, skorzystały ze standardowych klauzul, wskazanych poniżej. Standardowa
2.Prawo zachowania masy
 2.Prawo zachowania masy Zdefiniujmy najpierw pewne podstawowe pojęcia: Układ - obszar przestrzeni o określonych granicach Ośrodek ciągły - obszar przestrzeni którego rozmiary charakterystyczne są wystarczająco
2.Prawo zachowania masy Zdefiniujmy najpierw pewne podstawowe pojęcia: Układ - obszar przestrzeni o określonych granicach Ośrodek ciągły - obszar przestrzeni którego rozmiary charakterystyczne są wystarczająco
KONKURSY MATEMATYCZNE. Treść zadań
 KONKURSY MATEMATYCZNE Treść zadań Wskazówka: w każdym zadaniu należy wskazać JEDNĄ dobrą odpowiedź. Zadanie 1 Wlewamy 1000 litrów wody do rurki w najwyższym punkcie systemu rurek jak na rysunku. Zakładamy,
KONKURSY MATEMATYCZNE Treść zadań Wskazówka: w każdym zadaniu należy wskazać JEDNĄ dobrą odpowiedź. Zadanie 1 Wlewamy 1000 litrów wody do rurki w najwyższym punkcie systemu rurek jak na rysunku. Zakładamy,
SENSORYKA I PODSTAWY PERFUMERII. Agata. Jabłońska-Trypuć. Ryszard. Farbiszewski
 SENSORYKA I PODSTAWY PERFUMERII Agata Jabłońska-Trypuć Ryszard Farbiszewski SENSORYKA I PODSTAWY PERFUMERII Agata Jabłońska-Trypuć, Ryszard Farbiszewski Wydanie pierwsze MedPharm Polska SPIS TREŚCI Przedm
SENSORYKA I PODSTAWY PERFUMERII Agata Jabłońska-Trypuć Ryszard Farbiszewski SENSORYKA I PODSTAWY PERFUMERII Agata Jabłońska-Trypuć, Ryszard Farbiszewski Wydanie pierwsze MedPharm Polska SPIS TREŚCI Przedm
Spis treści. Nazewnictwo kwasów karboksylowych.
 Do tej klasy zaliczamy związki zawierające grupę karboksylową, zapisywaną w skrócie jako COOH. W tej grupie karbonylowy atom węgla jest związany dodatkowo z grupą hydroksylową. Z uwagi na hybrydyzację
Do tej klasy zaliczamy związki zawierające grupę karboksylową, zapisywaną w skrócie jako COOH. W tej grupie karbonylowy atom węgla jest związany dodatkowo z grupą hydroksylową. Z uwagi na hybrydyzację
Jakie są te obowiązki wg MSR 41 i MSR 1, a jakie są w tym względzie wymagania ustawy o rachunkowości?
 Jakie są te obowiązki wg MSR 41 i MSR 1, a jakie są w tym względzie wymagania ustawy o rachunkowości? Obowiązki sprawozdawcze według ustawy o rachunkowości i MSR 41 Przepisy ustawy o rachunkowości w zakresie
Jakie są te obowiązki wg MSR 41 i MSR 1, a jakie są w tym względzie wymagania ustawy o rachunkowości? Obowiązki sprawozdawcze według ustawy o rachunkowości i MSR 41 Przepisy ustawy o rachunkowości w zakresie
Stałe siłowe. Spektroskopia w podczerwieni. Spektrofotometria w podczerwieni otrzymywanie widm
 Spektroskopia w podczerwieni Spektrofotometria w podczerwieni otrzymywanie widm absorpcyjnych substancji o różnych stanach skupienia. Powiązanie widm ze strukturą pozwala na identyfikację związku. Widmo
Spektroskopia w podczerwieni Spektrofotometria w podczerwieni otrzymywanie widm absorpcyjnych substancji o różnych stanach skupienia. Powiązanie widm ze strukturą pozwala na identyfikację związku. Widmo
Harmonogramowanie projektów Zarządzanie czasem
 Harmonogramowanie projektów Zarządzanie czasem Zarządzanie czasem TOMASZ ŁUKASZEWSKI INSTYTUT INFORMATYKI W ZARZĄDZANIU Zarządzanie czasem w projekcie /49 Czas w zarządzaniu projektami 1. Pojęcie zarządzania
Harmonogramowanie projektów Zarządzanie czasem Zarządzanie czasem TOMASZ ŁUKASZEWSKI INSTYTUT INFORMATYKI W ZARZĄDZANIU Zarządzanie czasem w projekcie /49 Czas w zarządzaniu projektami 1. Pojęcie zarządzania
Karta pracy: Ćwiczenie 5.
 Imię i nazwisko: Grupa: Karta pracy: Ćwiczenie 5. Tytuł ćwiczenia: Optymalizacja geometrii prostych cząsteczek organicznych. Analiza populacyjna i rzędy wiązań. Zagadnienia do przygotowania: Przypomnij
Imię i nazwisko: Grupa: Karta pracy: Ćwiczenie 5. Tytuł ćwiczenia: Optymalizacja geometrii prostych cząsteczek organicznych. Analiza populacyjna i rzędy wiązań. Zagadnienia do przygotowania: Przypomnij
Alkohole to związki, w których grupy hydroksylowe przyłączone są do nasyconych atomów węgla o hybrydyzacji sp 3. COH
 Alkohole R Alkohole to związki, w których grupy hydroksylowe przyłączone są do nasyconych atomów węgla o hybrydyzacji sp 3. C Alkohole można uważać za organiczne pochodne wody --, w której jeden z atomów
Alkohole R Alkohole to związki, w których grupy hydroksylowe przyłączone są do nasyconych atomów węgla o hybrydyzacji sp 3. C Alkohole można uważać za organiczne pochodne wody --, w której jeden z atomów
KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW
 KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW WOJEWÓDZTWO WIELKOPOLSKIE Etap wojewódzki rok szkolny 2009/2010 Dane dotyczące ucznia (wypełnia Komisja Konkursowa po rozkodowaniu prac) wylosowany numer uczestnika
KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW WOJEWÓDZTWO WIELKOPOLSKIE Etap wojewódzki rok szkolny 2009/2010 Dane dotyczące ucznia (wypełnia Komisja Konkursowa po rozkodowaniu prac) wylosowany numer uczestnika
UKŁAD ROZRUCHU SILNIKÓW SPALINOWYCH
 UKŁAD ROZRUCHU SILNIKÓW SPALINOWYCH We współczesnych samochodach osobowych są stosowane wyłącznie rozruszniki elektryczne składające się z trzech zasadniczych podzespołów: silnika elektrycznego; mechanizmu
UKŁAD ROZRUCHU SILNIKÓW SPALINOWYCH We współczesnych samochodach osobowych są stosowane wyłącznie rozruszniki elektryczne składające się z trzech zasadniczych podzespołów: silnika elektrycznego; mechanizmu
Politechnika Krakowska im. Tadeusza Kościuszki. Karta przedmiotu. obowiązuje studentów rozpoczynających studia w roku akademickim 2013/2014
 Politechnika Krakowska im. Tadeusza Kościuszki Karta przedmiotu obowiązuje studentów rozpoczynających studia w roku akademickim 2013/2014 Wydział Inżynierii i Technologii Chemicznej Kierunek studiów: Inżynieria
Politechnika Krakowska im. Tadeusza Kościuszki Karta przedmiotu obowiązuje studentów rozpoczynających studia w roku akademickim 2013/2014 Wydział Inżynierii i Technologii Chemicznej Kierunek studiów: Inżynieria
7. REZONANS W OBWODACH ELEKTRYCZNYCH
 OBWODY SYGNAŁY 7. EZONANS W OBWODAH EEKTYZNYH 7.. ZJAWSKO EZONANS Obwody elektryczne, w których występuje zjawisko rezonansu nazywane są obwodami rezonansowymi lub drgającymi. ozpatrując bezźródłowy obwód
OBWODY SYGNAŁY 7. EZONANS W OBWODAH EEKTYZNYH 7.. ZJAWSKO EZONANS Obwody elektryczne, w których występuje zjawisko rezonansu nazywane są obwodami rezonansowymi lub drgającymi. ozpatrując bezźródłowy obwód
Lekcja 173, 174. Temat: Silniki indukcyjne i pierścieniowe.
 Lekcja 173, 174 Temat: Silniki indukcyjne i pierścieniowe. Silnik elektryczny asynchroniczny jest maszyną elektryczną zmieniającą energię elektryczną w energię mechaniczną, w której wirnik obraca się z
Lekcja 173, 174 Temat: Silniki indukcyjne i pierścieniowe. Silnik elektryczny asynchroniczny jest maszyną elektryczną zmieniającą energię elektryczną w energię mechaniczną, w której wirnik obraca się z
Agrofi k zy a Wyk Wy ł k ad V Marek Kasprowicz
 Agrofizyka Wykład V Marek Kasprowicz Spektroskopia p nauka o powstawaniu i interpretacji widm powstających w wyniku oddziaływań wszelkich rodzajów promieniowania na materię ę rozumianą jako zbiorowisko
Agrofizyka Wykład V Marek Kasprowicz Spektroskopia p nauka o powstawaniu i interpretacji widm powstających w wyniku oddziaływań wszelkich rodzajów promieniowania na materię ę rozumianą jako zbiorowisko
Wykład 9 I 2019 Żywienie
 Wykład 9 I 2019 Żywienie Witold Bekas SGGW www.bekas.pl Fluorowcopochodne (halogenki) 2 fluorowce aktywne niemetale pierwiastki elektroujemne Grupa główna 17 (VIIA) X = F, Cl, Br, I X2 = F2, Cl2, Br2,
Wykład 9 I 2019 Żywienie Witold Bekas SGGW www.bekas.pl Fluorowcopochodne (halogenki) 2 fluorowce aktywne niemetale pierwiastki elektroujemne Grupa główna 17 (VIIA) X = F, Cl, Br, I X2 = F2, Cl2, Br2,
Grupy główne wg malejcego pierwszestwa. Alkohole i fenole Grupa funkcyjna OH
 Alkohole i fenole Grupa funkcyjna OH Alkohole - zwizki posiadajce grup funkcyjn "z prawdziwego zdarzenia" - grup główn. Wizanie podwójne (lub potrójne) C-C zaliczane jest do grup funkcyjnych, ale w nazwie
Alkohole i fenole Grupa funkcyjna OH Alkohole - zwizki posiadajce grup funkcyjn "z prawdziwego zdarzenia" - grup główn. Wizanie podwójne (lub potrójne) C-C zaliczane jest do grup funkcyjnych, ale w nazwie
ZWIĄZKI MAGNEZOORGANICZNE. Krystyna Dzierzbicka
 ZWIĄZKI MAGNEZRGANIZNE Krystyna Dzierzbicka Związki metaloorganiczne, do których zaliczamy między innymi magnezo- i litoorganiczne są związkami posiadającymi bezpośrednie wiązanie węgiel-metal (np. Na,
ZWIĄZKI MAGNEZRGANIZNE Krystyna Dzierzbicka Związki metaloorganiczne, do których zaliczamy między innymi magnezo- i litoorganiczne są związkami posiadającymi bezpośrednie wiązanie węgiel-metal (np. Na,
Otrzymywanie halogenków alkilów
 Otrzymywanie halogenków alkilów 1) Wymiana grupy OH w alkoholach C O H HX 2) reakcja podstawienia alkanów C X H 3 C CH CH 2 HBr C H 3 OH H 3 C CH CH 2 C H 3 Br h + + CH CH 2 3 Cl 2 Cl HCl CH CH 3 3 CH
Otrzymywanie halogenków alkilów 1) Wymiana grupy OH w alkoholach C O H HX 2) reakcja podstawienia alkanów C X H 3 C CH CH 2 HBr C H 3 OH H 3 C CH CH 2 C H 3 Br h + + CH CH 2 3 Cl 2 Cl HCl CH CH 3 3 CH
Halogenki alkilowe- atom fluorowca jest związany z atomem węgla o hybrydyzacji sp 3 KLASYFIKACJA ZE WZGLĘDU NA BUDOWĘ FRAGMENTU ALKILOWEGO:
 FLUOROWCOPOCHODNE Halogenki alkilowe- atom fluorowca jest związany z atomem węgla o hybrydyzacji sp 3 KLASYFIKACJA ZE WZGLĘDU NA BUDOWĘ FRAGMENTU ALKILOWEGO: Cl CH 2 -CH 2 -CH 2 -CH 3 CH 3 -CH-CH 3 pierwszorzędowe
FLUOROWCOPOCHODNE Halogenki alkilowe- atom fluorowca jest związany z atomem węgla o hybrydyzacji sp 3 KLASYFIKACJA ZE WZGLĘDU NA BUDOWĘ FRAGMENTU ALKILOWEGO: Cl CH 2 -CH 2 -CH 2 -CH 3 CH 3 -CH-CH 3 pierwszorzędowe
W. Guzicki Zadanie 23 z Informatora Maturalnego poziom rozszerzony 1
 W. Guzicki Zadanie 3 z Informatora Maturalnego poziom rozszerzony 1 Zadanie 3. Rozwiąż równanie: sin 5x cos x + sin x = 0. W rozwiązaniach podobnych zadań często korzystamy ze wzorów trygonometrycznych
W. Guzicki Zadanie 3 z Informatora Maturalnego poziom rozszerzony 1 Zadanie 3. Rozwiąż równanie: sin 5x cos x + sin x = 0. W rozwiązaniach podobnych zadań często korzystamy ze wzorów trygonometrycznych
Badanie silnika asynchronicznego jednofazowego
 Badanie silnika asynchronicznego jednofazowego Cel ćwiczenia Celem ćwiczenia jest poznanie budowy i zasady funkcjonowania silnika jednofazowego. W ramach ćwiczenia badane są zmiany wartości prądu rozruchowego
Badanie silnika asynchronicznego jednofazowego Cel ćwiczenia Celem ćwiczenia jest poznanie budowy i zasady funkcjonowania silnika jednofazowego. W ramach ćwiczenia badane są zmiany wartości prądu rozruchowego
Regulamin Obrad Walnego Zebrania Członków Stowarzyszenia Lokalna Grupa Działania Ziemia Bielska
 Załącznik nr 1 do Lokalnej Strategii Rozwoju na lata 2008-2015 Regulamin Obrad Walnego Zebrania Członków Stowarzyszenia Lokalna Grupa Działania Ziemia Bielska Przepisy ogólne 1 1. Walne Zebranie Członków
Załącznik nr 1 do Lokalnej Strategii Rozwoju na lata 2008-2015 Regulamin Obrad Walnego Zebrania Członków Stowarzyszenia Lokalna Grupa Działania Ziemia Bielska Przepisy ogólne 1 1. Walne Zebranie Członków
ET AAS 1 - pierwiastkowa, GW ppb. ICP OES n - pierwiastkowa, GW ppm n - pierwiastkowa, GW <ppb
 Analiza instrumentalna Spektrometria mas F AAS 1 - pierwiastkowa, GW ppm ET AAS 1 - pierwiastkowa, GW ppb ICP OES n - pierwiastkowa, GW ppm ICP MS n - pierwiastkowa, GW
Analiza instrumentalna Spektrometria mas F AAS 1 - pierwiastkowa, GW ppm ET AAS 1 - pierwiastkowa, GW ppb ICP OES n - pierwiastkowa, GW ppm ICP MS n - pierwiastkowa, GW
Raport wojewódzki zawierający informacje o zakresie korzystania ze środowiska
 Dział 1. Emisja zanieczyszczeń do powietrza. Raport wojewódzki zawierający informacje o zakresie korzystania ze środowiska Województwo: opolskie Rok: 2013 Tabela A. Zestawienie wielkości emisji zanieczyszczeń
Dział 1. Emisja zanieczyszczeń do powietrza. Raport wojewódzki zawierający informacje o zakresie korzystania ze środowiska Województwo: opolskie Rok: 2013 Tabela A. Zestawienie wielkości emisji zanieczyszczeń
Zarówno 1 o aminy alifatyczne jak i aromatyczne reagują z kwasem azotowym(iii) (HNO 2 ) dając sole diazoniowe. Do przeprowadzenia procesu diazowania
 Zarówno 1 o aminy alifatyczne jak i aromatyczne reagują z kwasem azotowym(iii) (HNO 2 ) dając sole diazoniowe. Do przeprowadzenia procesu diazowania najczęściej wykorzystuje się reakcję amin z kwasem azotowym(iii)
Zarówno 1 o aminy alifatyczne jak i aromatyczne reagują z kwasem azotowym(iii) (HNO 2 ) dając sole diazoniowe. Do przeprowadzenia procesu diazowania najczęściej wykorzystuje się reakcję amin z kwasem azotowym(iii)
Budowa przestrzenna alkanów
 Wykład 3 Budowa przestrzenna alkanów Podobnie jak w przypadku metanu, wiązanie C-H w alkanach powstaje w wyniku nakładania się zhybrydyzowanych orbitali sp 3. Z uwagi na to, że wiązania w alkanach skierowane
Wykład 3 Budowa przestrzenna alkanów Podobnie jak w przypadku metanu, wiązanie C-H w alkanach powstaje w wyniku nakładania się zhybrydyzowanych orbitali sp 3. Z uwagi na to, że wiązania w alkanach skierowane
TEST Systematyka związków nieorganicznych; Wersja A
 TEST Systematyka związków nieorganicznych; Wersja A 1.Wskaż grupę tlenków kwasowych? A. Na 2 O, SO 2, CaO; B. CO 2, SO 3, N 2 O 5 ; C. MgO, CuO, N 2 O 3 ; D. ZnO, Al 2 O 3, BaO; 2. Właściwości CuO opisują
TEST Systematyka związków nieorganicznych; Wersja A 1.Wskaż grupę tlenków kwasowych? A. Na 2 O, SO 2, CaO; B. CO 2, SO 3, N 2 O 5 ; C. MgO, CuO, N 2 O 3 ; D. ZnO, Al 2 O 3, BaO; 2. Właściwości CuO opisują
Mat. powtórzeniowy: zad. dot. procesów wieloetapowych w chemii organicznej
 Mat. powtórzeniowy: zad. dot. procesów wieloetapowych w chemii organicznej Zad.1. Zapisz równania reakcji przedstawionych na poniższym schemacie, określ typ rekcji w chemii organicznej, nadaj nazwy systematyczne
Mat. powtórzeniowy: zad. dot. procesów wieloetapowych w chemii organicznej Zad.1. Zapisz równania reakcji przedstawionych na poniższym schemacie, określ typ rekcji w chemii organicznej, nadaj nazwy systematyczne
Projekt współfinansowany przez Unię Europejską w ramach Europejskiego Funduszu Społecznego ĆWICZENIE 5. Związki aromatyczne
 ĆWICENIE 5 wiązki aromatyczne wiązki aromatyczne są związkami pierścieniowymi o płaskich cząsteczkach zawierających zgodnie z regułą uckla (4n2) elektrony π (n=0,1,2, ). Przedstawicielem takich związków
ĆWICENIE 5 wiązki aromatyczne wiązki aromatyczne są związkami pierścieniowymi o płaskich cząsteczkach zawierających zgodnie z regułą uckla (4n2) elektrony π (n=0,1,2, ). Przedstawicielem takich związków
TABELA ZGODNOŚCI. W aktualnym stanie prawnym pracodawca, który przez okres 36 miesięcy zatrudni osoby. l. Pornoc na rekompensatę dodatkowych
 -...~.. TABELA ZGODNOŚCI Rozporządzenie Komisji (UE) nr 651/2014 z dnia 17 czerwca 2014 r. uznające niektóre rodzaje pomocy za zgodne z rynkiem wewnętrznym w zastosowaniu art. 107 i 108 Traktatu (Dz. Urz.
-...~.. TABELA ZGODNOŚCI Rozporządzenie Komisji (UE) nr 651/2014 z dnia 17 czerwca 2014 r. uznające niektóre rodzaje pomocy za zgodne z rynkiem wewnętrznym w zastosowaniu art. 107 i 108 Traktatu (Dz. Urz.
Addycje Nukleofilowe do Grupy Karbonylowej
 J 1 Addycje kleofilowe do Grupy Karbonylowej H H +H H H Slides 1 to 29 J 2 Addycja vs Substytucja Atom w grupie karbonylowej (δ( + ) jest podatny na atak odczynnika nukleofilowego ; w zaleŝno ności od
J 1 Addycje kleofilowe do Grupy Karbonylowej H H +H H H Slides 1 to 29 J 2 Addycja vs Substytucja Atom w grupie karbonylowej (δ( + ) jest podatny na atak odczynnika nukleofilowego ; w zaleŝno ności od
NUMER IDENTYFIKATORA:
 Społeczne Liceum Ogólnokształcące z Maturą Międzynarodową im. Ingmara Bergmana IB WORLD SCHOOL 53 ul. Raszyńska, 0-06 Warszawa, tel./fax 668 54 5 www.ib.bednarska.edu.pl / e-mail: liceum.ib@rasz.edu.pl
Społeczne Liceum Ogólnokształcące z Maturą Międzynarodową im. Ingmara Bergmana IB WORLD SCHOOL 53 ul. Raszyńska, 0-06 Warszawa, tel./fax 668 54 5 www.ib.bednarska.edu.pl / e-mail: liceum.ib@rasz.edu.pl
Atom poziom rozszerzony
 Atom poziom rozszerzony Zadanie 1. (1 pkt) Źródło: CKE 010 (PR), zad. 1. Atomy pierwiastka X tworz jony X 3+, których konfiguracj elektronow mo na zapisa : 1s s p 6 3s 3p 6 3d 10 Uzupe nij poni sz tabel,
Atom poziom rozszerzony Zadanie 1. (1 pkt) Źródło: CKE 010 (PR), zad. 1. Atomy pierwiastka X tworz jony X 3+, których konfiguracj elektronow mo na zapisa : 1s s p 6 3s 3p 6 3d 10 Uzupe nij poni sz tabel,
1. REAKCJA ZE ZWIĄZKAMI POSIADAJĄCYMI KWASOWY ATOM WODORU:
 B I T E C N L CEMIA G GANICZNA I A Własności chemiczne Związki magnezoorganiczne wykazują wysoką reaktywność. eagują samorzutnie z wieloma związkami dając produkty należące do różnych klas związków organicznych.
B I T E C N L CEMIA G GANICZNA I A Własności chemiczne Związki magnezoorganiczne wykazują wysoką reaktywność. eagują samorzutnie z wieloma związkami dając produkty należące do różnych klas związków organicznych.
Wpływ wiązań na budowę i właściwości cząsteczek
 Pewnego razu pewna dziewczyna zwróciła się do mnie o pomoc w zredagowaniu referatu na temat wiązań chemicznych. Niestety, nie potrafię dziś znaleźć kontaktu z nią, by poprosić o prawo do publikacji tej
Pewnego razu pewna dziewczyna zwróciła się do mnie o pomoc w zredagowaniu referatu na temat wiązań chemicznych. Niestety, nie potrafię dziś znaleźć kontaktu z nią, by poprosić o prawo do publikacji tej
Stowarzyszenie na Rzecz Dzieci z Zaburzeniami Genetycznymi Urlop bezpłatny a prawo do zasiłków związanych z chorobą i macierzyństwem
 Źródło: http://podatki.pl Co o urlopie bezpłatnym stanowi Kodeks pracy Zgodnie z Kodeksem pracy pracodawca może udzielić pracownikowi, na jego pisemny wniosek, urlopu bezpłatnego (art. 174 kp). Pracodawca,
Źródło: http://podatki.pl Co o urlopie bezpłatnym stanowi Kodeks pracy Zgodnie z Kodeksem pracy pracodawca może udzielić pracownikowi, na jego pisemny wniosek, urlopu bezpłatnego (art. 174 kp). Pracodawca,
STA T T A YSTYKA Korelacja
 STATYSTYKA Korelacja Pojęcie korelacji Korelacja (współzależność cech) określa wzajemne powiązania pomiędzy wybranymi zmiennymi. Charakteryzując korelację dwóch cech podajemy dwa czynniki: kierunek oraz
STATYSTYKA Korelacja Pojęcie korelacji Korelacja (współzależność cech) określa wzajemne powiązania pomiędzy wybranymi zmiennymi. Charakteryzując korelację dwóch cech podajemy dwa czynniki: kierunek oraz
pierwszorzędowe drugorzędowe trzeciorzędowe (1 ) (2 ) (3 )
 FLUOROWCOPOCODNE alogenki alkilowe- Cl C 2 -C 2 -C 2 -C 3 C 3 -C-C 3 C 2 -C-C 3 pierwszorzędowe drugorzędowe trzeciorzędowe (1 ) (2 ) (3 ) I C 3 C 3 Cl-C 2 -C=C 2 Cl-C-C=C 2 1 2 3 Allilowe atom fluorowca
FLUOROWCOPOCODNE alogenki alkilowe- Cl C 2 -C 2 -C 2 -C 3 C 3 -C-C 3 C 2 -C-C 3 pierwszorzędowe drugorzędowe trzeciorzędowe (1 ) (2 ) (3 ) I C 3 C 3 Cl-C 2 -C=C 2 Cl-C-C=C 2 1 2 3 Allilowe atom fluorowca
Plan dydaktyczny z chemii klasa: 2TRA 1 godzina tygodniowo- zakres podstawowy. Dział Zakres treści
 Anna Kulaszewicz Plan dydaktyczny z chemii klasa: 2TRA 1 godzina tygodniowo- zakres podstawowy lp. Dział Temat Zakres treści 1 Zapoznanie z przedmiotowym systemem oceniania i wymaganiami edukacyjnymi z
Anna Kulaszewicz Plan dydaktyczny z chemii klasa: 2TRA 1 godzina tygodniowo- zakres podstawowy lp. Dział Temat Zakres treści 1 Zapoznanie z przedmiotowym systemem oceniania i wymaganiami edukacyjnymi z
Materiały dodatkowe kwasy i pochodne
 Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe kwasy i pochodne Kwasy 1. Kwasowość Kwasy karboksylowe są kwasami o stosunkowo niewielkiej mocy. Ich stała dysocjacji
Uniwersytet Jagielloński, Collegium Medicum, Katedra Chemii rganicznej Materiały dodatkowe kwasy i pochodne Kwasy 1. Kwasowość Kwasy karboksylowe są kwasami o stosunkowo niewielkiej mocy. Ich stała dysocjacji
WĘGLOWODORY AROMATYCZNE.
 Spis treści 1 WĘGLOWODORY AROMATYCZNE. 2 Budowa i nomenklatura węglowodorów aromatycznych 3 Efekt mezomeryczny 4 Substytucja elektrofilowa w układach aromatycznych 4.1 Profil energetyczny reakcji. 4.2
Spis treści 1 WĘGLOWODORY AROMATYCZNE. 2 Budowa i nomenklatura węglowodorów aromatycznych 3 Efekt mezomeryczny 4 Substytucja elektrofilowa w układach aromatycznych 4.1 Profil energetyczny reakcji. 4.2
DZIA 3. CZENIE SIÊ ATOMÓW
 DZIA 3. CZENIE SIÊ ATOMÓW 1./3 Wyjaœnij, w jaki sposób powstaje: a) wi¹zanie jonowe b) wi¹zanie atomowe 2./3 Na podstawie po³o enia w uk³adzie okresowym pierwiastków: chloru i litu ustal, ile elektronów
DZIA 3. CZENIE SIÊ ATOMÓW 1./3 Wyjaœnij, w jaki sposób powstaje: a) wi¹zanie jonowe b) wi¹zanie atomowe 2./3 Na podstawie po³o enia w uk³adzie okresowym pierwiastków: chloru i litu ustal, ile elektronów
Fluorowcowęglowodory są to pochodne węglowodorów, gdzie jeden lub więcej atomów wodoru jest podstawione atomem fluorowca. Fluorowcowęglowodory mogą
 Fluorowcowęglowodory są to pochodne węglowodorów, gdzie jeden lub więcej atomów wodoru jest podstawione atomem fluorowca. Fluorowcowęglowodory mogą być alifatyczne i aromatyczne. Grupą funkcyjną dla tych
Fluorowcowęglowodory są to pochodne węglowodorów, gdzie jeden lub więcej atomów wodoru jest podstawione atomem fluorowca. Fluorowcowęglowodory mogą być alifatyczne i aromatyczne. Grupą funkcyjną dla tych
