CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
|
|
|
- Martyna Mazurek
- 7 lat temu
- Przeglądów:
Transkrypt
1 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Rozalin, 20 mg/ml, krople do oczu, roztwór. 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 20 mg dorzolamidu (Dorzolamidum) w postaci chlorowodorku dorzolamidu (22,26 mg). Substancje pomocnicze, patrz punkt POSTAĆ FARMACEUTYCZNA Krople do oczu, roztwór. 4. SZCZEGÓŁOWE DANE KLINICZNE 4.1 Wskazania do stosowania Leczenie zwiększonego ciśnienia wewnątrzgałkowego u pacjentów z: nadciśnieniem ocznym, jaskrą z otwartym kątem, jaskrą torebkową 4.2 Dawkowanie i sposób podawania Jeśli lek Rozalin jest stosowany w monoterapii, podaje się jedną kroplę do worka spojówkowego chorego oka (oczu) trzy razy na dobę. W leczeniu wspomagającym, wraz ze stosowanymi miejscowo lekami beta-adrenolitycznymi, podaje się do worka spojówkowego chorego oka (oczu) jedną kroplę preparatu Rozalin dwa razy na dobę. Chcąc zastąpić preparatem Rozalin inny, stosowany miejscowo środek przeciwjaskrowy, należy przerwać leczenie tym lekiem i rozpocząć stosowanie preparatu Rozalin w dniu następnym. Podczas stosowania kilku leków okulistycznych działających miejscowo należy zachowywać, co najmniej 10 minut przerwy między zakraplaniem kolejnych leków. 1
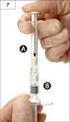
2 Pacjent powinien zostać poinformowany, że należy unikać kontaktu zakraplacza z powierzchnią lub okolicą oka. Należy pacjentowi udzielić informacji, że w przypadku nieprawidłowego postępowania krople do oczu mogą ulec zanieczyszczeniu powszechnie występującymi bakteriami, które mogą wywołać zakażenie oka. Stosowanie zanieczyszczonego roztworu może prowadzić do poważnych uszkodzeń oka, a w następstwie do utraty wzroku. Instrukcja stosowania: 1. Przed pierwszym użyciem leku należy upewnić się, że buteleczka jest oryginalnie zabezpieczona paskiem. W nowym opakowaniu szczelina występująca pomiędzy buteleczką i zakrętką jest prawidłowa. 2. Aby otworzyć butelkę należy przerwać pasek zabezpieczający odkręcając zakrętkę. 3. Przechylić głowę do tyłu i odciągnąć dolną powiekę w dół, aby utworzyć kieszonkę pomiędzy powieką i gałką oczną. 4. Odwrócić buteleczkę i delikatnie nacisnąć kciukiem lub palcem wskazującym na ściankę, aż do wyciśnięcia jednej kropli leku do oka. NIE NALEŻY DOTYKAĆ KOŃCÓWKĄ KROPLOMIERZA DO OKA, POWIEKI I INNYCH POWIERZCHNI. 5. Jeśli lekarz zlecił zakroplenie leku do drugiego oka, należy powtórzyć czynności z punktów 3 i Kroplomierz jest tak zaprojektowany, aby odmierzać dokładnie jedną kroplę, dlatego NIE NALEŻY powiększać otworu w kroplomierzu. 7. Po zakropleniu należy zakręcić buteleczkę. Nie należy jednak dokręcać jej zbyt mocno. 8. Po wykorzystaniu przepisanej przez lekarza ilości leku, w opakowaniu pozostaje jego niewielka, dodatkowa ilość. Jest to nadmiar dodany celowo, aby zapewnić możliwość wykorzystania leku w ilości przepisanej przez lekarza (5 ml). Nie należy, więc usiłować wycisnąć nadmiaru roztworu z opakowania. Stosowanie u dzieci: Ilość dostępnych danych klinicznych, dotyczących podawania dorzolamidu w trzech dawkach dobowych u dzieci jest ograniczona. (Celem uzyskania informacji dotyczących dawkowania leku u dzieci patrz punkt 5.1). 2
3 4.3 Przeciwwskazania Nadwrażliwość na którykolwiek składnik preparatu. Nie badano stosowania preparatu Rozalin u pacjentów z ciężką niewydolnością nerek (z klirensem kreatyniny mniejszym niż 30 ml/min) lub z kwasicą hiperchloremiczną. Z uwagi na to, że dorzolamid i jego metabolity są wydalane głównie przez nerki, stosowanie dorzolamidu u tych pacjentów nie jest zalecane. 4.4 Specjalne ostrzeżenia i środki ostrożności dotyczące stosowania Nie badano zastosowania dorzolamidu u pacjentów z niewydolnością wątroby, stąd zalecane jest zachowanie ostrożności podczas leczenia tych pacjentów. Leczenie pacjentów z ostrą jaskrą z zamkniętym kątem powoduje konieczność, poza podawaniem leków zmniejszających ciśnienie w gałce ocznej, także innych interwencji terapeutycznych. Nie badano zastosowania dorzolamidu u pacjentów z tym rozpoznaniem. Dorzolamid jest sulfonamidem i pomimo stosowania miejscowego jest wchłaniany do krążenia ogólnego. Wobec tego te same działania niepożądane, które występują po podaniu ogólnym sulfonamidów, mogą wystąpić po zastosowaniu miejscowym. W przypadku stwierdzenia ciężkich działań niepożądanych lub objawów nadwrażliwości należy przerwać stosowanie preparatu. Leczenie z zastosowaniem doustnych form inhibitorów anhydrazy węglanowej jest związane z występowaniem kamicy dróg moczowych, wynikającej z zaburzeń wodno-elektrolitowych, szczególnie u pacjentów z dodatnim wywiadem w kierunku kamicy nerkowej. Chociaż w przypadku stosowania dorzolamidu nie obserwowano występowania zaburzeń wodnoelektrolitowych, niemniej opisywano rzadkie przypadki kamicy dróg moczowych. Ponieważ dorzolamid jest miejscowo działającym inhibitorem anhydrazy węglanowej, ulegającym wchłanianiu do krążenia ogólnego, pacjenci z dodatnim wywiadem w kierunku kamicy nerkowej mogą stanowić grupę podwyższonego ryzyka występowania kamicy dróg moczowych w związku ze stosowaniem dorzolamidu. W badaniach klinicznych w czasie długotrwałego stosowania dorzolamidu obserwowano miejscowe objawy niepożądane, głównie zapalenie spojówek i podrażnienie powiek. Niektóre z 3
4 tych reakcji miały przebieg reakcji alergicznej, która ustępowała po zakończeniu stosowania leku. W tych sytuacjach należy rozważyć konieczność przerwania leczenia, dorzolamidem. Istnieje możliwość wystąpienia nasilenia działania ogólnego podczas stosowania inhibitorów anhydrazy węglanowej u pacjentów jednocześnie przyjmujących doustny inhibitor anhydrazy węglanowej i dorzolamid. Jednoczesne stosowanie dorzolamidu i doustnych inhibitorów anhydrazy węglanowej nie było przedmiotem badań i nie jest zalecane. U pacjentów z rozpoznanymi uprzednio przewlekłymi ubytkami rogówki i (lub) dodatnim wywiadem w kierunku zabiegów wewnątrzgałkowych, opisywano w trakcie stosowania dorzolamidu obrzęki rogówki oraz nieodwracalną dekompensację rogówki. U tych chorych dorzolamid, w postaci do podawania miejscowego, powinien być stosowany z zachowaniem ostrożności. Podczas stosowania środków hamujących wytwarzanie cieczy wodnistej po zabiegach filtracyjnych opisywano przypadki odwarstwienia naczyniówki. Rozalin zawiera środek konserwujący chlorek benzalkoniowy, który może powodować podrażnienie oczu. Soczewki kontaktowe należy zdjąć przed zakropleniem leku i włożyć ponownie nie wcześniej niż 15 minut po zakropleniu leku. Chlorek benzalkoniowy może powodować odbarwienie miękkich soczewek kontaktowych. Dzieci: Nie prowadzono badań dotyczących stosowania dorzolamidu o pacjentów przed 36 tygodniem życia płodowego oraz poniżej 1 tygodnia życia. U chorych z istotną niedojrzałością cewek nerkowych, dorzolamid należy stosować wyłącznie po dokładnym rozważeniu stosunku korzyści do ryzyka, z uwagi na możliwość wystąpienia kwasicy metabolicznej. 4.5 Interakcje z innymi lekami i inne rodzaje interakcji Nie prowadzono szczegółowych badań dotyczących interakcji dorzolamidu z innymi lekami. W badaniach klinicznych nie stwierdzono interakcji podczas jednoczesnego stosowania dorzolamidu z tymololem i betaksolem w postaci kropli do oczu, lekami działającymi ogólnie: inhibitorami konwertazy angiotensyny, antagonistami kanału wapniowego, lekami moczopędnymi 4
5 i niesteroidowymi lekami przeciwzapalnymi, w tym z kwasem acetylosalicylowym, a także ze środkami hormonalnymi (np. estrogeny, insulina, tyroksyna). Nie przeanalizowano w pełni możliwych interakcji pomiędzy dorzolamidem, lekami zwężającymi źrenicę i agonistami receptora adrenergicznego, występujących u chorych w trakcie leczenia jaskry. 4.6 Ciąża i laktacja Ciąża: Nie prowadzono odpowiednich, kontrolowanych badań dotyczących stosowania leku u kobiet w ciąży. Nie należy stosować dorzolamidu w trakcie ciąży. U królików, u których stosowano dawki leku toksyczne dla matek w związku z występującą kwasicą metaboliczną, obserwowano występowanie wad rozwojowych trzonów kręgów. Karmienie piersią: Nie wiadomo, czy dorzolamid jest wydzielany z pokarmem kobiecym. Dorzolamid nie powinien być stosowany w okresie karmienia piersią. U szczurów w trakcie laktacji obserwowano wpływ stosowania dorzolamidu na obniżenie tempa przyrostu masy ciała potomstwa. 4.7 Wpływ na zdolność prowadzenia pojazdów mechanicznych i obsługiwania urządzeń mechanicznych w ruchu U niektórych pacjentów stosujących dorzolamid istnieje możliwość wystąpienia działań niepożądanych takich jak zawroty głowy, zaburzenia widzenia, które mogą wpływać na zdolność prowadzenia pojazdów i obsługiwania maszyn (patrz pkt 4.8). 4.8 Działania niepożądane W przeprowadzonych długotrwałych badaniach klinicznych u pacjentów leczonych dorzolamidem w monoterapii lub jako lekiem uzupełniającym w leczeniu lekami beta-adrenolitycznymi w postaci okulistycznej, do najczęściej występujących działań niepożądanych związanych z przyjmowaniem dorzolamidu oraz objawów miejscowych należały: gorzki smak w ustach, pieczenie i kłucie oczu, niewyraźne widzenie, swędzenie oczu, łzawienie, ból głowy, zapalenie spojówek, zapalenie powiek, nudności, podrażnienie powiek oraz uczucie osłabienia i zmęczenia. Najczęstszym (u około 3% pacjentów) powodem przerwania leczenia preparatem Rozalin były działania niepożądane ze strony oczu, a przede wszystkim stwierdzenie polekowego zapalenia spojówek i 5
6 reakcji ze strony powiek. Rzadko obserwowano zapalenie tęczówki i ciała rzęskowego oraz wysypkę. W jednym przypadku stwierdzono kamicę moczową. Po wprowadzeniu leku zawierającego dorzolamid do lecznictwa zgłoszono następujące działania niepożądane: Bardzo często ( 1/10), często ( 1/100 do 1/10), niezbyt często ( 1/1 000 do 1/100), rzadko ( 1/ do 1/1 000), bardzo rzadko ( 1/10 000). Zaburzenia układu nerwowego: Często: bóle głowy Rzadko: parestezje, zawroty głowy Zaburzenia oka: Bardzo często: pieczenie i kłucie Często: powierzchniowe punkcikowate zapalenie rogówki, łzawienie, zapalenie spojówek, zapalenie powiek, swędzenie oczu, podrażnienie oczu, zaburzenia widzenia Niezbyt często: zapalenie tęczówki i ciała rzęskowego Rzadko: podrażnienie w tym zaczerwienienie, ból, sklejanie powiek, przemijająca krótkowzroczność (ustępująca po zaprzestaniu terapii), obrzęk rogówkowy, obniżone napięcie gałki ocznej, odwarstwienie naczyniówki po zabiegach filtracyjnych. Zaburzenia układu oddechowego, klatki piersiowej i śródpiersia: Rzadko: krwawienie z nosa Zaburzenia żołądka i jelit: Często: mdłości, gorzki posmak Rzadko: podrażnienie gardła, suchość w ustach 6
7 Zaburzenia skóry i tkanki podskórnej: Rzadko: kontaktowe zapalenie skóry Zaburzenia nerek i dróg moczowych: Rzadko: kamica moczowa Zaburzenia ogólne i stany w miejscu podania: Często: astenia/zmęczenie Rzadko: Nadwrażliwość: objawy podmiotowe i przedmiotowe reakcji miejscowych, w tym reakcji w obrębie powiek oraz objawy ogólnych reakcji alergicznych, w tym obrzęk naczynioruchowy, skurcz oskrzeli, pokrzywka, świąd. Wpływ leku na wyniki badań laboratoryjnych: Nie stwierdzono klinicznie istotnych zaburzeń elektrolitowych związanych ze stosowaniem dorzolamidu. Dzieci W badaniu klinicznym, u około 20% pacjentów leczonych z zastosowaniem dorzolamidu w monoterapii, obserwowano występowanie efektów ubocznych związanych ze stosowaniem leku. Większość z nich miała charakter miejscowych, łagodnych odczynów ocznych, takich jak uczucie pieczenia, kłucia w oku, przekrwienie spojówek oraz ból oka. W niewielkim odsetku przypadków <4% obserwowano obrzęk i przymglenie rogówki. Częstość występowania odczynów miejscowych była podobna jak w przypadku stosowania leku porównawczego (patrz pkt. 5.1). W trakcie obserwacji po wprowadzeniu produktu na rynek zgłaszano występowanie kwasicy metabolicznej u bardzo młodych chorych, szczególnie z towarzyszącą niedojrzałością i lub zaburzeniem funkcji nerek. 4.9 Przedawkowanie Istnieje ograniczona ilość informacji dotyczących skutków przedawkowania leku u ludzi, w wyniku przypadkowego lub celowego spożycia chlorowodorku dorzolamidu. Opisywano występowanie następujących objawów: po przyjęciu leku w formie doustnej - senność; po podaniu miejscowym: nudności, zawroty głowy, bóle głowy, uczucie zmęczenia, nietypowe sny i dysfagia. 7
8 Należy stosować leczenie objawowe i podtrzymujące. Możliwe jest wystąpienie zaburzeń elektrolitowych, rozwój kwasicy oraz objawów ze strony ośrodkowego układu nerwowego. Konieczne jest sprawdzanie stężenia elektrolitów (zwłaszcza potasu) w surowicy oraz pomiary ph krwi. 5. WŁAŚCIWOŚCI FARMAKOLOGICZNE 5.1. Właściwości farmakodynamiczne Grupa farmakoterapeutyczna: Inhibitory anhydrazy węglanowej Kod ATC: S 01 EC 03 Mechanizm działania Anhydraza węglanowa jest enzymem obecnym w wielu tkankach organizmu, w tym w oku.u ludzi anhydraza węglanowa występuje w postaci wielu izoenzymów, z których najbardziej aktywnym jest anhydraza węglanowa II, obecna przede wszystkim w krwinkach czerwonych, ale także w innych tkankach. Hamowanie aktywności anhydrazy węglanowej w wyrostkach rzęskowych oka powoduje zmniejszenie ilości wydzielanej cieczy wodnistej. W następstwie tego dochodzi do zmniejszenia ciśnienia wewnątrzgałkowego. Dorzolamid zawiera chlorowodorek dorzolamidu, silnie hamujący ludzką anhydrazę węglanową II. Po miejscowym podaniu do oka dorzolamid obniża zwiększone ciśnienie wewnątrzgałkowe, bez względu na to czy jest ono związane z jaskrą. Zwiększone ciśnienie wewnątrzgałkowe to jedna z głównych przyczyn uszkodzenia nerwu wzrokowego i utraty pola widzenia. Dorzolamid zmniejsza ciśnienie wewnątrzgałkowe nie powodując działań niepożądanych, takich jak nocna ślepota i skurcz akomodacyjny. W przeciwieństwie do stosowanych miejscowo leków betaadrenolitycznych, dorzolamid wywiera niewielki wpływ lub pozostaje bez wpływu na częstość akcji serca i ciśnienie tętnicze. Ciśnienie wewnątrzgałkowe zmniejszają także podawane miejscowo leki beta-adrenolityczne poprzez zmniejszenie wydzielania cieczy wodnistej oka, jednak mechanizm ich działania jest odmienny. Wykazano, że dodanie preparatu Rozalin do miejscowo stosowanego leku betaadrenolitycznego powoduje większe zmniejszenie ciśnienia wewnątrzgałkowego. Podobne działanie obserwowano w przypadku stosowania leków beta-adrenolitycznych i doustnych inhibitorów anhydrazy węglanowej. 8
9 Właściwości farmakodynamiczne: Działanie kliniczne Dorośli: Skuteczność dorzolamidu, stosowanego u chorych z jaskrą lub nadciśnieniem ocznym w monoterapii trzy razy na dobę (początkowe ciśnienie wewnątrzgałkowe 23 mmhg) lub dwa razy na dobę jako lek uzupełniający w leczeniu beta-adrenolitykiem w postaci kropli do oczu (początkowe ciśnienie wewnątrzgałkowe 22 mmhg), potwierdzono w szeroko zakrojonych badaniach klinicznych z okresem obserwacji do jednego roku. Podczas stosowania, zarówno w monoterapii, jak też jako lek uzupełniający, preparat zmniejszał ciśnienie wewnątrzgałkowe w ciągu całego dnia i efekt ten utrzymywał się w trakcie długotrwałego stosowania. Skuteczność leku po długotrwałym stosowaniu w monoterapii była podobna do skuteczności betaksololu i tylko nieznacznie słabsza niż skuteczność timololu. Stosowany jako lek uzupełniający w terapii lekami beta-adrenolitycznymi w postaci kropli do oczu, dorzolamid powodował dodatkowe zmniejszenie ciśnienia wewnątrzgałkowego podobnie, jak podczas stosowania pilokarpiny 2% cztery razy na dobę. Dzieci: Celem oceny bezpieczeństwa stosowania dorzolamidu, podawanego trzy razy dziennie, przeprowadzono badanie wieloośrodkowe, o czasie trwania wynoszącym trzy miesiące, z zastosowaniem podwójnie ślepej próby oraz aktywnie leczonej grupy kontrolnej, u 184 pacjentów pediatrycznych (122 w grupie otrzymującej dorzolamid) w wieku od jednego tygodnia do < 6 lat, z jaskrą lub podwyższonym ciśnieniem wewnątrzgałkowym (wyjściowa wartość IOP > 22 mmhg). U około połowy pacjentów w obu grupach leczonych rozpoznano jaskrę wrodzoną; inne często występujące podłoża etiologiczne to: zespół Sturge-Weber, dysgenezja mezodermalna tęczówki i rogówki, oraz pacjenci z bezsoczewkowością. Zaszeregowanie pacjentów w zależności od wieku oraz metod leczenia w fazie monoterapii przedstawiało się następująco: Grupa wiekowa < 2 lat Grupa wiekowa > 2 - < 6 lat Dorzolamid 2% n=56 Wiek: 1 do 23 miesięcy n=66 Wiek: 2 do 6 lat Tymolol Tymolol GS 0,25% n=27 Wiek: 0,25 do 22 miesięcy Tymolol 0,5% n=35 Wiek: 2 do 6 lat 9
10 W obrębie obu grup wiekowych, około 70 pacjentów otrzymywało leczenie przez okres co najmniej 61 dni, a około 50 pacjentów było leczonych przez okres dni. W przypadku nie uzyskania odpowiedniej kontroli IOP w trakcie monoterapii z zastosowaniem dorzolamidu lub tymololu w formie roztworów tworzących żel, dokonywano przejścia na terapię otwartą, zgodnie z następującym schematem: u 30 pacjentów w wieku < 2 lat dokonano zmiany sposobu leczenia na jednoczesne podawanie tymololu w formie roztworu tworzącego żel 0,25% dziennie oraz dorzolamidu 2% w trzech dawkach, u 30 pacjentów w wieku > 2 lat dokonano zmiany sposobu leczenia na terapię z użyciem stałej kombinacji 2% dorzolamidu/0,5% tymololu, podawanej dwa razy na dobę. Ogólnie, w trakcie badania nie stwierdzono dodatkowego ryzyka związanego ze stosowaniem leku u pacjentów pediatrycznych. Wyniki dotyczące skuteczności u pacjentów pediatrycznych sugerują, że średni spadek wartości IOP stwierdzany w grupie dorzolamidu był porównywalny ze średnim spadkiem wartości IOP, obserwowanym w grupie tymololu, przy niewielkiej, liczbowej przewadze obserwowanej w przypadku stosowania dorzolamidu. Brak jest dostępnych wyników badań dotyczących długotrwałego (> 12 tygodni) stosowania leku. 5.2 Właściwości farmakokinetyczne W przeciwieństwie do doustnych inhibitorów anhydrazy węglanowej podanie miejscowe chlorowodorku dorzolamidu umożliwia bezpośrednie działanie leku w obrębie oka po zastosowaniu znacznie mniejszych dawek, co w rezultacie zapewnia znacznie mniejszą ogólnoustrojową ekspozycję na lek. W związku z tym w badaniach klinicznych stwierdzono, że zmniejszeniu ciśnienia wewnątrzgałkowego nie towarzyszą zaburzenia równowagi kwasowozasadowej ani zaburzenia elektrolitowe charakterystyczne dla doustnych inhibitorów anhydrazy węglanowej. Po stosowaniu miejscowym dorzolamid przenika do krążenia ogólnego. W celu określenia jego siły działania jako układowego inhibitora anhydrazy węglanowej po podaniu miejscowym, zmierzono stężenia leku i jego metabolitów w erytrocytach i w osoczu krwi oraz stopień hamowania anhydrazy węglanowej w erytrocytach. Po długotrwałym stosowaniu dorzolamid gromadzi się w erytrocytach ze względu na selektywne wiązanie z izoenzymem anhydrazy węglanowej II, a stężenia wolnego leku w osoczu krwi pozostają skrajnie małe. Jedynym 10
11 metabolitem leku jest N-deetylo-dorzolamid, który hamuje anhydrazę węglanową II słabiej niż dorzolamid, ale hamuje także izoenzym o mniejszej aktywności (anhydrazę węglanową I). Metabolit ten gromadzi się również w erytrocytach, w których wiąże się głównie z anhydrazą węglanową I. Dorzolamid wiąże się w umiarkowanym stopniu z białkami osocza (około 33%). Dorzolamid jest wydalany głównie w moczu w postaci nie zmienionej. Jego metabolit jest także wydalany w moczu. Po zakończeniu przyjmowania leku następuje nieliniowe zmniejszanie stężenia dorzolamidu w erytrocytach. Początkowo następuje szybkie zmniejszenie stężenia leku, po czym następuje faza wolniejsza eliminacji z okresem półtrwania wynoszącym około 4 miesiące. Po doustnym podawaniu dorzolamidu w celu symulacji maksymalnej ekspozycji układowej możliwej po długotrwałym miejscowym stosowaniu dorzolamidu, stan równowagi osiągnięto w ciągu 13 tygodni. W stanie równowagi nie stwierdzono w osoczu obecności wolnego leku lub jego metabolitu. Stopień zahamowania aktywności anhydrazy węglanowej w erytrocytach był mniejszy niż ten, który prawdopodobnie wywiera działanie farmakologiczne na czynność nerek lub układu oddechowego. Podobne rezultaty farmakokinetyczne obserwowano po długotrwałym, miejscowym stosowaniu dorzolamidu. Jednak u niektórych pacjentów w wieku podeszłym z zaburzeniami czynności nerek (szacunkowy klirens kreatyniny ml/min) obserwowano większe stężenie metabolitu dorzolamidu w erytrocytach. Nie stwierdzono istotnych różnic dotyczących zahamowania aktywności anhydrazy węglanowej, ani klinicznie znamiennych ogólnych działań niepożądanych, które można z tym wiązać. 5.3 Przedkliniczne dane o bezpieczeństwie Wyniki badań na zwierzętach, którym podawano doustnie chlorowodorek dorzolamidu były związane z efektami farmakologicznymi ogólnego zahamowania aktywności anhydrazy węglanowej. Niektóre z uzyskanych wyników były specyficzne tylko dla określonych gatunków zwierząt i (lub) były następstwem kwasicy metabolicznej. W badaniach klinicznych u pacjentów nie stwierdzono objawów kwasicy metabolicznej ani zaburzeń stężenia elektrolitów w surowicy krwi, które wskazywałyby na układowe zahamowanie anhydrazy węglanowej. Z tego względu u pacjentów przyjmujących Rozalin w dawkach leczniczych nie należy się spodziewać wystąpienia takich zaburzeń, jakie obserwowano w badaniach na zwierzętach. 11
12 6. DANE FARMACEUTYCZNE 6.1. Wykaz substancji pomocniczych mannitol, sodu cytrynian, hydroksyetyloceluloza, benzalkoniowy chlorek, roztwór sodu wodorotlenek, roztwór 1 N woda do wstrzykiwań Niezgodności farmaceutyczne Nie stwierdzono. 6.3 Okres ważności 2 lata. Okres ważności po pierwszym użyciu: 4 tygodnie. 6.4 Specjalne środki ostrożności przy przechowywaniu Przechowywać w temperaturze poniżej 25 C. Przechowywać butelkę w opakowaniu zewnętrznym. 6.5 Rodzaj i zawartość opakowania 5 ml Biała butelka z kroplomierzem z LDPE z białą zakrętką z HDPE. 6.6 Instrukcja dotycząca przygotowania produktu leczniczego do stosowania i usuwania jego pozostałości Brak szczególnych wymagań. Patrz punkt 4.2 Ulotki dla pacjenta. 12
13 7. PODMIOT ODPOWIEDZIALNY POSIADAJĄCY POZWOLENIE NA DOPUSZCZENIE DO OBROTU Adamed Sp. z o.o. Pieńków Czosnów tel.: 022, fax.: 022, NUMER POZWOLENIA NA DOPUSZCZENIE DO OBROTU 9. DATA WYDANIA PIERWSZEGO POZWOLENIA NA DOPUSZCZENIE DO OBROTU/DATA PRZEDŁUŻENIA POZWOLENIA 10. DATA ZATWIERDZENIA LUB CZĘŚCIOWEJ ZMIANY TEKSTU CHARAKTERYSTYKI PRODUKTU LECZNICZEGO 13
Ulotka dołączona do opakowania: informacja dla pacjenta. ROZALIN, 20 mg/ml, krople do oczu, roztwór Dorzolamidum
 Ulotka dołączona do opakowania: informacja dla pacjenta ROZALIN, 20 mg/ml, krople do oczu, roztwór Dorzolamidum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona
Ulotka dołączona do opakowania: informacja dla pacjenta ROZALIN, 20 mg/ml, krople do oczu, roztwór Dorzolamidum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Dorzogen, 20 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 20 mg dorzolamidu (w postaci dorzolamidu
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Dorzogen, 20 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 20 mg dorzolamidu (w postaci dorzolamidu
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. 1 ml roztworu zawiera 22,26 mg chlorowodorku dorzolamidu co odpowiada 20 mg dorzolamidu (Dorzolamidum).
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO TRUSOPT, 20 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 22,26 mg chlorowodorku dorzolamidu co
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO TRUSOPT, 20 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 22,26 mg chlorowodorku dorzolamidu co
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. Jeden ml roztworu zawiera 20 mg dorzolamidu (w postaci chlorowodorku dorzolamidu).
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Glautic, 20 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml roztworu zawiera 20 mg dorzolamidu (w postaci chlorowodorku
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Glautic, 20 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml roztworu zawiera 20 mg dorzolamidu (w postaci chlorowodorku
Ulotka dołączona do opakowania: informacja dla użytkownika. TRUSOPT, 20 mg/ml, krople do oczu, roztwór Dorzolamidum
 Ulotka dołączona do opakowania: informacja dla użytkownika TRUSOPT, 20 mg/ml, krople do oczu, roztwór Dorzolamidum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera
Ulotka dołączona do opakowania: informacja dla użytkownika TRUSOPT, 20 mg/ml, krople do oczu, roztwór Dorzolamidum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Oftidor, 20 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każdy mililitr zawiera 22,26 mg dorzolamidu chlorowodorku co
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Oftidor, 20 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każdy mililitr zawiera 22,26 mg dorzolamidu chlorowodorku co
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. Każdy ml zawiera 20 mg dorzolamidu (w postaci 22,3 mg chlorowodorku dorzolamidu).
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Dorzolamid STADA, 20 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 2.1. Opis ogólny Każdy ml zawiera 20 mg dorzolamidu
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Dorzolamid STADA, 20 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 2.1. Opis ogólny Każdy ml zawiera 20 mg dorzolamidu
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO. Dorzolamid Tiefenbacher, 20 mg/ml, krople do oczu, roztwór
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Dorzolamid Tiefenbacher, 20 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każdy mililitr zawiera 22,26 mg dorzolamidu
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Dorzolamid Tiefenbacher, 20 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każdy mililitr zawiera 22,26 mg dorzolamidu
Dorzolamide Genoptim 20 mg/ml, krople do oczu, roztwór (Dorzolamidum)
 ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA Dorzolamide Genoptim 20 mg/ml, krople do oczu, roztwór (Dorzolamidum) Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA Dorzolamide Genoptim 20 mg/ml, krople do oczu, roztwór (Dorzolamidum) Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. Każdy ml zawiera 22,26 mg chlorowodorku dorzolamidu co odpowiada 20 mg dorzolamidu
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Dorzolamid Teva, 20 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każdy ml zawiera 22,26 mg chlorowodorku dorzolamidu
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Dorzolamid Teva, 20 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każdy ml zawiera 22,26 mg chlorowodorku dorzolamidu
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA. NODOM, 20 mg/ml, krople do oczu, roztwór Dorzolamidum
 ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA NODOM, 20 mg/ml, krople do oczu, roztwór Dorzolamidum Należy zapoznać się z treścią ulotki przed zastosowaniem leku. - Należy zachować tę ulotkę, aby w razie
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA NODOM, 20 mg/ml, krople do oczu, roztwór Dorzolamidum Należy zapoznać się z treścią ulotki przed zastosowaniem leku. - Należy zachować tę ulotkę, aby w razie
Ulotka dla pacjenta: informacja dla użytkownika. NODOM, 20 mg/ml, krople do oczu, roztwór Dorzolamidum
 Ulotka dla pacjenta: informacja dla użytkownika NODOM, 20 mg/ml, krople do oczu, roztwór Dorzolamidum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje
Ulotka dla pacjenta: informacja dla użytkownika NODOM, 20 mg/ml, krople do oczu, roztwór Dorzolamidum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje
Ulotka dołączona do opakowania: informacja dla pacjenta. Tobrosopt-DEX, (3 mg + 1 mg)/ml, krople do oczu, zawiesina Tobramycinum + Dexamethasonum
 Ulotka dołączona do opakowania: informacja dla pacjenta Tobrosopt-DEX, (3 mg + 1 mg)/ml, krople do oczu, zawiesina Tobramycinum + Dexamethasonum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem
Ulotka dołączona do opakowania: informacja dla pacjenta Tobrosopt-DEX, (3 mg + 1 mg)/ml, krople do oczu, zawiesina Tobramycinum + Dexamethasonum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem
6.2. Podsumowanie planu zarządzania ryzykiem dotyczącego produktu leczniczego DUOKOPT przeznaczone do wiadomości publicznej
 6.2. Podsumowanie planu zarządzania ryzykiem dotyczącego produktu leczniczego DUOKOPT przeznaczone do wiadomości publicznej 6.2.1. Podsumowanie korzyści wynikających z leczenia Co to jest T2488? T2488
6.2. Podsumowanie planu zarządzania ryzykiem dotyczącego produktu leczniczego DUOKOPT przeznaczone do wiadomości publicznej 6.2.1. Podsumowanie korzyści wynikających z leczenia Co to jest T2488? T2488
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO TOBROSOPT 0,3%, 3 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 3 mg Tobramycinum (tobramycyny).
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO TOBROSOPT 0,3%, 3 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 3 mg Tobramycinum (tobramycyny).
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. 1 ml produktu zawiera 0,345 mg wodorofumaranu ketotifenu, co odpowiada 0,25 mg ketotifenu (Ketotifenum).
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Zaditen, 0,25 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml produktu zawiera 0,345 mg wodorofumaranu ketotifenu,
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Zaditen, 0,25 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml produktu zawiera 0,345 mg wodorofumaranu ketotifenu,
Ulotka dołączona do opakowania: informacja dla użytkownika. Rozdol, 20 mg/ml, krople do oczu, roztwór Dorzolamidum
 Ulotka dołączona do opakowania: informacja dla użytkownika Rozdol, 20 mg/ml, krople do oczu, roztwór Dorzolamidum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera
Ulotka dołączona do opakowania: informacja dla użytkownika Rozdol, 20 mg/ml, krople do oczu, roztwór Dorzolamidum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera
Ulotka dołączona do opakowania: informacja dla użytkownika. Artelac 3,2 mg/ml, krople do oczu, roztwór (Hypromellosum)
 Ulotka dołączona do opakowania: informacja dla użytkownika Artelac 3,2 mg/ml, krople do oczu, roztwór (Hypromellosum) Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera
Ulotka dołączona do opakowania: informacja dla użytkownika Artelac 3,2 mg/ml, krople do oczu, roztwór (Hypromellosum) Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO POLCROM, 20 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 20 mg sodu kromoglikanu (Natrii cromoglicas).
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO POLCROM, 20 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 20 mg sodu kromoglikanu (Natrii cromoglicas).
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. Gaviscon o smaku mięty Saszetki, (500 mg + 267 mg + 160 mg)/10 ml, zawiesina doustna
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Gaviscon o smaku mięty Saszetki, (500 mg + 267 mg + 160 mg)/10 ml, zawiesina doustna 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Gaviscon o smaku
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Gaviscon o smaku mięty Saszetki, (500 mg + 267 mg + 160 mg)/10 ml, zawiesina doustna 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Gaviscon o smaku
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA. Bador, 20 mg/ml, krople do oczu, roztwór. Dorzolamidum
 ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA Bador, 20 mg/ml, krople do oczu, roztwór Dorzolamidum Należy zapoznać się z treścią ulotki przed zastosowaniem leku. - Należy zachować tę ulotkę, aby w razie
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA Bador, 20 mg/ml, krople do oczu, roztwór Dorzolamidum Należy zapoznać się z treścią ulotki przed zastosowaniem leku. - Należy zachować tę ulotkę, aby w razie
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Cusicrom 4%, 40 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 40 mg kromoglikanu disodu. Substancja
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Cusicrom 4%, 40 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 40 mg kromoglikanu disodu. Substancja
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. 1 ml roztworu zawiera 22,26 mg chlorowodorku dorzolamidu co odpowiada 20 mg dorzolamidu (Dorzolamidum).
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO TRUSOPT, 20 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 22,26 mg chlorowodorku dorzolamidu co
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO TRUSOPT, 20 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 22,26 mg chlorowodorku dorzolamidu co
Ulotka dołączona do opakowania: informacja dla pacjenta. Glautic, 20 mg/ml, krople do oczu, roztwór Dorzolamidum
 Ulotka dołączona do opakowania: informacja dla pacjenta Glautic, 20 mg/ml, krople do oczu, roztwór Dorzolamidum Należy zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje
Ulotka dołączona do opakowania: informacja dla pacjenta Glautic, 20 mg/ml, krople do oczu, roztwór Dorzolamidum Należy zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA WŁASNA PRODUKTU LECZNICZEGO CROTAMITON FARMAPOL płyn do stosowania na skórę, 100 mg/g 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY SUBSTANCJI CZYNNEJ 1 g płynu do stosowania
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA WŁASNA PRODUKTU LECZNICZEGO CROTAMITON FARMAPOL płyn do stosowania na skórę, 100 mg/g 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY SUBSTANCJI CZYNNEJ 1 g płynu do stosowania
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. 1 ml roztworu zawiera 0,15 mg polisulfonianu sodowego azapentacenu (Azapentaceni natrii polysulfonas).
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO QUINAX, 0,15 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 0,15 mg polisulfonianu sodowego azapentacenu
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO QUINAX, 0,15 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 0,15 mg polisulfonianu sodowego azapentacenu
Ulotka dołączona do opakowania: informacja dla pacjenta. Dolopt, 20 mg/ml krople do oczu, roztwór Dorzolamidum
 Ulotka dołączona do opakowania: informacja dla pacjenta Dolopt, 20 mg/ml krople do oczu, roztwór Dorzolamidum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona
Ulotka dołączona do opakowania: informacja dla pacjenta Dolopt, 20 mg/ml krople do oczu, roztwór Dorzolamidum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Oviderm, 250 mg, krem 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 gram kremu zawiera 250 mg glikolu propylenowego Substancja pomocnicza o znanym
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Oviderm, 250 mg, krem 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 gram kremu zawiera 250 mg glikolu propylenowego Substancja pomocnicza o znanym
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Dorzolamide/Timolol NTC, 20 mg/ml + 5 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 22,26 mg chlorowodorku
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Dorzolamide/Timolol NTC, 20 mg/ml + 5 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 22,26 mg chlorowodorku
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. 1. NAZWA PRODUKTU LECZNICZEGO 0,74 mg/ml (0,074%), roztwór do płukania jamy ustnej i gardła
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO GLIMBAX 0,74 mg/ml (0,074%), roztwór do płukania jamy ustnej i gardła 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 0,74 mg Diclofenacum
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO GLIMBAX 0,74 mg/ml (0,074%), roztwór do płukania jamy ustnej i gardła 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 0,74 mg Diclofenacum
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. CIECHOCIŃSKI SZLAM LECZNICZY, proszek do sporządzania roztworu na skórę
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO CIECHOCIŃSKI SZLAM LECZNICZY, proszek do sporządzania roztworu na skórę 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 kg proszku do sporządzania roztworu
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO CIECHOCIŃSKI SZLAM LECZNICZY, proszek do sporządzania roztworu na skórę 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 kg proszku do sporządzania roztworu
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Cholinex Intense, 2,5 mg + 1,2 mg, tabletki do ssania 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jedna tabletka do ssania zawiera 2,5 mg heksylorezorcynolu
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Cholinex Intense, 2,5 mg + 1,2 mg, tabletki do ssania 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jedna tabletka do ssania zawiera 2,5 mg heksylorezorcynolu
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Artelac, 3,2 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 3,2 mg hypromelozy (Hypromellosum).
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Artelac, 3,2 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 3,2 mg hypromelozy (Hypromellosum).
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Woodward s Gripe Water, płyn doustny, (0,46 mg + 10,5 mg)/ml 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Substancje czynne zawartość w 5 ml (1 łyżeczka)
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Woodward s Gripe Water, płyn doustny, (0,46 mg + 10,5 mg)/ml 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Substancje czynne zawartość w 5 ml (1 łyżeczka)
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO DIFADOL 0,1% 1 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml zawiera 1 mg diklofenaku sodowego (Diclofenacum natricum).
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO DIFADOL 0,1% 1 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml zawiera 1 mg diklofenaku sodowego (Diclofenacum natricum).
Ulotka dołączona do opakowania: informacja dla pacjenta. ALLERGODIL, 0,5 mg/ml, krople do oczu, roztwór Azelastini hydrochloridum
 Ulotka dołączona do opakowania: informacja dla pacjenta ALLERGODIL, 0,5 mg/ml, krople do oczu, roztwór Azelastini hydrochloridum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ
Ulotka dołączona do opakowania: informacja dla pacjenta ALLERGODIL, 0,5 mg/ml, krople do oczu, roztwór Azelastini hydrochloridum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ
Ulotka dołączona do opakowania: informacja dla pacjenta
 Ulotka dołączona do opakowania: informacja dla pacjenta BETADRIN, (1 mg + 0,33 mg)/ml, krople do oczu, roztwór Diphenhydramini hydrochloridum + Naphazolini nitras Należy uważnie zapoznać się z treścią
Ulotka dołączona do opakowania: informacja dla pacjenta BETADRIN, (1 mg + 0,33 mg)/ml, krople do oczu, roztwór Diphenhydramini hydrochloridum + Naphazolini nitras Należy uważnie zapoznać się z treścią
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. POLCROM 2%, 20 mg/ml (2,8 mg/dawkę donosową), aerozol do nosa, roztwór
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO POLCROM 2%, 20 mg/ml (2,8 mg/dawkę donosową), aerozol do nosa, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każdy ml roztworu zawiera 20 mg
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO POLCROM 2%, 20 mg/ml (2,8 mg/dawkę donosową), aerozol do nosa, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każdy ml roztworu zawiera 20 mg
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO. Azelastin POS, 0,5 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Azelastin POS, 0,5 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 0,05 % roztwór chlorowodorku azelastyny (0,50 mg/ml).
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Azelastin POS, 0,5 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 0,05 % roztwór chlorowodorku azelastyny (0,50 mg/ml).
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA. ALLERGODIL, 0,5 mg/ml, krople do oczu, roztwór Azelastini hydrochloridum
 ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA ALLERGODIL, 0,5 mg/ml, krople do oczu, roztwór Azelastini hydrochloridum Należy przeczytać uważnie całą ulotkę, ponieważ zawiera ona informacje ważne dla
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA ALLERGODIL, 0,5 mg/ml, krople do oczu, roztwór Azelastini hydrochloridum Należy przeczytać uważnie całą ulotkę, ponieważ zawiera ona informacje ważne dla
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. Każdy pojemnik jednodawkowy zawiera roztwór sodu kromoglikanu o stężeniu 20 mg/ml.
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Alleoptical, 20 mg/ml, krople do oczu, roztwór w pojemniku jednodawkowym. 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każdy pojemnik jednodawkowy
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Alleoptical, 20 mg/ml, krople do oczu, roztwór w pojemniku jednodawkowym. 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każdy pojemnik jednodawkowy
Ulotka dołączona do opakowania: informacja dla użytkownika. Oflodinex, 3 mg/ml, krople do oczu, roztwór Ofloxacinum
 Ulotka dołączona do opakowania: informacja dla użytkownika Oflodinex, 3 mg/ml, krople do oczu, roztwór Ofloxacinum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera
Ulotka dołączona do opakowania: informacja dla użytkownika Oflodinex, 3 mg/ml, krople do oczu, roztwór Ofloxacinum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA. DICLOABAK, 1 mg/ml, krople do oczu, roztwór Diclofenacum natricum
 ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA DICLOABAK, 1 mg/ml, krople do oczu, roztwór Diclofenacum natricum Należy zapoznać się z treścią ulotki przed zastosowaniem leku. - Należy zachować tę ulotkę,
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA DICLOABAK, 1 mg/ml, krople do oczu, roztwór Diclofenacum natricum Należy zapoznać się z treścią ulotki przed zastosowaniem leku. - Należy zachować tę ulotkę,
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. Substancja pomocnicza o znanym działaniu: benzalkoniowy chlorek, roztwór.
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO DIFADOL 0,1%, 1 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każdy ml zawiera 1 mg diklofenaku sodowego (Diclofenacum
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO DIFADOL 0,1%, 1 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każdy ml zawiera 1 mg diklofenaku sodowego (Diclofenacum
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO ATROPINUM SULFURICUM WZF 1%, 10 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 10 mg Atropini sulfas
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO ATROPINUM SULFURICUM WZF 1%, 10 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 10 mg Atropini sulfas
Oftahist, 1 mg/ml, krople do oczu, roztwór Olopatadyna
 Ulotka dołączona do opakowania: informacja dla użytkownika Oftahist, 1 mg/ml, krople do oczu, roztwór Olopatadyna Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera
Ulotka dołączona do opakowania: informacja dla użytkownika Oftahist, 1 mg/ml, krople do oczu, roztwór Olopatadyna Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO COSOPT, (20 mg+5 mg)/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 22,26 mg chlorowodorku dorzolamidu,
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO COSOPT, (20 mg+5 mg)/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 22,26 mg chlorowodorku dorzolamidu,
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO NIZAX ACTIV, 20 mg/g, szampon leczniczy 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 g szamponu leczniczego zawiera 20 mg ketokonazolu (Ketoconazolum).
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO NIZAX ACTIV, 20 mg/g, szampon leczniczy 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 g szamponu leczniczego zawiera 20 mg ketokonazolu (Ketoconazolum).
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO XYLOMETAZOLIN WZF, 0,05%, 0,5 mg/ml, krople do nosa, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 0,5 mg ksylometazoliny
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO XYLOMETAZOLIN WZF, 0,05%, 0,5 mg/ml, krople do nosa, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 0,5 mg ksylometazoliny
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Patentex Oval N, 75 mg, globulki dopochwowe 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 globulka (3,15 g) zawiera: Nonoksynol-9 (INN) 75 mg Pełny
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Patentex Oval N, 75 mg, globulki dopochwowe 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 globulka (3,15 g) zawiera: Nonoksynol-9 (INN) 75 mg Pełny
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. Jeden ml roztworu (22 krople) zawiera 5 mg butamiratu cytrynian (Butamirati citras).
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Sinecod, 5 mg/ml, krople doustne, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml roztworu (22 krople) zawiera 5 mg butamiratu cytrynian
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Sinecod, 5 mg/ml, krople doustne, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml roztworu (22 krople) zawiera 5 mg butamiratu cytrynian
Ulotka dołączona do opakowania: informacja dla pacjenta. DIFADOL 0,1%, 1 mg/ml, krople do oczu, roztwór Diclofenacum natricum
 Ulotka dołączona do opakowania: informacja dla pacjenta DIFADOL 0,1%, 1 mg/ml, krople do oczu, roztwór Diclofenacum natricum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ
Ulotka dołączona do opakowania: informacja dla pacjenta DIFADOL 0,1%, 1 mg/ml, krople do oczu, roztwór Diclofenacum natricum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ
Parafina ciekła Avena, 1g/ 1g, płyn doustny i do użytku zewnętrznego
 C H A R A K T E R Y S T Y K A P R O D U K T U L E C Z N I C Z E G O 1. NAZWA PRODUKTU LECZNICZEGO Parafina ciekła Avena, 1g/ 1g, płyn doustny i do użytku zewnętrznego 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1
C H A R A K T E R Y S T Y K A P R O D U K T U L E C Z N I C Z E G O 1. NAZWA PRODUKTU LECZNICZEGO Parafina ciekła Avena, 1g/ 1g, płyn doustny i do użytku zewnętrznego 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Oilatum 700 mg/g, żel 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 g żelu zawiera 700 mg parafiny ciekłej, lekkiej (Paraffinum perliquidum). Pełny
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Oilatum 700 mg/g, żel 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 g żelu zawiera 700 mg parafiny ciekłej, lekkiej (Paraffinum perliquidum). Pełny
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Sinecod; 1,5 mg/ml, syrop 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml syropu zawiera 1,5 mg butamiratu cytrynian (Butamirati citras). Substancje
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Sinecod; 1,5 mg/ml, syrop 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml syropu zawiera 1,5 mg butamiratu cytrynian (Butamirati citras). Substancje
Ulotka dołączona do opakowania: informacja dla pacjenta. Zaditen, 0,25 mg/ml, krople do oczu, roztwór. Ketotifenum
 Ulotka dołączona do opakowania: informacja dla pacjenta Zaditen, 0,25 mg/ml, krople do oczu, roztwór Ketotifenum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera
Ulotka dołączona do opakowania: informacja dla pacjenta Zaditen, 0,25 mg/ml, krople do oczu, roztwór Ketotifenum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA. Tymolamid, (20 mg + 5 mg)/ml, krople do oczu, roztwór. Dorzolamidum + Timololum
 +pharma (logo) ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA Tymolamid, (20 mg + 5 mg)/ml, krople do oczu, roztwór Dorzolamidum + Timololum Należy zapoznać się z treścią ulotki przed zastosowaniem leku.
+pharma (logo) ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA Tymolamid, (20 mg + 5 mg)/ml, krople do oczu, roztwór Dorzolamidum + Timololum Należy zapoznać się z treścią ulotki przed zastosowaniem leku.
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. Gaviscon Advance, (1000 mg mg)/10 ml, zawiesina doustna
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Gaviscon Advance, (1000 mg + 200 mg)/10 ml, zawiesina doustna 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml produktu leczniczego zawiera 100 mg
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Gaviscon Advance, (1000 mg + 200 mg)/10 ml, zawiesina doustna 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml produktu leczniczego zawiera 100 mg
Ulotka dla pacjenta: informacja dla użytkownika. Nodofree, 20 mg/ml, krople do oczu, roztwór Dorzolamidum
 Ulotka dla pacjenta: informacja dla użytkownika Nodofree, 20 mg/ml, krople do oczu, roztwór Dorzolamidum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje
Ulotka dla pacjenta: informacja dla użytkownika Nodofree, 20 mg/ml, krople do oczu, roztwór Dorzolamidum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje
Ulotka dołączona do opakowania: informacja dla pacjenta. Dorzostill, 20 mg/ml, krople do oczu, roztwór. Dorzolamidum
 Ulotka dołączona do opakowania: informacja dla pacjenta Dorzostill, 20 mg/ml, krople do oczu, roztwór Dorzolamidum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera
Ulotka dołączona do opakowania: informacja dla pacjenta Dorzostill, 20 mg/ml, krople do oczu, roztwór Dorzolamidum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Viru-POS, 30 mg/g, maść do oczu 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 g maści zawiera 30 mg acyklowiru (Aciclovirum) Pełny wykaz substancji
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Viru-POS, 30 mg/g, maść do oczu 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 g maści zawiera 30 mg acyklowiru (Aciclovirum) Pełny wykaz substancji
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA. Dorzolamid STADA, 20 mg/ml, krople do oczu, roztwór Dorzolamidum
 ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA Dorzolamid STADA, 20 mg/ml, krople do oczu, roztwór Dorzolamidum Należy zapoznać się z treścią ulotki przed zastosowaniem leku. - Należy zachować tę ulotkę,
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA Dorzolamid STADA, 20 mg/ml, krople do oczu, roztwór Dorzolamidum Należy zapoznać się z treścią ulotki przed zastosowaniem leku. - Należy zachować tę ulotkę,
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. 1 ml roztworu zawiera 3 mg Hypromellosum (hypromelozy) i 1 mg Dextranum (dekstranu 70).
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Tears Naturale II, (3 mg + 1 mg)/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 3 mg Hypromellosum
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Tears Naturale II, (3 mg + 1 mg)/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 3 mg Hypromellosum
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA. Dorzolamid STADA, 20 mg/ml, krople do oczu, roztwór Dorzolamidum
 ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA Dorzolamid STADA, 20 mg/ml, krople do oczu, roztwór Dorzolamidum Należy zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA Dorzolamid STADA, 20 mg/ml, krople do oczu, roztwór Dorzolamidum Należy zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO ATUSSAN MITE 0,8 mg/ml, syrop 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml syropu zawiera 0,8 mg butamiratu cytrynianu. 5 ml syropu zawiera 4,0
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO ATUSSAN MITE 0,8 mg/ml, syrop 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml syropu zawiera 0,8 mg butamiratu cytrynianu. 5 ml syropu zawiera 4,0
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Droteryn, 0,5 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml roztworu zawiera 0,5 mg tetryzoliny chlorowodorku
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Droteryn, 0,5 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml roztworu zawiera 0,5 mg tetryzoliny chlorowodorku
Ulotka dołączona do opakowania: informacja dla pacjenta. PILOCARPINUM WZF 2%, 20 mg/ml, krople do oczu, roztwór Pilocarpini hydrochloridum
 Ulotka dołączona do opakowania: informacja dla pacjenta PILOCARPINUM WZF 2%, 20 mg/ml, krople do oczu, roztwór Pilocarpini hydrochloridum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem
Ulotka dołączona do opakowania: informacja dla pacjenta PILOCARPINUM WZF 2%, 20 mg/ml, krople do oczu, roztwór Pilocarpini hydrochloridum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem
Leczenie ocznych objawów przedmiotowych i podmiotowych sezonowego alergicznego zapalenia spojówek.
 1. NAZWA PRODUKTU LECZNICZEGO Oftahist, 1 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml roztworu zawiera 1 mg olopatadyny (w postaci chlorowodorku). Substancje pomocnicze: chlorek
1. NAZWA PRODUKTU LECZNICZEGO Oftahist, 1 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml roztworu zawiera 1 mg olopatadyny (w postaci chlorowodorku). Substancje pomocnicze: chlorek
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. 1 ml roztworu zawiera 0,25 mg oksymetazoliny chlorowodorku (Oxymetazolini hydrochloridum).
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO OXALIN 0,025%; 0,25 mg/ml, krople do nosa, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 0,25 mg oksymetazoliny chlorowodorku
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO OXALIN 0,025%; 0,25 mg/ml, krople do nosa, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 0,25 mg oksymetazoliny chlorowodorku
Krople do oczu, roztwór. Arutidor jest przejrzystym, bezbarwnym lub lekko żółtym, jałowym roztworem kropli do oczu.
 CHARAKTERYSTYKA PRODUKTU LECZNCZEGO 1. NAZWA PRODUKTU LECZNICZEGO Arutidor, 20 mg/ml + 5 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każdy ml roztworu zawiera 22,26 mg dorzolamidu chlorowodorku,
CHARAKTERYSTYKA PRODUKTU LECZNCZEGO 1. NAZWA PRODUKTU LECZNICZEGO Arutidor, 20 mg/ml + 5 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każdy ml roztworu zawiera 22,26 mg dorzolamidu chlorowodorku,
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Azelamed, 0,5 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 0,5 mg azelastyny chlorowodorku. Każda
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Azelamed, 0,5 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 0,5 mg azelastyny chlorowodorku. Każda
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY SUBSTANCJI CZYNNYCH
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA WŁASNA PRODUKTU LECZNICZEGO LOCOID, 1 mg/ml, roztwór na skórę 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY SUBSTANCJI CZYNNYCH Jeden mililitr roztworu zawiera 1 mg 17-maślanu
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA WŁASNA PRODUKTU LECZNICZEGO LOCOID, 1 mg/ml, roztwór na skórę 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY SUBSTANCJI CZYNNYCH Jeden mililitr roztworu zawiera 1 mg 17-maślanu
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Oilatum Plus (525 mg + 60 mg + 20 mg)/g, roztwór do kąpieli 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 g roztworu do kąpieli zawiera 525 mg parafiny
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Oilatum Plus (525 mg + 60 mg + 20 mg)/g, roztwór do kąpieli 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 g roztworu do kąpieli zawiera 525 mg parafiny
Ulotka dołączona do opakowania: informacja dla pacjenta. TROPICAMIDUM WZF 0,5%, 5 mg/ml, krople do oczu, roztwór Tropicamidum
 Ulotka dołączona do opakowania: informacja dla pacjenta TROPICAMIDUM WZF 0,5%, 5 mg/ml, krople do oczu, roztwór Tropicamidum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ
Ulotka dołączona do opakowania: informacja dla pacjenta TROPICAMIDUM WZF 0,5%, 5 mg/ml, krople do oczu, roztwór Tropicamidum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ
Ulotka dołączona do opakowania: informacja dla pacjenta. Briglau PPH, 2 mg/ml, krople do oczu, roztwór. Brimonidini tartras
 Ulotka dołączona do opakowania: informacja dla pacjenta Briglau PPH, 2 mg/ml, krople do oczu, roztwór Brimonidini tartras Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ
Ulotka dołączona do opakowania: informacja dla pacjenta Briglau PPH, 2 mg/ml, krople do oczu, roztwór Brimonidini tartras Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO ALLERGODIL, 0,5 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml kropli zawiera 0,5 mg chlorowodorku azelastyny (Azelastini
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO ALLERGODIL, 0,5 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml kropli zawiera 0,5 mg chlorowodorku azelastyny (Azelastini
1. NAZWA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO XYLOGEL 0,1%; 1 mg/g, żel do nosa 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 g żelu do nosa zawiera 1 mg ksylometazoliny chlorowodorku (Xylometazolini
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO XYLOGEL 0,1%; 1 mg/g, żel do nosa 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 g żelu do nosa zawiera 1 mg ksylometazoliny chlorowodorku (Xylometazolini
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Zineryt 40 mg/ml + 12 mg/ml, proszek i rozpuszczalnik do sporządzania roztworu do stosowania na skórę 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Zineryt 40 mg/ml + 12 mg/ml, proszek i rozpuszczalnik do sporządzania roztworu do stosowania na skórę 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. 1 ml roztworu zawiera 20 mg pilokarpiny chlorowodorku (Pilocarpini hydrochloridum).
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO PILOCARPINUM WZF 2%, 20 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 20 mg pilokarpiny chlorowodorku
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO PILOCARPINUM WZF 2%, 20 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 20 mg pilokarpiny chlorowodorku
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Azelastin COMOD, 0,5 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 0,05 % roztwór chlorowodorku azelastyny (0,50 mg/ml).
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Azelastin COMOD, 0,5 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 0,05 % roztwór chlorowodorku azelastyny (0,50 mg/ml).
Miejscowe oczyszczanie skóry: Wetrzeć niewielką ilość emulsji do kąpieli w zwilżoną uprzednio skórę, a następnie spłukać wodą i osuszyć ręcznikiem.
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Oilatum 634 mg/g, emulsja do kąpieli 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 g emulsji do kąpieli zawiera 634 mg parafiny ciekłej, lekkiej (Paraffinum
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Oilatum 634 mg/g, emulsja do kąpieli 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 g emulsji do kąpieli zawiera 634 mg parafiny ciekłej, lekkiej (Paraffinum
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Toselix, 0,8 mg/ml, syrop 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml syropu zawiera 0,8 mg butamiratu cytrynianu (Butamirati citras). 5 ml syropu
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Toselix, 0,8 mg/ml, syrop 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml syropu zawiera 0,8 mg butamiratu cytrynianu (Butamirati citras). 5 ml syropu
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO BETADRIN, (1 mg + 0,33 mg)/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każdy ml roztworu zawiera jako substancje czynne:
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO BETADRIN, (1 mg + 0,33 mg)/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każdy ml roztworu zawiera jako substancje czynne:
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO ADDAMEL N, koncentrat do sporządzania roztworu do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml koncentratu zawiera: Substancje czynne
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO ADDAMEL N, koncentrat do sporządzania roztworu do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml koncentratu zawiera: Substancje czynne
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO CROTAMITON FARMAPOL płyn do stosowania na skórę, 100 mg/g 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 g płynu do stosowania na skórę zawiera 100
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO CROTAMITON FARMAPOL płyn do stosowania na skórę, 100 mg/g 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 g płynu do stosowania na skórę zawiera 100
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Olopatadine Zentiva, 1 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml roztworu zawiera 1 mg olopatadyny (w postaci
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Olopatadine Zentiva, 1 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml roztworu zawiera 1 mg olopatadyny (w postaci
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. 1 ml roztworu zawiera 10 mg substancji czynnej klotrymazolu (Clotrimazolum).
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Fungotac 10 mg/ml, krople do uszu, roztwór. 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 10 mg substancji czynnej klotrymazolu
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Fungotac 10 mg/ml, krople do uszu, roztwór. 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 10 mg substancji czynnej klotrymazolu
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO TROPICAMIDUM WZF 1%, 10 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 10 mg tropikamidu (Tropicamidum).
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO TROPICAMIDUM WZF 1%, 10 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 10 mg tropikamidu (Tropicamidum).
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Dropzol Tim, 20 mg/ml + 5 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każdy ml zawiera 20 mg dorzolamidu (w postaci
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Dropzol Tim, 20 mg/ml + 5 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każdy ml zawiera 20 mg dorzolamidu (w postaci
Ulotka dołączona do opakowania: informacja dla użytkownika. Ofloxamed, 3 mg/ml, krople do oczu, roztwór. Ofloxacinum
 Ulotka dołączona do opakowania: informacja dla użytkownika Ofloxamed, 3 mg/ml, krople do oczu, roztwór Ofloxacinum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera
Ulotka dołączona do opakowania: informacja dla użytkownika Ofloxamed, 3 mg/ml, krople do oczu, roztwór Ofloxacinum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. Każdy ml roztworu zawiera 0,25 mg oksymetazoliny chlorowodorku (Oxymetazolini hydrochloridum).
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO OXALIN 0,025%; 0,25 mg/ml, krople do nosa, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każdy ml roztworu zawiera 0,25 mg oksymetazoliny chlorowodorku
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO OXALIN 0,025%; 0,25 mg/ml, krople do nosa, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każdy ml roztworu zawiera 0,25 mg oksymetazoliny chlorowodorku
Ulotka dołączona do opakowania: informacja dla pacjenta. Vidisic 2 mg/g, żel do oczu, Carbomerum
 Ulotka dołączona do opakowania: informacja dla pacjenta Vidisic 2 mg/g, żel do oczu, Carbomerum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje ważne
Ulotka dołączona do opakowania: informacja dla pacjenta Vidisic 2 mg/g, żel do oczu, Carbomerum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje ważne
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. Azelastine - Brown, 0,5 mg/ml, krople do oczu, roztwór
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Azelastine - Brown, 0,5 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 0,05% roztwór azelastyny chlorowodorku (0,5 mg/ml).
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Azelastine - Brown, 0,5 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 0,05% roztwór azelastyny chlorowodorku (0,5 mg/ml).
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. Jeden ml roztworu (22 krople) zawiera 5 mg butamiratu cytrynianu (Butamirati citras).
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Sinecod, 5 mg/ml, krople doustne, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml roztworu (22 krople) zawiera 5 mg butamiratu cytrynianu
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Sinecod, 5 mg/ml, krople doustne, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden ml roztworu (22 krople) zawiera 5 mg butamiratu cytrynianu
Otrivin Katar i Zatoki jest przeznaczony do stosowania u dorosłych i młodzieży w wieku powyżej 12 lat.
 Otrivin Katar i Zatoki, aerozol do nosa, roztwór Jeden ml roztworu zawiera 1 mg ksylometazoliny chlorowodorku. Wskazania do stosowania Nadmierne przekrwienie błony śluzowej nosa występujące w przebiegu
Otrivin Katar i Zatoki, aerozol do nosa, roztwór Jeden ml roztworu zawiera 1 mg ksylometazoliny chlorowodorku. Wskazania do stosowania Nadmierne przekrwienie błony śluzowej nosa występujące w przebiegu
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO CONDYLINE, 5 mg/ml, roztwór na skórę 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu na skórę zawiera 5 mg podofilotoksyny (Podophyllotoxinum).
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO CONDYLINE, 5 mg/ml, roztwór na skórę 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu na skórę zawiera 5 mg podofilotoksyny (Podophyllotoxinum).
ULOTKA DOŁĄCZONA DO OPAKOWANIA: INFORMACJA DLA UŻYTKOWNIKA. Ofloxacin-POS, 3 mg/ml, krople do oczu, roztwór. Ofloksacyna
 ULOTKA DOŁĄCZONA DO OPAKOWANIA: INFORMACJA DLA UŻYTKOWNIKA Ofloxacin-POS, 3 mg/ml, krople do oczu, roztwór Ofloksacyna Należy zapoznać się z treścią ulotki przed zastosowaniem leku. - Należy zachować tę
ULOTKA DOŁĄCZONA DO OPAKOWANIA: INFORMACJA DLA UŻYTKOWNIKA Ofloxacin-POS, 3 mg/ml, krople do oczu, roztwór Ofloksacyna Należy zapoznać się z treścią ulotki przed zastosowaniem leku. - Należy zachować tę
Podsumowanie danych o bezpieczeństwie stosowania produktu leczniczego Demezon
 VI.2 VI.2.1 Podsumowanie danych o bezpieczeństwie stosowania produktu leczniczego Demezon Omówienie rozpowszechnienia choroby Deksametazonu sodu fosforan w postaci roztworu do wstrzykiwań stosowany jest
VI.2 VI.2.1 Podsumowanie danych o bezpieczeństwie stosowania produktu leczniczego Demezon Omówienie rozpowszechnienia choroby Deksametazonu sodu fosforan w postaci roztworu do wstrzykiwań stosowany jest
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Dolopt Plus, 20 mg/ml + 5 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden mililitr roztworu zawiera 20 mg dorzolamidu
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Dolopt Plus, 20 mg/ml + 5 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jeden mililitr roztworu zawiera 20 mg dorzolamidu
Ulotka dołączona do opakowania: informacja dla pacjenta
 Ulotka dołączona do opakowania: informacja dla pacjenta PRIMADEX (1 mg + 3 500 IU + 6 000 IU)/ml, krople do oczu, zawiesina Dexamethasonum + Neomycini sulfas + Polymyxini B sulfas Należy uważnie zapoznać
Ulotka dołączona do opakowania: informacja dla pacjenta PRIMADEX (1 mg + 3 500 IU + 6 000 IU)/ml, krople do oczu, zawiesina Dexamethasonum + Neomycini sulfas + Polymyxini B sulfas Należy uważnie zapoznać
