(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP (96) Data i numer zgłoszenia patentu europejskiego:
|
|
|
- Alicja Orzechowska
- 7 lat temu
- Przeglądów:
Transkrypt
1 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP Urząd Patentowy Rzeczypospolitej Polskiej (96) Data i numer zgłoszenia patentu europejskiego: (97) O udzieleniu patentu europejskiego ogłoszono: Europejski Biuletyn Patentowy 14/17 EP B1 (13) (1) T3 Int.Cl. A61K 9/12 (06.01) A61K 31/496 (06.01) A61K 31/7036 (06.01) A61P 11/00 (06.01) (4) Tytuł wynalazku: Kompozycje przeciwbakteryjne do leczenia infekcji górnych i dolnych dróg oddechowych (30) Pierwszeństwo: IT MI (43) Zgłoszenie ogłoszono: w Europejskim Biuletynie Patentowym nr 07/43 (4) O złożeniu tłumaczenia patentu ogłoszono: Wiadomości Urzędu Patentowego 14/09 (73) Uprawniony z patentu: Rottapharm S.p.A., Milano, IT (72) Twórca(y) wynalazku: PL/EP T3 PATRIZIA PATTINI, Milano, IT (74) Pełnomocnik: rzecz. pat. Sławomir Kotara POLSERVICE KANCELARIA RZECZNIKÓW PATENTOWYCH SP. Z O.O. ul. Bluszczańska Warszawa Uwaga: W ciągu dziewięciu miesięcy od publikacji informacji o udzieleniu patentu europejskiego, każda osoba może wnieść do Europejskiego Urzędu Patentowego sprzeciw dotyczący udzielonego patentu europejskiego. Sprzeciw wnosi się w formie uzasadnionego na piśmie oświadczenia. Uważa się go za wniesiony dopiero z chwilą wniesienia opłaty za sprzeciw (Art. 99 (1) Konwencji o udzielaniu patentów europejskich).
2 2 Opis [0001] Niniejszy wynalazek dotyczy kompozycji zawierających środek przeciwbakteryjny oraz odpowiedni nośnik, które mogą być podawane na drodze nebulizacji. Stan techniki [0002] Zakażenie Pseudomonas aeruginosa jest jednym z głównych niekorzystnych czynników prognostycznych dla pacjentów cierpiących na mukowiscydozę (CF). [0003] Choroba ta charakteryzuje się defektem genu, który powoduje nieprawidłowe funkcjonowanie CFTR (błonowego regulatora przewodnictwa), białka zaangażowanego w przezbłonowy transport soli. [0004] W efekcie zmienionego transportu jonowego w komórce, dochodzi do ujawnienia się mukowiscydozy w postaci zmiany wydzielin komórek nabłonkowych oskrzeli, zatok, trzustki, jelita, przewodów żółciowych oraz gruczołów potowych. [000] W rezultacie, pacjenci cierpiący na mukowiscydozę wytwarzają śluz, który jest bardzo gęsty oraz trudny do odkrztuszenia. Najbardziej poważne problemy zazwyczaj dotykają oskrzeli, gdzie lepkość śluzu powoduje, że rzęski oskrzelowe mają trudności z usunięciem zainhalowanych cząstek. Tym samym, śluz nie może pełnić swojego podstawowego zadania polegającego na ułatwianiu usuwania zainhalowanych cząstek, stwarzając tym samym warunki wysoce korzystne dla kolonizacji bakterii w wyniku zastoju w górnych i dolnych drogach oddechowych. W szczególności, niemal u wszystkich pacjentów rozwija się zakażenie Pseudomonas aeruginosa, które staje się nieuleczalne oraz wskutek tego przewlekłe. W rezultacie, pacjenci z CF są dotknięci utrwalającym się tercetem zdarzeń, które prowadzą do niemożliwego do zatrzymania zaniku funkcji oddechowych. [0006] Ten tercet zdarzeń jest znany jako niedrożność zakażenie stan zapalny. Śluz ochrania również bakterie przez działaniem antybiotyków, co oznacza, że niezbędne są bardzo wysokie dawki w celu zapewnienia działania bakteriobójczego. [0007] W przypadku aminoglikozydów, rodziny leków, które są najbardziej skuteczne przeciwko temu drobnoustrojowi oraz ogólnie bakteriom Gram-ujemnym, wymagane są stężenia 2 razy wyższe niż MIC, aby zapewnić działanie bakteriobójcze, ponieważ stężenia razy wyższe niż MIC są uważane za działające jedynie bakteriostatycznie.
3 [0008] W celu podawania powtarzanych cykli terapii antybiotykowej o wysokich stężeniach wymaganych w przewlekłym zakażeniu, od pewnego czasu stosowane są oparte na antybiotykach roztwory do inhalacji przeznaczone do nebulizacji jedynie w dolnych drogach oddechowych. Preparaty te umożliwiają, aby antybiotyk został przeniesiony do miejsca zakażenia, pozwalając na zastosowanie wysokich dawek oraz w tym samym czasie zmniejszając narażenie układowe. [0009] Kolonizacja bakteryjna przez Pseudomonas aeruginosa oraz inne patogeny ma miejsce na drodze bezpośredniego kontaktu, szczególnie na skutek zainhalowania cząstek bakterii w zawiesinie powietrza. Górne drogi oddechowe odgrywają kluczową rolę w tym procesie kolonizacji, stanowiąc korzystną drogę dostępu dla wielu drobnoustrojów. [00] W normalnych warunkach nos wytwarza śluz, którego funkcja polega na zatrzymywaniu drobnoustrojów, pyłków, kurzu oraz wszystkich innych cząstek zawartych w powietrzu, którym oddychamy, zapobiegając przed ich wniknięciem do wewnętrznych narządów oddechowych. [0011] Skrajne wysuszenie śluzu radykalnie zmniejsza skuteczność wydzielin nosowych, które nieuchronnie stają się idealnym podłożem dla wzrostu bakterii. [0012] Zanim stanie się przewlekłe, zakażenie Pseudomonas objawia się pierwszym zakażeniem, sygnalizowanym na początku pojawieniem się bakterii w plwocinie; na tym etapie, specyficznie ukierunkowane leczenie antybiotykiem może zwalczyć drobnoustrój oraz opóźnić przewlekłe zakażenie, lecz zakażenie później sporadycznie powraca, aż stanie się przewlekłe. Na tym etapie, wyeliminowanie drobnoustroju z zatok nosowych pełni znaczące działanie prewencyjne przeciwko kolonizacji bakteryjnej dolnych dróg oddechowych. [0013] Z tego powodu, określone preparaty przeciwbakteryjne skierowane przeciwko tym patogenom, są bardzo pożądane; takie preparaty powinny uwzględniać fizjologię zatok nosowych oraz zatok oskrzelowych oraz wykazywać działanie przeciwbakteryjne i przeciwzapalne, zapobiegając tym samym przewlekłemu zakażeniu oraz kolonizacji dolnych dróg oddechowych spowodowanej migracją bakterii z górnych dróg oddechowych, zmniejszać liczbę bakterii w momencie, gdy zakażenie nie może już zostać zwalczone, oraz w tym samym czasie zmniejszać powiązany stan zapalny. [0014] Jednakże, przewlekła kolonizacja bakteryjna, szczególnie drobnoustrojami Gramujemnymi oraz w szczególności Pseudomonas sp. stanowi możliwe i częste zdarzenie nawet u pacjentów nie cierpiących z powodu CF, szczególnie tych z PCD (pierwotną dyskinezą rzęsek), ciężką przewlekłą obturacyjną chorobą płuc (COPD), lub pacjentów ze
4 zmianami w funkcji zatok nosowych, którzy są szczególnie predysponowani na zakażenie bakteryjne oraz powiązane objawy zapalne. Na poziomie oskrzeli, pacjenci ze zmianami ścian oskrzeli wykazującymi obszary w kształcie torebek (rozstrzeń oskrzeli) są szczególnie narażeni na przewlekłe zakażenie. [001] Kwas hialuronowy stanowi naturalny biopolimer należący do rodziny glikozoaminoglikanów (GAG), oraz jest jednym z głównych składników macierzy tkanki łącznej. Płuca, razem ze skórą oraz jelitami, zawierają największe ilości kwasu hialuronowego. Spośród wielu znanych właściwości kwasu hialuronowego, możliwe że główną stanowi jego wiązanie i zatrzymywanie znaczącej ilości wody. [0016] Kwas hialuronowy jest również stosowany ze względu na swoje właściwości w licznych chorobach zapalnych. Na przykład, znane jest jego działanie na chrząstkę stawową; kwas hialuronowy jest stosowany drogą dostawową w celu zwiększenia właściwości przyczepnych mazi stawowej, oraz również dlatego, że wykazuje bezpośrednie działanie przeciwzapalne, zarówno w modelach ostrego stanu zapalnego jak też w przewlekłych stanach zapalnych. Właściwości przeciwzapalne kwasu hialuronowego są również wykorzystywane w stomatologii, chirurgii plastycznej oraz dermatologii. [0017] Niedawno została opisana również zdolność kwasu hialuronowego do zapobiegania skurczowi oskrzeli w teście stresowym, podczas jego podawania drogą inhalacji. [0018] Podawanie antybiotyków drogą inhalacji normalnie charakteryzuje się dobrą tolerancją układową z powodu niskiej absorpcji układowej, lecz często towarzyszą mu działania niepożądane, takie jak skurcz oskrzeli spowodowany reaktywnością miejscową. Zdarzenie to jest obserwowane u niektórych -1% pacjentów, którzy są wskutek tego zobligowani do zaprzestania przyjmowania antybiotyków, szczególnie tobramycyny. [0019] W terapii aerozolowej pacjentów z CF, ostatnio zasugerowano leczenie za pomocą hipertonicznego roztworu (6-7% NaCl) dodatkowo oprócz leczenia antybiotykiem, mając na względzie nawilżenie lepkich wydzielin, poprawiając tym samym ich reologię oraz ułatwiając ich eliminację. Odkryto, że to leczenie poprawia funkcję oddechową. [00] Jednakże, podawanie hipertonicznego roztworu powoduje istotne problemy, szczególnie w odniesieniu do jego tolerowania, ponieważ jego wdychanie powoduje stan zapalny błony śluzowej dróg oddechowych, zapalenie gardła, zapalenie krtani z zaczerwienieniem oraz miejscowym obrzękiem, co wymaga przerwania leczenia u dużej liczby pacjentów.
5 OPIS WYNALAZKU [0021] Obecnie odkryto, że podawanie antybiotyków aminoglikozydowych lub fluorochinolonowych związanych z kwasem hialuronowym, na drodze inhalacji (podawanie donosowe lub podawanie do górnych dróg oddechowych) lub podawanie dooskrzelowe, daje lepsze rezultaty terapeutyczne niż tradycyjne preparaty aerozolowe oraz znacznie lepszy profil tolerancji miejscowej. Kwas hialuronowy działa synergicznie z antybiotykiem zarówno w górnych jak i dolnych drogach oddechowych. [0022] W szczególności, wynalazek umożliwia bardziej skuteczne leczenie pacjentów z mukowiscydozą, ponieważ zwalcza utajone centra zakażenia w śluzie nosowym, zwalczając kolonizację dolnych dróg oddechowych oraz skutecznie zmniejszając nawroty zakażeń dróg oddechowych. Wynalazek umożliwia również leczenie pacjentów, którzy musieli przerwać leczenie antybiotykiem dolnych dróg oddechowych drogą inhalacji z powodu nietolerancji oskrzelowej. [0023] Odkryto również, że podawanie hipertonicznego roztworu, razem z kwasem hialuronowym lub jego solami, prowadzi do lepszej tolerancji miejscowej wraz ze zmniejszeniem komponentu zapalnego, wpływającego na błonę śluzową dróg oddechowych, mniejszego ryzyka przerwania terapii oraz lepszego stosowania się pacjentów do zaleceń. [0024] Przykłady aminoglikozydów obejmują tobramycynę, gentamycynę, amikacynę i tym podobne. Tobramycyna jest szczególnie korzystna. [002] Przykłady fluorochinolonów obejmują ciprofloksacynę, norfloksacynę, ofloksacynę i tym podobne. Ciprofloksacyna jest szczególnie korzystna. [0026] Kwas hialuronowy możliwy do zastosowania według wynalazku będzie miał korzystnie niską lub średnią masę cząsteczkową. [0027] W jego pierwszym aspekcie, wynalazek zapewnia zatem preparaty donosowe zawierające tobramycynę (lub inny aminoglikozyd) związane z kwasem hialuronowym lub jego dopuszczalnymi solami, przygotowane w postaci pojedynczej ampułki lub systemu do podawania na drodze inhalacji donosowej przez odpowiedni nebulizator. [0028] Według kolejnego aspektu, wynalazek zapewnia preparaty w postaci ampułki jednorazowego użytku zawierające tobramycynę (lub inny aminoglikozyd) w połączeniu z kwasem hialuronowym do nebulizacji w dolnych drogach oddechowych przez odpowiedni nebulizator.
6 [0029] Według kolejnego aspektu, wynalazek zapewnia preparaty w postaci ampułki jednorazowego użytku zawierające ciprofloksacyne lub inny fluorochinolon w połączeniu z kwasem hialuronowym do nebulizacji w dolnych drogach oddechowych przez odpowiedni nebulizator. [0030] Według jeszcze kolejnego aspektu, wynalazek zapewnia preparaty w postaci sprayów donosowych zawierające ciprofloksacynę lub inny fluorochinolon, związane z kwasem hialuronowym lub jego dopuszczalnymi solami, przygotowane w postaci pojedynczej ampułki lub systemu do podawania na drodze inhalacji donosowej przez odpowiedni nebulizator. [0031] Według kolejnego aspektu, wynalazek zapewnia preparaty w jałowych, jednodawkowych ampułkach z -7% hipertonicznym roztworem, zawierające kwas hialuronowy lub jego sól lub ester o niskiej masie cząsteczkowej lub średniej masie cząsteczkowej o stężeniu pomiędzy 0,01% i 1%, oraz korzystnie pomiędzy 0,01% i 0,1%. [0032] Preparaty te okazały się odpowiednie do podawania jako aerozole w dolnych drogach oddechowych na drodze nebulizacji przez kompresory z efektem Venturiego, takie jak Pari boy, Pari Turbo boy, Nebula, itd. oraz odpowiednie nebulizatory, lub przez system wibracyjny, taki jak Eflow rapid lub systemy do nebulizacji ultradźwiękowej takie jak I-neb AAD. [0033] Preparaty jednodawkowe według wynalazku będą korzystnie występowały w postaci jałowych roztworów wodnych. [0034] Zdolność do zatrzymywania wody typowa dla kwasu hialuronowego oraz w konsekwencji możliwość nawilżania śluzu i umożliwiania jego łatwiejszej eliminacji, jak również możliwość wspomagania działania antybiotyku poprzez ułatwianie jego wniknięcia do śluzu, wytwarza efekt synergiczny w leczeniu dolnych i górnych dróg oddechowych. [003] W celu podawania aerozoli w dolnych drogach oddechowych, roztwory mogą zostać poddane nebulizacji przez kompresor z efektem Venturiego, taki jak Pari boy, Pari Turbo boy, Nebula, itd. oraz odpowiednie nebulizatory, lub system wibracyjny, taki jak Eflow rapid, systemy do nebulizacji ultradźwiękowej, lub systemy, takie jak I- neb AAD. [0036] Każda ampułka jednorazowego użytku zazwyczaj ma objętość pomiędzy 2 i ml, oraz zawiera pomiędzy i 300 mg siarczanu tobramycyny. Kwas hialuronowy, jego sole (tak jak sól sodowa) lub estry mają masę cząsteczkową korzystnie pomiędzy 000 i Da, bardziej korzystnie pomiędzy 0000 i 0000, i występują w stężeniu
7 wynoszącym pomiędzy 0,01 i %. Średnia średnica aerodynamiczna cząstek w znebulizowanych roztworach wynosi korzystnie pomiędzy 2 i mikronów. [0037] Roztwór wykazuje ph pomiędzy, i 8,0, korzystnie pomiędzy ph 6 i 7, oraz jest hipotoniczny, w przybliżeniu pomiędzy 0 i 0 mosm/kg wody z (w przybliżeniu) 0,2 normalnej soli fizjologicznej, oraz korzystnie pomiędzy i 0 mosm/kg. [0038] W przypadku ciprofloksacyny, ampułki jednorazowego użytku mają objętość wynoszącą pomiędzy 2 i ml, oraz zawierają do 00 mg leku dodatkowo, oprócz kwasu hialuronowego, jak określono powyżej. [0039] Roztwory, które mają zostać poddane nebulizacji, opisane powyżej, mogą również zostać zastosowane do nebulizacji w górnych drogach oddechowych, przez odpowiedni system taki jak SinuNeb. [0040] W tym przypadku, dawki mogą być niższe: na przykład, siarczan tobramycyny od 0 do mg oraz ciprofloksacyna od 0 do mg. [0041] Roztwór donosowy wykazuje ph pomiędzy, i 7,, oraz korzystnie jest izotoniczny. [0042] Alternatywnie, roztwory donosowe w postaci sprayów są zawarte w, 1 lub ml wielodawkowej butelce ze sprayem lub 0-1 ml mikrodyfuzorze, które mogą dostarczyć pomiędzy 0, mg i 2 mg siarczanu tobramycyny na nozdrze przy każdym podaniu. [0043] Roztwór zawiera również kwas hialuronowy, jego sole lub estry, korzystnie o masie cząsteczkowej wynoszącej pomiędzy 0000 oraz 00000, w ilości wynoszącej pomiędzy 0,01% i % wagowych, korzystnie pomiędzy 0,0% i 1%, oraz bardziej korzystnie pomiędzy 0,0% i 0,%. Roztwór jest izotoniczny lub słabo hipotoniczny i wykazuje ph wynoszące pomiędzy i 7. [0044] Roztwór może zostać rozdzielony pomiędzy ml jednodawkowe butelki zawierające ten sam skład co wielodawkowy preparat. [004] Podobne preparaty ciprofloksacyny, zawarte w, 1 lub ml wielodawkowej butelce ze sprayem lub 0 lub 1 ml mikrodyfuzorze mogą dostarczyć pomiędzy mg i 7 mg ciprofloksacyny na nozdrze przy każdorazowym podaniu. [0046] Roztwór może występować w ml jednodawkowej butelce zawierającej ten sam skład co wielodawkowy preparat. [0047] Wynalazek jest przedstawiony w sposób bardziej szczegółowy w poniższych przykładach.
8 8 Przykład 1 [0048] 4 ml ampułka jednorazowego użytku zawiera: 300 mg Hialuronian sodu 0,1 % ph roztworu 6 Osmolarność 180 mosm/kg [0049] Lepkość jest dostosowana tak, aby uczynić preparat możliwym do nebulizacji na poziomie oskrzeli przez odpowiedni nebulizator. Przykład 2 [000] 3 ml ampułka jednorazowego użytku zawiera: 300 mg Hialuronian sodu 0,0% ph roztworu 6 Osmolarność 180 mosm/kg [001] Lepkość jest dostosowana tak, aby uczynić preparat możliwym do nebulizacji na poziomie oskrzeli przez odpowiedni nebulizator, taki jak Pari LCPLUS, Pari eflow rapid. 1 Przykład 3 [002] 4 ml ampułka jednorazowego użytku zawiera: Ciprofloksacyna 300 mg Hialuronian sodu 0,% ph roztworu 6
9 9 4 ml ampułka jednorazowego użytku zawiera: Osmolarność 180 mosm/kg [003] Lepkość jest dostosowana tak, aby uczynić preparat możliwym do nebulizacji na poziomie oskrzeli przez odpowiedni nebulizator. Przykład 4 [004] 4 ml ampułka jednorazowego użytku zawiera: Ciprofloksacyna 00 mg Hialuronian sodu 0,1 % ph roztworu 6 Osmolarność 180 mosm/kg [00] Lepkość jest dostosowana tak, aby uczynić preparat możliwym do nebulizacji na poziomie oskrzeli przez odpowiedni nebulizator. Przykład [006] 3 ml ampułka jednorazowego użytku zawiera: 0 mg Hialuronian sodu 0,1 % ph roztworu 7 1 [007] Roztwór jest przygotowany jako izotoniczny. Lepkość jest dostosowana tak, aby uczynić preparat możliwym do nebulizacji na poziomie oskrzeli przez odpowiedni nebulizator, taki jak SinuNeb. Przykład 6
10 [008] 3 ml ampułka jednorazowego użytku zawiera: Ciprofloksacyna mg Hialuronian sodu 0,1% ph roztworu 7 [009] Roztwór jest przygotowany jako izotoniczny. [0060] Lepkość jest dostosowana tak, aby uczynić preparat możliwym do nebulizacji na poziomie oskrzeli przez odpowiedni nebulizator, taki jak SinuNeb. Przykład 7 [0061] ml wielodawkowa butelka ze sprayem donosowym Zawiera: Hialuronian sodu 600 mg 0,2% wagowych Roztwór izotoniczny o ph 7 Każde rozpylenie dostarcza 0,1 0, ml 2 rozpylenia/nozdrze dwa razy dziennie Przykład 8 [0062] ml wielodawkowa butelka ze sprayem donosowym Zawiera: Hialuronian sodu 10 mg 0,% wagowych Roztwór izotoniczny o ph 7 Każde rozpylenie dostarcza 0,1 0, ml
11 11 ml wielodawkowa butelka ze sprayem donosowym Zawiera: 2 rozpylenia/nozdrze dwa razy dziennie Przykład 9 [0063] 1 ml wielodawkowa butelka ze sprayem donosowym Hialuronian sodu 40 mg 0,2% wagowych Roztwór izotoniczny o ph 7 Każde rozpylenie dostarcza 0,1 0, ml 2 rozpylenia/nozdrze dwa razy dziennie Przykład [0064] ml wielodawkowa butelka ze sprayem donosowym jak opisano w Przykładzie 7, zawierająca 70 mg ciprofloksacyny. Przykład 11 1 [006] ml wielodawkowa butelka ze sprayem donosowym jak opisano w Przykładzie 7, zawierająca 00 mg ciprofloksacyny. Przykład 12 [0066] 0 ml butelka mikrodyfuzyjna Zawiera: Hialuronian sodu 0 mg 0,2% wagowych
12 12 0 ml butelka mikrodyfuzyjna Zawiera: Roztwór izotoniczny o ph 7 Każde rozpylenie dostarcza 0,1 0, ml. Przykład 13 [0067] 0 ml butelka mikrodyfuzyjna Zawiera: Hialuronian sodu 70 mg 0,% wagowych Roztwór izotoniczny o ph 7 Każde rozpylenie dostarcza 0,1 0, ml 2 rozpylenia/nozdrze dwa razy dziennie Przykład 14 [0068] 0 ml butelka mikrodyfuzyjna jak opisano w Przykładzie 12, zawierająca 0 mg of ciprofloksacyny. Przykład 1 1 [0069] 0 ml butelka mikrodyfuzyjna jak opisano w Przykładzie 12, zawierająca 70 mg ciprofloksacyny. [0070] Lepkość jest dostosowana tak, aby uczynić preparat możliwym do nebulizacji na poziomie oskrzeli przez odpowiedni nebulizator. Przykład 16 [0071]
13 13 4 ml ampułka do jednorazowego użytku Jałowy roztwór NaCl 7% Hialuronian sodu 0,0% Przykład 17 [0072] 4 ml ampułka do jednorazowego użytku Jałowy roztwór NaCl 7% Hialuronian sodu 0,02% Przykład 18 [0073] Zestaw składający się ze 112 ampułek (28 dniowa terapia) 6 jałowych jednodawkowych ampułek 4 ml Tobramycyna 300 mg Hialuronian sodu 0,1% Roztwór o ph 6 6 x 4 ml jałowych jednodawkowych ampułek (28 dniowa terapia) Jałowy roztwór NaCl 7% Hialuronian sodu 0,02% Zastrzeżenia patentowe 1 1. Kompozycje do inhalacji możliwe do nebulizacji w postaci roztworów antybiotyków aminoglikozydowych lub fluorochinolonowych, związanych z kwasem hialuronowym.
14 Kompozycje jak zastrzeżono w zastrz. 1, podawane drogą donosową. 3. Kompozycje jak zastrzeżono w zastrz. 1 lub 2, w postaci jednodawkowych ampułek możliwych do nebulizacji. 4. Kompozycje jak zastrzeżono w którymkolwiek z zastrz. 1 do 3, możliwe do podawania za pomocą butelki do wielokrotnego rozpylania lub mikrodyfuzora.. Kompozycje jak zastrzeżono w którymkolwiek z zastrz. 1 do 4, zawierające tobramycynę, gentamycynę lub amikacynę. 6. Kompozycje jak zastrzeżono w zastrz. 4, zawierające tobramycynę. 7. Kompozycje jak zastrzeżono w którymkolwiek z zastrz. 1 do, zawierające ciprofloksacynę, norfloksacynę lub ofloksacynę. 8. Kompozycje jak zastrzeżono w zastrz. 7, zawierające ciprofloksacynę. 9. Kompozycje jak zastrzeżono w którymkolwiek z zastrz. 1 do 8, zawierające również kwas hialuronowy lub jego sól lub ester o niskiej lub średniej masie cząsteczkowej.. Kompozycje jak zastrzeżono w którymkolwiek z zastrz. 1 do 9, o ph wynoszącym między i 8,0 oraz o osmolarności między 0 i 0 mosm/kg. 11. Kompozycje jak zastrzeżono w którymkolwiek z zastrz. 1 do, zawierające do 300 mg siarczanu tobramycyny lub do 00 mg ciprofloksacyny do podawania w górnych drogach oddechowych, oraz 0 do mg siarczanu tobramycyny lub 0 do mg ciprofloksacyny do podawania donosowego, w celu zadozowania ilości wynoszącej 0, mg do 2 mg siarczanu tobramycyny lub mg do 2 mg ciprofloksacyny na nozdrze. 12. Kompozycje jak zastrzeżono w którymkolwiek z zastrz. 1 do 11, zawierające kwas hialuronowy lub jego sole lub estry, o masie cząsteczkowej między 0000 i Da, o stężeniu między 0,01 i %. 13. Kompozycje według zastrz do zastosowania w leczeniu zakażeń nosowych i oskrzelowo-płucnych. Rottapharm S.p.A. Pełnomocnik:
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP (96) Data i numer zgłoszenia patentu europejskiego:
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1968711 Urząd Patentowy Rzeczypospolitej Polskiej (96) Data i numer zgłoszenia patentu europejskiego: 05.01.2007 07712641.5
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1968711 Urząd Patentowy Rzeczypospolitej Polskiej (96) Data i numer zgłoszenia patentu europejskiego: 05.01.2007 07712641.5
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) (13) T3 (96) Data i numer zgłoszenia patentu europejskiego: 06.07.2004 04740699.
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1658064 (13) T3 (96) Data i numer zgłoszenia patentu europejskiego: 06.07.2004 04740699.6 (51) Int. Cl. A61K31/37 (2006.01)
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1658064 (13) T3 (96) Data i numer zgłoszenia patentu europejskiego: 06.07.2004 04740699.6 (51) Int. Cl. A61K31/37 (2006.01)
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP (96) Data i numer zgłoszenia patentu europejskiego:
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1773451 (96) Data i numer zgłoszenia patentu europejskiego: 08.06.2005 05761294.7 (13) (51) T3 Int.Cl. A61K 31/4745 (2006.01)
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1773451 (96) Data i numer zgłoszenia patentu europejskiego: 08.06.2005 05761294.7 (13) (51) T3 Int.Cl. A61K 31/4745 (2006.01)
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) (96) Data i numer zgłoszenia patentu europejskiego:
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1648484 Urząd Patentowy Rzeczypospolitej Polskiej (96) Data i numer zgłoszenia patentu europejskiego: 01.06.04 047366.4 (97)
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1648484 Urząd Patentowy Rzeczypospolitej Polskiej (96) Data i numer zgłoszenia patentu europejskiego: 01.06.04 047366.4 (97)
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP (96) Data i numer zgłoszenia patentu europejskiego:
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1787644 Urząd Patentowy Rzeczypospolitej Polskiej (96) Data i numer zgłoszenia patentu europejskiego: 07.11.2006 06123574.3
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1787644 Urząd Patentowy Rzeczypospolitej Polskiej (96) Data i numer zgłoszenia patentu europejskiego: 07.11.2006 06123574.3
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP (96) Data i numer zgłoszenia patentu europejskiego:
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1886669 Urząd Patentowy Rzeczypospolitej Polskiej (96) Data i numer zgłoszenia patentu europejskiego: 02.08.2007 07113670.9
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1886669 Urząd Patentowy Rzeczypospolitej Polskiej (96) Data i numer zgłoszenia patentu europejskiego: 02.08.2007 07113670.9
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP (96) Data i numer zgłoszenia patentu europejskiego:
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1737439 Urząd Patentowy Rzeczypospolitej Polskiej (96) Data i numer zgłoszenia patentu europejskiego: 31.03.2005 05731707.5
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1737439 Urząd Patentowy Rzeczypospolitej Polskiej (96) Data i numer zgłoszenia patentu europejskiego: 31.03.2005 05731707.5
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) (96) Data i numer zgłoszenia patentu europejskiego:
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1680075 (13) T3 Urząd Patentowy Rzeczypospolitej Polskiej (96) Data i numer zgłoszenia patentu europejskiego: 11.10.2004
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1680075 (13) T3 Urząd Patentowy Rzeczypospolitej Polskiej (96) Data i numer zgłoszenia patentu europejskiego: 11.10.2004
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) (96) Data i numer zgłoszenia patentu europejskiego:
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1711158 Urząd Patentowy Rzeczypospolitej Polskiej (96) Data i numer zgłoszenia patentu europejskiego: 16.11.2004 04806793.8
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1711158 Urząd Patentowy Rzeczypospolitej Polskiej (96) Data i numer zgłoszenia patentu europejskiego: 16.11.2004 04806793.8
LECZENIE PRZEWLEKŁYCH ZAKAŻEŃ PŁUC U PACJENTÓW
 Nazwa programu: Terapeutyczne Programy Zdrowotne 2012 Załącznik nr 30 do Zarządzenia Nr 59/2011/DGL Prezesa NFZ z dnia 10 października 2011 roku LECZENIE PRZEWLEKŁYCH ZAKAŻEŃ PŁUC U PACJENTÓW Z MUKOWISCYDOZĄ
Nazwa programu: Terapeutyczne Programy Zdrowotne 2012 Załącznik nr 30 do Zarządzenia Nr 59/2011/DGL Prezesa NFZ z dnia 10 października 2011 roku LECZENIE PRZEWLEKŁYCH ZAKAŻEŃ PŁUC U PACJENTÓW Z MUKOWISCYDOZĄ
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) (13) T3 (96) Data i numer zgłoszenia patentu europejskiego: 02.05.2005 05747547.
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1747298 (13) T3 (96) Data i numer zgłoszenia patentu europejskiego: 02.05.2005 05747547.7 (51) Int. Cl. C22C14/00 (2006.01)
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1747298 (13) T3 (96) Data i numer zgłoszenia patentu europejskiego: 02.05.2005 05747547.7 (51) Int. Cl. C22C14/00 (2006.01)
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP (96) Data i numer zgłoszenia patentu europejskiego:
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1854925 (96) Data i numer zgłoszenia patentu europejskiego: 16.12.2005 05826699.0 (13) (51) T3 Int.Cl. E03D 1/00 (2006.01)
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1854925 (96) Data i numer zgłoszenia patentu europejskiego: 16.12.2005 05826699.0 (13) (51) T3 Int.Cl. E03D 1/00 (2006.01)
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1879609. (96) Data i numer zgłoszenia patentu europejskiego: 04.05.2006 06742792.
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1879609 (96) Data i numer zgłoszenia patentu europejskiego: 04.05.2006 06742792.2 (13) (51) T3 Int.Cl. A61K 38/17 (2006.01)
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1879609 (96) Data i numer zgłoszenia patentu europejskiego: 04.05.2006 06742792.2 (13) (51) T3 Int.Cl. A61K 38/17 (2006.01)
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP (96) Data i numer zgłoszenia patentu europejskiego:
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 2190940 Urząd Patentowy Rzeczypospolitej Polskiej (96) Data i numer zgłoszenia patentu europejskiego: 11.09.2008 08802024.3
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 2190940 Urząd Patentowy Rzeczypospolitej Polskiej (96) Data i numer zgłoszenia patentu europejskiego: 11.09.2008 08802024.3
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP (96) Data i numer zgłoszenia patentu europejskiego:
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 2179743 (96) Data i numer zgłoszenia patentu europejskiego: 13.07.2009 09460028.5 (13) (51) T3 Int.Cl. A61K 38/18 (2006.01)
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 2179743 (96) Data i numer zgłoszenia patentu europejskiego: 13.07.2009 09460028.5 (13) (51) T3 Int.Cl. A61K 38/18 (2006.01)
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP (96) Data i numer zgłoszenia patentu europejskiego:
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1734922 Urząd Patentowy Rzeczypospolitej Polskiej (96) Data i numer zgłoszenia patentu europejskiego: 11.03.2005 05728244.4
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1734922 Urząd Patentowy Rzeczypospolitej Polskiej (96) Data i numer zgłoszenia patentu europejskiego: 11.03.2005 05728244.4
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) (96) Data i numer zgłoszenia patentu europejskiego: 18.05.2005 05010800.0
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1600805 (96) Data i numer zgłoszenia patentu europejskiego: 18.05.2005 05010800.0 (13) T3 (51) Int. Cl. G02C7/04 A01K13/00
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1600805 (96) Data i numer zgłoszenia patentu europejskiego: 18.05.2005 05010800.0 (13) T3 (51) Int. Cl. G02C7/04 A01K13/00
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP (96) Data i numer zgłoszenia patentu europejskiego:
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 213136 (96) Data i numer zgłoszenia patentu europejskiego: 14.03.2008 08723469.6 (13) (1) T3 Int.Cl. F24D 19/ (2006.01) Urząd
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 213136 (96) Data i numer zgłoszenia patentu europejskiego: 14.03.2008 08723469.6 (13) (1) T3 Int.Cl. F24D 19/ (2006.01) Urząd
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP (96) Data i numer zgłoszenia patentu europejskiego:
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1708988 Urząd Patentowy Rzeczypospolitej Polskiej (96) Data i numer zgłoszenia patentu europejskiego: 13.01.200 0706914.8
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1708988 Urząd Patentowy Rzeczypospolitej Polskiej (96) Data i numer zgłoszenia patentu europejskiego: 13.01.200 0706914.8
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 2052830. (96) Data i numer zgłoszenia patentu europejskiego: 21.10.2008 08018365.
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 202830 Urząd Patentowy Rzeczypospolitej Polskiej (96) Data i numer zgłoszenia patentu europejskiego: 21..2008 0801836.0 (97)
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 202830 Urząd Patentowy Rzeczypospolitej Polskiej (96) Data i numer zgłoszenia patentu europejskiego: 21..2008 0801836.0 (97)
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) (96) Data i numer zgłoszenia patentu europejskiego:
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1680966 (96) Data i numer zgłoszenia patentu europejskiego: 27.10.2004 04791390.0 (13) T3 (51) Int. Cl. A23L1/172 A23P1/08
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1680966 (96) Data i numer zgłoszenia patentu europejskiego: 27.10.2004 04791390.0 (13) T3 (51) Int. Cl. A23L1/172 A23P1/08
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP (96) Data i numer zgłoszenia patentu europejskiego:
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 21737 (96) Data i numer zgłoszenia patentu europejskiego: 16.12.2010 10790844.4 (13) (1) T3 Int.Cl. A47L 1/42 (2006.01) A47L
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 21737 (96) Data i numer zgłoszenia patentu europejskiego: 16.12.2010 10790844.4 (13) (1) T3 Int.Cl. A47L 1/42 (2006.01) A47L
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1505553. (96) Data i numer zgłoszenia patentu europejskiego: 05.08.2004 04018511.
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 3 (96) Data i numer zgłoszenia patentu europejskiego: 0.08.04 0401811.8 (13) (1) T3 Int.Cl. G08C 17/00 (06.01) Urząd Patentowy
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 3 (96) Data i numer zgłoszenia patentu europejskiego: 0.08.04 0401811.8 (13) (1) T3 Int.Cl. G08C 17/00 (06.01) Urząd Patentowy
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP (96) Data i numer zgłoszenia patentu europejskiego:
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1663252 Urząd Patentowy Rzeczypospolitej Polskiej (96) Data i numer zgłoszenia patentu europejskiego: 10.09.2004 04786930.0
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1663252 Urząd Patentowy Rzeczypospolitej Polskiej (96) Data i numer zgłoszenia patentu europejskiego: 10.09.2004 04786930.0
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP (96) Data i numer zgłoszenia patentu europejskiego:
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1799953 Urząd Patentowy Rzeczypospolitej Polskiej (96) Data i numer zgłoszenia patentu europejskiego: 18.08.2005 05770398.5
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1799953 Urząd Patentowy Rzeczypospolitej Polskiej (96) Data i numer zgłoszenia patentu europejskiego: 18.08.2005 05770398.5
MAXimus. Ul. Wita Stwosza 4. 71-173 Szczecin. tel: 071-718-18-96. fax: 071-718-18-97. biuro@kriokomora.com. www.kriokomora.com
 MAXimus Ul. Wita Stwosza 4 71-173 Szczecin tel: 071-718-18-96 fax: 071-718-18-97 biuro@kriokomora.com www.kriokomora.com 1434 MAXimus s.c., Wita Stwosza 4, 71-173 Szczecin STANOWISKO DO INHALACJI MAGIC
MAXimus Ul. Wita Stwosza 4 71-173 Szczecin tel: 071-718-18-96 fax: 071-718-18-97 biuro@kriokomora.com www.kriokomora.com 1434 MAXimus s.c., Wita Stwosza 4, 71-173 Szczecin STANOWISKO DO INHALACJI MAGIC
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP (96) Data i numer zgłoszenia patentu europejskiego:
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 2555663 (96) Data i numer zgłoszenia patentu europejskiego: 06.04.2011 11730434.5 (13) (51) T3 Int.Cl. A47L 15/42 (2006.01)
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 2555663 (96) Data i numer zgłoszenia patentu europejskiego: 06.04.2011 11730434.5 (13) (51) T3 Int.Cl. A47L 15/42 (2006.01)
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP (96) Data i numer zgłoszenia patentu europejskiego:
 PL/EP 1699990 T3 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1699990 (96) Data i numer zgłoszenia patentu europejskiego: 09.11.2004 04800186.1 (13) (51) T3 Int.Cl. E04G
PL/EP 1699990 T3 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1699990 (96) Data i numer zgłoszenia patentu europejskiego: 09.11.2004 04800186.1 (13) (51) T3 Int.Cl. E04G
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP (96) Data i numer zgłoszenia patentu europejskiego:
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 223771 (96) Data i numer zgłoszenia patentu europejskiego: 06.12.08 0886773.1 (13) (1) T3 Int.Cl. A47L 1/42 (06.01) Urząd
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 223771 (96) Data i numer zgłoszenia patentu europejskiego: 06.12.08 0886773.1 (13) (1) T3 Int.Cl. A47L 1/42 (06.01) Urząd
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP (96) Data i numer zgłoszenia patentu europejskiego:
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 240040 Urząd Patentowy Rzeczypospolitej Polskiej (96) Data i numer zgłoszenia patentu europejskiego: 09.07. 007077.0 (97)
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 240040 Urząd Patentowy Rzeczypospolitej Polskiej (96) Data i numer zgłoszenia patentu europejskiego: 09.07. 007077.0 (97)
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP (96) Data i numer zgłoszenia patentu europejskiego:
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 2353894 (96) Data i numer zgłoszenia patentu europejskiego: 19.02.2010 10001703.7 (13) (51) T3 Int.Cl. B60D 5/00 (2006.01)
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 2353894 (96) Data i numer zgłoszenia patentu europejskiego: 19.02.2010 10001703.7 (13) (51) T3 Int.Cl. B60D 5/00 (2006.01)
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) (96) Data i numer zgłoszenia patentu europejskiego:
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1782818 (13) T3 Urząd Patentowy Rzeczypospolitej Polskiej (96) Data i numer zgłoszenia patentu europejskiego: 29.03.06 0642217.4
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1782818 (13) T3 Urząd Patentowy Rzeczypospolitej Polskiej (96) Data i numer zgłoszenia patentu europejskiego: 29.03.06 0642217.4
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) (96) Data i numer zgłoszenia patentu europejskiego:
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1755549 Urząd Patentowy Rzeczypospolitej Polskiej (96) Data i numer zgłoszenia patentu europejskiego: 22.04.2005 05780098.9
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1755549 Urząd Patentowy Rzeczypospolitej Polskiej (96) Data i numer zgłoszenia patentu europejskiego: 22.04.2005 05780098.9
Najczęstsze choroby błony śluzowej nosa i zatok. Poradnik dla pacjenta Dr Grzegorz Warkowski
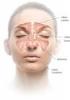 Najczęstsze choroby błony śluzowej nosa i zatok Poradnik dla pacjenta Dr Grzegorz Warkowski 1. Błona śluzowa nosa i zatok. Budowa i znaczenie dla organizmu Bariera przeciw zakażeniom i zanieczyszczeniom
Najczęstsze choroby błony śluzowej nosa i zatok Poradnik dla pacjenta Dr Grzegorz Warkowski 1. Błona śluzowa nosa i zatok. Budowa i znaczenie dla organizmu Bariera przeciw zakażeniom i zanieczyszczeniom
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) (13) T3 (96) Data i numer zgłoszenia patentu europejskiego:
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1586320 (13) T3 (96) Data i numer zgłoszenia patentu europejskiego: 02.02.2005 05472001.6 (51) Int. Cl. A61K31/435 (2006.01)
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1586320 (13) T3 (96) Data i numer zgłoszenia patentu europejskiego: 02.02.2005 05472001.6 (51) Int. Cl. A61K31/435 (2006.01)
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) (96) Data i numer zgłoszenia patentu europejskiego:
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1886585 Urząd Patentowy Rzeczypospolitej Polskiej (96) Data i numer zgłoszenia patentu europejskiego: 24.07.2006 06291197.9
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1886585 Urząd Patentowy Rzeczypospolitej Polskiej (96) Data i numer zgłoszenia patentu europejskiego: 24.07.2006 06291197.9
Aerozol pulsujący. Nowa jakość w leczeniu zapalenia zatok. skuteczne, dokładne i bezpieczne leczenie zapalenia zatok
 Nowa jakość w leczeniu zapalenia zatok Aerozol pulsujący skuteczne, dokładne i bezpieczne leczenie zapalenia zatok PARI SINUS Terapia inhalacyjna stosowana w ostrych i przewlekłych chorobach górnych dróg
Nowa jakość w leczeniu zapalenia zatok Aerozol pulsujący skuteczne, dokładne i bezpieczne leczenie zapalenia zatok PARI SINUS Terapia inhalacyjna stosowana w ostrych i przewlekłych chorobach górnych dróg
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP (96) Data i numer zgłoszenia patentu europejskiego:
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 22799 Urząd Patentowy Rzeczypospolitej Polskiej (96) Data i numer zgłoszenia patentu europejskiego:.04. 0040.9 (97) O udzieleniu
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 22799 Urząd Patentowy Rzeczypospolitej Polskiej (96) Data i numer zgłoszenia patentu europejskiego:.04. 0040.9 (97) O udzieleniu
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) (13) T3 (96) Data i numer zgłoszenia patentu europejskiego: 27.10.2004 04791425.
 PL/EP 1809944 T3 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1809944 (13) T3 (96) Data i numer zgłoszenia patentu europejskiego: 27.10.2004 04791425.4 (51) Int. Cl.
PL/EP 1809944 T3 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1809944 (13) T3 (96) Data i numer zgłoszenia patentu europejskiego: 27.10.2004 04791425.4 (51) Int. Cl.
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP (96) Data i numer zgłoszenia patentu europejskiego:
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 2259949 (96) Data i numer zgłoszenia patentu europejskiego: 11.02.2009 09727379.1 (13) (51) T3 Int.Cl. B60L 11/00 (2006.01)
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 2259949 (96) Data i numer zgłoszenia patentu europejskiego: 11.02.2009 09727379.1 (13) (51) T3 Int.Cl. B60L 11/00 (2006.01)
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) (96) Data i numer zgłoszenia patentu europejskiego:
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1671552 (96) Data i numer zgłoszenia patentu europejskiego: 02.12.2005 05026319.3 (13) T3 (51) Int. Cl. A23L1/305 A23J3/16
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1671552 (96) Data i numer zgłoszenia patentu europejskiego: 02.12.2005 05026319.3 (13) T3 (51) Int. Cl. A23L1/305 A23J3/16
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) (96) Data i numer zgłoszenia patentu europejskiego:
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1659297 Urząd Patentowy Rzeczypospolitej Polskiej (96) Data i numer zgłoszenia patentu europejskiego: 12.10.2005 05354036.5
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1659297 Urząd Patentowy Rzeczypospolitej Polskiej (96) Data i numer zgłoszenia patentu europejskiego: 12.10.2005 05354036.5
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP (96) Data i numer zgłoszenia patentu europejskiego:
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1732433 Urząd Patentowy Rzeczypospolitej Polskiej (96) Data i numer zgłoszenia patentu europejskiego: 27.01.2005 05702820.1
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1732433 Urząd Patentowy Rzeczypospolitej Polskiej (96) Data i numer zgłoszenia patentu europejskiego: 27.01.2005 05702820.1
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) (13) T3 (96) Data i numer zgłoszenia patentu europejskiego:
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 198480 (13) T3 (96) Data i numer zgłoszenia patentu europejskiego: 21.04.08 08007708.4 (1) Int. Cl. B60H1/24 (06.01) (97)
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 198480 (13) T3 (96) Data i numer zgłoszenia patentu europejskiego: 21.04.08 08007708.4 (1) Int. Cl. B60H1/24 (06.01) (97)
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY SUBSTANCJI CZYNNYCH
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA WŁASNA PRODUKTU LECZNICZEGO PIMAFUCORT (10 mg + 10 mg + 3500 I.U.)/g, maść 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY SUBSTANCJI CZYNNYCH Jeden gram maści zawiera 10
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA WŁASNA PRODUKTU LECZNICZEGO PIMAFUCORT (10 mg + 10 mg + 3500 I.U.)/g, maść 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY SUBSTANCJI CZYNNYCH Jeden gram maści zawiera 10
Temat: Higiena i choroby układu oddechowego.
 Temat: Higiena i choroby układu oddechowego. 1. Sprawność układu oddechowego - ważnym czynnikiem zdrowotnym. a) zanieczyszczenia powietrza Pyły miedzi, aluminium, żelaza, ołowiu, piaskowe, węglowe, azbestowe,
Temat: Higiena i choroby układu oddechowego. 1. Sprawność układu oddechowego - ważnym czynnikiem zdrowotnym. a) zanieczyszczenia powietrza Pyły miedzi, aluminium, żelaza, ołowiu, piaskowe, węglowe, azbestowe,
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 2131847. (96) Data i numer zgłoszenia patentu europejskiego: 27.02.2008 08716068.
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 2131847 Urząd Patentowy Rzeczypospolitej Polskiej (96) Data i numer zgłoszenia patentu europejskiego: 27.02.2008 08716068.5
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 2131847 Urząd Patentowy Rzeczypospolitej Polskiej (96) Data i numer zgłoszenia patentu europejskiego: 27.02.2008 08716068.5
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) (96) Data i numer zgłoszenia patentu europejskiego:
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1624265 (96) Data i numer zgłoszenia patentu europejskiego: 06.07.2005 05106119.0 (13) T3 (51) Int. Cl. F25D23/06 F25D25/02
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1624265 (96) Data i numer zgłoszenia patentu europejskiego: 06.07.2005 05106119.0 (13) T3 (51) Int. Cl. F25D23/06 F25D25/02
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) (13) T3 (96) Data i numer zgłoszenia patentu europejskiego: 09.12.2005 05077837.
 RZECZPSPLITA PLSKA (12) TŁUMACZENIE PATENTU EURPEJSKIEG (19) PL (11) PL/EP 1671547 (13) T3 (96) Data i numer zgłoszenia patentu europejskiego: 09.12.2005 05077837.2 (51) Int. Cl. A23B7/154 (2006.01) (97)
RZECZPSPLITA PLSKA (12) TŁUMACZENIE PATENTU EURPEJSKIEG (19) PL (11) PL/EP 1671547 (13) T3 (96) Data i numer zgłoszenia patentu europejskiego: 09.12.2005 05077837.2 (51) Int. Cl. A23B7/154 (2006.01) (97)
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP (96) Data i numer zgłoszenia patentu europejskiego:
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1591364 Urząd Patentowy Rzeczypospolitej Polskiej (96) Data i numer zgłoszenia patentu europejskiego: 22.04.2005 05103299.3
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1591364 Urząd Patentowy Rzeczypospolitej Polskiej (96) Data i numer zgłoszenia patentu europejskiego: 22.04.2005 05103299.3
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) (13) T3 (96) Data i numer zgłoszenia patentu europejskiego: 08.09.2005 05789871.
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1791422 (13) T3 (96) Data i numer zgłoszenia patentu europejskiego: 08.09.2005 05789871.0 (51) Int. Cl. A01N1/02 (2006.01)
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1791422 (13) T3 (96) Data i numer zgłoszenia patentu europejskiego: 08.09.2005 05789871.0 (51) Int. Cl. A01N1/02 (2006.01)
Czy to nawracające zakażenia układu oddechowego, czy może nierozpoznana astma oskrzelowa? Zbigniew Doniec
 Czy to nawracające zakażenia układu oddechowego, czy może nierozpoznana astma oskrzelowa? Zbigniew Doniec Klinika Pneumonologii, Instytut Gruźlicy i Chorób Płuc OT w Rabce-Zdroju Epidemiologia Zakażenia
Czy to nawracające zakażenia układu oddechowego, czy może nierozpoznana astma oskrzelowa? Zbigniew Doniec Klinika Pneumonologii, Instytut Gruźlicy i Chorób Płuc OT w Rabce-Zdroju Epidemiologia Zakażenia
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) (13) T3 (96) Data i numer zgłoszenia patentu europejskiego:
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1477128 (13) T3 (96) Data i numer zgłoszenia patentu europejskiego: 14.05.2004 04076445.8 (51) Int. Cl. A61D1/02 (2006.01)
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1477128 (13) T3 (96) Data i numer zgłoszenia patentu europejskiego: 14.05.2004 04076445.8 (51) Int. Cl. A61D1/02 (2006.01)
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP (96) Data i numer zgłoszenia patentu europejskiego:
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 2122 (96) Data i numer zgłoszenia patentu europejskiego: 2..07 07866441.4 (13) (1) T3 Int.Cl. D21H 19/06 (06.01) Urząd Patentowy
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 2122 (96) Data i numer zgłoszenia patentu europejskiego: 2..07 07866441.4 (13) (1) T3 Int.Cl. D21H 19/06 (06.01) Urząd Patentowy
Fizjoterapia w praktyce Czyli jak pomóc swojemu koniowi w zaciszu własnej stajni
 Fizjoterapia w praktyce Czyli jak pomóc swojemu koniowi w zaciszu własnej stajni AEROZOLOTERAPIA Choroby układu oddechowego koni stanowią ogromny problem. Po zaburzeniach ortopedycznych są drugą najważniejszą
Fizjoterapia w praktyce Czyli jak pomóc swojemu koniowi w zaciszu własnej stajni AEROZOLOTERAPIA Choroby układu oddechowego koni stanowią ogromny problem. Po zaburzeniach ortopedycznych są drugą najważniejszą
Przedmowa... Skróty...
 VII Przedmowa.............................................................. Skróty................................................................... Przedmowa..........................................................
VII Przedmowa.............................................................. Skróty................................................................... Przedmowa..........................................................
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) (96) Data i numer zgłoszenia patentu europejskiego: 10.03.2006 06707521.8
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 186966 (13) T3 Urząd Patentowy Rzeczypospolitej Polskiej (96) Data i numer zgłoszenia patentu europejskiego:.03.06 0670721.8
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 186966 (13) T3 Urząd Patentowy Rzeczypospolitej Polskiej (96) Data i numer zgłoszenia patentu europejskiego:.03.06 0670721.8
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) (96) Data i numer zgłoszenia patentu europejskiego:
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1668001 Urząd Patentowy Rzeczypospolitej Polskiej (96) Data i numer zgłoszenia patentu europejskiego: 24.09.2004 04784968.2
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1668001 Urząd Patentowy Rzeczypospolitej Polskiej (96) Data i numer zgłoszenia patentu europejskiego: 24.09.2004 04784968.2
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) (96) Data i numer zgłoszenia patentu europejskiego:
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1802536 (96) Data i numer zgłoszenia patentu europejskiego: 20.09.2004 04774954.4 (13) T3 (51) Int. Cl. B65D77/20 B65D85/72
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1802536 (96) Data i numer zgłoszenia patentu europejskiego: 20.09.2004 04774954.4 (13) T3 (51) Int. Cl. B65D77/20 B65D85/72
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP (96) Data i numer zgłoszenia patentu europejskiego:
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1890558 Urząd Patentowy Rzeczypospolitej Polskiej (96) Data i numer zgłoszenia patentu europejskiego: 18.05.2006 06755505.2
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1890558 Urząd Patentowy Rzeczypospolitej Polskiej (96) Data i numer zgłoszenia patentu europejskiego: 18.05.2006 06755505.2
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) (13) T3 (96) Data i numer zgłoszenia patentu europejskiego:
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1712702 (13) T3 (96) Data i numer zgłoszenia patentu europejskiego: 28.03.2006 06006359.1 (51) Int. Cl. E04F15/02 (2006.01)
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1712702 (13) T3 (96) Data i numer zgłoszenia patentu europejskiego: 28.03.2006 06006359.1 (51) Int. Cl. E04F15/02 (2006.01)
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP (96) Data i numer zgłoszenia patentu europejskiego:
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 2047071 Urząd Patentowy Rzeczypospolitej Polskiej (96) Data i numer zgłoszenia patentu europejskiego: 21.07.2007 07786251.4
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 2047071 Urząd Patentowy Rzeczypospolitej Polskiej (96) Data i numer zgłoszenia patentu europejskiego: 21.07.2007 07786251.4
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP (96) Data i numer zgłoszenia patentu europejskiego:
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1561894 (96) Data i numer zgłoszenia patentu europejskiego: 25.01.2005 05001385.3 (13) (51) T3 Int.Cl. E06B 3/66 (2006.01)
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1561894 (96) Data i numer zgłoszenia patentu europejskiego: 25.01.2005 05001385.3 (13) (51) T3 Int.Cl. E06B 3/66 (2006.01)
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 2242492. (96) Data i numer zgłoszenia patentu europejskiego: 16.02.2009 09712902.
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 2242492 (96) Data i numer zgłoszenia patentu europejskiego: 16.02.09 09712902.7 (13) (1) T3 Int.Cl. A61K 31/473 (06.01) A61P
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 2242492 (96) Data i numer zgłoszenia patentu europejskiego: 16.02.09 09712902.7 (13) (1) T3 Int.Cl. A61K 31/473 (06.01) A61P
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) (13) T3 (96) Data i numer zgłoszenia patentu europejskiego:
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 149678 (13) T3 (96) Data i numer zgłoszenia patentu europejskiego: 0.07.04 040744.8 (1) Int. Cl. A22B3/00 (06.01) (97) O
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 149678 (13) T3 (96) Data i numer zgłoszenia patentu europejskiego: 0.07.04 040744.8 (1) Int. Cl. A22B3/00 (06.01) (97) O
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) (13) T3 (96) Data i numer zgłoszenia patentu europejskiego:
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1660738 (13) T3 (96) Data i numer zgłoszenia patentu europejskiego: 28.04.2005 05737864.8 (51) Int. Cl. E04G1/32 (2006.01)
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1660738 (13) T3 (96) Data i numer zgłoszenia patentu europejskiego: 28.04.2005 05737864.8 (51) Int. Cl. E04G1/32 (2006.01)
Mukowiscydoza i pierwotna dyskineza rzęsek. Klinika Pneumonologii i Alergologii Wieku Dziecięcego WUM
 Mukowiscydoza i pierwotna dyskineza rzęsek Klinika Pneumonologii i Alergologii Wieku Dziecięcego WUM Mukowiscydoza, zwłóknienie torbielowate (cystis fibrosis, CF) najczęstsza choroba genetycznie uwarunkowana
Mukowiscydoza i pierwotna dyskineza rzęsek Klinika Pneumonologii i Alergologii Wieku Dziecięcego WUM Mukowiscydoza, zwłóknienie torbielowate (cystis fibrosis, CF) najczęstsza choroba genetycznie uwarunkowana
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) (96) Data i numer zgłoszenia patentu europejskiego: 06.09.2005 05788867.9
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1786660 (96) Data i numer zgłoszenia patentu europejskiego: 06.09.2005 05788867.9 (13) T3 (51) Int. Cl. B62D25/08 B60G15/06
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1786660 (96) Data i numer zgłoszenia patentu europejskiego: 06.09.2005 05788867.9 (13) T3 (51) Int. Cl. B62D25/08 B60G15/06
Ulotka dołączona do opakowania: informacja dla użytkownika. Pulmozyme 1 mg/ml, roztwór do nebulizacji 2500 U/2,5 ml Dornasum alfa
 Ulotka dołączona do opakowania: informacja dla użytkownika Pulmozyme 1 mg/ml, roztwór do nebulizacji 2500 U/2,5 ml Dornasum alfa Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ
Ulotka dołączona do opakowania: informacja dla użytkownika Pulmozyme 1 mg/ml, roztwór do nebulizacji 2500 U/2,5 ml Dornasum alfa Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP (96) Data i numer zgłoszenia patentu europejskiego:
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 2086467 (96) Data i numer zgłoszenia patentu europejskiego: 26.11.2007 07824706.1 (13) (51) T3 Int.Cl. A61F 2/16 (2006.01)
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 2086467 (96) Data i numer zgłoszenia patentu europejskiego: 26.11.2007 07824706.1 (13) (51) T3 Int.Cl. A61F 2/16 (2006.01)
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP (96) Data i numer zgłoszenia patentu europejskiego:
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 2321656 (96) Data i numer zgłoszenia patentu europejskiego:.08.09 09807498.2 (13) (51) T3 Int.Cl. G01R /18 (06.01) G01R 19/
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 2321656 (96) Data i numer zgłoszenia patentu europejskiego:.08.09 09807498.2 (13) (51) T3 Int.Cl. G01R /18 (06.01) G01R 19/
Ulotka dołączona do opakowania: informacja dla użytkownika. Mucofluid, 50 mg/ml, aerozol do nosa, roztwór. Mesnum
 Ulotka dołączona do opakowania: informacja dla użytkownika Mucofluid, 50 mg/ml, aerozol do nosa, roztwór Mesnum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona
Ulotka dołączona do opakowania: informacja dla użytkownika Mucofluid, 50 mg/ml, aerozol do nosa, roztwór Mesnum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP (96) Data i numer zgłoszenia patentu europejskiego:
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 2814723 (96) Data i numer zgłoszenia patentu europejskiego: 15.02.2013 13704452.5 (13) (51) T3 Int.Cl. B63G 8/39 (2006.01)
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 2814723 (96) Data i numer zgłoszenia patentu europejskiego: 15.02.2013 13704452.5 (13) (51) T3 Int.Cl. B63G 8/39 (2006.01)
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP (96) Data i numer zgłoszenia patentu europejskiego:
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 221611 (96) Data i numer zgłoszenia patentu europejskiego: 19.01. 000481.1 (13) (1) T3 Int.Cl. B28C /42 (06.01) B60P 3/16
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 221611 (96) Data i numer zgłoszenia patentu europejskiego: 19.01. 000481.1 (13) (1) T3 Int.Cl. B28C /42 (06.01) B60P 3/16
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) (13) T3 (96) Data i numer zgłoszenia patentu europejskiego:
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 161679 (13) T3 (96) Data i numer zgłoszenia patentu europejskiego: 24.06.0 064.7 (1) Int. Cl. B60R21/01 (06.01) (97) O udzieleniu
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 161679 (13) T3 (96) Data i numer zgłoszenia patentu europejskiego: 24.06.0 064.7 (1) Int. Cl. B60R21/01 (06.01) (97) O udzieleniu
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 2074843. (96) Data i numer zgłoszenia patentu europejskiego: 27.09.2007 07818485.
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 74843 (96) Data i numer zgłoszenia patentu europejskiego: 27.09.07 0781848.0 (13) (1) T3 Int.Cl. H04W 4/12 (09.01) Urząd
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 74843 (96) Data i numer zgłoszenia patentu europejskiego: 27.09.07 0781848.0 (13) (1) T3 Int.Cl. H04W 4/12 (09.01) Urząd
WSPÓŁCZESNE PODEJŚCIE DO MIEJSCOWEJ ANTYBIOTYKOTERAPII ZAPALEŃ DRÓG ODDECHOWYCH
 WSPÓŁCZESNE PODEJŚCIE DO MIEJSCOWEJ ANTYBIOTYKOTERAPII ZAPALEŃ DRÓG ODDECHOWYCH Wprowadzenie antybiotyków do lecznictwa było wielkim przełomem w medycynie. W chwili obecnej posiadamy bogate, 50-letnie
WSPÓŁCZESNE PODEJŚCIE DO MIEJSCOWEJ ANTYBIOTYKOTERAPII ZAPALEŃ DRÓG ODDECHOWYCH Wprowadzenie antybiotyków do lecznictwa było wielkim przełomem w medycynie. W chwili obecnej posiadamy bogate, 50-letnie
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP (96) Data i numer zgłoszenia patentu europejskiego:
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 2638340 (96) Data i numer zgłoszenia patentu europejskiego: 10.11.2011 11781794.0 (13) (51) T3 Int.Cl. F25D 23/00 (2006.01)
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 2638340 (96) Data i numer zgłoszenia patentu europejskiego: 10.11.2011 11781794.0 (13) (51) T3 Int.Cl. F25D 23/00 (2006.01)
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP (96) Data i numer zgłoszenia patentu europejskiego:
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 2084998 (96) Data i numer zgłoszenia patentu europejskiego: 29.01.2009 09151619.5 (13) (51) T3 Int.Cl. A47F 3/14 (2006.01)
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 2084998 (96) Data i numer zgłoszenia patentu europejskiego: 29.01.2009 09151619.5 (13) (51) T3 Int.Cl. A47F 3/14 (2006.01)
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 2120618. (96) Data i numer zgłoszenia patentu europejskiego: 28.02.2008 08719309.
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 2120618 (96) Data i numer zgłoszenia patentu europejskiego: 28.02.2008 08719309.0 (13) (1) T3 Int.Cl. A41B 11/02 (2006.01)
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 2120618 (96) Data i numer zgłoszenia patentu europejskiego: 28.02.2008 08719309.0 (13) (1) T3 Int.Cl. A41B 11/02 (2006.01)
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP (96) Data i numer zgłoszenia patentu europejskiego:
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 2224595 (96) Data i numer zgłoszenia patentu europejskiego: 10.02.2010 10001353.1 (13) (51) T3 Int.Cl. H03K 17/96 (2006.01)
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 2224595 (96) Data i numer zgłoszenia patentu europejskiego: 10.02.2010 10001353.1 (13) (51) T3 Int.Cl. H03K 17/96 (2006.01)
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) (96) Data i numer zgłoszenia patentu europejskiego:
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 182634 (96) Data i numer zgłoszenia patentu europejskiego: 19.04.07 070963.1 (13) T3 (1) Int. Cl. F16H/17 F16H7/04 (06.01)
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 182634 (96) Data i numer zgłoszenia patentu europejskiego: 19.04.07 070963.1 (13) T3 (1) Int. Cl. F16H/17 F16H7/04 (06.01)
Podstawy leczenia PCD
 Podstawy leczenia PCD Henryk Mazurek Klinika Pneumonologii i Mukowiscydozy IGiChP OT w Rabce - Zdroju Podstawy leczenia Brak badań wykonanych wg EBM w PCD Zasady leczenia proponowane wg doświadczeń w innych
Podstawy leczenia PCD Henryk Mazurek Klinika Pneumonologii i Mukowiscydozy IGiChP OT w Rabce - Zdroju Podstawy leczenia Brak badań wykonanych wg EBM w PCD Zasady leczenia proponowane wg doświadczeń w innych
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) (96) Data i numer zgłoszenia patentu europejskiego: 27.05.2005 05746418.2
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1817186 (96) Data i numer zgłoszenia patentu europejskiego: 27.05.2005 05746418.2 (13) T3 (51) Int. Cl. B60G21/055 F16D1/06
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1817186 (96) Data i numer zgłoszenia patentu europejskiego: 27.05.2005 05746418.2 (13) T3 (51) Int. Cl. B60G21/055 F16D1/06
(96) Data i numer zgłoszenia patentu europejskiego:
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1690978 (96) Data i numer zgłoszenia patentu europejskiego: 11.02.2005 05101042.9 (13) T3 (51) Int. Cl. D06F81/08 (2006.01)
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1690978 (96) Data i numer zgłoszenia patentu europejskiego: 11.02.2005 05101042.9 (13) T3 (51) Int. Cl. D06F81/08 (2006.01)
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP (96) Data i numer zgłoszenia patentu europejskiego:
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1999308 (96) Data i numer zgłoszenia patentu europejskiego: 28.03.2007 07727422.3 (13) (51) T3 Int.Cl. D06F 35/00 (2006.01)
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1999308 (96) Data i numer zgłoszenia patentu europejskiego: 28.03.2007 07727422.3 (13) (51) T3 Int.Cl. D06F 35/00 (2006.01)
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP (96) Data i numer zgłoszenia patentu europejskiego:
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1810954 (96) Data i numer zgłoszenia patentu europejskiego: 06.12.2006 06025226.9 (13) (51) T3 Int.Cl. C03B 9/41 (2006.01)
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1810954 (96) Data i numer zgłoszenia patentu europejskiego: 06.12.2006 06025226.9 (13) (51) T3 Int.Cl. C03B 9/41 (2006.01)
Czym jest mukowiscydoza?
 Czym jest mukowiscydoza? Mukowiscydoza (z ang. cystic fibrosis, CF) jest najczęściej występującą chorobą genetyczną w ludzkiej populacji. Według najnowszych badań, co 25 osoba jest nosicielem nieprawidłowego
Czym jest mukowiscydoza? Mukowiscydoza (z ang. cystic fibrosis, CF) jest najczęściej występującą chorobą genetyczną w ludzkiej populacji. Według najnowszych badań, co 25 osoba jest nosicielem nieprawidłowego
Ulotka dołączona do opakowania: informacja dla pacjenta. Bramitob, 300 mg/4 ml, roztwór do nebulizacji Tobramycinum
 Ulotka dołączona do opakowania: informacja dla pacjenta Bramitob, 300 mg/4 ml, roztwór do nebulizacji Tobramycinum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera
Ulotka dołączona do opakowania: informacja dla pacjenta Bramitob, 300 mg/4 ml, roztwór do nebulizacji Tobramycinum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera
Przestrzeganie zaleceń terapeutycznych przez pacjentów chorych na mukowiscydozę badanie COMPLIANCE. Raport końcowy
 Przestrzeganie zaleceń terapeutycznych przez pacjentów chorych na mukowiscydozę badanie COMPLIANCE Raport końcowy Cel badania Celem badania była weryfikacja zgodności sposobu przyjmowania tobramycyny wziewnej
Przestrzeganie zaleceń terapeutycznych przez pacjentów chorych na mukowiscydozę badanie COMPLIANCE Raport końcowy Cel badania Celem badania była weryfikacja zgodności sposobu przyjmowania tobramycyny wziewnej
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 2584058. (96) Data i numer zgłoszenia patentu europejskiego: 21.10.2011 11186244.
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 2584058 (96) Data i numer zgłoszenia patentu europejskiego: 21.10.2011 11186244.7 (13) (51) T3 Int.Cl. C22C 38/40 (2006.01)
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 2584058 (96) Data i numer zgłoszenia patentu europejskiego: 21.10.2011 11186244.7 (13) (51) T3 Int.Cl. C22C 38/40 (2006.01)
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1947302. (96) Data i numer zgłoszenia patentu europejskiego: 03.12.2007 07122193.
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1947302 (96) Data i numer zgłoszenia patentu europejskiego: 03.12.2007 07122193.1 (13) (51) T3 Int.Cl. F01M 11/00 (2006.01)
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1947302 (96) Data i numer zgłoszenia patentu europejskiego: 03.12.2007 07122193.1 (13) (51) T3 Int.Cl. F01M 11/00 (2006.01)
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA. Beclonasal Aqua 50 mikrogramów/dawkę, aerozol do nosa, zawiesina Beclometasoni dipropionas
 ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA Beclonasal Aqua 50 mikrogramów/dawkę, aerozol do nosa, zawiesina Beclometasoni dipropionas Należy zapoznać się z treścią ulotki przed zastosowaniem leku.
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA Beclonasal Aqua 50 mikrogramów/dawkę, aerozol do nosa, zawiesina Beclometasoni dipropionas Należy zapoznać się z treścią ulotki przed zastosowaniem leku.
Prawidłowe zasady podawania leków donosowo
 Prawidłowe zasady podawania leków donosowo WSKAZANIA do podawania leków donosowo 1) ostre infekcyjne zapalenie błony śluzowej nosa 2) alergiczne zapalenie błony śluzowej nosa 3) idiopatyczny nieżyt nosa
Prawidłowe zasady podawania leków donosowo WSKAZANIA do podawania leków donosowo 1) ostre infekcyjne zapalenie błony śluzowej nosa 2) alergiczne zapalenie błony śluzowej nosa 3) idiopatyczny nieżyt nosa
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) (96) Data i numer zgłoszenia patentu europejskiego:
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1449961 (96) Data i numer zgłoszenia patentu europejskiego: 14.04.2004 04405227.2 (13) T3 (51) Int. Cl. E01B9/14 F16B13/00
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 1449961 (96) Data i numer zgłoszenia patentu europejskiego: 14.04.2004 04405227.2 (13) T3 (51) Int. Cl. E01B9/14 F16B13/00
Zabiegi fizjoterapeutyczne. SPA-Centrum «Respect»
 Zabiegi fizjoterapeutyczne SPA-Centrum «Respect» Usługi medyczne Nazwazabiegu Czas 1. Początkowa konsultacja lekarza ogólnego 4 min. bezpłatnie 2. Ponowna konsultacja lekarza ogólnego 30 min. bezpłatnie
Zabiegi fizjoterapeutyczne SPA-Centrum «Respect» Usługi medyczne Nazwazabiegu Czas 1. Początkowa konsultacja lekarza ogólnego 4 min. bezpłatnie 2. Ponowna konsultacja lekarza ogólnego 30 min. bezpłatnie
2011-05-30 AEROZOLOTERAPIA. AEROZOLOTERAPIA vs INNE METODY LECZENIA. AEROZOLOTERAPIA vs INNE METODY LECZENIA WSKAZANIA DO TERAPII AEROZOLOWEJ
 AEROZOLOTERAPIA praktyczne wskazówki Aerozol - zawiesina cieczy lub substancji stałej na nośniku gazowym (powietrze lub tlen) Inhalator - urządzenie wytwarzające aerozol Marcin Grabicki Klinika Pulmonologii,
AEROZOLOTERAPIA praktyczne wskazówki Aerozol - zawiesina cieczy lub substancji stałej na nośniku gazowym (powietrze lub tlen) Inhalator - urządzenie wytwarzające aerozol Marcin Grabicki Klinika Pulmonologii,
PRZEWODNIK DLA PACJENTÓW JAK DBAĆ O GARDŁO I KRTAŃ? Przewlekły nieżyt gardła i krtani
 PRZEWODNIK DLA PACJENTÓW JAK DBAĆ O GARDŁO I KRTAŃ? Przewlekły nieżyt gardła i krtani 1 W codziennej praktyce lekarskiej rozróżnia się zapalenie gardła, będące procesem zapalnym, rozwijającym się bez udziału
PRZEWODNIK DLA PACJENTÓW JAK DBAĆ O GARDŁO I KRTAŃ? Przewlekły nieżyt gardła i krtani 1 W codziennej praktyce lekarskiej rozróżnia się zapalenie gardła, będące procesem zapalnym, rozwijającym się bez udziału
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 2312535. (96) Data i numer zgłoszenia patentu europejskiego: 15.10.2009 09450196.
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 2312535 (96) Data i numer zgłoszenia patentu europejskiego: 15.10.2009 09450196.2 (13) (51) T3 Int.Cl. G07B 15/00 (2011.01)
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 2312535 (96) Data i numer zgłoszenia patentu europejskiego: 15.10.2009 09450196.2 (13) (51) T3 Int.Cl. G07B 15/00 (2011.01)
(12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP (96) Data i numer zgłoszenia patentu europejskiego:
 RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 2057877 (96) Data i numer zgłoszenia patentu europejskiego: 03.11.2008 08019246.1 (13) (51) T3 Int.Cl. A01C 23/00 (2006.01)
RZECZPOSPOLITA POLSKA (12) TŁUMACZENIE PATENTU EUROPEJSKIEGO (19) PL (11) PL/EP 2057877 (96) Data i numer zgłoszenia patentu europejskiego: 03.11.2008 08019246.1 (13) (51) T3 Int.Cl. A01C 23/00 (2006.01)
