(materiał w kolorze niebieskim nadobowiązkowy) CHEMIA ORGANICZNA CHEMIA ZWIĄZKÓW PIERWIASTKA WĘGLA
|
|
|
- Jolanta Popławska
- 8 lat temu
- Przeglądów:
Transkrypt
1 1 EMIA RGANIZNA (materiał w kolorze niebieskim nadobowiązkowy) EMIA RGANIZNA EMIA ZWIĄZKÓW PIERWIASTKA WĘGLA WYJĄTKI: TENEK WĘGLA(II) TLENEK WĘGLA (IV) KWAS WĘGLWY + SLE KWASU WĘGLWEG I. WĘGLWDRY WĘGLWDRY: ZWIĄZKI WĘGLA i WDRU I.1. PDZIAŁ: WĘGLWDRY ŁAŃUWE (ALIFATYZNE) NASYNE NIENASYNE YKLIZNE (związki karbocykliczne) ALKANY ALKENY ALKADIENY ALKINY JEDNPIERŚIENIWE WIELPIERŚIENIWE NASYNE NIENASYNE ARMATYZNE SKNDENSWANE YKLALKANY YKLALKENY ARENY
2 2 I.2. WĘGLWDRY ŁAŃUWE NASYNE NIENASYNE ALKANANY ALKENY ALKINY ALKADIENY I.2.1. WĘGLWDRY NASYNE: ALKANY PRSTE RZGAŁĘZINE ALKANY PRSTE: ZWIĄZKI WĘGLA i WDRU WZRZE: n 2n+2 ALKANY: TYLK PJEDYNZE WIĄZANIA PMIĘDZY ATMAMI WĘGLA SZEREG MLGIZNY ALKANÓW Metan 4 4 Etan Propan Butan Pentan eksan eptan ktan Nonan Dekan RDNIK ALKILWY: n 2n+1 - np.: Metyl, Propyl, Butyl
3 3 ALKANY RZGAŁĘZINE: ALKANY PRSTE + PDSTAWNIKI metyloheptan 2. 4,4-dimetyloheptan 3. 4-etylo-6-metyloheptan 4. 6-etylo-4-metylo-heptan WYSTĘPWANIE: GAZ ZIEMNY i RPA NAFTWA GAZ ZIEMNY: metan-~78%, etan-~13%, propan-~6% oraz ~3% wyższych alkanów. RPA NAFTWA: skład: WŁAŚIWŚI: SKŁAD LIZBA ATMÓW WĘLA TEMPERATURA DESTYLAJI, [ o ] Gaz 1-4 poniżej 20 Eter naftowy Lekka nafta Benzyna surowa cykloalkany Nafta areny lej gazowy 12 i wyższe powyżej 275 lej smarowy połączone alkany proste nielotna ciecz z cykloalkanami Asfalt lub koks n. policykloalkany nielotne ciało stałe Fizyczne: gazy, ciecze, ciała stałe, nierozpuszczalne w wodzie. hemiczne: związki mało reaktywne - typowe reakcje : o 1. halogenowanie: alkan + X 2 halogenoalkan + X; X=F 2,l 2, Br 2, I 2 np.: 3 + I 2 = 3 I + I 2. spalanie: n 2n = n 2 + (n+1) 2 + (ciepło spalania) o, kat. 3. kraking (piroliza): alkan 2 + alkany o mniejszej liczbie + alkeny katalizator 4. katalityczny reforming: alkany, cykloalkany areny + 2 ZASTWANIE: PALIWA, SMARY, SYNTEZA RGANIZNA
4 4 I.2.2. WĘGLWDRY NIENASYNE: ALKENY ALKINY ALKADIENY ALKENY: ZWIĄZKI WĘGLA i WDRU WZRZE: n 2n ALKENY: JEDN PDWÓJNE WIĄZANIE MIĘDZY ATMAMI WĘGLA SZEREG MLGIZNY ALKENÓW: Eten = 2 Propen = 2 Buten = 2 Penten = 2 eksen = 2 RDNIK ALKENYLWY: n 2n-1 - np.: Etenyl, 1-Butenyl ALKADIENY: ZWIĄZKI WĘGLA i WDRU WZRZE: n 2n-2 ALKADIENY: DWA PDWÓJNE WIĄZANIA MIĘDZY ATMAMI WĘGLA SZEREG MLGIZNY ALKDIENÓW: SPRZĘŻNY UKŁAD WIĄZAŃ PDWÓJNY 1,3-butadien =-= 2 1,3-pentadien =-= 2 1,3-heksadien =-= 2 1,3-heptadien =-= 2 IZLWANY UKŁAD WIĄZAŃ PDWÓJNY 1,4-pentadien =- 2 -= 2 SKUMULWANY UKŁAD WIĄZAŃ PDWÓJNY 1,2-pentadien == 2
5 5 WYSTĘPWANIE/TRZYMYWANIE ALKENY 1. destylacja ropy naftowej (alkeny do pięciu atomów węgla w cząsteczce) 2. kraking ropy naftowej, np.: ogrzewanie = 2 katalizator 3. reakcje eliminacji (dehydratacja alkoholi, dehydrohalogenacja), np.: kwas = 2 K l 3 2 = 2 ETANL ALKADIENY: np. : 1,3-butadien: 1. kraking: 2. dehydratacja dialkoholi WŁAŚIWŚI: ogrzewanie =-= 2 katalizator ogrzewanie =-- 3 kwas Fizyczne: gazy, ciecze, nierozpuszczalne w odzie, rozpuszczalne w rozpuszczalnikach niepolarnych hemiczne: reakcje addycji (wodoru, wody, halogenu, halogenowodoru): 3 = 2 Br 2 w l 4 3 Br 2 Br substytucji (podstawienia) 3 = 2 l o faza gazowa l- 2 = 2 + l polimeryzacji 2, ogrzewanie, ciśnienie n 2 = 2 ( ) n ZASTSWANIE: produkcja detergentów, synteza tworzyw sztucznych
6 6 ALKINY: ZWIĄZKI WĘGLA i WDRU WZRZE: n 2n-2 SZEREG MLGIZNY ALKINÓW Etyn 2 2 Propyn Butyn Pentyn eksyn eptyn ktyn Nonyn Dekyn RDNIK ALKINYLWY: n 2n-3 - np.: ETYNYL, 1-PRPYNYL, 1-BUTYNYL TRZYMYWANIE: ETYN (AETYLEN): 1. Rozkład wodą węgliku wapnia a 2 węgiel kamień wapienny koks a 2000 o 2 a Kontrolowane, częściowe utlenianie metanu: 1500 o INNE ALKINY Np.: Dehydrohalogenacja dihalogenoalkanów: =Br propyn Br Br
7 7 WŁAŚIWŚI: Fizyczne: gazy, ciecze, nierozpuszczalne w wodzie, rozpuszczalne w rozpuszczalnikach o małej polarności hemiczne: reakcje typowe: np.: addycja (halogenów, halogenowodorów, wody, wodoru), 3 + Br 2 3 -= Br Br tworzenie soli (metali grupy 1 i ciężkich u, Ag), np.: (acetylidy) ZASTSWANIE: N 3 ciekły + Na - -Na + 1/2 2 etanid monosodu spawanie synteza organiczna, np.: kwas octowy tworzywa sztuczne, np.: kauczuk
8 8 I.3. WĘGLWDRY YLKLIZNE WĘGLWDRY ALIYKLIZNE I.3. WĘGLWDRY YKLIZNE ALIFATYZNE NASYNE NIENASYNE YKLALKANANY YKLALKENY YKLALKINY YKLALKADIENY I.3.1 YKLALKANY YKLALKANY: YKLIZNE ZWIĄZKI WĘGLA i WDRU WZRZE: n 2n YKLALKANY: TYLK PJEDYNZ WIĄZANIA PMIĘDZY ATMAMI WĘGLA SZEREG MLGIZNY YKLALKANÓW 2 yklopropan yklobutan yklopentan ykloheksan
9 9 WYSTĘPWANIE/TRZYMYWANIE 1. destylacja ropy naftowej 2. hydrogenacja benzenu: Ni, o MPa 3 cyklizacja 2 2 -l Zn, NaI l 2 WŁAŚIWŚI Fizyczne: gazy, ciecze, nierozpuszczalne w wodzie, rozpuszczalne w rozpuszczalnikach niepolarnych hemiczne: analogiczne do alkanów łańcuchowych: 1. reakcje substytucji (podstawiania) halogenowanie l 2 światło 3 5 l + l 2. katalityczny reforming (dehydrogenacja - odwodornienie) ZASTSWANIE: rozpuszczalniki, synteza, np.: areny
10 10 I.3.2. YKLALKENY i YKLALKADIENY YKLALKENY: YKLIZNE ZWIĄZKI WĘGLA i WDRU WZRZE: n 2n-2 YKLALKENY: JEDN PDWÓJNE WIĄZANIA PMIĘDZY ATMAMI WĘGLA SZEREG MLGIZNY YKLALKENÓW yklopropen yklobuten yklopenten ykloheksen YKLALKADIENY: DWA PDWÓJNE WIĄZANIA PMIĘDZY ATMAMI WĘGLA 2 2 1,3-cykloheksadien 6 8 TRZYMYWANIE: YKLIZAJA WŁASNŚI Fizyczne: ciecze, nierozpuszczalne w wodzie hemiczne: analogiczne do alkenów łańcuchowych, np.: reakcje addycji ZASTSWANIE: rozpuszczalniki, synteza organiczna
11 11 I.4. WĘGLWDRY YKLIZNE ARMATYZNE ARENY WĘGLWDRY ARMATYZNE (areny): YKLIZNE ZWIĄZKI WĘGLA i WDRU PSIADAJĄE 4n+2 ZDELKALIZWANY ELEKTNÓW π BENZEN: ARMATYZNY WĘGLWDÓR WZRZE: 6 6 PISYWANY NASTĘPUJĄYM WZRAMI STRUKTURALNYMI: symbol chmury sześciu zdelokalizowanych elektronów ZDELKALIZWANE ELEKTRNY: UKŁAD: PDWÓJNE WIĄZANIE PJEDYNZE WIĄZANIE PDWÓJNE - WIĄZANIE + WĘGLWDÓR YKLIZNY WZÓR STRUKTURALNY BENZENU KEKULE`G: UPRSZZNY WZÓR BENZENU:
12 12 ARENY JENPIERŚIENIWE WIELPIERŚIENIWE SKNDENSWANE LINIW SKNDENSWANE KĄTW BENZEN: WZÓR SUMARYZNY: 6 6 WZÓR STRUKTURALNY: NAFTALEN :WZÓR SUMARYZNY: 10 8 WZÓR STRUKTURALNY: ANTRAEN:WZÓR SUMARYZNY: WZÓR STRUKTURALNY: FENANTREN:WZÓR SUMARYZNY: WZÓR STRUKTURALNY:
13 13 SZEREG MLGIZNY ARENÓW (BENZENU) WZÓR GÓLNY: n 2n-6 BENZEN 6 6 METYLENBENZEN toluen ETYLBENZEN FENYLETYLEN 6 5 -= 2 styren ,2-DIMETYLBENZEN o-ksylen 1,3-DIMETYLBENZEN m-ksylen 1,4-DIMETYLBENZEN p-ksylen
14 14 WYSTĘPWANIE/TRZYMYWANIE 1. SMŁA WĘGLWA - WYDZIELANIE 2 RPA NAFTWA - SYNTEZA: REFRMING, YKLIZAJA SMŁA WĘGLWA: PRDUKT SUEJ DESTYLAJI WĘGLA KAMIENNEG WĘGIEL KAMIENNY GRZEWANIE BEZ DSTĘPU PWIETRZA SMŁA WĘGLWA kg 55 kg 55 kg smoły węglowej zawiera: benzen naftalen toluen ksyleny fenol krezole 0.90 kg 2.25 kg 0.05 kg 0.05 kg 0.23 kg 0.90 kg WŁASNŚI Fizyczne: ciecze i ciała stałe, nierozpuszczalne w wodzie hemiczne: substytucja w pierścieniu, substytucja w rodniku alkilowym, addycja w rodniku alkenylowym, utlenianie ZASTSWANIE: benzyny wysokooktanowe (50% produkcji benzenu) rozpuszczalniki, chemikalia, leki, synteza organiczna.
15 15 II. PDNE WĘGLWDRÓW WĘGLWDRY Z GRUPAMI FUNKYJNYMI GRUPY FUNKYJNE: PDSTAWNIKI ATM GRUPA ATMÓW JEDNFUNKYJNE PDNE: WĘGLWDÓR + 1 GRUPA FUNKYJNA WIELFUNKYJNE PDNE: WĘGLWDÓR + n GRUP FUNKYJNY GRUPY FUNKYJNE 1.1. takich samych 1.2. różnych ALGENWA - X ; X = fluorowiec: -F, -l, -Br, -I ALKLWA YDRKSYLWA ALDEYDWA - = KETNWA KARBNYLWA KARBKSYLWA = = ETERWA ESTRWA AMINWA -N 2 AMIDWA NITRWA -N 2 SULFNWA
16 16 FLURWPDNE FLURWPDNE: PDNE WĘGLWDRÓW ZAWIERAJĄE ATM (ATMY) FLURWA: -F -l -Br -J -X SZEREG MLGIZNY FLURWPDNY: hlorometan 3 -l Trójchlorometan -l 3 zterochlorometan l 4 Freon l 2 F 2 hloroeten 2 3 -l 2 =-l zterofluoroeten 2 F 4 F 2 =F 2 hloropren 4 5 l 2 =l=- 2 yklobromoheksan Br hlorobenzen l TRZYMYWANIE: alogenowanie: R- + X 2 = R-X + X Wymiana grupy : R- + X R-X + 2 Addycja halogenowodorów do alkenów: --=- + X --X- WŁASNŚI: Fizyczne: gazy, ciecze, nierozpuszczalne w wodzie hemiczne- reaktywne ZASTSWANIE: rozpuszczalniki, synteza
17 17 ALKLE ALKLE: PDNE YDRKSYLWE WEGLWDRÓW ALKLE MNYDRKSYLWE PLIYDRKSYLWE ALKLE: WĘGLWDRY W KTÓRY JEDEN LUB KILKA ATMÓW WDRU ZASTĄPIN GUPĄ FUNKYJNĄ YDRKSYLWĄ: SZEREGI MLGIZNE ALKLI: - Metanol (Alkohol metylowy) Etanol (Alkohol etylowy) Alkohol winylowy =- 2-pentyn-1-ol ykloheksanol (Al. cykloheksylowy) 2 2 Fenylometanol (Al. benzylowy) 7 7 Fenol (benzenol) naftalenol (a-naftol) 10 7
18 18 PLIALKLE PLIALKLE: WĘGLWDRY ZAWIERAJĄE WIĘEJ NIŻ JEDNĄ GRUPĘ YDRKSYLWĄ 1,2-pentanadiol glikol etylenowy glicerol gliceryna D-(+)-glukoza hydrochinon WŁASNŚI Fizyczne: ciecze i ciała stałe, rozpuszczalne w wodzie hemiczne: Etery, Estry, Alkoholany, ZASTSWANIE: rozpuszczalniki, chemikalia, leki, synteza organiczna.
19 19 ALDEYDY ALDEYDY: WĘGLWDRY W KTÓRY JEDEN LUB KILKA ATMÓW WDRU ZASTĄPIN GRUPĄ FUNKYJNĄ ALDEYDWĄ: = ALDEYDY MNALDEYDY DIALDEYDY SZEREGI MLGIZNE ALDEYDÓW: Metanal = (Aldehyd mrówkowy) Etanal 3 = (Acetaldehyd) Butanal = (Aldehyd n-masłowy) Butano di al 2 2 = 2 2 = yklopentanokarboaldehyd 5 9 = Benzaldehyd (Aldehyd benzoesowy) 6 5 = 1,2-Benzenodikarboaldehyd 6 4 () 2 = = 2,3-Naftalenodikarboaldehyd 10 6 () 2 = =
20 20 KETNY KETNY: WĘGLWDRY W KTÓRY ATM WDRU ZASTĄPIN GUPĄ FUNKYJNĄ KARBNYLWĄ (KETNWĄ): = KETNY KETNY ŁAŃUWE KETNY YKLIZNE SZEREGI MLGIZNE KETNÓW: Propanon 2 6 = 3 3 (Aceton) 2-Butanon (keton etylowo-metylowy) yklopentanon 5 8 Acetofenon Benzofenon 12 10
21 21 TRZYMYWANIE 1. Utlenianie alkoholi pierwszorzędowych (ALDEYDY): R 2 alkohol 1 o K2r27 R- aldehyd alkohol n-butylowy K2r27, 2S aldehyd masłowy 2. Utlenianie alkoholi drugorzędowych (KETNY): R()R` alkohol 2 o K2r27 R--R` keton WŁASNŚI Fizyczne: ciecze, ciała stałe, rozpuszczalne w wodzie i rozpuszczalnikach hemiczne: reaktywne chemicznie, reakcje: UTLENIANIA: Do kwasów Aldehydy: do odpowiednich kwasów: R, Ar KMn4 R, Ar Ketony: trudniej do mieszaniny kwasów o krótszych łańcuchach REDUKJI: Do alkoholi i do odpowiednich węglowodorów: -, = 2 + Pt =- ADDYJI : Alkoholi: tworzenie acetali, pochodnych amoniaku ZASTSWANIE: rozpuszczalniki, chemikalia, synteza organiczna.
22 22 ETERY ETERY: ZWIĄZKI RGANIZNE PISYWANE WZRAMI GÓLNYMI: (Ar) R R (Ar) R R Ar R Ar - Ar ETERY: ZWIĄZKI RGANIZNE ZAWIERAJAE ATM TLENU PŁĄZNY Z DWMA ATMAMI WĘGLA NAJWAŻNIEJSZE ETERY: ETER DIETYLWY ETER METYLW-WINYLWY METKSYETYLEN ETER DIFENYLWY ETER ETYLW-FENYLWY KSIRAN TLENEK ETYLENU PIERŚIEŃ KSIRANWY (PIERŚIEŃ EPKSYDWY)
23 23 TRZYMYWANIE: 1. DEYDRATAJA (DWDNIENIE) ALKLI W BENŚI 2 S 4, np.: (ETER SYMETRYZNE) 2 S ALKL ETYLWY + ALKL ETYLWY = ETER DIETYLWY 2. SYNTEZA WILLIAMSNA WŁASNŚI Fizyczne: gazy i ciecze rozpuszczalne w wodzie hemiczne: słabo reaktywne, utlenianie do nadtlenków (niebezpieczne), rozszczepianie przez kwasy ZASTSWANIE: synteza organiczna.
24 24 KWASY KWASY: ZWIĄZKI RGANIZNE W KTÓRY JEDEN LUB KILKA ATMÓW WDRU ZSTAŁY ZATĄPINE GRUPĄ KARBKSYLWĄ SZEREG MLGIZNY KWASÓW: Kwas metanowy (mrówkowy) Kwas etanowy (octowy) Kwas butanowy (masłowy)` Kwas oktadekanowy (stearynowy) Kwas propenowy (akrylowy) Kwas 2-metylopropenowy (metakrylowy) Kwas propynowy Kwas benzenokarboksylowy (benzoesowy) Kwas 2naftalenokarboksylowy (b-naftoesowy)
25 25 KWASY DIKARBKSYLWE Kwas etanodiowy (szczawiowy) Kwas hesanodiowy (adypinowy) ( 2 ) 4 Kwas 1,4-benzenodikarboksylowy (teraftalowy YDRKSYKWASY YDRKSYKWASY: KWASY W KTÓRY ATM (ATMY) WDRU PDSTAWIN GRUPĄ YDRKSYLWĄ Kwas hydroksyetanowy (glikolowy) 2 Kwas 2-hydroksypropanowy (mlekowy) 3 2 Kwas 2,3-dihydroksypropanowy (glicerynowy) 2 Kwas o-hydroksybenzoesowy (salicylowy)
26 26 TRZYMYWANIE: 1. Utlenianie alkoholi pierwszorzędowych: R- 2 KMn4 R- 2. Utlenianie alkilowych pochodnych benzenu: Ar-R Ar- 2 KMn4 KMn4 Ar- Ar- 3. Utlenianie aldehydów i ketonów. WŁASNŚI Fizyczne: ciecze i ciała stałe rozpuszczalne w wodzie, eterach, alkoholach, charakterystyczny zapach hemiczne: charakter kwasowy, reaktywne REAKJE: Z METALAMI: SLE Zn ( 3 ) 2 Zn + 2 octan cynku ( 2 ) 4 + 2K K +- ( 2 ) 4 -+ K adypinian dipotasu REDUKJA D ALKLI R- LiAl4 R- 2 Z ALKLAMI: ESTRY Z AMINAMI: AMIDY ZASTSWANIE: synteza organiczna, przemysł spożywczy (kwas octowy, benzoesowy), przemysł chemiczny -rozpuszczalniki
27 27 ESTRY ESTRY: ZWIĄZKI RGANIZNE ZAWIERAJAE GRUPĘ FUNKYJNĄ: -- ESTRY 2 KWASÓW MNKARBKSYLWY DIKARBKSYLWY PRZYKŁADY: ctan etylu Benzoesan butylu Ftalan dibutylu 4 9 Wodoroftalan butylu TRZYMYWANIE REAKJA ESTRYFIKAJI: kwas + alkohol = ESTER + WDA REAKJA:KNDNENSAJA 2 S = 2-2 WŁASNŚI Fizyczne: ciecze rozpuszczalne w wodzie, charakterystyczne zapachy hemiczne: hydroliza ZASTSWANIE: kosmetyki, chemia spożywcza.
28 28 AMIDY AMIDY: ZWIĄZKI RGANIZNE ZAWIERAJAE GRUPĘ FUNKYJNĄ: -N 2 - N 2 AMIDY KWASÓW MNKARBKSYLWY DIKARBKSYLWY PRZYKŁADY: Formamid N 2 Acetamid 3 N 2 N 2 Benzamid TRZYMYWANIE REAKJA : amoniak + bezwodnik kwasu karboksylowego = AMID + WDA REAKJA KNDENSAJI + N 3 = N 2-2 WŁASNŚI Fizyczne: ciecze i ciała stałe, bez zapachu hemiczne: hydroliza ZASTSWANIE: synteza chemiczna.
29 29 AMINY AMINY: PDNE AMNIAKU, W KTÓRYM JEDEN, DWA LUB TRZY ATMY WDRU ZSTAŁY ZASTĄPINE ALKILEM LU ARYLEM AMINY PIERWSZRZĘDWE: WĘGLWDRY, W KTÓRY ATM WDRU ZSTAŁ ZASTĄPINY GRUPĄ AMINWĄ: N 2 N AMINY MNAMINY PLIAMINY SZEREGI MLGIZNE AMIN: Metyloamina 3 N 2 Propyloamina N 2 ykklopentyloamina N 2 Anilina N 2 1-Naftyloamina N 2 eksametylenodiamina 2 N-( 2 ) 6 -N 2 TRZYMYWANIE REAKJA AMNIAKU Z LRPDNYMI WĘGLWDRÓW WŁASNŚI Fizyczne: gazy i ciecze, rozpuszczalne w wodzie, przykry zapach, trujące hemiczne: reaktywne (tworzą sole, utleniają się) ZASTSWANIE: synteza chemiczna, barwniki.
30 30 AMINKWASY AMINKWASY: KWASY RGANIZNE, W KTÓRY JEDEN LUB WIĘEJ WDRÓW ZSTAŁ PDSTAWINY GRUPĄ AMINWĄ AMINKWASY: ZWIĄZKI ZAWIERAJĄE GRUPY FUNKYJNE: AMINWĄ i KARBKSYLWĄ: UWAGA: SKŁADNIKAMI BIAŁEK SĄ AMINKWASY, W KTÓRY GRUPY AMINWA i KARBKSYLWA ZNAJDUJĄ SIĘ PRZY JEDNYM WĘGLU: N 2 PRZYKŁADY: Kwas 6-aminomasłowy 2 N Kwas 3-aminoheptanowy 3 2 N 2 Kwas 2-amino-etanowy (aminokwas glicyna) Kwas 2-aminopropanowy (aminokwas alanina) 2 N N 2 REAKJE KNDENSAJI Kwas dikarbolsylowy (adypinowy) + diamina (heksametylenoamina) = amid + woda ( 2 ) 4 + ( 2 ) 6 = N N 2 ( 2 ) 4 N ( 2 ) 6 N 2 Dwa aminokwasy = peptyd + woda + N = N 2 N 2 N + 2
Elementy chemii organicznej
 Elementy chemii organicznej węglowodory alifatyczne węglowodory aromatyczne halogenopochodne węglowodorów alkohole etery aldehydy i ketony kwasy karboksylowe estry aminy Alkany C n H 2n+2 struktura Kekulégo
Elementy chemii organicznej węglowodory alifatyczne węglowodory aromatyczne halogenopochodne węglowodorów alkohole etery aldehydy i ketony kwasy karboksylowe estry aminy Alkany C n H 2n+2 struktura Kekulégo
Węgiel i jego związki z wodorem
 Węgiel i jego związki z wodorem 1. Związki organiczne i nieorganiczne są to związki chemiczne, które w swoich cząsteczkach zawierają atomy węgla są to związki chemiczne, które w swoich cząsteczkach nie
Węgiel i jego związki z wodorem 1. Związki organiczne i nieorganiczne są to związki chemiczne, które w swoich cząsteczkach zawierają atomy węgla są to związki chemiczne, które w swoich cząsteczkach nie
Wymagania edukacyjne na poszczególne oceny
 Wymagania edukacyjne na poszczególne oceny VII. Węgiel i jego związki z wodorem podaje kryteria podziału chemii na organiczną i nieorganiczną określa, czym zajmuje się chemia organiczna definiuje pojęcie
Wymagania edukacyjne na poszczególne oceny VII. Węgiel i jego związki z wodorem podaje kryteria podziału chemii na organiczną i nieorganiczną określa, czym zajmuje się chemia organiczna definiuje pojęcie
CHEMIA ORGANICZA - węglowodory. Podział węglowodorów
 EMIA ORGANIZA - węglowodory Podział węglowodorów Najprostsze związki organiczne Alkany są to węglowodory nasycone, w których występują tylko pojedyncze wiązania węgiel węgiel Wszystkie nazwy alkanów charakteryzuje
EMIA ORGANIZA - węglowodory Podział węglowodorów Najprostsze związki organiczne Alkany są to węglowodory nasycone, w których występują tylko pojedyncze wiązania węgiel węgiel Wszystkie nazwy alkanów charakteryzuje
Aleksander Kołodziejczyk Krystyna Dzierzbicka CHEMII. organicznej Tom 1
 Aleksander Kołodziejczyk Krystyna Dzierzbicka CHEMII organicznej Tom 1 Gdansk 2014 PRZEWODNICZĄCY KOMITETU REDAKCYJNEGO WYDAWNICTWA POLITECHNIKI GDAŃSKIEJ Janusz T. Cieśliński RECENZENT Elżbieta Luboch
Aleksander Kołodziejczyk Krystyna Dzierzbicka CHEMII organicznej Tom 1 Gdansk 2014 PRZEWODNICZĄCY KOMITETU REDAKCYJNEGO WYDAWNICTWA POLITECHNIKI GDAŃSKIEJ Janusz T. Cieśliński RECENZENT Elżbieta Luboch
FESTIWAL NAUKI PYTANIA Z CHEMII ORGANICZNEJ
 FESTIWAL NAUKI PYTANIA Z CHEMII ORGANICZNEJ Agata Ołownia-Sarna 1. Chemia organiczna to chemia związków: a) Węgla, b) Tlenu, c) Azotu. 2. Do związków organicznych zaliczamy: a) Metan, b) Kwas węglowy,
FESTIWAL NAUKI PYTANIA Z CHEMII ORGANICZNEJ Agata Ołownia-Sarna 1. Chemia organiczna to chemia związków: a) Węgla, b) Tlenu, c) Azotu. 2. Do związków organicznych zaliczamy: a) Metan, b) Kwas węglowy,
KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW
 KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW WOJEWÓDZTWO WIELKOPOLSKIE Etap wojewódzki rok szkolny 2009/2010 Dane dotyczące ucznia (wypełnia Komisja Konkursowa po rozkodowaniu prac) wylosowany numer uczestnika
KONKURS CHEMICZNY DLA UCZNIÓW GIMNAZJÓW WOJEWÓDZTWO WIELKOPOLSKIE Etap wojewódzki rok szkolny 2009/2010 Dane dotyczące ucznia (wypełnia Komisja Konkursowa po rozkodowaniu prac) wylosowany numer uczestnika
Kierunki chemicznejprzeróbki frakcji ropy naftowej. Destylacja ropy naftowej. Proces oligomeryzacji. Proces alkilowania. Proces oligomeryzacji
 Destylacja ropy naftowej Kierunki chemicznejprzeróbki frakcji ropy naftowej frakcja proces Gazowe Benzyna lekka Benzyna cięŝka Nafta napędowy mazut lekki średni gudron cięŝki izomeryzacja Reformowanie
Destylacja ropy naftowej Kierunki chemicznejprzeróbki frakcji ropy naftowej frakcja proces Gazowe Benzyna lekka Benzyna cięŝka Nafta napędowy mazut lekki średni gudron cięŝki izomeryzacja Reformowanie
WYMAGANIA EDUKACYJNE w klasie III
 WYMAGANIA EDUKACYJNE w klasie III Nr lekcji Temat lekcji Treści nauczania (pismem pogrubionym zostały zaznaczone treści Podstawy Programowej) Węgiel i jego związki z wodorem Wymagania i kryteria ocen Uczeń:
WYMAGANIA EDUKACYJNE w klasie III Nr lekcji Temat lekcji Treści nauczania (pismem pogrubionym zostały zaznaczone treści Podstawy Programowej) Węgiel i jego związki z wodorem Wymagania i kryteria ocen Uczeń:
Spis treści 1. Struktura elektronowa związków organicznych 2. Budowa przestrzenna cząsteczek związków organicznych
 Spis treści 1. Struktura elektronowa związków organicznych 13 2. Budowa przestrzenna cząsteczek związków organicznych 19 2.1. Zadania... 28 3. Zastosowanie metod spektroskopowych do ustalania struktury
Spis treści 1. Struktura elektronowa związków organicznych 13 2. Budowa przestrzenna cząsteczek związków organicznych 19 2.1. Zadania... 28 3. Zastosowanie metod spektroskopowych do ustalania struktury
Węglowodory. Michał Szewczyk Kl. IV TI
 Węglowodory Michał Szewczyk Kl. IV TI Węglowodory nasycone (Alkany) Węglowodory nasycone (Alkany)- to związki węgla z wodorem, w których pomiędzy atomami węgla występują tylko pojedyncze wiązania. Wzór
Węglowodory Michał Szewczyk Kl. IV TI Węglowodory nasycone (Alkany) Węglowodory nasycone (Alkany)- to związki węgla z wodorem, w których pomiędzy atomami węgla występują tylko pojedyncze wiązania. Wzór
Wymagania na poszczególne oceny z chemii w klasie III VII. Węgiel i jego związki z wodorem
 Wymagania na poszczególne oceny z chemii w klasie III VII. Węgiel i jego związki z wodorem 1 Uczeń: wyjaśnia, czym zajmuje się chemiaorganiczna (2) definiuje pojęcie węglowodory (2) wymienia naturalne
Wymagania na poszczególne oceny z chemii w klasie III VII. Węgiel i jego związki z wodorem 1 Uczeń: wyjaśnia, czym zajmuje się chemiaorganiczna (2) definiuje pojęcie węglowodory (2) wymienia naturalne
Wymagania edukacyjne chemia klasa 3 gimnazjum. Węgiel i jego związki z wodorem. Wymagania edukacyjne. Tytuł rozdziału w podręczniku
 1 Wymagania edukacyjne chemia klasa 3 gimnazjum Tytuł rozdziału w podręczniku Temat lekcji Treści nauczania podstawowe (P) Wymagania edukacyjne ponadpodstawowe (PP) Węgiel i jego związki z wodorem 1. Poznajemy
1 Wymagania edukacyjne chemia klasa 3 gimnazjum Tytuł rozdziału w podręczniku Temat lekcji Treści nauczania podstawowe (P) Wymagania edukacyjne ponadpodstawowe (PP) Węgiel i jego związki z wodorem 1. Poznajemy
I. Węgiel i jego związki z wodorem
 NaCoBeZU z chemii dla klasy 3 I. Węgiel i jego związki z wodorem 1. Poznajemy naturalne źródła węglowodorów wymieniam kryteria podziału chemii na organiczną i nieorganiczną wyjaśniam, czym zajmuje się
NaCoBeZU z chemii dla klasy 3 I. Węgiel i jego związki z wodorem 1. Poznajemy naturalne źródła węglowodorów wymieniam kryteria podziału chemii na organiczną i nieorganiczną wyjaśniam, czym zajmuje się
Oznaczanie właściwości tłuszczów
 znaczanie właściwości tłuszczów Prowadzący: mgr inż. Maciej Chrubasik Wstęp teoretyczny Lipidy Lipidy ( tłuszcze ) są estrami kwasów tłuszczowych : - gdy alkoholem jest gliceryna ( 1,2,3-trihydroksy propan;
znaczanie właściwości tłuszczów Prowadzący: mgr inż. Maciej Chrubasik Wstęp teoretyczny Lipidy Lipidy ( tłuszcze ) są estrami kwasów tłuszczowych : - gdy alkoholem jest gliceryna ( 1,2,3-trihydroksy propan;
CHEMIA ORGANICZNA. dr hab. Włodzimierz Gałęzowski Wydział Chemii UAM (61)
 EMIA ORGANIZNA dr hab. Włodzimierz Gałęzowski Wydział hemii UAM (61) 829 1477 wlodgal@amu.edu.pl Materiał wymagany na egzaminie: wykłady ćwiczenia szkoła średnia http://staff.amu.edu.pl/~wlodgal Podręczniki
EMIA ORGANIZNA dr hab. Włodzimierz Gałęzowski Wydział hemii UAM (61) 829 1477 wlodgal@amu.edu.pl Materiał wymagany na egzaminie: wykłady ćwiczenia szkoła średnia http://staff.amu.edu.pl/~wlodgal Podręczniki
KLASA TRZECIA. Węgiel i jego związki z wodorem 1. Poznajemy naturalne źródła węglowodorów. Wymagania edukacyjne. Tytuł rozdziału w podręczniku
 1 KLASA TRZECIA Tytuł rozdziału w podręczniku Temat lekcji Treści nauczania Wymagania edukacyjne podstawowe (P) ponadpodstawowe (PP) Węgiel i jego związki z wodorem 1. Poznajemy naturalne źródła 2.1. Szereg
1 KLASA TRZECIA Tytuł rozdziału w podręczniku Temat lekcji Treści nauczania Wymagania edukacyjne podstawowe (P) ponadpodstawowe (PP) Węgiel i jego związki z wodorem 1. Poznajemy naturalne źródła 2.1. Szereg
Plan wynikowy i wymagania edukacyjne w klasie 3 gimnazjum. Węgiel i jego związki z wodorem. Wymagania edukacyjne. Tytuł rozdziału w podręczniku
 1 Plan wynikowy i wymagania edukacyjne w klasie 3 gimnazjum Tytuł rozdziału w podręczniku Temat lekcji Treści nauczania podstawowe (P) Wymagania edukacyjne ponadpodstawowe (PP) Węgiel i jego związki z
1 Plan wynikowy i wymagania edukacyjne w klasie 3 gimnazjum Tytuł rozdziału w podręczniku Temat lekcji Treści nauczania podstawowe (P) Wymagania edukacyjne ponadpodstawowe (PP) Węgiel i jego związki z
Zaznacz odpowiedê, w której do ka dej substancji przyporzàdkowano êródło jej pochodzenia. F. potrójne H. odbarwiajà jà
 Grupaa W giel i jego zwiàzki z wodorem I Naturalne êródła w glowodorów to: 1 p. I. gaz ziemny II. w gle kopalne np. w giel kamienny III. ropa naftowa. Zaznacz odpowiedê w której do ka dej substancji przyporzàdkowano
Grupaa W giel i jego zwiàzki z wodorem I Naturalne êródła w glowodorów to: 1 p. I. gaz ziemny II. w gle kopalne np. w giel kamienny III. ropa naftowa. Zaznacz odpowiedê w której do ka dej substancji przyporzàdkowano
Spis treści 1. WOJEWÓDZTWO PODKARPACKIE - DANE ZA ROK 2001 2 2. WOJEWÓDZTWO PODKARPACKIE - DANE ZA ROK 2002 7
 Spis treści 1. WOJEWÓDZTWO PODKARPACKIE - DANE ZA ROK 2001 2 2. WOJEWÓDZTWO PODKARPACKIE - DANE ZA ROK 2002 7 3. WOJEWÓDZTWO PODKARPACKIE - DANE ZA ROK 2003 13 4. MIELEC - DANE ZA ROK 2001 19 5. MIELEC
Spis treści 1. WOJEWÓDZTWO PODKARPACKIE - DANE ZA ROK 2001 2 2. WOJEWÓDZTWO PODKARPACKIE - DANE ZA ROK 2002 7 3. WOJEWÓDZTWO PODKARPACKIE - DANE ZA ROK 2003 13 4. MIELEC - DANE ZA ROK 2001 19 5. MIELEC
Plan wynikowy z chemii do klasy III gimnazjum w roku szkolnym 2017/2018. Liczba godzin tygodniowo: 1.
 1 Plan wynikowy z chemii do klasy III gimnazjum w roku szkolnym 2017/2018. Liczba godzin tygodniowo: 1. Tytuł rozdziału w podręczniku Temat lekcji podstawowe Węgiel i jego związki z wodorem 1.Omówienie
1 Plan wynikowy z chemii do klasy III gimnazjum w roku szkolnym 2017/2018. Liczba godzin tygodniowo: 1. Tytuł rozdziału w podręczniku Temat lekcji podstawowe Węgiel i jego związki z wodorem 1.Omówienie
PODSTAWY OBLICZEŃ CHEMICZNYCH DLA MECHANIKÓW
 PODSTAWY OBLICZEŃ CHEMICZNYCH DLA MECHANIKÓW Opracowanie: dr inż. Krystyna Moskwa, dr Wojciech Solarski 1. Termochemia. Każda reakcja chemiczna związana jest z wydzieleniem lub pochłonięciem energii, najczęściej
PODSTAWY OBLICZEŃ CHEMICZNYCH DLA MECHANIKÓW Opracowanie: dr inż. Krystyna Moskwa, dr Wojciech Solarski 1. Termochemia. Każda reakcja chemiczna związana jest z wydzieleniem lub pochłonięciem energii, najczęściej
NIEBEZPIECZNE REAKCJE CHEMICZNE
 NIBPICN RAKCJ CHMICN Niniejsze zestawienie stanowi jedynie wybór i obejmuje jedynie niektóre reakcje niebezpieczne. Wymienione związki mogą ulegać również innym reakcjom niebezpiecznym. Brak na niniejszej
NIBPICN RAKCJ CHMICN Niniejsze zestawienie stanowi jedynie wybór i obejmuje jedynie niektóre reakcje niebezpieczne. Wymienione związki mogą ulegać również innym reakcjom niebezpiecznym. Brak na niniejszej
Wytrzymałość chemiczna krat z tworzywa
 Wytrzymałość chemiczna krat z tworzywa 2 A Aceton 25 50 częściowo odporne odporne odporne Aceton 100 każda nieodporne nieodporne nieodporne Aldehyd mrówkowy 44 45 nieodporne częściowo odporne odporne Aldehyd
Wytrzymałość chemiczna krat z tworzywa 2 A Aceton 25 50 częściowo odporne odporne odporne Aceton 100 każda nieodporne nieodporne nieodporne Aldehyd mrówkowy 44 45 nieodporne częściowo odporne odporne Aldehyd
Cząsteczki wieloatomowe - hybrydyzacja. Czy w oparciu o koncepcję orbitali molekularnych można wytłumaczyć budowę cząsteczek?
 ząsteczki wieloatomowe - hybrydyzacja zy w oparciu o koncepcję orbitali molekularnych można wytłumaczyć budowę cząsteczek? Koncepcja OA OA O zdelokalizowane OA hyb OA O zlokalizowane OA hyb OA hyb OA orbitale
ząsteczki wieloatomowe - hybrydyzacja zy w oparciu o koncepcję orbitali molekularnych można wytłumaczyć budowę cząsteczek? Koncepcja OA OA O zdelokalizowane OA hyb OA O zlokalizowane OA hyb OA hyb OA orbitale
Skala ocen: ndst 0 20, dst , dst , db , db , bdb Informacja:
 Kolokwium III Autorzy: A. Berlicka, E. Dudziak Imię i nazwisko Kierunek studiów azwisko prowadzącego Data Wersja B czas: 60 minut Skala ocen: ndst 0 20, dst 20.5 24, dst 24.5 28, db 28.5 32, db 32.5 36,
Kolokwium III Autorzy: A. Berlicka, E. Dudziak Imię i nazwisko Kierunek studiów azwisko prowadzącego Data Wersja B czas: 60 minut Skala ocen: ndst 0 20, dst 20.5 24, dst 24.5 28, db 28.5 32, db 32.5 36,
Odporność chemiczna. Chemikalia 20 C 50 C Aceton 100% - - Żywica poliestrowa
 Aceton 100% - - kwas adypinowy, wszystkie konc.. + 0 Ałun,wszystkie konc. + 0 Alkohol (butylowy-), 100% + - Alkohol (etylowy), 10% + 0 Alkohol (etylowy), 50% + 0 Alkohol (etylowy), 100% 0 - Alkohol (metylowy),
Aceton 100% - - kwas adypinowy, wszystkie konc.. + 0 Ałun,wszystkie konc. + 0 Alkohol (butylowy-), 100% + - Alkohol (etylowy), 10% + 0 Alkohol (etylowy), 50% + 0 Alkohol (etylowy), 100% 0 - Alkohol (metylowy),
Plan wynikowy z chemii dla klasy II Liceum profilowanego i Technikum III Liceum ogólnokształcącego. 2003/2004 r.
 Plan wynikowy z chemii dla klasy II Liceum profilowanego i Technikum III Liceum ogólnokształcącego. 2003/2004 r. Lp. Temat lekcji 1. Szereg homologiczny alkanów. 2. Izomeria konstytucyjna w alkanach. 3.
Plan wynikowy z chemii dla klasy II Liceum profilowanego i Technikum III Liceum ogólnokształcącego. 2003/2004 r. Lp. Temat lekcji 1. Szereg homologiczny alkanów. 2. Izomeria konstytucyjna w alkanach. 3.
Elementy chemii organicznej
 Elementy chemii organicznej Węglowodory alifatyczne Alkany C n H 2n+2 Alkeny C n H 2n Alkiny C n H 2n-2 Alkany C n H 2n+2 struktura Kekulégo wzór skrócony model Dreidinga metan etan propan butan Nazewnictwo
Elementy chemii organicznej Węglowodory alifatyczne Alkany C n H 2n+2 Alkeny C n H 2n Alkiny C n H 2n-2 Alkany C n H 2n+2 struktura Kekulégo wzór skrócony model Dreidinga metan etan propan butan Nazewnictwo
Cząsteczki wieloatomowe - hybrydyzacja. Czy w oparciu o koncepcję orbitali molekularnych można wytłumaczyć budowę cząsteczek?
 ząsteczki wieloatomowe - hybrydyzacja zy w oparciu o koncepcję orbitali molekularnych można wytłumaczyć budowę cząsteczek? Fakty doświadczalne Wiązanie ząsteczka Długość wiązania [pm] - - 97-2 96-2 2 97-3
ząsteczki wieloatomowe - hybrydyzacja zy w oparciu o koncepcję orbitali molekularnych można wytłumaczyć budowę cząsteczek? Fakty doświadczalne Wiązanie ząsteczka Długość wiązania [pm] - - 97-2 96-2 2 97-3
Plan wynikowy do serii Chemia Nowej Ery - klasa 3
 Plan wynikowy do serii Chemia Nowej Ery - klasa 3 Na podstawie Programu nauczania chemii w gimnazjum autorstwa Teresy Kulawik i Marii Litwin oraz Wymagań programowych na poszczególne oceny przygotowanych
Plan wynikowy do serii Chemia Nowej Ery - klasa 3 Na podstawie Programu nauczania chemii w gimnazjum autorstwa Teresy Kulawik i Marii Litwin oraz Wymagań programowych na poszczególne oceny przygotowanych
Test dla kl. II Związki jednofunkcyjne
 .. imię i nazwisko Test dla kl. II Związki jednofunkcyjne.. klasa. A. Podaj nazwy niżej podanych związków: a) CH 3 -CH 2 -CH 2 -H - b) CH 3 -C-CH 3 - c) CH 3 -CH - d) HCH - e) CH 3 CCH 3-2. Napisz wzory
.. imię i nazwisko Test dla kl. II Związki jednofunkcyjne.. klasa. A. Podaj nazwy niżej podanych związków: a) CH 3 -CH 2 -CH 2 -H - b) CH 3 -C-CH 3 - c) CH 3 -CH - d) HCH - e) CH 3 CCH 3-2. Napisz wzory
Podstawowe pojęcia i prawa chemiczne
 Podstawowe pojęcia i prawa chemiczne Pierwiastki, nazewnictwo i symbole. Budowa atomu, izotopy. Przemiany promieniotwórcze, okres półtrwania. Układ okresowy. Właściwości pierwiastków a ich położenie w
Podstawowe pojęcia i prawa chemiczne Pierwiastki, nazewnictwo i symbole. Budowa atomu, izotopy. Przemiany promieniotwórcze, okres półtrwania. Układ okresowy. Właściwości pierwiastków a ich położenie w
Wyróżnione wymagania programowe odpowiadają wymaganiom ogólnym i szczegółowym zawartym w treściach nauczania podstawy programowej.
 Wymagania programowe na poszczególne oceny (IV etap edukacyjny) przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego
Wymagania programowe na poszczególne oceny (IV etap edukacyjny) przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego
Materiały do zajęć dokształcających z chemii organicznej
 hemia Warta Poznania - nowa JAKOŚĆ studiowania -zwiększenie liczby absolwentów oraz atrakcyjności studiów na kierunku EMIA na Uniwersytecie im. A. Mickiewicza w Poznaniu Materiały do zajęć dokształcających
hemia Warta Poznania - nowa JAKOŚĆ studiowania -zwiększenie liczby absolwentów oraz atrakcyjności studiów na kierunku EMIA na Uniwersytecie im. A. Mickiewicza w Poznaniu Materiały do zajęć dokształcających
Plan pracy dydaktycznej na chemii w klasach trzecich w roku szkolnym 2015/2016
 1 Agnieszka Wróbel nauczyciel biologii i chemii Wrocław,01.09.2015r. Plan pracy dydaktycznej na chemii w klasach trzecich w roku szkolnym 2015/2016 Poziom wymagań Ocena Opis wymagań podstawowe niedostateczna
1 Agnieszka Wróbel nauczyciel biologii i chemii Wrocław,01.09.2015r. Plan pracy dydaktycznej na chemii w klasach trzecich w roku szkolnym 2015/2016 Poziom wymagań Ocena Opis wymagań podstawowe niedostateczna
Wymagania programowe na poszczególne oceny
 Przedmiot: chemia Klasa: IIIa, IIIb Nauczyciel: Agata SROKA Wymagania programowe na poszczególne oceny VII. Węgiel i jego związki z wodorem podaje kryteria podziału chemii na organiczną i nieorganiczną
Przedmiot: chemia Klasa: IIIa, IIIb Nauczyciel: Agata SROKA Wymagania programowe na poszczególne oceny VII. Węgiel i jego związki z wodorem podaje kryteria podziału chemii na organiczną i nieorganiczną
Odporność chemiczna - PVC
 dporność chemiczna - PVC dporność chemiczna nieplastyfikowanego PVC niepodlegającego naprężeniu mechanicznemu na płyny przy 20 C i 60 C L.p Chemikalia lub produkty Stężenie Temperatura 20 C 60 C 1. Aceton
dporność chemiczna - PVC dporność chemiczna nieplastyfikowanego PVC niepodlegającego naprężeniu mechanicznemu na płyny przy 20 C i 60 C L.p Chemikalia lub produkty Stężenie Temperatura 20 C 60 C 1. Aceton
Def. Kwasy karboksylowe to związki, których cząsteczki zawierają jedną lub więcej grup
 Cz. XXV - Kwasy karboksylowe Def. Kwasy karboksylowe to związki, których cząsteczki zawierają jedną lub więcej grup karboksylowych - CH ( - C - H ), atom C w grupie funkcyjnej jest na hybrydyzacji sp 2,
Cz. XXV - Kwasy karboksylowe Def. Kwasy karboksylowe to związki, których cząsteczki zawierają jedną lub więcej grup karboksylowych - CH ( - C - H ), atom C w grupie funkcyjnej jest na hybrydyzacji sp 2,
PLAN WYNIKOWY NAUCZANIA CHEMII W GIMNAZJUM KLASA III
 Publiczne Gimzjum Wadowice Górne PLAN WYNIKOWY NAUCZANIA CHEMII W GIMNAZJUM KLASA III Nowa Podstawa Programowa Graży Bieniek Plan uczania chemii w klasie III NOWA PODSTAWA PROGRAMOWA Plan wynikowy uczania
Publiczne Gimzjum Wadowice Górne PLAN WYNIKOWY NAUCZANIA CHEMII W GIMNAZJUM KLASA III Nowa Podstawa Programowa Graży Bieniek Plan uczania chemii w klasie III NOWA PODSTAWA PROGRAMOWA Plan wynikowy uczania
l. at C Wzór sumaryczny pół strukturalny Nazwa systematyczna Nazwa zwyczajowa 1 HCOOH
 KWASY KARBOKSYLOWE Temat: Szereg homologiczny kwasów karboksylowych 1) Występowanie kwasów karboksylowych 2) Podział kwasów karboksylowych 3) Wzory i nazwy kwasów karboksylowych Ad.1 - kwas octowy - kwas
KWASY KARBOKSYLOWE Temat: Szereg homologiczny kwasów karboksylowych 1) Występowanie kwasów karboksylowych 2) Podział kwasów karboksylowych 3) Wzory i nazwy kwasów karboksylowych Ad.1 - kwas octowy - kwas
11.Chemia organiczna. Irena Zubel Wydział Elektroniki Mikrosystemów i Fotoniki Politechnika Wrocławska (na prawach rękopisu)
 11.Chemia organiczna. Irena Zubel Wydział Elektroniki Mikrosystemów i Fotoniki Politechnika Wrocławska (na prawach rękopisu) Związki organiczne CHEMIA ORGANICZNA Def. 1. (Gmelin 1848, Kekule 1851 ) chemia
11.Chemia organiczna. Irena Zubel Wydział Elektroniki Mikrosystemów i Fotoniki Politechnika Wrocławska (na prawach rękopisu) Związki organiczne CHEMIA ORGANICZNA Def. 1. (Gmelin 1848, Kekule 1851 ) chemia
17. DODATKI Tabela 1. Symbole okre laj ce wielokrotno ci i podwielokrotno ci ułamków dziesi tnych Symbol Okre lenie Wielokrotno Tabela 2.
 17. DDATKI Tabela 1. Symbole określające wielokrotności i podwielokrotności ułamków dziesiętnych Symbol kreślenie Wielokrotność T tera 10 12 G giga 10 9 M mega 10 6 k kilo 10 3 h hekto 10 2 da deka 10
17. DDATKI Tabela 1. Symbole określające wielokrotności i podwielokrotności ułamków dziesiętnych Symbol kreślenie Wielokrotność T tera 10 12 G giga 10 9 M mega 10 6 k kilo 10 3 h hekto 10 2 da deka 10
CHEMIA klasa 3 Wymagania programowe na poszczególne oceny do Programu nauczania chemii w gimnazjum. Chemia Nowej Ery.
 CHEMIA klasa 3 Wymagania programowe na poszczególne oceny do Programu nauczania chemii w gimnazjum. Chemia Nowej Ery. Dział - Węgiel i jego związki. określa, czym zajmuje się chemia organiczna definiuje
CHEMIA klasa 3 Wymagania programowe na poszczególne oceny do Programu nauczania chemii w gimnazjum. Chemia Nowej Ery. Dział - Węgiel i jego związki. określa, czym zajmuje się chemia organiczna definiuje
WYMAGANIA EDUKACYJNE z chemii dla klasy trzeciej
 Lucyna Krupa Rok szkolny 2016/2017 Anna Mikrut WYMAGANIA EDUKACYJNE z chemii dla klasy trzeciej Wyróżnia się wymagania na: ocenę dopuszczającą ocenę dostateczną (obejmują wymagania na ocenę dopuszczającą)
Lucyna Krupa Rok szkolny 2016/2017 Anna Mikrut WYMAGANIA EDUKACYJNE z chemii dla klasy trzeciej Wyróżnia się wymagania na: ocenę dopuszczającą ocenę dostateczną (obejmują wymagania na ocenę dopuszczającą)
WYMAGANIA EDUKACYJNE KLASA 3B - CHEMIA 2018/19. Chemia organiczna jako chemia związków węgla
 Jarosław Kuśnierz WYMAGANIA EDUKACYJNE KLASA 3B - CHEMIA 2018/19 Chemia organiczna jako chemia związków węgla Ocena dopuszczająca [1] pojęcie chemii organicznej pierwiastki chemiczne wchodzące w skład
Jarosław Kuśnierz WYMAGANIA EDUKACYJNE KLASA 3B - CHEMIA 2018/19 Chemia organiczna jako chemia związków węgla Ocena dopuszczająca [1] pojęcie chemii organicznej pierwiastki chemiczne wchodzące w skład
Plan wynikowy do serii Chemia Nowej Ery
 1 Plan wynikowy do serii Chemia Nowej Ery Materiał opracowała Anna Remin na podstawie Programu nauczania chemii w gimnazjum autorstwa Teresy Kulawik i Marii Litwin oraz Wymagań programowych na poszczególne
1 Plan wynikowy do serii Chemia Nowej Ery Materiał opracowała Anna Remin na podstawie Programu nauczania chemii w gimnazjum autorstwa Teresy Kulawik i Marii Litwin oraz Wymagań programowych na poszczególne
Wymagania programowe na poszczególne oceny z chemii w klasie III.
 Wymagania programowe na poszczególne oceny z chemii w klasie III. VII. Węgiel i jego związki z wodorem podaje kryteria podziału chemii na organiczną i nieorganiczną określa, czym zajmuje się chemia organiczna
Wymagania programowe na poszczególne oceny z chemii w klasie III. VII. Węgiel i jego związki z wodorem podaje kryteria podziału chemii na organiczną i nieorganiczną określa, czym zajmuje się chemia organiczna
Ocena dobra [ ] Uczeń:
![Ocena dobra [ ] Uczeń: Ocena dobra [ ] Uczeń:](/thumbs/67/57994710.jpg) Chemia - klasa III Wymagania edukacyjne 1.Węglowodory Ocena dopuszczająca [1] definiuje pojęcia: węglowodory, alkany, alkeny, alkiny, szereg homologiczny, grupa alkilowa, reakcje podstawiania (substytucji),
Chemia - klasa III Wymagania edukacyjne 1.Węglowodory Ocena dopuszczająca [1] definiuje pojęcia: węglowodory, alkany, alkeny, alkiny, szereg homologiczny, grupa alkilowa, reakcje podstawiania (substytucji),
Wyróżnione wymagania programowe odpowiadają wymaganiom ogólnym i szczegółowym zawartym w treściach nauczania podstawy programowej.
 Wymagania programowe z chemii na poszczególne oceny. IV etap edukacyjny - przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. Podręcznika dla liceum
Wymagania programowe z chemii na poszczególne oceny. IV etap edukacyjny - przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. Podręcznika dla liceum
Wymagania edukacyjne na poszczególne stopnie szkolne z chemii w klasie III.
 Wymagania edukacyjne na poszczególne stopnie szkolne z chemii w klasie III. Stopień dopuszczający: podaje kryteria podziału chemii na organiczną i nieorganiczną określa, czym zajmuje się chemia organiczna
Wymagania edukacyjne na poszczególne stopnie szkolne z chemii w klasie III. Stopień dopuszczający: podaje kryteria podziału chemii na organiczną i nieorganiczną określa, czym zajmuje się chemia organiczna
Wymagania edukacyjne niezbędne do uzyskania oceny klasyfikacyjnej z chemii klasa trzecia -chemia organiczna
 Wymagania edukacyjne niezbędne do uzyskania oceny klasyfikacyjnej z chemii klasa trzecia -chemia organiczna 1. Chemia organiczna jako chemia związków węgla Ocena dopuszczająca Ocena dostateczna Ocena dobra
Wymagania edukacyjne niezbędne do uzyskania oceny klasyfikacyjnej z chemii klasa trzecia -chemia organiczna 1. Chemia organiczna jako chemia związków węgla Ocena dopuszczająca Ocena dostateczna Ocena dobra
1. Chemia organiczna jako chemia związków węgla. 2. Węglowodory
 Propozycje wymagań programowych na poszczególne oceny przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego
Propozycje wymagań programowych na poszczególne oceny przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego
CHEMIA KLASA Chemia organiczna jako chemia związków węgla. 2. Węglowodory
 CHEMIA KLASA 3 Wymagania programowe na poszczególne oceny przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego
CHEMIA KLASA 3 Wymagania programowe na poszczególne oceny przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego
Wymagania programowe na poszczególne oceny. Klasa 3 I semestr
 Wymagania programowe na poszczególne oceny. Klasa 3 I semestr VII. Węgiel i jego związki z wodorem podaje kryteria podziału chemii na organiczną i nieorganiczną określa, czym zajmuje się chemia organiczna
Wymagania programowe na poszczególne oceny. Klasa 3 I semestr VII. Węgiel i jego związki z wodorem podaje kryteria podziału chemii na organiczną i nieorganiczną określa, czym zajmuje się chemia organiczna
Plan dydaktyczny z chemii klasa: 2TRA 1 godzina tygodniowo- zakres podstawowy. Dział Zakres treści
 Anna Kulaszewicz Plan dydaktyczny z chemii klasa: 2TRA 1 godzina tygodniowo- zakres podstawowy lp. Dział Temat Zakres treści 1 Zapoznanie z przedmiotowym systemem oceniania i wymaganiami edukacyjnymi z
Anna Kulaszewicz Plan dydaktyczny z chemii klasa: 2TRA 1 godzina tygodniowo- zakres podstawowy lp. Dział Temat Zakres treści 1 Zapoznanie z przedmiotowym systemem oceniania i wymaganiami edukacyjnymi z
Wyróżnione wymagania programowe odpowiadają wymaganiom ogólnym i szczegółowym zawartym w treściach nauczania podstawy programowej.
 Propozycje wymagań programowych na poszczególne oceny (IV etap edukacyjny) przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum
Propozycje wymagań programowych na poszczególne oceny (IV etap edukacyjny) przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum
PRZYKŁADOWE ZADANIA KWASY
 PRZYKŁADOWE ZADANIA KWASY Zadanie 1014 (3 pkt) Pr.XII/2004 A2 Określ typ podanych niżej reakcji: I. C 17 H 33 COOH + Br 2 C 17 H 33 Br 2 COOH Al 2O 3, temp II. C 2 H 5 OH C 2 H 4 + H 2 O hγ III. CH 4 +
PRZYKŁADOWE ZADANIA KWASY Zadanie 1014 (3 pkt) Pr.XII/2004 A2 Określ typ podanych niżej reakcji: I. C 17 H 33 COOH + Br 2 C 17 H 33 Br 2 COOH Al 2O 3, temp II. C 2 H 5 OH C 2 H 4 + H 2 O hγ III. CH 4 +
Pochodne węglowodorów, w cząsteczkach których jeden atom H jest zastąpiony grupą hydroksylową (- OH ).
 Cz. XXII - Alkohole monohydroksylowe Pochodne węglowodorów, w cząsteczkach których jeden atom jest zastąpiony grupą hydroksylową (- ). 1. Klasyfikacja alkoholi monohydroksylowych i rodzaje izomerii, rzędowość
Cz. XXII - Alkohole monohydroksylowe Pochodne węglowodorów, w cząsteczkach których jeden atom jest zastąpiony grupą hydroksylową (- ). 1. Klasyfikacja alkoholi monohydroksylowych i rodzaje izomerii, rzędowość
Wymagania programowe na poszczególne oceny CHEMIA klasa III
 Wymagania programowe na poszczególne oceny CHEMIA klasa III I. Węgiel i jego związki z wodorem podaje kryteria podziału chemii na organiczną i nieorganiczną określa, czym zajmuje się chemia organiczna
Wymagania programowe na poszczególne oceny CHEMIA klasa III I. Węgiel i jego związki z wodorem podaje kryteria podziału chemii na organiczną i nieorganiczną określa, czym zajmuje się chemia organiczna
Ocena dobra [ ] Uczeń:
![Ocena dobra [ ] Uczeń: Ocena dobra [ ] Uczeń:](/thumbs/55/35935976.jpg) KLASA III A Wymagania edukacyjne na poszczególne oceny przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego
KLASA III A Wymagania edukacyjne na poszczególne oceny przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego
Wyróżnione wymagania programowe odpowiadają wymaganiom ogólnym i szczegółowym zawartym w treściach nauczania podstawy programowej.
 Wymagania na poszczególne oceny (IV etap edukacyjny) przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego i
Wymagania na poszczególne oceny (IV etap edukacyjny) przygotowane na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego i
WYMAGANIA PROGRAMOWE Z CHEMII DLA KLAS TRZECICH ZAKRES ROZSZERZONY
 WYMAGANIA PROGRAMOWE Z CHEMII DLA KLAS TRZECICH ZAKRES ROZSZERZONY Opracowano na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego
WYMAGANIA PROGRAMOWE Z CHEMII DLA KLAS TRZECICH ZAKRES ROZSZERZONY Opracowano na podstawie treści zawartych w podstawie programowej, programie nauczania oraz w części 2. podręcznika dla liceum ogólnokształcącego
Odporność chemiczna PVC
 Odporność chemiczna PVC Chemikalia lub produkty Stężenie Temperatura 20 o c 60 o c Aceton 100% N Akrylan etylu 100% N N Aldehyd benzoesowy 0.1% N N Aldehyd krotonowy 100% N N Aldehyd octowy 40% N - Aldehyd
Odporność chemiczna PVC Chemikalia lub produkty Stężenie Temperatura 20 o c 60 o c Aceton 100% N Akrylan etylu 100% N N Aldehyd benzoesowy 0.1% N N Aldehyd krotonowy 100% N N Aldehyd octowy 40% N - Aldehyd
CHEMIA KLASA III LICEUM OGÓLNOKSZTAŁCĄCEGO - wymagania edukacyjne. zakres rozszerzony
 CHEMIA KLASA III LICEUM OGÓLNOKSZTAŁCĄCEGO - wymagania edukacyjne. zakres rozszerzony Wymagania na poszczególne oceny zostały sformułowane dla każdego działu. Mają one charakter spiralny, co oznacza, ze
CHEMIA KLASA III LICEUM OGÓLNOKSZTAŁCĄCEGO - wymagania edukacyjne. zakres rozszerzony Wymagania na poszczególne oceny zostały sformułowane dla każdego działu. Mają one charakter spiralny, co oznacza, ze
Tabela Odpornoœci Materia³ów
 ACETON 70 - X X O O O O O O O O O O O O O X X X O X X X O ACETYLEN, (Wybuchowy w kontrakcie z 100 100 O O O O O X X X O O O O O O O X X X O X X X O Cu) ALDEHYD AKRYLOWY Akroleina 100 100 X X L L L X X
ACETON 70 - X X O O O O O O O O O O O O O X X X O X X X O ACETYLEN, (Wybuchowy w kontrakcie z 100 100 O O O O O X X X O O O O O O O X X X O X X X O Cu) ALDEHYD AKRYLOWY Akroleina 100 100 X X L L L X X
Szczegółowe kryteria oceniania z chemii w klasie III (wymagania programowe)
 o VI. Sole Szczegółowe kryteria oceniania z chemii w klasie III (wymagania programowe) opracowane w oparciu o program nauczania chemii w gimnazjum Chemia Nowej Ery opisuje budowę soli wskazuje metal i
o VI. Sole Szczegółowe kryteria oceniania z chemii w klasie III (wymagania programowe) opracowane w oparciu o program nauczania chemii w gimnazjum Chemia Nowej Ery opisuje budowę soli wskazuje metal i
Stopień celujący mogą otrzymać uczniowie, którzy spełniają kryteria na stopień bardzo dobry oraz:
 Wymagania z chemii na poszczególne oceny Klasa 3 gimnazjum Stopień celujący mogą otrzymać uczniowie, którzy spełniają kryteria na stopień bardzo dobry oraz: Potrafią wykryć obecność węgla i wodoru w związkach
Wymagania z chemii na poszczególne oceny Klasa 3 gimnazjum Stopień celujący mogą otrzymać uczniowie, którzy spełniają kryteria na stopień bardzo dobry oraz: Potrafią wykryć obecność węgla i wodoru w związkach
Kuratorium Oświaty w Lublinie
 Kuratorium Oświaty w Lublinie ZESTAW ZADAŃ KONKURSOWYCH Z CHEMII DLA UCZNIÓW GIMNAZJÓW ROK SZKOLNY 2014/2015 KOD UCZNIA ETAP OKRĘGOWY Instrukcja dla ucznia 1. Zestaw konkursowy zawiera 12 zadań. 2. Przed
Kuratorium Oświaty w Lublinie ZESTAW ZADAŃ KONKURSOWYCH Z CHEMII DLA UCZNIÓW GIMNAZJÓW ROK SZKOLNY 2014/2015 KOD UCZNIA ETAP OKRĘGOWY Instrukcja dla ucznia 1. Zestaw konkursowy zawiera 12 zadań. 2. Przed
C OH ALKOHOLE ETERY R OH R O R R' O FENOLE. Ar OH NOMENKLATURA ALKOHOLE ZWIĄZKI ORGANICZNE ZAWIERAJĄCE W STRUKTURZE ATOMY TLENU C O C OH CH 3 OH
 ZWIĄZKI GANIZNE ZAWIEAJĄE W STUKTUZE ATMY TLENU 8 1s2 2s 2 2p 4 okres 2; grupa VI w związkach jest dwuwiążący, z dwoma niewiążącymi parami elektronów drugi w skali elektroujemności Paulinga 3.5 (za fluorem)
ZWIĄZKI GANIZNE ZAWIEAJĄE W STUKTUZE ATMY TLENU 8 1s2 2s 2 2p 4 okres 2; grupa VI w związkach jest dwuwiążący, z dwoma niewiążącymi parami elektronów drugi w skali elektroujemności Paulinga 3.5 (za fluorem)
Wymagania edukacyjne z chemii dla klasy III
 Wymagania edukacyjne z chemii dla klasy III VII. Węgiel i jego związki z wodorem Ocena dopuszczająca [1] podaje kryteria podziału chemii na organiczną i nieorganiczną określa, czym zajmuje się chemia organiczna
Wymagania edukacyjne z chemii dla klasy III VII. Węgiel i jego związki z wodorem Ocena dopuszczająca [1] podaje kryteria podziału chemii na organiczną i nieorganiczną określa, czym zajmuje się chemia organiczna
Węgiel i jego związki z wodorem
 Węgiel i jego związki z wodorem Ocena dopuszczająca [1] podaje kryteria podziału chemii na organiczną i nieorganiczną określa, czym zajmuje się chemia organiczna definiuje pojęcie węglowodory wymienia
Węgiel i jego związki z wodorem Ocena dopuszczająca [1] podaje kryteria podziału chemii na organiczną i nieorganiczną określa, czym zajmuje się chemia organiczna definiuje pojęcie węglowodory wymienia
ODPORNOŚD CHEMICZNA TERMOPLASTÓW
 PMMA PC PU PCV PVDF PTFE PP PE PET POMH POMC PA66 PA6 ODPORNOŚD CHEMICZNA TERMOPLASTÓW Odporny. Niewielkie lub żadne zmiany w masie. Nieznaczny wpływ na właściwości mechaniczne. Częściowo odporny. Wraz
PMMA PC PU PCV PVDF PTFE PP PE PET POMH POMC PA66 PA6 ODPORNOŚD CHEMICZNA TERMOPLASTÓW Odporny. Niewielkie lub żadne zmiany w masie. Nieznaczny wpływ na właściwości mechaniczne. Częściowo odporny. Wraz
CHEMIA - KLASA III VII. Węgiel i jego związki z wodorem I półrocze
 CHEMIA - KLASA III VII. Węgiel i jego związki z wodorem I półrocze Ocena dopuszczająca (1) podaje kryteria podziału chemii na organiczną i nieorganiczną określa, czym zajmuje się chemia organiczna definiuje
CHEMIA - KLASA III VII. Węgiel i jego związki z wodorem I półrocze Ocena dopuszczająca (1) podaje kryteria podziału chemii na organiczną i nieorganiczną określa, czym zajmuje się chemia organiczna definiuje
Wymagania programowe na poszczególne oceny dla uczniów klas III gimnazjum
 CHEMIA: Wymagania programowe na poszczególne oceny dla uczniów klas III gimnazjum VII. Węgiel i jego związki z wodorem podaje kryteria podziału chemii na organiczną i nieorganiczną określa, czym zajmuje
CHEMIA: Wymagania programowe na poszczególne oceny dla uczniów klas III gimnazjum VII. Węgiel i jego związki z wodorem podaje kryteria podziału chemii na organiczną i nieorganiczną określa, czym zajmuje
Wymagania edukacyjne chemia kl. III Gimnazjum Rok szkolny 2015/2016. Sole
 Wymagania edukacyjne chemia kl. III Gimnazjum Rok szkolny 2015/2016 Sole Poziom podstawowy Poziom ponadpodstawowy Dopuszczający (K) Dostateczny (P) Dobry (R) Bardzo dobry (D) Celujący (W) Uczeń : opisuje
Wymagania edukacyjne chemia kl. III Gimnazjum Rok szkolny 2015/2016 Sole Poziom podstawowy Poziom ponadpodstawowy Dopuszczający (K) Dostateczny (P) Dobry (R) Bardzo dobry (D) Celujący (W) Uczeń : opisuje
Program nauczania CHEMIA KLASA 8
 Program nauczania CHEMIA KLASA 8 DZIAŁ VII. Kwasy (12 godzin lekcyjnych) Wzory i nazwy kwasów Kwasy beztlenowe Kwas siarkowy(vi), kwas siarkowy(iv) tlenowe kwasy siarki Przykłady innych kwasów tlenowych
Program nauczania CHEMIA KLASA 8 DZIAŁ VII. Kwasy (12 godzin lekcyjnych) Wzory i nazwy kwasów Kwasy beztlenowe Kwas siarkowy(vi), kwas siarkowy(iv) tlenowe kwasy siarki Przykłady innych kwasów tlenowych
Br Br. Br Br OH 2 OH NH NH 2 2. Zakład Chemii Organicznej: kopiowanie zabronione
 Kolokwium III Autorzy: A. Berlicka, M. Cebrat, E. Dudziak, A. Kluczyk, Imię i nazwisko Kierunek studiów azwisko prowadzącego Data Wersja A czas: 45 minut Skala ocen: ndst 0 20, dst 20.5 24, dst 24.5 28,
Kolokwium III Autorzy: A. Berlicka, M. Cebrat, E. Dudziak, A. Kluczyk, Imię i nazwisko Kierunek studiów azwisko prowadzącego Data Wersja A czas: 45 minut Skala ocen: ndst 0 20, dst 20.5 24, dst 24.5 28,
WYMAGANIA EDUKACYJNE na poszczególne oceny śródroczne i roczne. Z CHEMII W KLASIE III gimnazjum
 WYMAGANIA EDUKACYJNE na poszczególne oceny śródroczne i roczne Z CHEMII W KLASIE III gimnazjum Program nauczania chemii w gimnazjum autorzy: Teresa Kulawik, Maria Litwin Program realizowany przy pomocy
WYMAGANIA EDUKACYJNE na poszczególne oceny śródroczne i roczne Z CHEMII W KLASIE III gimnazjum Program nauczania chemii w gimnazjum autorzy: Teresa Kulawik, Maria Litwin Program realizowany przy pomocy
Ewa Trybel Kompała rok szkolny 2018/2019
 Ewa Trybel Kompała rok szkolny 2018/2019 Szkoła Podstawowa nr 5 klasa 3a, 3b, 3c, 3d w Chorzowie nauczyciel chemii i matematyki Wymagania programowej na poszczególne oceny przygotowana na podstawie treści
Ewa Trybel Kompała rok szkolny 2018/2019 Szkoła Podstawowa nr 5 klasa 3a, 3b, 3c, 3d w Chorzowie nauczyciel chemii i matematyki Wymagania programowej na poszczególne oceny przygotowana na podstawie treści
WYMAGANIA EDUKACYJNE KLASA 3A - CHEMIA rok szkolny2018/19. Węglowodory
 WYMAGANIA EDUKACYJNE KLASA 3A - CHEMIA rok szkolny2018/19 Jarosław Kuśnierz Ocena dopuszczająca [1] definiuje pojęcia: węglowodory, alkany, alkeny, alkiny, szereg homologiczny, grupa alkilowa, reakcje
WYMAGANIA EDUKACYJNE KLASA 3A - CHEMIA rok szkolny2018/19 Jarosław Kuśnierz Ocena dopuszczająca [1] definiuje pojęcia: węglowodory, alkany, alkeny, alkiny, szereg homologiczny, grupa alkilowa, reakcje
WĘGLOWODORY. Uczeń: Przykłady wymagań nadobowiązkowych Uczeń:
 WĘGLOWODORY Wymagania na ocenę dopuszczającą dostateczną dobrą bardzo dobrą pisze wzory sumaryczne, zna nazwy czterech początkowych węglowodorów nasyconych; zna pojęcie: szereg homologiczny; zna ogólny
WĘGLOWODORY Wymagania na ocenę dopuszczającą dostateczną dobrą bardzo dobrą pisze wzory sumaryczne, zna nazwy czterech początkowych węglowodorów nasyconych; zna pojęcie: szereg homologiczny; zna ogólny
Wymagania programowe na poszczególne oceny klasa 3- chemia
 VII. Węgiel i jego związki z wodorem Ocena dopuszczająca [1] podaje kryteria podziału chemii na organiczną i nieorganiczną określa, czym zajmuje się chemia organiczna definiuje pojęcie węglowodory wymienia
VII. Węgiel i jego związki z wodorem Ocena dopuszczająca [1] podaje kryteria podziału chemii na organiczną i nieorganiczną określa, czym zajmuje się chemia organiczna definiuje pojęcie węglowodory wymienia
Wymagania programowe na poszczególne oceny chemia kl. III 2014/2015
 Wymagania programowe na poszczególne oceny chemia kl. III 2014/2015 VI. Sole opisuje budowę soli wskazuje metal i resztę kwasową we wzorze soli zapisuje wzory sumaryczne soli (chlorków, arczków) tworzy
Wymagania programowe na poszczególne oceny chemia kl. III 2014/2015 VI. Sole opisuje budowę soli wskazuje metal i resztę kwasową we wzorze soli zapisuje wzory sumaryczne soli (chlorków, arczków) tworzy
Grupa karbonylowa. Grupa karbonylowa to grupa funkcyjna, w której atom tlenu połączony jest z atomem węgla podwójnym wiązaniem
 ALDEHYDY I KETNY Spis treści Grupa karbonylowa Aldehydy i ketony Aldehydy Nazewnictwo trzymywanie Właściwości chemiczne Aldehydy nienasycone Aldehydy aromatyczne Ketony Nazewnictwo trzymywanie Właściwości
ALDEHYDY I KETNY Spis treści Grupa karbonylowa Aldehydy i ketony Aldehydy Nazewnictwo trzymywanie Właściwości chemiczne Aldehydy nienasycone Aldehydy aromatyczne Ketony Nazewnictwo trzymywanie Właściwości
Wymagania edukacyjne niezbędne do uzyskania poszczególnych śródrocznych i rocznych ocen klasyfikacyjnych CHEMIA klasa III Oceny śródroczne:
 Wymagania edukacyjne niezbędne do uzyskania poszczególnych śródrocznych i rocznych ocen klasyfikacyjnych CHEMIA klasa III Oceny śródroczne: Ocenę dopuszczającą otrzymuje uczeń, który: -określa, co to są
Wymagania edukacyjne niezbędne do uzyskania poszczególnych śródrocznych i rocznych ocen klasyfikacyjnych CHEMIA klasa III Oceny śródroczne: Ocenę dopuszczającą otrzymuje uczeń, który: -określa, co to są
Rozdział 6. Odpowiedzi i rozwiązania zadań. Chemia organiczna. Zdzisław Głowacki. Zakres podstawowy i rozszerzony
 Zdzisław Głowacki Chemia organiczna Zakres podstawowy i rozszerzony 2b Odpowiedzi i rozwiązania zadań Rozdział 6 Oficyna Wydawnicza TUTOR Wydanie I. Toruń 2013 r. Podpowiedzi Aldehydy i ketony Zadanie
Zdzisław Głowacki Chemia organiczna Zakres podstawowy i rozszerzony 2b Odpowiedzi i rozwiązania zadań Rozdział 6 Oficyna Wydawnicza TUTOR Wydanie I. Toruń 2013 r. Podpowiedzi Aldehydy i ketony Zadanie
WYMAGANIA EDUKACYJNE NA POSZCZEGÓLNE OCENY DLA KLASY III LO To jest chemia 2. Chemia organiczna, zakres rozszerzony.
 WYMAGANIA EDUKACYJNE NA POSZCZEGÓLNE OCENY DLA KLASY III LO To jest chemia 2. Chemia organiczna, zakres rozszerzony. Wyróżnione wymagania programowe odpowiadają wymaganiom ogólnym i szczegółowym zawartym
WYMAGANIA EDUKACYJNE NA POSZCZEGÓLNE OCENY DLA KLASY III LO To jest chemia 2. Chemia organiczna, zakres rozszerzony. Wyróżnione wymagania programowe odpowiadają wymaganiom ogólnym i szczegółowym zawartym
Konspekt wykładu Chemia Organiczna dla studentów Wydziału Inżynierii Chemicznej i Procesowej
 Konspekt wykładu hemia Organiczna dla studentów Wydziału Inżynierii hemicznej i Procesowej ALKANY 2 godz. 1. Wzór sumaryczny: n 2n+2 (n = liczba naturalna) - węglowodory posiadające tylko wiązania pojedyncze
Konspekt wykładu hemia Organiczna dla studentów Wydziału Inżynierii hemicznej i Procesowej ALKANY 2 godz. 1. Wzór sumaryczny: n 2n+2 (n = liczba naturalna) - węglowodory posiadające tylko wiązania pojedyncze
Wymagania programowe na poszczególne oceny
 Wymagania programowe na poszczególne oceny VII. Węgiel i jego związki z wodorem Ocena dopuszczająca Ocena dostateczna Ocena dobra Ocena bardzo dobra [1] [1 + 2] [1 + 2 + 3] [1 + 2 + 3 + 4] podaje kryteria
Wymagania programowe na poszczególne oceny VII. Węgiel i jego związki z wodorem Ocena dopuszczająca Ocena dostateczna Ocena dobra Ocena bardzo dobra [1] [1 + 2] [1 + 2 + 3] [1 + 2 + 3 + 4] podaje kryteria
Węglowodory nienasycone
 AUTORZY SKRYPTU Szymon Michalski OPIEKUN MERYTORYCZNY mgr Adam Makówka Węglowodory nienasycone Alkeny Spis treści: 1.Określenie i wzór ogólny alkenów 2.Szereg homologiczny alkenów 3.Nazewnictwo alkenów
AUTORZY SKRYPTU Szymon Michalski OPIEKUN MERYTORYCZNY mgr Adam Makówka Węglowodory nienasycone Alkeny Spis treści: 1.Określenie i wzór ogólny alkenów 2.Szereg homologiczny alkenów 3.Nazewnictwo alkenów
VII. Węgiel i jego związki z wodorem
 Ocena dopuszczająca podaje kryteria podziału chemii na organiczną i nieorganiczną określa, czym zajmuje się chemia organiczna definiuje pojęcie węglowodory wymienia naturalne źródła stosuje zasady BHP
Ocena dopuszczająca podaje kryteria podziału chemii na organiczną i nieorganiczną określa, czym zajmuje się chemia organiczna definiuje pojęcie węglowodory wymienia naturalne źródła stosuje zasady BHP
WYMAGANIA EDUKACYJNE Z CHEMII. klasa III G. rok szkolny 2017/2018. zgodne z podstawą programową z dnia 27 sierpnia 2012r.
 WYMAGANIA EDUKACYJNE Z CHEMII klasa III G rok szkolny 2017/2018 zgodne z podstawą programową z dnia 27 sierpnia 2012r. I. Węgiel i jego związki z wodorem Ocena dopuszczająca [1] Ocena dostateczna [1 +
WYMAGANIA EDUKACYJNE Z CHEMII klasa III G rok szkolny 2017/2018 zgodne z podstawą programową z dnia 27 sierpnia 2012r. I. Węgiel i jego związki z wodorem Ocena dopuszczająca [1] Ocena dostateczna [1 +
Podział związków organicznych
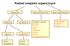 Podział związków organicznych węglowodory związki jednofunkcyjne związki wielofunkcyjne alifatyczne nasycone aromatyczne nienasycone halogenki alkilowe alkohole fenole etery aldehydy ketony aminy kwasy
Podział związków organicznych węglowodory związki jednofunkcyjne związki wielofunkcyjne alifatyczne nasycone aromatyczne nienasycone halogenki alkilowe alkohole fenole etery aldehydy ketony aminy kwasy
Wymagania edukacyjne z chemii oraz sposoby sprawdzania wiedzy i umiejętności
 Wymagania edukacyjne z chemii oraz sposoby sprawdzania wiedzy i umiejętności Kwasy Wymagania edukacyjne z podstawy programowej - klasa VIII Uczeń: definiuje pojęcie kwasy zgodnie z teorią Arrheniusa opisuje
Wymagania edukacyjne z chemii oraz sposoby sprawdzania wiedzy i umiejętności Kwasy Wymagania edukacyjne z podstawy programowej - klasa VIII Uczeń: definiuje pojęcie kwasy zgodnie z teorią Arrheniusa opisuje
WYMAGANIA EDUKACYJNE
 GIMNAZJUM NR 2 W RYCZOWIE WYMAGANIA EDUKACYJNE niezbędne do uzyskania poszczególnych śródrocznych i rocznych ocen klasyfikacyjnych z CHEMII w klasie III GIMNAZJUM Wymagania edukacyjne niezbędne do uzyskania
GIMNAZJUM NR 2 W RYCZOWIE WYMAGANIA EDUKACYJNE niezbędne do uzyskania poszczególnych śródrocznych i rocznych ocen klasyfikacyjnych z CHEMII w klasie III GIMNAZJUM Wymagania edukacyjne niezbędne do uzyskania
Stechiometria równań reakcji chemicznych, objętość gazów w warunkach odmiennych od warunków normalnych (0 o C 273K, 273hPa)
 Karta pracy I/2a Stechiometria równań reakcji chemicznych, objętość gazów w warunkach odmiennych od warunków normalnych (0 o C 273K, 273hPa) I. Stechiometria równań reakcji chemicznych interpretacja równań
Karta pracy I/2a Stechiometria równań reakcji chemicznych, objętość gazów w warunkach odmiennych od warunków normalnych (0 o C 273K, 273hPa) I. Stechiometria równań reakcji chemicznych interpretacja równań
Wymagania programowe na poszczególne oceny z chemii dla klasy trzeciej
 Wymagania programowe na poszczególne oceny z chemii dla klasy trzeciej Dział programu: Sole opisuje budowę soli wskazuje metal i resztę kwasową we wzorze soli zapisuje wzory sumaryczne soli (chlorków,
Wymagania programowe na poszczególne oceny z chemii dla klasy trzeciej Dział programu: Sole opisuje budowę soli wskazuje metal i resztę kwasową we wzorze soli zapisuje wzory sumaryczne soli (chlorków,
WYMAGANIA EDUKACYJNE z chemii dla klasy trzeciej gimnazjum
 Lucyna Krupa Rok szkolny 2018/2019 Anna Mikrut WYMAGANIA EDUKACYJNE z chemii dla klasy trzeciej gimnazjum Wyróżnia się wymagania na: ocenę dopuszczającą ocenę dostateczną (obejmują wymagania na ocenę dopuszczającą)
Lucyna Krupa Rok szkolny 2018/2019 Anna Mikrut WYMAGANIA EDUKACYJNE z chemii dla klasy trzeciej gimnazjum Wyróżnia się wymagania na: ocenę dopuszczającą ocenę dostateczną (obejmują wymagania na ocenę dopuszczającą)
