Protezy stomatologiczne jako wyroby medyczne w świetle aktów normatywnych
|
|
|
- Dagmara Nowicka
- 8 lat temu
- Przeglądów:
Transkrypt
1 PROT. STOM., 2005, LV, 6 Protezy stomatologiczne jako wyroby medyczne w świetle aktów normatywnych Dental prosthesis as medical devices in the light of normative acts Danuta Nowakowska 1*, Halina Panek 2 Z dniem wejścia do Unii Europejskiej w Rzeczpospolitej Polskiej zaczęła obowiązywać Ustawa o wyrobach medycznych, a w dziedzinie normalizacji Polski Komitet Normalizacyjny (PKN), będący członkiem Międzynarodowej Organizacji Normalizacyjnej (ISO), stał się pełnoprawnym członkiem Europejskiego Komitetu Normalizacyjnego (CEN) i Europejskiego Komitetu Normalizacyjnego Elektrotechniki (CENELEC). W artykule podjęto próbę określenia miejsca protez i wszczepów stomatologicznych jako wyrobów medycznych w świetle tej Ustawy. Przedstawiono także wybrane zagadnienia z zakresu zasad normalizacji materiałów i urządzeń stomatologicznych. On the day of access to the European Union in the Republic of Poland Medical Devices Act entered into force, and the Polish Committee for Standardization (PKN), which is a member of International Organization for Standarization (ISO), has become a right full member of Comité Européen de Normalisation (CEN) and Comité Européen de Normalisation Electrotechnique (CENELEC). In this article an attempt has been taken to classsify the place of dental prosthesis and implants as medical devices in the light of above mentioned Act. Selected issues in the field of normalization principles of dental materials and devices were presented. HASŁA INDEKSOWE: Wyroby medyczne, wyroby medyczne używane w stomatologii, znak CE, polskie normy KEY WORDS: Medical devices, medical devices used in dentistry, Mark CE, polish standards Wprowadzenie W wyniku europejskich procesów zjednoczeniowych w latach osiemdziesiątych i dziewięćdziesiątych ubiegłego wieku rozpoczęła się procedura ujednolicania postanowień prawnych dotyczących wytwarzania i stosowania wyrobów medycznych, a więc i stomatologicznych. W okresie tym w krajach Z Katedry Protetyki Stomatologicznej AM we Wrocławiu 2 Kierownik: dr hab. n. med. H. Panek Z Zakładu Materiałoznawstwa 1 p. o. Kierownika: dr n. med. D. Nowakowska Adres autorów: Wrocław, ul. Krakowska 26 należących do ówczesnej Europejskiej Wspólnoty Gospodarczej ukazało się kilka dyrektyw Rady Wspólnot Europejskich, w tym: Dyrektywa 90/385/ EWG z dnia 20 czerwca 1990 r. w sprawie zbliżenia ustawodawstwa Państw Członkowskich odnosząca się do wyrobów medycznych aktywnego osadzania (1) oraz Dyrektywa z dnia 4 czerwca 1993 roku w sprawie wyrobów medycznych (2), które stały się punktem wyjścia dla opracowania prawa o wyrobach medycznych w państwach Wspólnoty, np. niemieckiego prawa o wyrobach medycznych *Członek Komitetu Technicznego nr 283 ds. Materiałów Stomatologicznych Polskiego Komitetu Normalizacyjnego od 2003 roku. 456
2 Protezy w świetle aktów normatywnych MPG w 1994 roku i MPV w 1997 (cyt. wg 3). W Dyrektywach tych określono, że wyroby medyczne powinny osiągnąć parametry działania przypisane im przez wytwórcę oraz zapewnić pacjentom, użytkownikom i osobom trzecim wysoki poziom bezpieczeństwa ich stosowania. Posiadanie jednolitych norm europejskich jest bardzo pożądane, ponieważ umożliwia sprawdzenie zgodności z podstawowymi wymaganiami oraz zabezpiecza przed niebezpieczeństwami związanymi z projektowaniem, wytwarzaniem i pakowaniem wyrobów medycznych. Takie spójne normy europejskie są redagowane i zatwierdzane przez powołane w tym celu: Międzynarodową Organizację Normalizacyjną ISO (International Organization for Standarization), Europejski Komitet Normalizacyjny CEN (Comité Européen de Normalisation) oraz Europejski Komitet Normalizacyjny Elektrotechniki CENELEC (Comité Européen de Normalisation Electrotechnique). Krajową jednostką normalizacyjną jest Polski Komitet Normalizacyjny, który z dniem wejścia Rzeczpospolitej Polskiej do Unii Europejskiej stał się pełnoprawnym członkiem tych organizacji. W tym samym czasie w Polsce zaczęła obowiązywać Ustawa o wyrobach medycznych z dnia 20 kwietnia 2004 roku opublikowana w Dzienniku Ustaw w dniu 30 kwietnia 2004 roku (8). Poniżej przedstawiamy zasady ogólne, podstawowe pojęcia, klasyfikację wyrobów medycznych i wytyczne dotyczące oceny klinicznej badanych wyrobów w świetle obowiązującej Ustawy oraz wybrane zagadnienia z zakresu zasad normalizacji wyrobów medycznych używanych w stomatologii. Zasady ogólne W przepisach ogólnych Ustawa ta określa zasady wprowadzania do obrotu i do używania wyrobów medycznych oraz oceny klinicznej tych wyrobów. Następnie podaje warunki nadzoru nad wytwarzaniem, wprowadzaniem do obrotu i używaniem wyrobów medycznych oraz nadzoru nad wyrobami medycznymi wprowadzanymi już do obrotu i do używania. Z kolei w Ustawie opisano zasady zgłaszania incydentów medycznych z wyrobami medycznymi oraz dalszego postępowania po ich zgłoszeniu, sposób prowadzenia Rejestru wyrobów medycznych i podmiotów odpowiedzialnych za ich wprowadzenie do obrotu i do używania, zasady i tryb autoryzowania, notyfikowania, nadzorowania, ograniczania i cofania autoryzacji jednostek notyfikowanych w zakresie wyrobów medycznych oraz określono organy właściwe w tych sprawach, następnie klasyfikację i kwalifikację wyrobów medycznych oraz ocenę zgodności wyrobów medycznych i wymagania zasadnicze stawiane tym wyrobom. Wyroby medyczne Ustawa definiuje wiele pojęć, między innymi szczególnie istotne dla stomatologii, takie jak: wyrób medyczny, aktywny wyrób medyczny do implantacji, inwazyjny wyrób medyczny i wyrób medyczny wykonywany na zamówienie. W myśl Ustawy przez wyrób medyczny należy rozumieć narzędzie, przyrząd, aparat, sprzęt, materiał lub inny artykuł, stosowany samodzielnie lub w połączeniu, włączając oprogramowanie niezbędne do właściwego stosowania wyrobu, przeznaczone przez wytwórcę do stosowania u ludzi w celu: diagnozowania, zapobiegania, monitorowania, leczenia lub łagodzenia przebiegu chorób oraz kompensowania urazów lub upośledzeń, badania, zastępowania lub modyfikowania budowy anatomicznej lub prowadzenia procesu fizjologicznego oraz regulacji poczęć który nie osiąga swojego zasadniczego zamierzonego działania w ciele lub na ciele ludzkim środkami farmakologicznymi, immunologicznymi lub metabolicznymi, lecz którego działanie może być przez nie wspomagane. Aktywnym wyrobem medycznym do implantacji jest wyrób medyczny, którego prawidłowe funkcjonowanie zależy od źródła energii elektrycznej lub jakiegokolwiek źródła zasilania innego niż energia generowana bezpośrednio przez organizm ludzki lub przez siłę ciężkości, przeznaczony do umieszczenia w ciele ludzkim częściowo lub w całości, za pomocą zabiegu chirurgicznego lub medycznego, lub w naturalnych otworach ciała za pomocą zabiegu medycznego, celem pozostawienia go w tym ciele. Natomiast jako inwazyjny wyrób medyczny należy rozumieć wyrób medyczny do różnego przeznaczenia, który jest wprowadzany w części lub całości do organizmu ludzkiego przez otwory ciała lub przez jego powierzchnię. Z kolei wyrób medyczny wykonany na zamówienie to wyrób medyczny wykonywany 457
3 D. Nowakowska, H. Panek zgodnie z pisemną instrukcją wskazującą jego właściwości i zastosowanie, sporządzoną przez lekarza lub inne osoby posiadające odpowiednie kwalifikacje zawodowe, i na ich odpowiedzialność, przeznaczony do używania przez określonego pacjenta. Wprowadzanie wyrobów medycznych do obrotu i używania (znak CE) Do obrotu i do używania mogą być wprowadzone wyłącznie wyroby medyczne spełniające wymagania określone w Ustawie. Taki wyrób medyczny powinien być właściwie dostarczony, prawidłowo zainstalowany i konserwowany oraz używany zgodnie z zastosowaniem przewidzianym przez wytwórcę. Wyrób ten nie może stwarzać zagrożenia dla bezpieczeństwa i zdrowia pacjentów, użytkowników i osób trzecich. Podmiot uprawniony, który wprowadza wyrób medyczny na terytorium Rzeczypospolitej Polskiej, jest obowiązany oznakować wyrób medyczny w języku polskim oraz dostarczyć użytkownikowi instrukcję używania i etykiety tego wyrobu w języku polskim. Zezwolenie na wprowadzenie do użytkowania produktów medycznych wynika ze spełnienia warunków postępowania z materiałami i ich eksploatacji. Należy określić, czy wyrób odpowiada podstawowym wymogom i czy jest zgodny z przyjętymi zasadami użytkowania, które zawarte są w określonych normach. Po pozytywnej ocenie zgodności producent może stosować znak zgodności CE, co oznacza, że wyroby medyczne oznaczone tym znakiem mogą być wprowadzone do obrotu i do używania. Znak CE umieszcza się na wyrobie medycznym po przeprowadzeniu odpowiednich dla niego procedur oceny zgodności z wymaganiami zasadniczymi. Produkty medyczne ze znakiem CE mogą być rozpowszechniane we wszystkich państwach Unii Europejskiej. Znakiem tym nie oznacza się jednak wyrobu medycznego wykonywanego na zamówienie, przeznaczonego do badań klinicznych oraz wyrobu medycznego do diagnostyki przeznaczonego do oceny działania in vitro. Klasyfikacja i kwalifikacja produktów medycznych W Ustawie podano również zasady klasyfikacji i kwalifikacji wyrobów medycznych, zgodnie z którymi wyroby medyczne w zależności od potencjalnego ryzyka związanego z ich stosowaniem, podlegają klasyfikacji na 4 klasy: I, II a, II b i III. Klasyfikację i kwalifikację wyrobu medycznego przeprowadza wytwórca. Podział wyrobów medycznych na 4 klasy zależy zarówno od stopnia ich inwazyjności, jak i czasu ich stosowania. Za wartość graniczną uznano nabłonkową barierę ciała ludzkiego, a w przypadku wyrobów stomatologicznych nabłonka jamy ustnej. Produkty, które nie przekraczają granicy nabłonkowej, są zaliczane do klasy I, o ile pozostają w jamie ustnej tymczasowo, albo do klasy II, jeżeli pozostają w niej dłużej, ale nie mają oddziaływania farmakologicznego. Do klasy I należy więc zaliczyć takie produkty, jak np.: łyżki wyciskowe standardowe i indywidualne, masy wyciskowe, woski czy materiały do rejestracji zwarcia. Na tych wyrobach, należących do klasy najniższego ryzyka producent może sam, po własnej ocenie zgodności z normą lub normami umieścić znak CE, pod warunkiem, że będzie gwarantował, że każdy jego wyrób będzie spełniał określone przez odpowiednie normy wymogi. Protezy i wszczepy stomatologiczne W jaki sposób w świetle tego podziału należałoby sklasyfikować protezy stomatologiczne? Czy są one wyrobami medycznymi, a jeśli tak, to do której klasy należałoby je zaliczyć? Otóż wszystkie protezy, zarówno stałe jak i ruchome, których przewidywany okres posługiwania się nimi, czyli przebywania w jamie ustnej pacjenta będzie długi, należy zaliczyć do klasy II a, ale tak długo, dopóki nie przewiduje się ich oddziaływania farmakologicznego. Wykonaniu protez muszą towarzyszyć jednak pewne ograniczenia. Protezy stomatologiczne mogą być wytwarzane wyłącznie z materiałów zgodnych z podstawowymi normami i opatrzonymi znakiem zgodności CE. Jeżeli materiały te będą przetwarzane ściśle ze wskazanymi przez producenta procesami technologicznymi i ich przebieg może być udokumentowany, wówczas można założyć, że końcowy produkt, w postaci protezy, odpowiada również podstawowym wymaganiom zawartym w normach. Proteza może być wówczas uznana za 458
4 Protezy w świetle aktów normatywnych wyrób medyczny. Czy powinna być wówczas oznakowana znakiem CE? Podobnie jak w ustawodawstwie niemieckim ( cyt. wg 3) należałoby się tutaj odnieść do definicji wyrobu medycznego wykonanego na zamówienie, w myśl której jest on wykonany zgodnie z pisemną instrukcją lekarza, na jego odpowiedzialność i przeznaczony do używania przez określonego pacjenta. W takim ujęciu, proteza jako wyrób specjalnego zastosowania, przypisany znanemu z nazwiska pacjentowi, nie musi być oznaczana znakiem CE. Następne zagadnienie to klasyfikacja wszelkiego typu wszczepów stomatologicznych. Implanty jako produkty, które na stałe przekraczają granicę nabłonkową ciała, należy zaliczyć już do klasy II b. Produkty klasy II i III wymagają dokładnego określenia miejsca w klasyfikacji. Określa to sam producent, ale sprawdza się tę ocenę poprzez procedurę oceny zgodności wyrobów medycznych z wymaganiami zasadniczymi. Przyjmuje się domniemanie zgodności wyrobu medycznego z wymaganiami zasadniczymi, jeżeli stwierdzono jego zgodność z krajowymi normami (Polskimi Normami PN) przyjętymi Przez Polski Komitet Normalizacyjny (PKN) na podstawie zharmonizowanych norm europejskich. Normy te dotyczą aktywnych wyrobów do implantacji, wyrobów medycznych do diagnostyki in vitro i do wyrobów medycznych do różnego przeznaczenia. Dla tych trzech grup Minister Zdrowia określa wymagania zasadnicze, procedury zgodności oraz wykaz procedur zgodności, które mogą być przeprowadzane przez autoryzowanego przedstawiciela, uwzględniając przeznaczenie wyrobu, system jakości wytwórcy oraz bezpieczeństwo, a także ochronę życia i zdrowia pacjentów. Ocena kliniczna wyrobów medycznych W myśl Ustawy dla produktów medycznych do różnego przeznaczenia i aktywnych wyrobów medycznych do implantacji niezbędna jest ocena kliniczna, czyli takie postępowanie, które ma na celu potwierdzenie, czy wyrób medyczny w normalnych warunkach używania spełnia odnoszące się do niego wymagania zasadnicze i nie wykazuje niepożądanych działań ubocznych. Ocena kliniczna takich wyrobów medycznych jest wykonywana na podstawie: 1) zestawionych danych uzyskanych z właściwego, aktualnie dostępnego piśmiennictwa naukowego, dotyczącego przewidzianego wykorzystania wyrobu i zastosowanych technik lub 2) pisemnego opracowania zawierającego krytyczną ocenę tych zestawionych danych lub 3) wyników badań klinicznych wykonanych zgodnie z przepisami Ustawy. Badania kliniczne przeprowadza się dla wyrobów medycznych różnego przeznaczenia i aktywnych wyrobów medycznych do implantacji, jeżeli dane w punkcie 1 i 2 nie są wystarczające do dokonywania oceny klinicznej. Takie badanie kliniczne jest eksperymentem medycznym z użyciem wyrobu medycznego przeprowadzanym na ludziach w rozumieniu przepisów Ustawy o zawodzie lekarza z dnia 5 grudnia 1996 r. z późniejszymi zmianami (7). Warunkiem rozpoczęcia badania klinicznego jest uzyskanie pozytywnej opinii odpowiedniej komisji bioetycznej, co określa art. 29 poprzednio wymienionej Ustawy, oraz pozwolenie Prezesa Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych. Ustawa określa również, że badania klinicznego nie stanowią badania medyczne prowadzone za pomocą wyrobów medycznych, które zostały oznaczone znakiem CE na podstawie odpowiednich procedur oceny zgodności, o ile przedmiotem tych badań nie jest zastosowanie wyrobu medycznego inne niż przewidziane przez wytwórcę i przedstawione w procedurze oceny zgodności. Normalizacja wyrobów medycznych Wobec bardzo dużej liczby dostępnych na rynku wyrobów medycznych (kilkaset tysięcy) nie można ustalać norm specyficznych dla pojedynczego wyrobu. Wszędzie, gdzie w Ustawie o wyrobach medycznych mówi się o normach krajowych przyjętych na podstawie zharmonizowanych norm europejskich należy przyjąć, że do Polskich Norm (PN) ustanowionych i oznaczonych przez Polski Komitet Normalizacyjny (PKN), który jest krajową jednostką normalizacyjną działającą z mocy Ustawy z 3 kwietnia 1993 r. o normalizacji (6) jako organ kolegialny, podległy Prezesowi Rady Ministrów. PKN organizuje i prowadzi działalność na szczeblu krajowym oraz uczestniczy w pracach międzynarodowych i regionalnych organizacji 459
5 D. Nowakowska, H. Panek normalizacyjnych. Polski Komitet Normalizacyjny jest członkiem Międzynarodowej Organizacji Normalizacyjnej ISO (International Organization for Standarization) i innych Komisji, a po wejściu Polski do Unii Europejskiej stał się członkiem CEN i CENELEC. Międzynarodowa Organizacja Normalizacyjna (ISO) jest ogólnoświatową federacją krajowych jednostek normalizacyjnych (organizacji członkowskich ISO). Prace związane z przygotowaniem norm międzynarodowych są zwykle wykonywane przez komitety techniczne ISO. Dla stomatologii został powołany Komitet Techniczny ISO/TC 106, Stomatologia. Organami wykonawczymi PKN są: Biuro Komitetu (organ instytucjonalny) i normalizacyjne Komisje Problemowe (organy kolegialne), między innymi Komitet Techniczny nr 283 ds. Materiałów Stomatologicznych, który zajmuje się opracowaniem norm badania właściwości materiałów i sprzętu stomatologicznego przeprowadzanymi w warunkach in vitro oraz Normalizacyjna Komisja Problemowa nr 247 ds. Materiałów Medycznych i Biomateriałów, która ustala zasady badań przedklinicznych i klinicznych. Zgodnie z normami warunkiem wstępnym do przeprowadzenia badania klinicznego jest istnienie wyników oceny przedklinicznej. Mogą to być badania techniczne lub biologiczne. W polskiej wersji normy europejskiej PN-EN ISO 7405: Stomatologia- Przedkliniczna ocena biozgodności wyrobów medycznych używanych w stomatologii Metody badania materiałów stomatologicznych (4), w definicji wyrobu medycznego uściśla się, że termin urządzenie medyczne obejmuje urządzenia stomatologiczne i materiały stomatologiczne, a za materiał stomatologiczny uważa się substancję lub kombinację substancji specjalnie spreparowanych i/lub przygotowanych do użycia przez osoby upoważnione w praktyce stomatologicznej i/lub w związanych z nią postępowaniach. W normie tej podaje się również szczegółową klasyfikację wyrobów medycznych używanych w stomatologii opierającą się na podziale ze względu na sposób i na czas trwania kontaktu wyrobu z ciałem pacjenta. Podział pierwszy wyróżnia wyroby, przy których nie dochodzi do kontaktu z ciałem pacjenta ani pośrednio, ani bezpośrednio oraz wyroby, kontaktujące się z powierzchnią niezmienionej lub nienaruszonej skóry, z powierzchnią niezmienionej lub nienaruszonej błony śluzowej jamy ustnej i które kontaktują się z powierzchniami twardych tkanek zębów włączając szkliwo, zębinę i kostniwo z uwagą, że zębina i kostniwo są uznawane za powierzchnie po recesji dziąsła. Następnie w podziale wyróżnia się wyroby kontaktujące się zewnętrznie, czyli urządzenia stomatologiczne, które wnikają i są w kontakcie z błoną śluzową, twardymi tkankami zęba, miazgą lub kością, lub z ich kombinacją i są wystawione na kontakt ze środowiskiem jamy ustnej. Następną grupą są wszczepy, jako wyroby, zawierające zestawy i wszczepy, które całkowicie lub częściowo są wprowadzane do tkanek miękkich, kości lub systemu miazgowo-zębinowego zęba, albo też innej ich kombinacji i nie są wystawione na kontakt zewnętrzny ze środowiskiem jamy ustnej. Drugi podział wyrobów medycznych opiera się na kryterium czasu trwania kontaktu. W tym ujęciu wyróżnia się: 1) wyroby o ograniczonej ekspozycji, czyli takie, których jednorazowe lub wielokrotne użycie albo kontakt trwa zazwyczaj do 24 godzin, 2) o przedłużonej ekspozycji, których jednorazowe, wielokrotne, lub długoterminowe użycie albo kontakt jest dłuższe niż 24 godziny, ale nie 30 dni oraz 3) wyroby o stałym kontakcie, których podobne jak poprzednich, użycie lub kontakt przekracza 30 dni. Badania biologiczne natomiast muszą być wykonane zgodnie z ogólnymi wytycznymi doboru badań oceny biologicznej podanymi w PN-EN ISO (5) oraz zaleca się, aby były one wybrane spośród metod opisanych w normach serii ISO Szczegółowe warunki wykonania takich badań ustala ekspert, który dysponuje odpowiednimi danymi chemicznymi, fizycznymi i biologicznymi dotyczącymi badanego wyrobu i który jest świadomy przewidywanych warunków jego użycia. Każda metoda z wymienionych w normach badań ma swoje ograniczenia i prowadzi do wyników, które wymagają odpowiedniej interpretacji. Pełna interpretacja jest możliwa tylko w zestawieniu z wieloma wynikami badań wykonanych w warunkach in vitro. Nawet wykorzystanie bardzo szerokiej bazy danych doświadczalnych, z badaniami na zwierzętach włącznie, nie jest pozbawione pewnego ryzyka. Na podstawie samych badań biologicznych nie można przesądzać o klinicznej przydatności wyrobów i materiałów stomatologicznych. Biologiczne me- 460
6 Protezy w świetle aktów normatywnych tody badania mają jednak znaczenie dla oceny potencjalnego ryzyka zastosowania określonego wyrobu medycznego. Piśmiennictwo 1. Dyrektywa Rady 90/385/EWG z dnia 20 czerwca 1990 r. w sprawie zbliżenia ustawodawstwa Państw Członkowskich odnoszących się do wyrobów medycznych aktywnego osadzania. 2. Dyrektywa Rady 93/ 42/EWG z dnia 14 czerwca 1993 r. dotycząca wyrobów medycznych. 3. Koeck B.: Korony i mosty, rozdz. 7 Aspekty materiałoznawstwa, (red. wyd. polskiego T. Maślanka), Wyd. Urban & Partner, Wrocław Polska Norma PN-EN ISO 7405 listopad 2000, Stomatologia Przedkliniczna ocena biozgodności wyrobów medycznych używanych w stomatologii Metody badania materiałów stomatologicznych. 5. Polska Norma PN-EN ISO , luty 2004, Biologiczna ocena wyrobów medycznych Część 1: Ocena i badanie. 6. Ustawa z dnia 3 kwietnia 1993 r. o normalizacji (Dz. U. nr 55, poz.251 z późn. zm.). 7. Ustawa o zawodzie lekarza z dnia 5 grudnia 1996 r. a (Dz. U. z 2002 r. Nr 21) Zmiany tekstu jednolitego wymienionej ustawy zostały ogłoszone w Dz. U. z 2002 r. nr 76, poz. 691, Nr 152, poz i Nr 153, poz oraz z 2003 r. Nr 90, poz Ustawa z dnia 20 kwietnia 2004 r. o wyrobach medycznych (Dz. U. z dnia 30 kwietnia 2004 r.) Otrzymano: 20.I.2005 r. 461
Formalne uwarunkowania dopuszczenia do obrotu wyrobów medycznych
 Instytut Arcana Member of LASER Analytica Group Ul. Płk. Dąbka 8, 30 732 Kraków tel/fax +48 12 263 60 38 www.inar.pl www.la-ser.com Formalne uwarunkowania dopuszczenia do obrotu wyrobów medycznych >Michał
Instytut Arcana Member of LASER Analytica Group Ul. Płk. Dąbka 8, 30 732 Kraków tel/fax +48 12 263 60 38 www.inar.pl www.la-ser.com Formalne uwarunkowania dopuszczenia do obrotu wyrobów medycznych >Michał
USTAWA z dnia 20 kwietnia 2004 r. o wyrobach stosowanych w medycynie weterynaryjnej 1)
 Kancelaria Sejmu s. 1/9 USTAWA z dnia 20 kwietnia 2004 r. Opracowano na podstawie: Dz.U. z 2004 r. Nr 93, poz. 893. o wyrobach stosowanych w medycynie weterynaryjnej 1) Art. 1. Ustawa określa: 1) wprowadzanie
Kancelaria Sejmu s. 1/9 USTAWA z dnia 20 kwietnia 2004 r. Opracowano na podstawie: Dz.U. z 2004 r. Nr 93, poz. 893. o wyrobach stosowanych w medycynie weterynaryjnej 1) Art. 1. Ustawa określa: 1) wprowadzanie
Wytwarzanie wyrobów sterylnych w szpitalu w świetle aktualnych przepisów. Mgr Jarosław Czapliński Wojewódzki Szpital Zespolony w Elblągu
 Wytwarzanie wyrobów sterylnych w szpitalu w świetle aktualnych przepisów. Mgr Jarosław Czapliński Wojewódzki Szpital Zespolony w Elblągu HISTORIA - PRL Produkcja opatrunków podstawy prawne. Ustawa z dnia
Wytwarzanie wyrobów sterylnych w szpitalu w świetle aktualnych przepisów. Mgr Jarosław Czapliński Wojewódzki Szpital Zespolony w Elblągu HISTORIA - PRL Produkcja opatrunków podstawy prawne. Ustawa z dnia
Znak CE dla akceleratorów medycznych. Jan Kopeć
 Znak CE dla akceleratorów medycznych Szkoła Fizyki Akceleratorów Medycznych, Świerk 2007 Znaczenie znaku CE dla wyrobów medycznych Znak CE, który producent umieszcza na wyrobie medycznym oznacza spełnienie
Znak CE dla akceleratorów medycznych Szkoła Fizyki Akceleratorów Medycznych, Świerk 2007 Znaczenie znaku CE dla wyrobów medycznych Znak CE, który producent umieszcza na wyrobie medycznym oznacza spełnienie
WYROK. Zespołu Arbitrów z dnia 5 grudnia 2005 r. Arbitrzy: Leszek Witold Natora. Protokolant Katarzyna Kawulska
 Sygn. akt UZP/ZO/0-3611/05 WYROK Zespołu Arbitrów z dnia 5 grudnia 2005 r. Zespół Arbitrów w składzie: Przewodniczący Zespołu Arbitrów Maria Alicja Litwa Arbitrzy: Leszek Witold Natora Elżbieta Małgorzata
Sygn. akt UZP/ZO/0-3611/05 WYROK Zespołu Arbitrów z dnia 5 grudnia 2005 r. Zespół Arbitrów w składzie: Przewodniczący Zespołu Arbitrów Maria Alicja Litwa Arbitrzy: Leszek Witold Natora Elżbieta Małgorzata
USTAWA z dnia 27 lipca 2001 r. o wyrobach medycznych. Rozdział 1 Przepisy ogólne
 Kancelaria Sejmu s. 1/17 USTAWA z dnia 27 lipca 2001 r. o wyrobach medycznych Opracowano na podstawie: Dz.U. z 2001 r. Nr 126, poz. 1380, z 2002 r. Nr 152, poz. 1264; Rozdział 1 Przepisy ogólne Art. 1.
Kancelaria Sejmu s. 1/17 USTAWA z dnia 27 lipca 2001 r. o wyrobach medycznych Opracowano na podstawie: Dz.U. z 2001 r. Nr 126, poz. 1380, z 2002 r. Nr 152, poz. 1264; Rozdział 1 Przepisy ogólne Art. 1.
Warszawa, dnia 19 lutego 2016 r. Poz. 206
 Warszawa, dnia 19 lutego 2016 r. Poz. 206 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 17 lutego 2016 r. zmieniające rozporządzenie w sprawie wymagań zasadniczych oraz procedur oceny zgodności aktywnych wyrobów
Warszawa, dnia 19 lutego 2016 r. Poz. 206 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 17 lutego 2016 r. zmieniające rozporządzenie w sprawie wymagań zasadniczych oraz procedur oceny zgodności aktywnych wyrobów
Obowiązuje od 1.01.2002 r. USTAWA z dnia 27 lipca 2001 r. o wyrobach medycznych. Rozdział 1 Przepisy ogólne
 Kancelaria Sejmu s. 1/15 Obowiązuje od 1.01.2002 r. USTAWA z dnia 27 lipca 2001 r. Opracowano na podstawie: Dz.U. z 2001 r. Nr 126, poz. 1380. o wyrobach medycznych Rozdział 1 Przepisy ogólne Art. 1. Ustawa
Kancelaria Sejmu s. 1/15 Obowiązuje od 1.01.2002 r. USTAWA z dnia 27 lipca 2001 r. Opracowano na podstawie: Dz.U. z 2001 r. Nr 126, poz. 1380. o wyrobach medycznych Rozdział 1 Przepisy ogólne Art. 1. Ustawa
- o wyrobach medycznych wraz z projektami aktów wykonawczych.
 SEJM RZECZYPOSPOLITEJ POLSKIEJ VI kadencja Prezes Rady Ministrów RM 10-154-09 Druk nr 2668 cz. II Warszawa, 8 stycznia 2010 r. Pan Bronisław Komorowski Marszałek Sejmu Rzeczypospolitej Polskiej Szanowny
SEJM RZECZYPOSPOLITEJ POLSKIEJ VI kadencja Prezes Rady Ministrów RM 10-154-09 Druk nr 2668 cz. II Warszawa, 8 stycznia 2010 r. Pan Bronisław Komorowski Marszałek Sejmu Rzeczypospolitej Polskiej Szanowny
USTAWA z dnia 20 kwietnia 2004 r. o wyrobach medycznych 1) Rozdział 1 Przepisy ogólne
 Kancelaria Sejmu s. 1/38 USTAWA z dnia 20 kwietnia 2004 r. o wyrobach medycznych 1) Rozdział 1 Przepisy ogólne Opracowano na podstawie: Dz.U. z 2004 r. Nr 93, poz. 896. Art. 1. 1. Ustawa określa: 1) wprowadzanie
Kancelaria Sejmu s. 1/38 USTAWA z dnia 20 kwietnia 2004 r. o wyrobach medycznych 1) Rozdział 1 Przepisy ogólne Opracowano na podstawie: Dz.U. z 2004 r. Nr 93, poz. 896. Art. 1. 1. Ustawa określa: 1) wprowadzanie
USTAWA. z dnia 20 maja 2010 r. o wyrobach medycznych 1) Rozdział 1. Przepisy ogólne
 Kancelaria Sejmu s. 1/93 USTAWA z dnia 20 maja 2010 r o wyrobach medycznych 1) Rozdział 1 Przepisy ogólne Opracowano na podstawie: Dz. U. z 2010 r. Nr 107, poz. 679, z 2011 r. Nr 102, poz. 586, Nr 113,
Kancelaria Sejmu s. 1/93 USTAWA z dnia 20 maja 2010 r o wyrobach medycznych 1) Rozdział 1 Przepisy ogólne Opracowano na podstawie: Dz. U. z 2010 r. Nr 107, poz. 679, z 2011 r. Nr 102, poz. 586, Nr 113,
Incydent medyczny a odpowiedzialność wytwórcy wyrobów medycznych
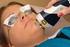 Incydent medyczny a odpowiedzialność wytwórcy wyrobów medycznych Ustawa o wyrobach medycznych, implementująca tzw. medyczne dyrektywy unijne 1 dotyczące bezpieczeństwa wdrażania, użytkowania oraz korzystania
Incydent medyczny a odpowiedzialność wytwórcy wyrobów medycznych Ustawa o wyrobach medycznych, implementująca tzw. medyczne dyrektywy unijne 1 dotyczące bezpieczeństwa wdrażania, użytkowania oraz korzystania
USTAWA z dnia 20 kwietnia 2004 r. o wyrobach medycznych 1) Rozdział 1 Przepisy ogólne
 Kancelaria Sejmu s. 1/1 USTAWA z dnia 20 kwietnia 2004 r. o wyrobach medycznych 1) Opracowano na podstawie: Dz.U. z 2004 r. Nr 93, poz. 896, z 2005 r. Nr 64, poz. 565. Rozdział 1 Przepisy ogólne Art. 1.
Kancelaria Sejmu s. 1/1 USTAWA z dnia 20 kwietnia 2004 r. o wyrobach medycznych 1) Opracowano na podstawie: Dz.U. z 2004 r. Nr 93, poz. 896, z 2005 r. Nr 64, poz. 565. Rozdział 1 Przepisy ogólne Art. 1.
USTAWA. z dnia 20 maja 2010 r. o wyrobach medycznych1), 2) in vitro;
 Dziennik Ustaw Nr 107 8990 Poz. 679 679 USTAWA z dnia 20 maja 2010 r. o wyrobach medycznych1), 2) Rozdział 1 Przepisy ogólne Art. 1. Ustawa określa: 1) zasady wprowadzania do obrotu i do używania: a) wyrobów
Dziennik Ustaw Nr 107 8990 Poz. 679 679 USTAWA z dnia 20 maja 2010 r. o wyrobach medycznych1), 2) Rozdział 1 Przepisy ogólne Art. 1. Ustawa określa: 1) zasady wprowadzania do obrotu i do używania: a) wyrobów
Dz.U Nr 107 poz. 679 USTAWA. z dnia 20 maja 2010 r. o wyrobach medycznych
 Kancelaria Sejmu s. 1/101 Dz.U. 2010 Nr 107 poz. 679 USTAWA z dnia 20 maja 2010 r. 1), o wyrobach medycznych Opracowano na podstawie: t.j. Dz. U. z 2015 r. poz. 876, 1918. 1) 2) Ustawa w zakresie
Kancelaria Sejmu s. 1/101 Dz.U. 2010 Nr 107 poz. 679 USTAWA z dnia 20 maja 2010 r. 1), o wyrobach medycznych Opracowano na podstawie: t.j. Dz. U. z 2015 r. poz. 876, 1918. 1) 2) Ustawa w zakresie
DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ. Warszawa, dnia 30 stycznia 2019 r. Poz. 175
 DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ Warszawa, dnia 30 stycznia 2019 r. Poz. 175 OBWIESZCZENIE MARSZAŁKA SEJMU RZECZYPOSPOLITEJ POLSKIEJ z dnia 13 grudnia 2018 r. w sprawie ogłoszenia jednolitego tekstu
DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ Warszawa, dnia 30 stycznia 2019 r. Poz. 175 OBWIESZCZENIE MARSZAŁKA SEJMU RZECZYPOSPOLITEJ POLSKIEJ z dnia 13 grudnia 2018 r. w sprawie ogłoszenia jednolitego tekstu
Dz.U Nr 107 poz. 679 USTAWA. z dnia 20 maja 2010 r. o wyrobach medycznych. Rozdział 1
 Dz.U. 2010 Nr 107 poz. 679 USTAWA z dnia 20 maja 2010 r. 1), 2) o wyrobach medycznych Opracowano na podstawie: t.j. Dz. U. z 2015 r. poz. 876, 1918, z 2016 r. poz. 542. Rozdział 1 1) 2) Ustawa w zakresie
Dz.U. 2010 Nr 107 poz. 679 USTAWA z dnia 20 maja 2010 r. 1), 2) o wyrobach medycznych Opracowano na podstawie: t.j. Dz. U. z 2015 r. poz. 876, 1918, z 2016 r. poz. 542. Rozdział 1 1) 2) Ustawa w zakresie
Data aktualizacji: r.
 Nazwa ośrodka: Centrum Euro Info w Gdańsku Tytuł pakietu: Dyrektywa dotycząca kompatybilności elektromagnetycznej oznakowanie CE Grupa: Jakość - normalizacja - certyfikacja - standaryzacja Autor: Anna
Nazwa ośrodka: Centrum Euro Info w Gdańsku Tytuł pakietu: Dyrektywa dotycząca kompatybilności elektromagnetycznej oznakowanie CE Grupa: Jakość - normalizacja - certyfikacja - standaryzacja Autor: Anna
USTAWA z dnia 20 maja 2010 r. o wyrobach medycznych 1) Rozdział 1 Przepisy ogólne
 Kancelaria Sejmu s. 1/69 USTAWA z dnia 20 maja 2010 r. Opracowano na podstawie: Dz. U. z 2010 r. Nr 107, poz. 679. o wyrobach medycznych 1) Rozdział 1 Przepisy ogólne Art. 1. Ustawa określa: 1) zasady
Kancelaria Sejmu s. 1/69 USTAWA z dnia 20 maja 2010 r. Opracowano na podstawie: Dz. U. z 2010 r. Nr 107, poz. 679. o wyrobach medycznych 1) Rozdział 1 Przepisy ogólne Art. 1. Ustawa określa: 1) zasady
ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 2 lutego 2011 r.
 Dziennik Ustaw Nr 33 2534 Poz. 167 167 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 2 lutego 2011 r. w sprawie kryteriów raportowania zdarzeń z wyrobami, sposobu zgłaszania incydentów medycznych i działań
Dziennik Ustaw Nr 33 2534 Poz. 167 167 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 2 lutego 2011 r. w sprawie kryteriów raportowania zdarzeń z wyrobami, sposobu zgłaszania incydentów medycznych i działań
DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ
 DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ Warszawa, dnia 8 czerwca 2016 r. Poz. 806 ROZPORZĄDZENIE MINISTRA ROZWOJU 1) z dnia 2 czerwca 2016 r. w sprawie wymagań dla sprzętu elektrycznego 2) Na podstawie
DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ Warszawa, dnia 8 czerwca 2016 r. Poz. 806 ROZPORZĄDZENIE MINISTRA ROZWOJU 1) z dnia 2 czerwca 2016 r. w sprawie wymagań dla sprzętu elektrycznego 2) Na podstawie
Ustawa o wyrobach medycznych 1)
 Ustawa o wyrobach medycznych 1) z dnia 20 maja 2010 r. (Dz.U. Nr 107, poz. 679) tj. z dnia 26 maja 2015 r. (Dz.U. z 2015 r. poz. 876) tj. z dnia 17 stycznia 2017 r. (Dz.U. z 2017 r. poz. 211) (zm. Dz.U.
Ustawa o wyrobach medycznych 1) z dnia 20 maja 2010 r. (Dz.U. Nr 107, poz. 679) tj. z dnia 26 maja 2015 r. (Dz.U. z 2015 r. poz. 876) tj. z dnia 17 stycznia 2017 r. (Dz.U. z 2017 r. poz. 211) (zm. Dz.U.
Tekst ustawy ustalony ostatecznie po rozpatrzeniu poprawek Senatu. USTAWA z dnia 20 maja 2010 r. o wyrobach medycznych
 Tekst ustawy ustalony ostatecznie po rozpatrzeniu poprawek Senatu USTAWA z dnia 20 maja 2010 r. 1), 2) o wyrobach medycznych 1) Ustawa w zakresie swojej regulacji wdraża postanowienia: 1) dyrektywy Rady
Tekst ustawy ustalony ostatecznie po rozpatrzeniu poprawek Senatu USTAWA z dnia 20 maja 2010 r. 1), 2) o wyrobach medycznych 1) Ustawa w zakresie swojej regulacji wdraża postanowienia: 1) dyrektywy Rady
Norma to dokument przyjęty na zasadzie konsensu i zatwierdzony do powszechnego stosowania przez
 KONCEPCJA SYSTEMU JAKOŚCI zgodnie z wymaganiami norm ISO serii 9000 dr Lesław Lisak Co to jest norma? Norma to dokument przyjęty na zasadzie konsensu i zatwierdzony do powszechnego stosowania przez upoważnioną
KONCEPCJA SYSTEMU JAKOŚCI zgodnie z wymaganiami norm ISO serii 9000 dr Lesław Lisak Co to jest norma? Norma to dokument przyjęty na zasadzie konsensu i zatwierdzony do powszechnego stosowania przez upoważnioną
Praca Poglądowa Zdr Publ 2009;119(1):99-104 Review Article
 Praca Poglądowa Zdr Publ 2009;119(1):99-104 Review Article REGINA BOREK-WOJCIECHOWSKA, SYLWIA KŁOKOW Oznakowanie jako niezbędny wymóg swobodnego obrotu i używania wyrobów medycznych marking as a necessary
Praca Poglądowa Zdr Publ 2009;119(1):99-104 Review Article REGINA BOREK-WOJCIECHOWSKA, SYLWIA KŁOKOW Oznakowanie jako niezbędny wymóg swobodnego obrotu i używania wyrobów medycznych marking as a necessary
Ustawa o wyrobach medycznych
 Komentarz Ustawa o wyrobach medycznych z dnia 20 maja 2010 r. (Dz.U. Nr 107, poz. 679 ze zm.) (zm.: Dz.U. 2011, Nr 102, poz. 586, Nr 113, poz. 657) Spis treści Art. Rozdział 1. Przepisy ogólne............................
Komentarz Ustawa o wyrobach medycznych z dnia 20 maja 2010 r. (Dz.U. Nr 107, poz. 679 ze zm.) (zm.: Dz.U. 2011, Nr 102, poz. 586, Nr 113, poz. 657) Spis treści Art. Rozdział 1. Przepisy ogólne............................
Dyrektywa 90/385/EWG
 Dyrektywa 90/385/EWG Załącznik nr 1 Załącznik nr 1 Polskie Normy zharmonizowane opublikowane do 31.12.2013 Wykaz norm z dyrektywy znajduje się również na www.pkn.pl Według Dziennika Urzędowego UE (20013/C
Dyrektywa 90/385/EWG Załącznik nr 1 Załącznik nr 1 Polskie Normy zharmonizowane opublikowane do 31.12.2013 Wykaz norm z dyrektywy znajduje się również na www.pkn.pl Według Dziennika Urzędowego UE (20013/C
KOMERCJALIZACJA PROJEKTU WYROBU MEDYCZNEGO NA RYNKU W KONTEKŚCIE PRZEPISÓW PRAWA
 KOMERCJALIZACJA PROJEKTU WYROBU MEDYCZNEGO NA RYNKU W KONTEKŚCIE PRZEPISÓW PRAWA Adam Sobantka 28.06.2018 r. Przepisy odnoszące się do wyrobów medycznych Ustawa z dnia 20 maja 2010 r. o wyrobach medycznych
KOMERCJALIZACJA PROJEKTU WYROBU MEDYCZNEGO NA RYNKU W KONTEKŚCIE PRZEPISÓW PRAWA Adam Sobantka 28.06.2018 r. Przepisy odnoszące się do wyrobów medycznych Ustawa z dnia 20 maja 2010 r. o wyrobach medycznych
USTAWA. z dnia 20 maja 2010 r. o wyrobach medycznych. (Dz. U. z dnia 17 czerwca 2010 r.) Rozdział 1. Przepisy ogólne
 Dz.U.2010.107.679 2012.01.01 zm. Dz.U.2011.113.657 art. 52 USTAWA z dnia 20 maja 2010 r. 1), 2) o wyrobach medycznych (Dz. U. z dnia 17 czerwca 2010 r.) Rozdział 1 Przepisy ogólne Art. 1. Ustawa określa:
Dz.U.2010.107.679 2012.01.01 zm. Dz.U.2011.113.657 art. 52 USTAWA z dnia 20 maja 2010 r. 1), 2) o wyrobach medycznych (Dz. U. z dnia 17 czerwca 2010 r.) Rozdział 1 Przepisy ogólne Art. 1. Ustawa określa:
USTAWA. z dnia 20 maja 2010 r. o wyrobach medycznych. Rozdział 1. Przepisy ogólne
 LexPolonica nr 2289766. Stan prawny 2014-10-30 Dz.U.2010.107.679 (U) Wyroby medyczne USTAWA z dnia 20 maja 2010 r. o wyrobach medycznych Rozdział 1 Przepisy ogólne Art. 1. Ustawa określa: 1) zasady wprowadzania
LexPolonica nr 2289766. Stan prawny 2014-10-30 Dz.U.2010.107.679 (U) Wyroby medyczne USTAWA z dnia 20 maja 2010 r. o wyrobach medycznych Rozdział 1 Przepisy ogólne Art. 1. Ustawa określa: 1) zasady wprowadzania
(Informacje) INFORMACJE INSTYTUCJI, ORGANÓW I JEDNOSTEK ORGANIZACYJNYCH UNII EUROPEJSKIEJ KOMISJA EUROPEJSKA
 30.8.2012 Dziennik Urzędowy Unii Europejskiej C 262/1 IV (Informacje) INFORMACJE INSTYTUCJI, ORGANÓW I JEDNOSTEK ORGANIZACYJNYCH UNII EUROPEJSKIEJ KOMISJA EUROPEJSKA Komunikat Komisji w ramach wdrażania
30.8.2012 Dziennik Urzędowy Unii Europejskiej C 262/1 IV (Informacje) INFORMACJE INSTYTUCJI, ORGANÓW I JEDNOSTEK ORGANIZACYJNYCH UNII EUROPEJSKIEJ KOMISJA EUROPEJSKA Komunikat Komisji w ramach wdrażania
Tekst pierwotny: Dz.U.2010.107.679. Wersja z dnia: 2014-12-02 USTAWA z dnia 20 maja 2010 r. o wyrobach medycznych (1)(2)
 Tekst pierwotny: Dz.U.2010.107.679 Wersja z dnia: 2014-12-02 USTAWA z dnia 20 maja 2010 r. o wyrobach medycznych (1)(2) Poprzednia zmiana: 2012-01-01 przez Dz.U.2011.113.657 art. 52 Następna zmiana: 2015-01-01
Tekst pierwotny: Dz.U.2010.107.679 Wersja z dnia: 2014-12-02 USTAWA z dnia 20 maja 2010 r. o wyrobach medycznych (1)(2) Poprzednia zmiana: 2012-01-01 przez Dz.U.2011.113.657 art. 52 Następna zmiana: 2015-01-01
Zmiany normalizacyjne w obszarze bezpieczeństwa przeciwwybuchowego. mgr inż. Wojciech Kwiatkowski
 Zmiany normalizacyjne w obszarze bezpieczeństwa przeciwwybuchowego mgr inż. Wojciech Kwiatkowski 1 Polski Komitet Normalizacyjny 1994- Polski Komitet Normalizacyjny (PKN) - Ustawa o normalizacji z dnia
Zmiany normalizacyjne w obszarze bezpieczeństwa przeciwwybuchowego mgr inż. Wojciech Kwiatkowski 1 Polski Komitet Normalizacyjny 1994- Polski Komitet Normalizacyjny (PKN) - Ustawa o normalizacji z dnia
REGULACJE PRAWNE W ZAKRESIE UŻYTKOWANIA WYROBÓW MEDYCZNYCH. Małgorzata Nowicka
 REGULACJE PRAWNE W ZAKRESIE UŻYTKOWANIA WYROBÓW MEDYCZNYCH Małgorzata Nowicka Regulacje prawne w zakresie użytkowania wyrobów medycznych znajdują się w trzech aktach prawnych: Ustawa o wyrobach medycznych
REGULACJE PRAWNE W ZAKRESIE UŻYTKOWANIA WYROBÓW MEDYCZNYCH Małgorzata Nowicka Regulacje prawne w zakresie użytkowania wyrobów medycznych znajdują się w trzech aktach prawnych: Ustawa o wyrobach medycznych
o rządowym projekcie ustawy o uchyleniu ustawy o wyrobach stosowanych w medycynie weterynaryjnej oraz o zmianie innych ustaw (druk nr 2732).
 SEJM RZECZYPOSPOLITEJ POLSKIEJ VI kadencja Druk nr 2790 S P R A W O Z D A N I E KOMISJI ROLNICTWA I ROZWOJU WSI ORAZ KOMISJI ZDROWIA o rządowym projekcie ustawy o uchyleniu ustawy o wyrobach stosowanych
SEJM RZECZYPOSPOLITEJ POLSKIEJ VI kadencja Druk nr 2790 S P R A W O Z D A N I E KOMISJI ROLNICTWA I ROZWOJU WSI ORAZ KOMISJI ZDROWIA o rządowym projekcie ustawy o uchyleniu ustawy o wyrobach stosowanych
ZKP gwarancją jakości
 dr inż. Jadwiga Szuba Zielonogórskie Kopalnie Surowców Mineralnych S.A. gwarancją jakości kruszyw dla ich użytkowników Państwa członkowskie Unii Europejskiej zobowiązane są do stosowania ujednoliconych
dr inż. Jadwiga Szuba Zielonogórskie Kopalnie Surowców Mineralnych S.A. gwarancją jakości kruszyw dla ich użytkowników Państwa członkowskie Unii Europejskiej zobowiązane są do stosowania ujednoliconych
USTAWA z dnia 20 kwietnia 2004 r. o wyposażeniu morskim 1)
 Kancelaria Sejmu s. 1/9 USTAWA z dnia 20 kwietnia 2004 r. o wyposażeniu morskim 1) Art. 1. 1. Ustawa określa szczegółowe zasady: 1) funkcjonowania systemu oceny zgodności z wymaganiami dotyczącymi wyposażenia
Kancelaria Sejmu s. 1/9 USTAWA z dnia 20 kwietnia 2004 r. o wyposażeniu morskim 1) Art. 1. 1. Ustawa określa szczegółowe zasady: 1) funkcjonowania systemu oceny zgodności z wymaganiami dotyczącymi wyposażenia
(Informacje) INFORMACJE INSTYTUCJI, ORGANÓW I JEDNOSTEK ORGANIZACYJNYCH UNII EUROPEJSKIEJ KOMISJA EUROPEJSKA
 27.4.2012 Dziennik Urzędowy Unii Europejskiej C 123/1 IV (Informacje) INFORMACJE INSTYTUCJI, ORGANÓW I JEDNOSTEK ORGANIZACYJNYCH UNII EUROPEJSKIEJ KOMISJA EUROPEJSKA Komunikat Komisji w ramach wdrażania
27.4.2012 Dziennik Urzędowy Unii Europejskiej C 123/1 IV (Informacje) INFORMACJE INSTYTUCJI, ORGANÓW I JEDNOSTEK ORGANIZACYJNYCH UNII EUROPEJSKIEJ KOMISJA EUROPEJSKA Komunikat Komisji w ramach wdrażania
Warszawa, dnia 7 czerwca 2017 r. Poz ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 6 czerwca 2017 r.
 DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ Warszawa, dnia 7 czerwca 2017 r. Poz. 1104 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 6 czerwca 2017 r. w sprawie niepowtarzalnego oznakowania, sposobu oznaczania
DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ Warszawa, dnia 7 czerwca 2017 r. Poz. 1104 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 6 czerwca 2017 r. w sprawie niepowtarzalnego oznakowania, sposobu oznaczania
Obowiązuje od r. USTAWA z dnia 27 lipca 2001 r. o Urzędzie Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych
 Kancelaria Sejmu s. 1/5 Obowiązuje od 1.01.2002 r. USTAWA z dnia 27 lipca 2001 r. o Urzędzie Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych Opracowano na podstawie: Dz.U.
Kancelaria Sejmu s. 1/5 Obowiązuje od 1.01.2002 r. USTAWA z dnia 27 lipca 2001 r. o Urzędzie Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych Opracowano na podstawie: Dz.U.
ROZPORZĄDZENIE PARLAMENTU EUROPEJSKIEGO I RADY (WE) NR 2232/96. z dnia 28 października 1996 r.
 Dz.U.UE.L.96.299.1 Dz.U.UE-sp.13-18-42 ROZPORZĄDZENIE PARLAMENTU EUROPEJSKIEGO I RADY (WE) NR 2232/96 z dnia 28 października 1996 r. ustanawiające wspólnotową procedurę dla substancji aromatycznych używanych
Dz.U.UE.L.96.299.1 Dz.U.UE-sp.13-18-42 ROZPORZĄDZENIE PARLAMENTU EUROPEJSKIEGO I RADY (WE) NR 2232/96 z dnia 28 października 1996 r. ustanawiające wspólnotową procedurę dla substancji aromatycznych używanych
Spis treści. Przedmowa...
 Przedmowa............................................. Wykaz skrótów.......................................... XIII Wykaz literatury......................................... XVII Komentarz............................................
Przedmowa............................................. Wykaz skrótów.......................................... XIII Wykaz literatury......................................... XVII Komentarz............................................
PL Dziennik Urzędowy Unii Europejskiej. 13/t. 12. DYREKTYWA RADY 93/42/EWG z dnia 14 czerwca 1993 r. dotycząca wyrobów medycznych
 82 31993L0042 12.7.1993 DZIENNIK URZĘDOWY WSPÓLNOT EUROPEJSKICH L169/1 DYREKTYWA RADY 93/42/EWG z dnia 14 czerwca 1993 r. dotycząca wyrobów medycznych RADA WSPÓLNOT EUROPEJSKICH, uwzględniając Traktat
82 31993L0042 12.7.1993 DZIENNIK URZĘDOWY WSPÓLNOT EUROPEJSKICH L169/1 DYREKTYWA RADY 93/42/EWG z dnia 14 czerwca 1993 r. dotycząca wyrobów medycznych RADA WSPÓLNOT EUROPEJSKICH, uwzględniając Traktat
Zasady wprowadzania wyrobów medycznych do obrotu i dystrybucji na terenie Rzeczypospolitej Polskiej w świetle nowej ustawy o wyrobach medycznych
 Zasady wprowadzania wyrobów medycznych do obrotu i dystrybucji na terenie Rzeczypospolitej Polskiej w świetle nowej ustawy o wyrobach medycznych The rules of introducing medical devices into marketing
Zasady wprowadzania wyrobów medycznych do obrotu i dystrybucji na terenie Rzeczypospolitej Polskiej w świetle nowej ustawy o wyrobach medycznych The rules of introducing medical devices into marketing
Dz.U Nr 107 poz. 679
 Dz.U. 2010 Nr 107 poz. 679 tj. Dz.U. 2017 poz. 211 OBWIESZCZENIE MARSZAŁKA SEJMU RZEC ZYPOSPOLITEJ POLSKIEJ z dnia 17 stycznia 2017 r. w sprawie ogłoszenia jednolitego tekstu ustawy o wyrobach medycznych
Dz.U. 2010 Nr 107 poz. 679 tj. Dz.U. 2017 poz. 211 OBWIESZCZENIE MARSZAŁKA SEJMU RZEC ZYPOSPOLITEJ POLSKIEJ z dnia 17 stycznia 2017 r. w sprawie ogłoszenia jednolitego tekstu ustawy o wyrobach medycznych
USTAWA z dnia 30 października 2003 r. o zmianie ustawy o kosmetykach
 Kancelaria Sejmu s. 1/5 USTAWA z dnia 30 października 2003 r. o zmianie ustawy o kosmetykach Opracowano na podstawie: Dz.U. z 2003 r. Nr 208, poz. 2019. Art. 1. W ustawie z dnia 30 marca 2001 r. o kosmetykach
Kancelaria Sejmu s. 1/5 USTAWA z dnia 30 października 2003 r. o zmianie ustawy o kosmetykach Opracowano na podstawie: Dz.U. z 2003 r. Nr 208, poz. 2019. Art. 1. W ustawie z dnia 30 marca 2001 r. o kosmetykach
P6_TA-PROV(2005)0329 Ochrona zdrowia i bezpieczeństwo pracy: narażenie pracowników na promieniowanie optyczne ***II
 P6_TA-PROV(2005)0329 Ochrona zdrowia i bezpieczeństwo pracy: narażenie pracowników na promieniowanie optyczne ***II Rezolucja legislacyjna Parlamentu Europejskiego w sprawie wspólnego stanowiska Rady mającego
P6_TA-PROV(2005)0329 Ochrona zdrowia i bezpieczeństwo pracy: narażenie pracowników na promieniowanie optyczne ***II Rezolucja legislacyjna Parlamentu Europejskiego w sprawie wspólnego stanowiska Rady mającego
USTAWA z dnia 6 września 2001 r.
 Kancelaria Sejmu s. 1/9 USTAWA z dnia 6 września 2001 r. Opracowano na podstawie: Dz.U. z 2001 r. Nr 126, poz. 1382. Przepisy wprowadzające ustawę - Prawo farmaceutyczne, ustawę o wyrobach medycznych oraz
Kancelaria Sejmu s. 1/9 USTAWA z dnia 6 września 2001 r. Opracowano na podstawie: Dz.U. z 2001 r. Nr 126, poz. 1382. Przepisy wprowadzające ustawę - Prawo farmaceutyczne, ustawę o wyrobach medycznych oraz
Warszawa, dnia 6 grudnia 2016 r. Poz ROZPORZĄDZENIE MINISTRA INFRASTRUKTURY I BUDOWNICTWA 1) z dnia 17 listopada 2016 r.
 DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ Warszawa, dnia 6 grudnia 2016 r. Poz. 1968 ROZPORZĄDZENIE MINISTRA INFRASTRUKTURY I BUDOWNICTWA 1) z dnia 17 listopada 2016 r. w sprawie krajowych ocen technicznych
DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ Warszawa, dnia 6 grudnia 2016 r. Poz. 1968 ROZPORZĄDZENIE MINISTRA INFRASTRUKTURY I BUDOWNICTWA 1) z dnia 17 listopada 2016 r. w sprawie krajowych ocen technicznych
WZÓR WNIOSEK O WYDANIE POZWOLENIA NA PROWADZENIE BADANIA KLINICZNEGO / WNIOSEK O WYDANIE OPINII PRZEZ KOMISJĘ BIOETYCZNĄ O BADANIU KLINICZNYM
 Załączniki do rozporządzenia Ministra Zdrowia z dnia 17 lutego 2016 r. (poz. 208) Załącznik nr 1 WZÓR WNIOSEK O WYDANIE POZWOLENIA NA PROWADZENIE BADANIA KLINICZNEGO / WNIOSEK O WYDANIE OPINII PRZEZ KOMISJĘ
Załączniki do rozporządzenia Ministra Zdrowia z dnia 17 lutego 2016 r. (poz. 208) Załącznik nr 1 WZÓR WNIOSEK O WYDANIE POZWOLENIA NA PROWADZENIE BADANIA KLINICZNEGO / WNIOSEK O WYDANIE OPINII PRZEZ KOMISJĘ
Wyroby budowlane wprowadzone do obrotu w świetle obowiązujących przepisów.
 Wyroby budowlane wprowadzone do obrotu w świetle obowiązujących przepisów. Wyroby budowlane w świetle ustawy Prawo Budowlane Art. 10 Stosownie do postanowień art. 10 ustawy z dnia 7 lipca 1994r. Prawo
Wyroby budowlane wprowadzone do obrotu w świetle obowiązujących przepisów. Wyroby budowlane w świetle ustawy Prawo Budowlane Art. 10 Stosownie do postanowień art. 10 ustawy z dnia 7 lipca 1994r. Prawo
(Publikacja tytułów i odniesień do norm zharmonizowanych na mocy prawodawstwa harmonizacyjnego Unii) (Tekst mający znaczenie dla EOG) (2016/C 173/02)
 C 173/92 PL Dziennik Urzędowy Unii Europejskiej 13.5.2016 Komunikat Komisji w ramach wdrażania dyrektywy Rady 90/385/EWG w sprawie zbliżenia ustawodawstw państw członkowskich odnoszących się do wyrobów
C 173/92 PL Dziennik Urzędowy Unii Europejskiej 13.5.2016 Komunikat Komisji w ramach wdrażania dyrektywy Rady 90/385/EWG w sprawie zbliżenia ustawodawstw państw członkowskich odnoszących się do wyrobów
DYREKTYWA RADY 93/42/EWG. z dnia 14 czerwca 1993 r. dotycząca wyrobów medycznych
 DYREKTYWA RADY 93/42/EWG z dnia 14 czerwca 1993 r. dotycząca wyrobów medycznych RADA WSPÓLNOT EUROPEJSKICH, uwzględniając Traktat ustanawiający Europejską Wspólnotę Gospodarczą, w szczególności jego art.
DYREKTYWA RADY 93/42/EWG z dnia 14 czerwca 1993 r. dotycząca wyrobów medycznych RADA WSPÓLNOT EUROPEJSKICH, uwzględniając Traktat ustanawiający Europejską Wspólnotę Gospodarczą, w szczególności jego art.
System zarządzania jakością w przedsiębiorstwach wytwarzających wyroby medyczne
 Zeszyty Naukowe nr 653 Akademii Ekonomicznej w Krakowie 2004 Katedra Towaroznawstwa Ogólnego i Zarządzania Jakością System zarządzania jakością w przedsiębiorstwach wytwarzających wyroby medyczne 1. Wprowadzenie
Zeszyty Naukowe nr 653 Akademii Ekonomicznej w Krakowie 2004 Katedra Towaroznawstwa Ogólnego i Zarządzania Jakością System zarządzania jakością w przedsiębiorstwach wytwarzających wyroby medyczne 1. Wprowadzenie
(Publikacja tytułów i odniesień do norm zharmonizowanych na mocy prawodawstwa harmonizacyjnego Unii) (Tekst mający znaczenie dla EOG) (2017/C 389/02)
 C 389/22 PL Dziennik Urzędowy Unii Europejskiej 17.11.2017 Komunikat Komisji w ramach wdrażania dyrektywy Rady w sprawie zbliżenia ustawodawstw państw członkowskich odnoszących się do wyrobów medycznych
C 389/22 PL Dziennik Urzędowy Unii Europejskiej 17.11.2017 Komunikat Komisji w ramach wdrażania dyrektywy Rady w sprawie zbliżenia ustawodawstw państw członkowskich odnoszących się do wyrobów medycznych
Dyrektywa 2006/121/WE Parlamentu Europejskiego i Rady. z dnia 18 grudnia 2006 r.
 30.12.2006 PL Dziennik Urzędowy Unii Europejskiej L 396/795 Dyrektywa 2006/121/WE Parlamentu Europejskiego i Rady z dnia 18 grudnia 2006 r. zmieniająca dyrektywę Rady 67/548/EWG w sprawie zbliżenia przepisów
30.12.2006 PL Dziennik Urzędowy Unii Europejskiej L 396/795 Dyrektywa 2006/121/WE Parlamentu Europejskiego i Rady z dnia 18 grudnia 2006 r. zmieniająca dyrektywę Rady 67/548/EWG w sprawie zbliżenia przepisów
ROZPORZĄDZENIE KOMISJI (WE) NR 2023/2006. z dnia 22 grudnia 2006 r.
 Dz.U.UE.L.06.384.75 2008.04.17 zm. Dz.U.UE.L.2008.86.9 art. 15 ROZPORZĄDZENIE KOMISJI (WE) NR 2023/2006 z dnia 22 grudnia 2006 r. w sprawie dobrej praktyki produkcyjnej w odniesieniu do materiałów i wyrobów
Dz.U.UE.L.06.384.75 2008.04.17 zm. Dz.U.UE.L.2008.86.9 art. 15 ROZPORZĄDZENIE KOMISJI (WE) NR 2023/2006 z dnia 22 grudnia 2006 r. w sprawie dobrej praktyki produkcyjnej w odniesieniu do materiałów i wyrobów
(Dz.U. L 169 z , str. 1)
 1993L0042 PL 11.10.2007 005.002 1 Dokument ten służy wyłącznie do celów dokumentacyjnych i instytucje nie ponoszą żadnej odpowiedzialności za jego zawartość B DYREKTYWA RADY 93/42/EWG z dnia 14 czerwca
1993L0042 PL 11.10.2007 005.002 1 Dokument ten służy wyłącznie do celów dokumentacyjnych i instytucje nie ponoszą żadnej odpowiedzialności za jego zawartość B DYREKTYWA RADY 93/42/EWG z dnia 14 czerwca
Stare i nowe podejście legislacyjne do harmonizacji technicznej dla potrzeb wspólnego rynku w Unii Europejskiej
 Stare i nowe podejście legislacyjne do harmonizacji technicznej dla potrzeb wspólnego rynku w Unii Europejskiej Wojciech Rzepka Warszawa, 19 marca 2012 r. 1 1. Wprowadzenie - idea wspólnego rynku - fundamenty
Stare i nowe podejście legislacyjne do harmonizacji technicznej dla potrzeb wspólnego rynku w Unii Europejskiej Wojciech Rzepka Warszawa, 19 marca 2012 r. 1 1. Wprowadzenie - idea wspólnego rynku - fundamenty
(Tekst mający znaczenie dla EOG)
 1.6.2016 L 144/27 ROZPORZĄDZENIE KOMISJI (UE) 2016/863 z dnia 31 maja 2016 r. zmieniające załączniki VII i VIII do rozporządzenia (WE) nr 1907/2006 Parlamentu Europejskiego i Rady w sprawie rejestracji,
1.6.2016 L 144/27 ROZPORZĄDZENIE KOMISJI (UE) 2016/863 z dnia 31 maja 2016 r. zmieniające załączniki VII i VIII do rozporządzenia (WE) nr 1907/2006 Parlamentu Europejskiego i Rady w sprawie rejestracji,
upoważniony przedstawiciel, dokonał oceny zgodności i wydał na swoją wyłączną odpowiedzialność, krajową deklarację zgodności z Polską Normą wyrobu
 INFORMACJA GUNB Ustawa z dnia 13 czerwca 2013 r. o zmianie ustawy o wyrobach budowlanych oraz ustawy o systemie oceny zgodności (Dz. U. poz. 898) dostosowuje regulacje dotyczące wprowadzania do obrotu
INFORMACJA GUNB Ustawa z dnia 13 czerwca 2013 r. o zmianie ustawy o wyrobach budowlanych oraz ustawy o systemie oceny zgodności (Dz. U. poz. 898) dostosowuje regulacje dotyczące wprowadzania do obrotu
DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ
 DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ Warszawa, dnia 16 września 2016 r. Poz. 1488 OBWIESZCZENIE MINISTRA ZDROWIA z dnia 9 września 2016 r. w sprawie ogłoszenia jednolitego tekstu rozporządzenia Ministra
DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ Warszawa, dnia 16 września 2016 r. Poz. 1488 OBWIESZCZENIE MINISTRA ZDROWIA z dnia 9 września 2016 r. w sprawie ogłoszenia jednolitego tekstu rozporządzenia Ministra
ROZPORZĄDZENIE DELEGOWANE KOMISJI (UE) / z dnia r.
 KOMISJA EUROPEJSKA Bruksela, dnia 4.9.2017 r. C(2017) 5467 final ROZPORZĄDZENIE DELEGOWANE KOMISJI (UE) / z dnia 4.9.2017 r. ustanawiające naukowe kryteria określania właściwości zaburzających funkcjonowanie
KOMISJA EUROPEJSKA Bruksela, dnia 4.9.2017 r. C(2017) 5467 final ROZPORZĄDZENIE DELEGOWANE KOMISJI (UE) / z dnia 4.9.2017 r. ustanawiające naukowe kryteria określania właściwości zaburzających funkcjonowanie
ROZPORZĄDZENIE WYKONAWCZE KOMISJI (UE) NR
 24.11.2012 Dziennik Urzędowy Unii Europejskiej L 326/3 ROZPORZĄDZENIE WYKONAWCZE KOMISJI (UE) NR 1097/2012 z dnia 23 listopada 2012 r. zmieniające rozporządzenie (UE) nr 142/2011 w sprawie wykonania rozporządzenia
24.11.2012 Dziennik Urzędowy Unii Europejskiej L 326/3 ROZPORZĄDZENIE WYKONAWCZE KOMISJI (UE) NR 1097/2012 z dnia 23 listopada 2012 r. zmieniające rozporządzenie (UE) nr 142/2011 w sprawie wykonania rozporządzenia
ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 12 stycznia 2011 r.
 Dziennik Ustaw Nr 16 1261 Poz. 76 76 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 12 stycznia 2011 r. w sprawie wymagań zasadniczych oraz procedur oceny zgodności aktywnych wyrobów medycznych do implantacji
Dziennik Ustaw Nr 16 1261 Poz. 76 76 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 12 stycznia 2011 r. w sprawie wymagań zasadniczych oraz procedur oceny zgodności aktywnych wyrobów medycznych do implantacji
Projekt nowej ustawy o wyrobach medycznych
 Projekt nowej ustawy o wyrobach medycznych Dlaczego pojawia się nowa ustawa o wyrobach medycznych? Projekt Nowej ustawy o wyrobach medycznych pojawił się w związku z przyjęciem dwóch rozporządzeń unijnych.
Projekt nowej ustawy o wyrobach medycznych Dlaczego pojawia się nowa ustawa o wyrobach medycznych? Projekt Nowej ustawy o wyrobach medycznych pojawił się w związku z przyjęciem dwóch rozporządzeń unijnych.
Normy ISO serii 9000. www.greber.com.pl. Normy ISO serii 9000. Tomasz Greber (www.greber.com.pl) dr inż. Tomasz Greber. www.greber.com.
 Normy ISO serii 9000 dr inż. Tomasz Greber www.greber.com.pl www.greber.com.pl 1 Droga do jakości ISO 9001 Organizacja tradycyjna TQM/PNJ KAIZEN Organizacja jakościowa SIX SIGMA Ewolucja systemów jakości
Normy ISO serii 9000 dr inż. Tomasz Greber www.greber.com.pl www.greber.com.pl 1 Droga do jakości ISO 9001 Organizacja tradycyjna TQM/PNJ KAIZEN Organizacja jakościowa SIX SIGMA Ewolucja systemów jakości
IV VII VIII Tak było.. VIII
 IV VII VIII Tak było.. VIII Ogólnopolskie Seminarium SYGOS IX System gospodarowania substancjami chemicznymi i odpadami niebezpiecznymi szkołach wyższych i jednostkach badawczych - wymogi, regulacje prawne,
IV VII VIII Tak było.. VIII Ogólnopolskie Seminarium SYGOS IX System gospodarowania substancjami chemicznymi i odpadami niebezpiecznymi szkołach wyższych i jednostkach badawczych - wymogi, regulacje prawne,
Warszawa, dnia 19 lutego 2016 r. Poz. 208 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 17 lutego 2016 r.
 DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ Warszawa, dnia 19 lutego 2016 r. Poz. 208 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 17 lutego 2016 r. w sprawie wzorów wniosków związanych z badaniem klinicznym
DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ Warszawa, dnia 19 lutego 2016 r. Poz. 208 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 17 lutego 2016 r. w sprawie wzorów wniosków związanych z badaniem klinicznym
Obowiązki podmiotów gospodarczych, nowi uczestnicy łańcucha. Krzysztof Zawiślak Departament Bezpieczeństwa Gospodarczego.
 Obowiązki podmiotów gospodarczych, nowi uczestnicy łańcucha Krzysztof Zawiślak Departament Bezpieczeństwa Gospodarczego 1 Wspólne obowiązki w każdej z dyrektyw nowego podejścia DECYZJA PARLAMENTU EUROPEJSKIEGO
Obowiązki podmiotów gospodarczych, nowi uczestnicy łańcucha Krzysztof Zawiślak Departament Bezpieczeństwa Gospodarczego 1 Wspólne obowiązki w każdej z dyrektyw nowego podejścia DECYZJA PARLAMENTU EUROPEJSKIEGO
Artykuł 1. Lp. Tekst dyrektywy (tekst polski) Odniesienie w prawie polskim projekt ustawy z dnia 29.07.2009 1. Preambuła. nie wymaga transpozycji
 Tabela transpozycji dyrektywy 2007/47/WE Parlamentu Europejskiego i Rady z dnia 5 września 2007 zmieniającej dyrektywę Rady 90/385/EWG w sprawie zbliżenia ustawodawstw państw członkowskich odnoszących
Tabela transpozycji dyrektywy 2007/47/WE Parlamentu Europejskiego i Rady z dnia 5 września 2007 zmieniającej dyrektywę Rady 90/385/EWG w sprawie zbliżenia ustawodawstw państw członkowskich odnoszących
ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 18 października 2010 r. w sprawie sposobu dokonywania zgłoszeń i powiadomień dotyczących wyrobów
 1341 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 18 października 2010 r. w sprawie sposobu dokonywania zgłoszeń i powiadomień dotyczących wyrobów Na podstawie art. 65 ust. 2 ustawy z dnia 20 maja 2010 r.
1341 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 18 października 2010 r. w sprawie sposobu dokonywania zgłoszeń i powiadomień dotyczących wyrobów Na podstawie art. 65 ust. 2 ustawy z dnia 20 maja 2010 r.
USTAWA. z dnia 27 lipca 2001 r. (Dz. U. z dnia 31 października 2001 r.)
 Dz.U.01.126.1379 2002.10.01 zm. Dz.U.2002.152.1263 art. 1 2004.05.01 zm. Dz.U.2004.93.896 art. 88 2006.10.27 zm. Dz.U.2006.170.1217 art. 61 2007.05.01 zm. Dz.U.2007.75.492 art. 2 2009.03.24 zm. Dz.U.2008.227.1505
Dz.U.01.126.1379 2002.10.01 zm. Dz.U.2002.152.1263 art. 1 2004.05.01 zm. Dz.U.2004.93.896 art. 88 2006.10.27 zm. Dz.U.2006.170.1217 art. 61 2007.05.01 zm. Dz.U.2007.75.492 art. 2 2009.03.24 zm. Dz.U.2008.227.1505
Zarządzanie jakością, środowiskiem oraz bezpieczeństwem w praktyce gospodarczej. Maciej Urbaniak.
 Zarządzanie jakością, środowiskiem oraz bezpieczeństwem w praktyce gospodarczej. Maciej Urbaniak. Książka stanowi szerokie kompendium wiedzy z zakresu systemów zarządzania. Stanowić ona może cenną pomoc
Zarządzanie jakością, środowiskiem oraz bezpieczeństwem w praktyce gospodarczej. Maciej Urbaniak. Książka stanowi szerokie kompendium wiedzy z zakresu systemów zarządzania. Stanowić ona może cenną pomoc
Wniosek ROZPORZĄDZENIE RADY
 KOMISJA EUROPEJSKA Bruksela, dnia 19.1.2017 r. COM(2017) 23 final 2017/0010 (NLE) Wniosek ROZPORZĄDZENIE RADY zmieniające załącznik III do dyrektywy Parlamentu Europejskiego i Rady 2008/98/WE w odniesieniu
KOMISJA EUROPEJSKA Bruksela, dnia 19.1.2017 r. COM(2017) 23 final 2017/0010 (NLE) Wniosek ROZPORZĄDZENIE RADY zmieniające załącznik III do dyrektywy Parlamentu Europejskiego i Rady 2008/98/WE w odniesieniu
KONFERENCJA. Blok operacyjny i sterylizatornia partnerami w zarządzaniu jakością." USTAWY O WYROBACH MEDYCZNYCH, SZJ ORAZ
 KONFERENCJA Blok operacyjny i sterylizatornia partnerami w zarządzaniu jakością." KWALIFIKACJA SPRZĘTU I WYROBÓW MEDYCZNYCH W ŚWIETLE USTAWY O WYROBACH MEDYCZNYCH, SZJ ORAZ ROZPORZĄDZENIA W SPRAWIE WYMAGAŃ
KONFERENCJA Blok operacyjny i sterylizatornia partnerami w zarządzaniu jakością." KWALIFIKACJA SPRZĘTU I WYROBÓW MEDYCZNYCH W ŚWIETLE USTAWY O WYROBACH MEDYCZNYCH, SZJ ORAZ ROZPORZĄDZENIA W SPRAWIE WYMAGAŃ
PL Dziennik Urzędowy Unii Europejskiej. 13/t. 11
 200 31992R1768 2.7.1992 DZIENNIK URZĘDOWY WSPÓLNOT EUROPEJSKICH L182/1 ROZPORZĄDZENIE RADY (EWG) NR 1768/92 z dnia 18 czerwca 1992 r. dotyczące stworzenia dodatkowego świadectwa ochronnego dla produktów
200 31992R1768 2.7.1992 DZIENNIK URZĘDOWY WSPÓLNOT EUROPEJSKICH L182/1 ROZPORZĄDZENIE RADY (EWG) NR 1768/92 z dnia 18 czerwca 1992 r. dotyczące stworzenia dodatkowego świadectwa ochronnego dla produktów
Marek Trajdos Klub Paragraf 34 SBT
 Marek Trajdos Klub Paragraf 34 SBT 1. Dyrektywa maszynowa, a inne dyrektywy Wymagania zasadnicze dotyczą maszyn wprowadzanych do obrotu po raz pierwszy na terenie Europejskiego Obszaru Gospodarczego. Są
Marek Trajdos Klub Paragraf 34 SBT 1. Dyrektywa maszynowa, a inne dyrektywy Wymagania zasadnicze dotyczą maszyn wprowadzanych do obrotu po raz pierwszy na terenie Europejskiego Obszaru Gospodarczego. Są
(Dz.U. L 66 z , s. 26)
 1999L0004 PL 18.11.2013 003.001 1 Dokument ten służy wyłącznie do celów dokumentacyjnych i instytucje nie ponoszą żadnej odpowiedzialności za jego zawartość B DYREKTYWA 1999/4/WE PARLAMENTU EUROPEJSKIEGO
1999L0004 PL 18.11.2013 003.001 1 Dokument ten służy wyłącznie do celów dokumentacyjnych i instytucje nie ponoszą żadnej odpowiedzialności za jego zawartość B DYREKTYWA 1999/4/WE PARLAMENTU EUROPEJSKIEGO
Normy zharmonizowane z dyrektywą maszynową
 Normy zharmonizowane z dyrektywą maszynową Alicja Gach Dyrektor Wydziału Certyfikacji Polski Komitet Normalizacyjny 1 Normy zharmonizowane z dyrektywą 2006/42/WE W sektorze maszyn normy opracowują: - CEN
Normy zharmonizowane z dyrektywą maszynową Alicja Gach Dyrektor Wydziału Certyfikacji Polski Komitet Normalizacyjny 1 Normy zharmonizowane z dyrektywą 2006/42/WE W sektorze maszyn normy opracowują: - CEN
Rada Unii Europejskiej Bruksela, 26 lipca 2017 r. (OR. en)
 Rada Unii Europejskiej Bruksela, 26 lipca 2017 r. (OR. en) 11526/17 PISMO PRZEWODNIE Od: Komisja Europejska Data otrzymania: 24 lipca 2017 r. Do: Nr dok. Kom.: D050725/02 Dotyczy: Sekretariat Generalny
Rada Unii Europejskiej Bruksela, 26 lipca 2017 r. (OR. en) 11526/17 PISMO PRZEWODNIE Od: Komisja Europejska Data otrzymania: 24 lipca 2017 r. Do: Nr dok. Kom.: D050725/02 Dotyczy: Sekretariat Generalny
USTAWA z dnia 13 czerwca 2013 r. o zmianie ustawy o wyrobach budowlanych oraz ustawy o systemie oceny zgodności 1)
 Kancelaria Sejmu s. 1/5 USTAWA z dnia 13 czerwca 2013 r. Opracowano na podstawie: Dz. U. z 2013 r. poz. 898. o zmianie ustawy o wyrobach budowlanych oraz ustawy o systemie oceny zgodności 1) Art. 1. W
Kancelaria Sejmu s. 1/5 USTAWA z dnia 13 czerwca 2013 r. Opracowano na podstawie: Dz. U. z 2013 r. poz. 898. o zmianie ustawy o wyrobach budowlanych oraz ustawy o systemie oceny zgodności 1) Art. 1. W
PLAN DZIAŁANIA KT 283 ds. Materiałów Stomatologicznych
 Strona 1 PLAN DZIAŁANIA KT 283 ds. Materiałów Stomatologicznych STRESZCZENIE Zadaniem Komitetu Technicznego 283 ds. Materiałów Stomatologicznych powołanego w ramach Polskiego Komitetu Normalizacyjnego
Strona 1 PLAN DZIAŁANIA KT 283 ds. Materiałów Stomatologicznych STRESZCZENIE Zadaniem Komitetu Technicznego 283 ds. Materiałów Stomatologicznych powołanego w ramach Polskiego Komitetu Normalizacyjnego
Normy a prawo. Dr inż. Grażyna Ożarek. UKSW, Warszawa, Listopad 2015 mgr Artur Staśkiewicz
 Normy a prawo Dr inż. Grażyna Ożarek UKSW, Warszawa, Listopad 2015 mgr Artur Staśkiewicz Projekt Badawczo- Rozwojowy realizowany na rzecz bezpieczeństwa i obronności Państwa współfinansowany ze środków
Normy a prawo Dr inż. Grażyna Ożarek UKSW, Warszawa, Listopad 2015 mgr Artur Staśkiewicz Projekt Badawczo- Rozwojowy realizowany na rzecz bezpieczeństwa i obronności Państwa współfinansowany ze środków
UWARUNKOWANIA PRAWNE W OBSZARZE TELEMEDYCYNY
 UWARUNKOWANIA PRAWNE W OBSZARZE TELEMEDYCYNY prof. n. dr hab. Dariusz Szostek QUO VADIS? Telemedycyna najbardziej rozwojowa dziedzina rozwoju informatyki edokumentacja Jeden z podstawowych celów Agendy
UWARUNKOWANIA PRAWNE W OBSZARZE TELEMEDYCYNY prof. n. dr hab. Dariusz Szostek QUO VADIS? Telemedycyna najbardziej rozwojowa dziedzina rozwoju informatyki edokumentacja Jeden z podstawowych celów Agendy
USTAWA. z dnia 6 września 2001 r.
 USTAWA z dnia 6 września 2001 r. Przepisy wprowadzające ustawę - Prawo farmaceutyczne, ustawę o wyrobach medycznych oraz ustawę o Urzędzie Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów
USTAWA z dnia 6 września 2001 r. Przepisy wprowadzające ustawę - Prawo farmaceutyczne, ustawę o wyrobach medycznych oraz ustawę o Urzędzie Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów
ROZPORZĄDZENIE MINISTRA ZDROWIA1)2)
 Dz.U.07.138.973 ROZPORZĄDZENIE MINISTRA ZDROWIA 1)2) z dnia 16 lipca 2007 r. w sprawie szczegółowych warunków pobierania, przechowywania i przeszczepiania komórek, tkanek i narządów Na podstawie art. 36
Dz.U.07.138.973 ROZPORZĄDZENIE MINISTRA ZDROWIA 1)2) z dnia 16 lipca 2007 r. w sprawie szczegółowych warunków pobierania, przechowywania i przeszczepiania komórek, tkanek i narządów Na podstawie art. 36
Wyroby budowlane Ocena zgodności a ocena właściwości użytkowych. mgr inż. Ewa Kozłowska Gdańsk, r.
 Wyroby budowlane Ocena zgodności a ocena właściwości użytkowych mgr inż. Ewa Kozłowska Gdańsk, 27.01.2017 r. Ważne definicje Producent to osoba fizyczna lub prawna albo jednostka organizacyjna nieposiadająca
Wyroby budowlane Ocena zgodności a ocena właściwości użytkowych mgr inż. Ewa Kozłowska Gdańsk, 27.01.2017 r. Ważne definicje Producent to osoba fizyczna lub prawna albo jednostka organizacyjna nieposiadająca
Projekt rozporządzenia Ministra Zdrowia. w sprawie sposobu i zakresu kontroli systemu monitorowania bezpieczeństwa stosowania produktów leczniczych
 Projekt rozporządzenia Ministra Zdrowia w sprawie sposobu i zakresu kontroli systemu monitorowania bezpieczeństwa stosowania produktów leczniczych Przekazany do uzgodnień zewnętrznych w dniu 26 kwietnia
Projekt rozporządzenia Ministra Zdrowia w sprawie sposobu i zakresu kontroli systemu monitorowania bezpieczeństwa stosowania produktów leczniczych Przekazany do uzgodnień zewnętrznych w dniu 26 kwietnia
DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ
 DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ Warszawa, dnia 24 czerwca 2015 r. Poz. 876 OBWIESZCZENIE MARSZAŁKA SEJMU RZECZYPOSPOLITEJ POLSKIEJ z dnia 26 maja 2015 r. w sprawie ogłoszenia jednolitego tekstu
DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ Warszawa, dnia 24 czerwca 2015 r. Poz. 876 OBWIESZCZENIE MARSZAŁKA SEJMU RZECZYPOSPOLITEJ POLSKIEJ z dnia 26 maja 2015 r. w sprawie ogłoszenia jednolitego tekstu
Dyrektywa 90/385/EWG WYKAZ POLSKICH NORM ZHARMONIZOWANYCH DYREKTYW A 90/385/EWG. Monitor Polski Nr Poz. 746
 Dyrektywa 90/385/EWG WYKAZ POLSKICH NORM ZHARMONIZOWANYCH DYREKTYW A 90/385/EWG Polskie Normy opublikowane do 30.06.2011 Wykaz norm z dyrektywy znajduje si równie na www.pkn.pl Na podstawie publikacji
Dyrektywa 90/385/EWG WYKAZ POLSKICH NORM ZHARMONIZOWANYCH DYREKTYW A 90/385/EWG Polskie Normy opublikowane do 30.06.2011 Wykaz norm z dyrektywy znajduje si równie na www.pkn.pl Na podstawie publikacji
o rządowym projekcie ustawy o wyposażeniu morskim (druk nr 2635)
 SEJM RZECZYPOSPOLITEJ POLSKIEJ Druk nr 2701 IV kadencja S P R A W O Z D A N I E KOMISJI EUROPEJSKIEJ o rządowym projekcie ustawy o wyposażeniu morskim (druk nr 2635) Marszałek Sejmu na podstawie art. 37
SEJM RZECZYPOSPOLITEJ POLSKIEJ Druk nr 2701 IV kadencja S P R A W O Z D A N I E KOMISJI EUROPEJSKIEJ o rządowym projekcie ustawy o wyposażeniu morskim (druk nr 2635) Marszałek Sejmu na podstawie art. 37
Ustawa prawo farmaceutyczne
 Ustawa prawo farmaceutyczne Ustawa z dnia 6 września 2001 r. Prawo farmaceutyczne. Ustawa opublikowana w Dzienniku Ustaw 2001 nr 126 poz. 1381. Tekst ujednolicony ustawy do pobrania w naszym dziale plików
Ustawa prawo farmaceutyczne Ustawa z dnia 6 września 2001 r. Prawo farmaceutyczne. Ustawa opublikowana w Dzienniku Ustaw 2001 nr 126 poz. 1381. Tekst ujednolicony ustawy do pobrania w naszym dziale plików
DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ
 DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ Warszawa, dnia 15 maja 2015 r. Poz. 675 USTAWA z dnia 20 marca 2015 r. o zmianie ustawy o substancjach chemicznych i ich mieszaninach 1) Art. 1. W ustawie z dnia
DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ Warszawa, dnia 15 maja 2015 r. Poz. 675 USTAWA z dnia 20 marca 2015 r. o zmianie ustawy o substancjach chemicznych i ich mieszaninach 1) Art. 1. W ustawie z dnia
Rozporządzenie CLP. Dr inż. Monika Wasiak-Gromek
 Rozporządzenie CLP Dr inż. Monika Wasiak-Gromek Title Rozporządzenie of the presentation CLP Date 23.04.13 # 2 Rozporządzenie CLP System GHS wdrożony został rozporządzeniem Parlamentu Europejskiego i Rady
Rozporządzenie CLP Dr inż. Monika Wasiak-Gromek Title Rozporządzenie of the presentation CLP Date 23.04.13 # 2 Rozporządzenie CLP System GHS wdrożony został rozporządzeniem Parlamentu Europejskiego i Rady
Dziennik Urzędowy Unii Europejskiej
 13/t. 19 PL Dziennik Urzędowy Unii Europejskiej 357 31997L0069 13.12.1997 DZIENNIK URZĘDOWY WSPÓLNOT EUROPEJSKICH L 343/19 DYREKTYWA KOMISJI 97/69/WE z dnia 5 grudnia 1997 r. dostosowująca po raz dwudziesty
13/t. 19 PL Dziennik Urzędowy Unii Europejskiej 357 31997L0069 13.12.1997 DZIENNIK URZĘDOWY WSPÓLNOT EUROPEJSKICH L 343/19 DYREKTYWA KOMISJI 97/69/WE z dnia 5 grudnia 1997 r. dostosowująca po raz dwudziesty
Rozdział 1 Przepisy ogólne
 Dz.U.04.195.2011 ROZPORZĄDZENIE MINISTRA INFRASTRUKTURY 1) z dnia 11 sierpnia 2004 r. w sprawie systemów oceny zgodności, wymagań, jakie powinny spełniać notyfikowane jednostki uczestniczące w ocenie zgodności,
Dz.U.04.195.2011 ROZPORZĄDZENIE MINISTRA INFRASTRUKTURY 1) z dnia 11 sierpnia 2004 r. w sprawie systemów oceny zgodności, wymagań, jakie powinny spełniać notyfikowane jednostki uczestniczące w ocenie zgodności,
DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ
 DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ Warszawa, dnia 19 listopada 2015 r. Poz. 1918 USTAWA z dnia 11 września 2015 r. 1), 2) o zmianie ustawy o wyrobach medycznych oraz niektórych innych ustaw Art.
DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ Warszawa, dnia 19 listopada 2015 r. Poz. 1918 USTAWA z dnia 11 września 2015 r. 1), 2) o zmianie ustawy o wyrobach medycznych oraz niektórych innych ustaw Art.
Leszek Oszczygiel Polska Izba Odzieżowo-Tekstylna Polish Federation of Apparel & Textiles
 Ocena systemu zgodności i wybrane zagadnienia dotyczące certyfikacji i standaryzacji (Conformity assessment and selected issues of certification and standardization) Opracowano na podstawie materiałów
Ocena systemu zgodności i wybrane zagadnienia dotyczące certyfikacji i standaryzacji (Conformity assessment and selected issues of certification and standardization) Opracowano na podstawie materiałów
Rozporządzenie Ministra Infrastruktury i Budownictwa w sprawie krajowych ocen technicznych
 Rozporządzenie Ministra Infrastruktury i Budownictwa w sprawie krajowych ocen technicznych z dnia 17 pobierz plik pdf do wydruku Rozporządzenie Ministra Infrastruktury i Budownictwa w sprawie krajowych
Rozporządzenie Ministra Infrastruktury i Budownictwa w sprawie krajowych ocen technicznych z dnia 17 pobierz plik pdf do wydruku Rozporządzenie Ministra Infrastruktury i Budownictwa w sprawie krajowych
