ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. Produkt leczniczy bez ważnego pozwolenia na dopuszczenie do obrotu
|
|
|
- Kinga Brzezińska
- 8 lat temu
- Przeglądów:
Transkrypt
1 ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1
2 1. NAZWA PRODUKTU LECZNICZEGO ImmunoGam 312 j.m./ml, roztwór do wstrzykiwań. 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każdy mililitr zawiera 312 j.m. immunoglobuliny ludzkiej przeciw wirusowi zapalenia wątroby typu B, co odpowiada zawartości białka wynoszącej mg/ml, w tym co najmniej 96% immunoglobuliny typu G (IgG). Jedna fiolka zwiera 312 j.m. przeciwciał anty-hbs w 1 ml Jedna fiolka zwiera 1560 j.m. przeciwciał anty-hbs w 5 ml Podklasy immunoglobulin IgG: IgG1: 64-67% IgG2: 25-27% IgG3: 7-9% IgG4: 0,1-0,3% Zawartość IgA jest mniejsza niż 40 mikrogramów/ml. Pełny wykaz substancji pomocniczych, patrz punkt POSTAĆ FARMACEUTYCZNA Roztwór do wstrzykiwań. Lek ImmunoGam jest przezroczystym lub lekko opalizującym, bezbarwnym lub jasnożółtym płynem. 4. SZCZEGÓŁOWE DANE KLINICZNE 4.1 Wskazania do stosowania Immunoprofilaktyka wirusowego zapalenia wątroby typu B - U pacjentów niezaszczepionych mających przypadkowy kontakt z wirusem (włącznie z osobami o szczepieniu niepełnym lub nieudokumentowanym). - U pacjentów hemodializowanych, dopóki szczepienie nie stanie się skuteczne. - U noworodków, których matki są nosicielkami wirusa zapalenia wątroby typu B. - U pacjentów niewykazujących odpowiedzi immunologicznej (brak mierzalnego poziomu przeciwciał przeciw wirusowi zapalenia wątroby typu B) po szczepieniu oraz pacjentów, u których niezbędna jest ciągła profilaktyka z powodu stałego zagrożenia zakażeniem wirusem zapalenia wątroby typu B. Należy również uwzględnić inne oficjalne zalecenia i wytyczne dotyczące właściwego stosowania immunoglobuliny ludzkiej przeciw wirusowi zapalenia wątroby typu B podawanej domięśniowo. 2
3 4.2 Dawkowanie i sposób podawania Dawkowanie - Zapobieganie wirusowemu zapaleniu wątroby typu B w razie przypadkowego kontaktu z wirusem u pacjentów niezaszczepionych: Co najmniej 500 j.m., w zależności od intensywności narażenia, jak najszybciej po narażeniu, najlepiej w ciągu godzin. - Immunoprofilaktyka wirusowego zapalenia wątroby typu B u pacjentów hemodializowanych: 8 12 j.m./kg, maksymalnie 500 j.m., co 2 miesiące, do czasu uzyskania serokonwersji po szczepieniu. - Zapobieganie wirusowemu zapaleniu wątroby typu B u noworodków, których matki są nosicielkami wirusa zapalenia wątroby typu B, zaraz po urodzeniu lub jak najszybciej po urodzeniu: j.m./kg. Podanie immunoglobuliny przeciw wirusowi zapalenia wątroby typu B może wymagać powtarzania do czasu uzyskania serokonwersji po szczepieniu. We wszystkich tych przypadkach zdecydowanie zaleca się szczepienie przeciw wirusowi zapalenia wątroby typu B. Pierwszą dawkę szczepionki można wstrzyknąć tego samego dnia co immunoglobulinę ludzką przeciw wirusowi zapalenia wątroby typu B, ale w inne miejsce. U pacjentów niewykazujących odpowiedzi immunologicznej (niemierzalny poziom przeciwciał przeciw wirusowi zapalenia wątroby typu B) po szczepieniu oraz u pacjentów, u których konieczna jest ciągła profilaktyka, można rozważyć podawanie 500 j.m. w przypadku dorosłych i 8 j.m./kg w przypadku dzieci co 2 miesiące, biorąc pod uwagę, że minimalne ochronne miano przeciwciał wynosi 10 mj.m./ml. Należy również uwzględniać dawki i schematy dawkowania dla immunoglobuliny ludzkiej przeciw wirusowi zapalenia wątroby typu B podawanej domięśniowo, zalecane w innych oficjalnych wytycznych. Sposób podawania ImmunoGam należy podawać domięśniowo. Jeżeli konieczne jest podanie dużej objętości produktu leczniczego (>2 ml u dzieci lub >5 ml u dorosłych), zaleca się podanie podzielonych dawek w różne miejsca. Jeżeli niezbędne jest jednoczesne szczepienie, immunoglobulinę i szczepionkę należy podać w dwa różne miejsca. Jeśli podanie domięśniowe jest przeciwwskazane (zaburzenia krzepnięcia), produkt można podać we wstrzyknięciu podskórnym, jeśli nie jest dostępny produkt leczniczy podawany dożylnie. Jednakże należy zwrócić uwagę, że nie ma danych klinicznych potwierdzających skuteczność podawania produktu drogą podskórną. 4.3 Przeciwwskazania Nadwrażliwość na którykolwiek ze składników. Nadwrażliwość na immunoglobuliny ludzkie, szczególnie w bardzo rzadkich przypadkach niedoboru IgA, gdy pacjent ma przeciwciała przeciw IgA. 3
4 4.4 Specjalne ostrzeżenia i środki ostrożności dotyczące stosowania Z uwagi na ryzyko wystąpienia wstrząsu należy upewnić się, że produkt ImmunoGam nie jest podawany do naczynia krwionośnego. Jeżeli biorca jest nosicielem HBsAg, podanie tego produktu leczniczego nie niesie ze sobą żadnych korzyści. Rzeczywiste reakcje nadwrażliwości występują rzadko. Lek ImmunoGam zawiera małą ilość IgA (poniżej 40 mikrogramów/ml). Osoby z niedoborem IgA mogą wytwarzać przeciwciała przeciw IgA i mogą wystąpić u nich reakcje anafilaktyczne po podaniu składników krwi zawierających IgA. Dlatego lekarz musi rozważyć korzyści wynikające z leczenia z zastosowaniem leku ImmunoGam z możliwym ryzykiem wystąpienia reakcji nadwrażliwości. W rzadkich przypadkach podanie immunoglobuliny ludzkiej przeciw wirusowi zapalenia wątroby typu B może spowodować spadek ciśnienia krwi z reakcją anafilaktyczną, nawet u tych pacjentów, którzy wcześniej tolerowali leczenie immunoglobulinami. W razie podejrzenia wystąpienia reakcji alergicznej lub anafilaktycznej należy natychmiast przerwać wstrzykiwanie. W przypadku wystąpienia wstrząsu należy zastosować powszechnie przyjęte postępowanie w terapii wstrząsu. Standardowe działania podejmowane w celu zapobiegania zakażeniom wynikającym ze stosowania produktów leczniczych przygotowywanych z ludzkiej krwi lub osocza obejmują selekcję dawców, badania przesiewowe indywidualnych pobrań i pul osocza w kierunku swoistych markerów zakażenia oraz wprowadzenie do procesu produkcji skutecznych etapów inaktywowania/usuwania wirusów. Mimo to, podając produkty lecznicze przygotowane z ludzkiej krwi lub osocza, nie można całkowicie wykluczyć możliwości przeniesienia czynników zakaźnych. Dotyczy to również nieznanych lub nowych wirusów i innych patogenów. Podejmowane działania uważa się za skuteczne w przypadku wirusów otoczkowych, takich jak HIV, HBV i HCV. Podejmowane działania mogą mieć ograniczoną wartość w przypadku wirusów bezotoczkowych, takich jak HAV i parwowirus B19. Coraz więcej doświadczeń klinicznych wskazuje na nieprzenoszenie wraz z immunoglobulinami wirusowego zapalenia wątroby typu A oraz parwowirusa B19. Ponadto uznaje się, że do zabezpieczenia przed wirusami w dużym stopniu przyczynia się skład przeciwciał. Zdecydowanie zaleca się, aby przy każdym podaniu pacjentowi produktu ImmunoGam zapisywać nazwę i numer serii produktu leczniczego, aby móc odtworzyć powiązanie pacjenta z serią produktu leczniczego. ImmunoGam zawiera 0,16 g maltozy w dawce 500 j.m. Należy to wziąć pod uwagę w przypadku pacjentów z cukrzycą. 4.5 Interakcje z innymi lekami i inne rodzaje interakcji Szczepionki zawierające żywe atenuowane wirusy Podanie immunoglobulin może wpływać na powstanie odpowiedzi immunologicznej na szczepionki zawierające żywe atenuowane wirusy, takie jak szczepionki przeciw różyczce, śwince, odrze i ospie wietrznej, przez okres 3 miesięcy. 4
5 Po podaniu tego produktu leczniczego należy zachować co najmniej 3 miesiące przerwy przed podaniem szczepionek zawierających żywe atenuowane wirusy. Immunoglobulinę ludzką przeciw wirusowi zapalenia wątroby typu B należy podać trzy do czterech tygodni po podaniu szczepionki zawierającej żywe atenuowane wirusy. W przypadku, gdy podanie immunoglobuliny ludzkiej przeciw wirusowi zapalenia wątroby typu B jest niezbędne przed upływem trzech do czterech tygodni po szczepieniu, ponowne szczepienie należy wykonać trzy miesiące po podaniu immunoglobuliny przeciw wirusowi zapalenia wątroby typu B. Wpływ na wyniki badań Badania serologiczne Po wstrzyknięciu immunoglobuliny przejściowy wzrost stężenia we krwi pacjenta różnych biernie przenoszonych przeciwciał może spowodować fałszywie dodatnie wyniki badań serologicznych. Pasywne przenoszenie przeciwciał przeciw antygenom erytrocytów, np. A, B, D może wpływać na niektóre badania serologiczne dla alloprzeciwciał krwinek czerwonych (np. test Coombsa). Badanie stężenia glukozy we krwi Niektóre rodzaje badań służących określaniu stężenia glukozy we krwi (na przykład wykorzystujące metody oparte na dehydrogenazie glukozowej-pirolochinolinochinonu (GDH-PQQ) lub glukozie-barwniku i oksydoreduktazie) fałszywie interpretują maltozę znajdującą się w produkcie ImmunoGam jako glukozę. Może to spowodować uzyskanie fałszywie zawyżonych odczytów stężenia glukozy i w konsekwencji niewłaściwe podawanie insuliny, prowadzące do zagrażającej życiu hipoglikemii. Ponadto przypadki rzeczywistej hipoglikemii mogą pozostać nierozpoznane i nieleczone, jeżeli stan hipoglikemii został zamaskowany fałszywie podwyższonymi odczytami stężenia glukozy. W związku z tym, podając ImmunoGam lub inne produkty do podawania pozajelitowego zawierające maltozę, pomiar stężenia glukozy we krwi należy przeprowadzić metodą swoistą dla glukozy. Należy dokładnie zapoznać się z informacjami dotyczącymi urządzeń do badania stężenia glukozy we krwi, włącznie z informacjami o paskach testowych, w celu ustalenia, czy urządzenie można stosować z produktami do podawania pozajelitowego zawierającymi maltozę. W przypadku wątpliwości należy skontaktować się z producentem urządzenia w celu ustalenia, czy można je stosować z produktami do podawania pozajelitowego zawierającymi maltozę. 4.6 Ciąża i laktacja Ciąża Bezpieczeństwo stosowania tego produktu leczniczego w czasie ciąży u ludzi nie zostało określone w kontrolowanych badaniach klinicznych. Obserwacje kliniczne związane ze stosowaniem immunoglobulin wskazują, iż nie należy spodziewać się występowania szkodliwego wpływu na przebieg ciąży, płód lub noworodka. Laktacja Immunoglobuliny są wydzielane do mleka matki, ale nie przypuszcza się, by wywierały szkodliwy wpływ na noworodka. 4.7 Wpływ na zdolność prowadzenia pojazdów mechanicznych i obsługiwania urządzeń mechanicznych w ruchu Nie stwierdzono wpływu na zdolność prowadzenia pojazdów mechanicznych i obsługiwania urządzeń mechanicznych w ruchu. 5
6 4.8 Działania niepożądane Na ogół w przypadku produktów zawierających immunoglobuliny mogą od czasu do czasu wystąpić działania niepożądane, takie jak dreszcze, ból głowy, gorączka, wymioty, reakcje alergiczne, nudności, ból stawów, niskie ciśnienie krwi i umiarkowany ból dolnej części kręgosłupa. Poniższa tabela zawiera działania niepożądane związane z podaniem produktu leczniczego ImmunoGam występujące w ciągu 7 dni od podania w badaniach klinicznych, w których stosowano podanie domięśniowe. Klasyfikacja układów i narządów wg konwencji MedDRA Zaburzenia układu nerwowego Zaburzenia naczyniowe Zaburzenia żołądka i jelit Zaburzenia mięśniowo-szkieletowe i tkanki łącznej Zaburzenia ogólne i stany w miejscu podania Ból głowy 6 Działania niepożądane Zawroty głowy Nudności Ból stawów, kręgosłupa i mięśni Zmęczenie, stwardnienie, złe samopoczucie, ból, gorączka Kategoria częstości ADR* Niezbyt często ( 1/1 000 do <1/100) Niezbyt często ( 1/1 000 do <1/100) Niezbyt często ( 1/1 000 do <1/100) Niezbyt często ( 1/1 000 do <1/100) Niezbyt często ( 1/1 000 do <1/100) * Częstość występowania określono z użyciem następujących kryteriów: bardzo często ( 1/10), często ( 1/100 do <1/10), niezbyt często ( 1/1 000 do <1/100). Dane uzyskane po wprowadzeniu produktu do obrotu: Po wprowadzeniu do obrotu produktu leczniczego ImmunoGam nie zgłaszano zdarzeń niepożądanych wynikających z jego stosowania w immunoprofilaktyce wirusowego zapalenia wątroby typu B. Informacje na temat bezpieczeństwa dotyczące czynników zakaźnych, patrz punkt Przedawkowanie Nie zgłoszono żadnego przypadku przedawkowania. 5. WŁAŚCIWOŚCI FARMAKOLOGICZNE 5.1 Właściwości farmakodynamiczne Grupa farmakoterapeutyczna: Immunoglobulina przeciw wirusowi zapalenia wątroby typu B, kod ATC: J06BB04 Immunoglobulina ludzka przeciw wirusowi zapalenia wątroby typu B zawiera głównie immunoglobulinę typu G (IgG) ze specyficznie dużą zawartością przeciwciał przeciw antygenowi powierzchniowemu wirusa zapalenia wątroby typu B (HBsAg).
7 5.2 Właściwości farmakokinetyczne Immunoglobulina ludzka przeciw wirusowi zapalenia wątroby typu B do podawania domięśniowego jest biologicznie dostępna w układzie krążenia biorcy po 2 3 dniach od podania. Okres połowicznej eliminacji produktu leczniczego ImmunoGam wynosi 3 4 tygodnie. Okres ten może różnić się u poszczególnych pacjentów. Immunoglobuliny IgG i kompleksy IgG ulegają rozpadowi w układzie siateczkowo-śródbłonkowym. 5.3 Przedkliniczne dane o bezpieczeństwie Immunoglobuliny są naturalnymi składnikami organizmu ludzkiego. Badania toksyczności ostrej u zwierząt nie mają znaczenia, gdyż większe dawki powodują przeciążenie krwiobiegu. Badania toksyczności wielokrotnej, embriotoksyczności i toksycznego wpływu na płód nie są w praktyce wykonywane z powodu indukcji przeciwciał i ich interferencji z produktem leczniczym. Nie badano działania produktu leczniczego na układ immunologiczny noworodków. 6. DANE FARMACEUTYCZNE 6.1 Wykaz substancji pomocniczych Maltoza Polisorbat Niezgodności farmaceutyczne Produktu leczniczego nie wolno mieszać z innymi lekami poza podanymi w punkcie Okres ważności 3 lata. 6.4 Specjalne środki ostrożności przy przechowywaniu Przechowywać w lodówce (od 2 C do 8 C). Nie zamrażać. Fiolkę należy przechowywać w zewnętrznym opakowaniu kartonowym w celu ochrony przed światłem. 6.5 Rodzaj i zawartość opakowania Produkt leczniczy ImmunoGam dostarczany jest w fiolkach szklanych typu 1, z korkiem z gumy bromobutylowej, aluminiową osłoną i plastikowym zamknięciem typu flip-off. 1 fiolka w opakowaniu. 7
8 6.6 Szczególne środki ostrożności dotyczące usuwania i przygotowania leku do stosowania Przed użyciem produkt leczniczy ImmunoGam powinien osiągnąć temperaturę pokojową (około 20ºC do 25ºC). Roztwór powinien być przezroczysty lub lekko opalizujący, bezbarwny lub jasnożółty. Nie wolno stosować roztworów mętnych lub zawierających osad. Wszelkie resztki niewykorzystanego produktu leczniczego lub jego odpady należy usunąć w sposób zgodny z lokalnymi przepisami. 7. PODMIOT ODPOWIEDZIALNY POSIADAJĄCY POZWOLENIE NA DOPUSZCZENIE DO OBROTU Cangene Europe Limited Parkshot House 5 Kew Road Richmond, Surrey TW9 2PR Wielka Brytania 8. NUMER(Y) POZWOLENIA(Ń) NA DOPUSZCZENIE DO OBROTU 9. DATA WYDANIA PIERWSZEGO POZWOLENIA NA DOPUSZCZENIE DO OBROTU/DATA PRZEDŁUŻENIA POZWOLENIA 10. DATA ZATWIERDZENIA LUB CZĘŚCIOWEJ ZMIANY TEKSTU CHARAKTERYSTYKI PRODUKTU LECZNICZEGO Szczegółowa informacja o tym produkcie leczniczym jest dostępna na stronie internetowej Europejskiej Agencji ds. Produktów Leczniczych: 8
9 ANEKS II A. WYTWÓRCA SUBSTANCJI BIOLOGICZNIE CZYNNEJ ORAZ WYTWÓRCA ODPOWIEDZIALNY ZA ZWOLNIENIE SERII B. WARUNKI POZWOLENIA NA DOPUSZCZENIE DO OBROTU 9
10 A. WYTWÓRCA SUBSTANCJI BIOLOGICZNIE CZYNNEJ ORAZ WYTWÓRCA ODPOWIEDZIALNY ZA ZWOLNIENIE SERII Nazwa i adres wytwórcy substancji biologicznie czynnej Cangene Corporation 155 Innovation Drive Winnipeg, Manitoba R3T 5Y3 Kanada Nazwa i adres wytwórcy odpowiedzialnego za zwolnienie serii Baxter S.A. Boulevard René Branquart, 80 B-7860 Lessines Belgia B. WARUNKI POZWOLENIA NA DOPUSZCZENIE DO OBROTU KATEGORIA DOSTĘPNOŚCI Produkt leczniczy wydawany na receptę. WARUNKI LUB OGRANICZENIA DOTYCZĄCE BEZPIECZNEGO I SKUTECZNEGO STOSOWANIA PRODUKTU LECZNICZEGO Nie dotyczy INNE WARUNKI System nadzoru nad bezpieczeństwem stosowania produktów leczniczych Podmiot odpowiedzialny musi zapewnić, że system nadzoru nad bezpieczeństwem stosowania produktów leczniczych, opisany w wersji 2.0 przedstawionej w Module wniosku o dopuszczenie do obrotu, jest zorganizowany i będzie prawidłowo funkcjonował przed i po dopuszczeniu produktu leczniczego do obrotu. Podmiot odpowiedzialny zobowiązuje się do przeprowadzenia badań i innych działań w zakresie nadzoru nad bezpieczeństwem stosowania produktów leczniczych, które zostały wyszczególnione w planie monitorowania bezpieczeństwa zgodnie z wersją 1.3 Planu Zarządzania Ryzykiem (RMP, ang. Risk Management Plan), przedstawioną w Module wniosku o dopuszczenie do obrotu i wszelkimi jego kolejnymi aktualizacjami uzgodnionymi z Komitetem ds. Produktów Leczniczych Stosowanych u Ludzi (CHMP, ang. Committee for Medicinal Products for Human Use). Zgodnie z Wytycznymi CHMP, dotyczącymi Systemów Zarządzania Ryzykiem dla produktów leczniczych stosowanych u ludzi, każdy uaktualniony RMP należy złożyć jednocześnie z kolejnym okresowym raportem o bezpieczeństwie (PSUR, ang. Periodic Safety Update Report). 10
11 Ponadto, uaktualniony RMP należy przedstawiać: jeśli uzyskano nowe informacje, które istotnie wpływają na aktualną specyfikację dotyczącą bezpieczeństwa, plan monitorowania bezpieczeństwa lub działania służące ograniczeniu ryzyka; w ciagu 60 dni od uzyskania istotnych informacji dotyczących bezpieczeństwa stosowania produktu leczniczego lub odnoszących się do minimalizacji ryzyka; na żądanie EMEA. Oficjalne zwolnienie serii: zgodnie z artykułem 114 Dyrektywy 2001/83/WE z poprawkami, seria zostanie oficjalnie zwolniona przez laboratorium państwowe lub przez laboratorium wyznaczone do tego celu. 11
12 ANEKS III OZNAKOWANIE OPAKOWAŃ I ULOTKA DLA PACJENTA 12
13 A. OZNAKOWANIE OPAKOWAŃ 13
14 INFORMACJE ZAMIESZCZANE NA OPAKOWANIACH ZEWNĘTRZNYCH OPAKOWANIE KARTONOWE 1. NAZWA PRODUKTU LECZNICZEGO ImmunoGam 312 j.m./ml, roztwór do wstrzykiwań Immunoglobulina ludzka przeciw wirusowi zapalenia wątroby typu B 2. ZAWARTOŚĆ SUBSTANCJI CZYNNEJ(YCH) Każdy mililitr zawiera 312 j.m. immunoglobuliny ludzkiej przeciw wirusowi zapalenia wątroby typu B, co odpowiada zawartości białka wynoszącej mg/ml, w tym co najmniej 96% immunoglobuliny typu G (IgG). Jedna fiolka o pojemności 1 ml zwiera 312 j.m. przeciwciał anty-hbs. Jedna fiolka o pojemności 5 ml zawiera 1560 j.m. przeciwciał anty-hbs. 3. WYKAZ SUBSTANCJI POMOCNICZYCH Substancje pomocnicze: Maltoza (dalsze informacje, patrz ulotka dla pacjenta) oraz polisorbat POSTAĆ FARMACEUTYCZNA I ZAWARTOŚĆ OPAKOWANIA Roztwór do wstrzykiwań 1 fiolka (312 j.m./1 ml) 1 fiolka (1560 j.m./5 ml) 5. SPOSÓB I DROGA(I) PODANIA Należy zapoznać się z treścią ulotki przed zastosowaniem leku. Do stosowania domięśniowego 6. OSTRZEŻENIE DOTYCZĄCE PRZECHOWYWANIA PRODUKTU LECZNICZEGO W MIEJSCU NIEDOSTĘPNYM I NIEWIDOCZNYM DLA DZIECI Przechowywać w miejscu niedostępnym i niewidocznym dla dzieci. 7. INNE OSTRZEŻENIA SPECJALNE, JEŚLI KONIECZNE 8. TERMIN WAŻNOŚCI Termin ważn.: 9. WARUNKI PRZECHOWYWANIA Przechowywać w lodówce (od 2 do 8 C). Nie zamrażać. 14
15 10. SPECJALNE ŚRODKI OSTROŻNOŚCI DOTYCZĄCE USUWANIA NIEZUŻYTEGO PRODUKTU LECZNICZEGO LUB POCHODZĄCYCH Z NIEGO ODPADÓW, JEŚLI WŁAŚCIWE 11. NAZWA I ADRES PODMIOTU ODPOWIEDZIALNEGO Cangene Europe Limited Parkshot House 5 Kew Road Richmond, Surrey TW9 2PR Wielka Brytania 12. NUMER(Y) POZWOLENIA(Ń) NA DOPUSZCZENIE DO OBROTU 13. NUMER SERII Seria nr: 14. KATEGORIA DOSTĘPNOŚCI Lek wydawany na receptę. 15. INSTRUKCJA UŻYCIA 16. INFORMACJA PODANA BRAJLEM [Zaakceptowano uzasadnienie braku podania informacji brajlem] 15
16 MINIMUM INFORMACJI ZAMIESZCZANYCH NA MAŁYCH OPAKOWANIACH BEZPOŚREDNICH OZNAKOWANIE FIOLKI 1. NAZWA PRODUKTU LECZNICZEGO I DROGA(I) PODANIA ImmunoGam 312 j.m./ml, roztwór do wstrzykiwań Immunoglobulina ludzka przeciw wirusowi zapalenia wątroby typu B IM 2. SPOSÓB PODAWANIA Należy zapoznać się z treścią ulotki przed zastosowaniem leku 3. TERMIN WAŻNOŚCI Termin ważn.: 4. NUMER SERII Seria nr: 5. ZAWARTOŚĆ OPAKOWANIA Z PODANIEM MASY, OBJĘTOŚCI LUB LICZBY JEDNOSTEK 312 j.m./1 ml 1560 j.m./5 ml 6. INNE Tu zostanie wstawione logo firmy Cangene 16
17 B. ULOTKA DLA PACJENTA 17
18 ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA ImmunoGam 312 j.m./ml, roztwór do wstrzykiwań Immunoglobulina ludzka przeciw wirusowi zapalenia wątroby typu B Należy zapoznać się z treścią ulotki przed zastosowaniem leku. - Należy zachować tę ulotkę, aby w razie potrzeby móc ją ponownie przeczytać. - Należy zwrócić się do lekarza, gdy potrzebna jest rada lub dodatkowa informacja. - Jeśli nasili się którykolwiek z objawów niepożądanych lub wystąpią jakiekolwiek objawy niepożądane niewymienione w ulotce, należy powiadomić lekarza. Spis treści ulotki: 1. Co to jest ImmunoGam i w jakim celu się go stosuje 2. Informacje ważne przed zastosowaniem leku ImmunoGam 3. Jak stosować ImmunoGam 4. Możliwe działania niepożądane 5. Jak przechowywać ImmunoGam 6. Inne informacje 1. CO TO JEST IMMUNOGAM I W JAKIM CELU SIĘ GO STOSUJE Co to jest ImmunoGam Lek ImmunoGam należy do grupy leków zawierających immunoglobuliny (przeciwciała, które mogą chronić przed pewnymi zakażeniami) obecne we krwi ludzkiej. Lek ImmunoGam zawiera podwyższone stężenia immunoglobulin ludzkich przeciw wirusowi zapalenia wątroby typu B, głównie immunoglobulinę typu G (IgG) i jest otrzymywany z osocza krwi dawców z USA, poddanych badaniom przesiewowym. W jakim celu stosuje się ImmunoGam Lek ImmunoGam zapewnia ochronę przed wirusem zapalenia wątroby typu B przez krótki okres i jest stosowany w następujących przypadkach: - U pacjentów niezaszczepionych mających przypadkowy kontakt z wirusem (włącznie z osobami o szczepieniu niepełnym lub nieudokumentowanym). - U pacjentów hemodializowanych, dopóki szczepienie nie stanie się skuteczne. - U noworodków, których matki są nosicielkami wirusa zapalenia wątroby typu B. - U pacjentów niewykazujących odpowiedzi immunologicznej (przeciwciała przeciw wirusowi zapalenia wątroby typu B niemierzalne) po szczepieniu oraz u pacjentów, w przypadku których niezbędna jest ciągła profilaktyka z powodu stałego zagrożenia zakażeniem wirusem zapalenia wątroby typu B. 2. INFORMACJE WAŻNE PRZED ZASTOSOWANIEM LEKU IMMUNOGAM NIE wolno stosować leku ImmunoGam - jeżeli wcześniej wystąpiła reakcja alergiczna na immunoglobuliny ludzkie, inne produkty krwiopochodne lub którykolwiek składnik leku ImmunoGam. - jeżeli u pacjenta występuje niedobór IgA, powodujący wystąpienie reakcji alergicznej na produkty zawierające IgA. 18
19 Kiedy zachować szczególną ostrożność stosując lek ImmunoGam Ogólne ostrzeżenia związane z lekiem ImmunoGam: Na ogół immunoglobuliny mogą powodować działania niepożądane, takie jak dreszcze, ból głowy, gorączka, wymioty, reakcje alergiczne, nudności, artralgia (ból stawów), niskie ciśnienie krwi i umiarkowany ból dolnego odcinka kręgosłupa. Należy regularnie monitorować u pacjentów przeciwciała przeciw immunoglobulinie ludzkiej przeciw wirusowi zapalenia wątroby typu B. Podanie immunoglobuliny ludzkiej przeciw wirusowi zapalenia wątroby typu B może spowodować spadek ciśnienia krwi z reakcją alergiczną, nawet u tych pacjentów, którzy wcześniej tolerowali leczenie immunoglobulinami. W razie podejrzenia wystąpienia reakcji alergicznej lub anafilaktycznej należy natychmiast przerwać wstrzykiwanie. W przypadku wystąpienia wstrząsu należy zastosować powszechnie przyjęte postępowanie w terapii wstrząsu. Immunoglobulina A: Należy powiedzieć lekarzowi o braku immunoglobuliny typu A (IgA) we krwi. Lek ImmunoGam zawiera małe ilości IgA. U pacjentów z niedoborem IgA może wystąpić reakcja alergiczna na ten lek. Lek ImmunoGam zawiera maltozę (10% wagowo). Badania serologiczne ImmunoGam może powodować wzrost stężenia różnych przenoszonych przeciwciał, co może spowodować fałszywie dodatnie wyniki niektórych badań surowicy krwi. Również przeniesienie przeciwciał do antygenów grupy krwi może wpływać na wyniki pewnych badań krwi dla alloprzeciwciał krwinek czerwonych (np. test Coombsa). Badanie stężenia glukozy we krwi Badanie stężenia glukozy we krwi: podając lek ImmunoGam pomiar stężenia glukozy we krwi należy przeprowadzić metodą swoistą dla glukozy. Zalecenie to wynika z tego, że niektóre rodzaje urządzeń do pomiaru stężenia glukozy we krwi fałszywie interpretują maltozę znajdującą się w leku ImmunoGam jako glukozę. Może to spowodować fałszywie podwyższone odczyty stężenia glukozy i w konsekwencji niewłaściwe podanie insuliny, prowadzące do zagrażającej życiu hipoglikemii. Ponadto przypadki rzeczywistej hipoglikemii mogą pozostać nieleczone, jeżeli hipoglikemia zostałaby zamaskowana fałszywie podwyższonymi odczytami stężenia glukozy. Bezpieczeństwo wirusowe Jeżeli leki są wytwarzane z ludzkiej krwi lub osocza, podejmuje się szereg kroków w celu zapobiegania zakażeniom przekazywanym od dawców krwi do pacjentów. Obejmują one staranną selekcję dawców krwi lub osocza w celu wykluczenia zagrożenia przeniesienia zakażenia oraz badanie każdej donacji i pul osocza w kierunku obecności wirusa/zakażenia. Wytwórcy tych produktów podejmują dodatkowe kroki w przetwarzaniu krwi i osocza, które mogą inaktywować lub usunąć wirusy. Pomimo tych środków, podając leki przygotowane z ludzkiej krwi lub osocza, nie można całkowicie wykluczyć możliwości przeniesienia zakażenia. Dotyczy to również wszelkich nieznanych lub nowo zagrażających wirusów czy innych rodzajów zakażeń. Podejmowane działania uważa się za skuteczne w przypadku wirusów otoczkowych, takich jak ludzki wirus niedoboru odporności (HIV), wirus zapalenia wątroby typu B i wirus zapalenia wątroby typu C. Podejmowane działania mogą mieć ograniczoną wartość w przypadku wirusów bezotoczkowych, takich jak wirus zapalenia wątroby typu A i parwowirus B19. Podawanie immunoglobulin nie jest wiązane z przypadkami zakażeń wirusem zapalenia wątroby typu A lub parwowirusem B19 być może również dlatego, że znajdujące się w produkcie przeciwciała przeciw tym zakażeniom wykazują działanie ochronne. 19
20 Zdecydowanie zaleca się, aby po każdym podaniu dawki leku ImmunoGam zapisać nazwę i numer serii produktu w karcie pacjenta w celu zachowania spisu zastosowanych serii. Stosowanie leku ImmunoGam z innymi lekami Należy powiedzieć lekarzowi lub pielęgniarce o wszystkich przyjmowanych ostatnio lekach, włącznie z tymi, które wydawane są bez recepty, np. o lekach ziołowych. Należy poinformować lekarza o planowanym przyjęciu szczepionki lub odbyciu szczepienia w minionych trzech miesiącach. Powodem jest fakt, że lek ImmunoGam może wpływać na odpowiedź na niektóre szczepionki atenuowane, takie jak szczepionki przeciw różyczce, śwince, odrze i ospie wietrznej. Nie ma dostępnych danych na temat interakcji leku ImmunoGam z innymi lekami. Ciąża i karmienie piersią Przed zastosowaniem tego leku należy poradzić się lekarza. Lekarz prowadzący zdecyduje, czy lek ImmunoGam może być stosowany w czasie ciąży i karmienia piersią. Prowadzenie pojazdów i obsługa maszyn Lek ImmunoGam nie wpływa na zdolność prowadzenia pojazdów mechanicznych i obsługiwania urządzeń mechanicznych w ruchu. Ważne informacje o niektórych składnikach leku ImmunoGam Lek ImmunoGam zawiera 0,16 g maltozy w dawce 500 j.m. Należy to wziąć pod uwagę w przypadku pacjentów z cukrzycą. 3. JAK STOSOWAĆ LEK IMMUNOGAM Wymagana ilość leku ImmunoGam zostanie ustalona przez lekarza lub pielęgniarkę. Poniższa tabela zawiera zalecane dawki. Zdecydowanie zaleca się szczepienie przeciw wirusowi zapalenia wątroby typu B. Pierwszą dawkę szczepionki można wstrzyknąć w tym samym dniu co immunoglobulinę ludzką przeciw wirusowi zapalenia wątroby typu B, ale w inne miejsce. Wskazanie Dawka Częstość podawania Zapobieganie wirusowemu zapaleniu wątroby typu B w razie przypadkowego kontaktu z wirusem u pacjentów niezaszczepionych Co najmniej 500 j.m. w zależności od intensywności kontaktu, jak najszybciej po kontakcie z wirusem, najlepiej w ciągu godzin. Immunoprofilaktyka wirusowego zapalenia wątroby typu B u pacjentów 8 12 j.m./kg, maksymalnie co 2 miesiące do czasu uzyskania serokonwersji po szczepieniu. hemodializowanych 500 j.m. Zapobieganie wirusowemu zapaleniu wątroby typu B u noworodków, których matki są nosicielkami wirusa zapalenia wątroby typu B, zaraz po urodzeniu lub jak najszybciej po urodzeniu j.m./kg Podanie immunoglobuliny przeciw wirusowi zapalenia wątroby typu B może wymagać powtarzania do czasu uzyskania serokonwersji po szczepieniu. Instrukcja użycia Przed użyciem lek ImmunoGam powinien osiągnąć temperaturę pokojową (około 20ºC do 25ºC). Roztwór powinien być przezroczysty lub lekko opalizujący, bezbarwny lub jasnożółty, zasadniczo pozbawiony obcych cząstek. Nie wolno stosować roztworów mętnych lub zawierających osad. W przypadku podania domięśniowego lek ImmunoGam należy wstrzyknąć do górnej części ramienia (mięsień naramienny), lub do prawej strony z przodu mięśnia uda (część przednio-boczna) noworodka. 20
21 Jeżeli konieczna jest podanie dużej objętości leku (powyżej 2 ml w przypadku dzieci lub powyżej 5 ml w przypadku dorosłych), zaleca się podanie leku ImmunoGam w dawkach podzielonych w różne miejsca. Jeżeli niezbędne jest jednoczesne szczepienie, immunoglobulinę i szczepionkę należy podać w dwa różne miejsca. Zastosowanie większej niż zalecana dawki leku ImmunoGam Nie ma dostępnych danych w przypadku przedawkowania. W przypadku podania domięśniowego leku ImmunoGam jedyną oznaką przedawkowania może być ból i tkliwość uciskowa w miejscu wstrzyknięcia. 4. MOŻLIWE DZIAŁANIA NIEPOŻĄDANE Jak każdy lek, ImmunoGam może powodować działania niepożądane, chociaż nie u każdego one wystąpią. Częstotliwość występowania możliwych działań niepożądanych wymienionych poniżej zdefiniowano według następujących kryteriów: - bardzo często (dotyczy więcej niż 1 na 10 pacjentów), - często (dotyczy od 1 do 10 pacjentów na 100), - niezbyt często (dotyczy od 1 do 10 pacjentów na 1 000), - rzadko (dotyczy od 1 do 10 pacjentów na ), - bardzo rzadko (dotyczy mniej niż 1 na pacjentów), - nieznane (częstość nie może być określona na podstawie dostępnych danych). Działania niepożądane zgłoszone w trakcie badań klinicznych leku ImmunoGam podawanego domięśniowo (wstrzykniętego do mięśnia) występowały niezbyt często (dotyczyły 1 do 10 pacjentów na 1 000). Następujące działania niepożądane zgłaszano w ciągu pierwszych 7 dni po przyjęciu leku ImmunoGam: nudności, zmęczenie, stwardnienie (obrzmienie i twardość) w miejscu wstrzyknięcia, złe samopoczucie, ból, gorączka, ból stawów, ból pleców, ból mięśni, ból głowy i zawroty głowy. Opisane poniżej działanie niepożądane może być poważne i było obserwowane sporadycznie. Reakcja alergiczna: Istnieje prawdopodobieństwo wystąpienia reakcji alergicznej po podaniu niniejszego leku. Należy natychmiast powiedzieć lekarzowi o wystąpieniu któregokolwiek z następujących objawów po otrzymaniu leku ImmunoGam: o pokrzywka, zaczerwieniona skóra lub wysypka, obrzęk określonego miejsca, takiego jak miejsce wstrzyknięcia lub twarz; o ucisk w klatce piersiowej, brak tchu, świszczący oddech; o szybkie przyspieszenie akcji serca, nagły spadek ciśnienia krwi i/lub wstrząs. Te objawy mogą być wczesnymi oznakami reakcji alergicznej. W zależności od rodzaju i stopnia ciężkości reakcji alergicznej, lekarz może zastosować dodatkowe leczenie lub podjąć decyzję o natychmiastowym przerwaniu wstrzykiwania. W przypadku podania domięśniowego może od czasu do czasu wystąpić pewien dyskomfort w miejscu wstrzyknięcia, taki jak miejscowy ból lub tkliwość uciskowa. U pacjentów z ciężką trombocytopenią lub jakimikolwiek zaburzeniami krzepnięcia, które mogą być przeciwwskazaniami do wstrzyknięć domięśniowych, lek ImmunoGam należy podać tylko wtedy, gdy spodziewane korzyści przeważają nad potencjalnymi zagrożeniami. Jeśli nasili się którekolwiek z działań niepożądanych wymienionych w tej ulotce lub wystąpią jakiekolwiek działania niepożądane niewymienione w tej ulotce, należy powiadomić lekarza, pielęgniarkę lub farmaceutę. 21
22 5. JAK PRZECHOWYWAĆ LEK IMMUNOGAM Przechowywać w miejscu niedostępnym i niewidocznym dla dzieci. Nie stosować leku ImmunoGam po upływie terminu ważności zamieszczonego na etykiecie i opakowaniu zewnętrznym. Termin ważności oznacza ostatni dzień danego miesiąca. Przechowywać w lodówce (od 2 do 8 C). Nie zamrażać. Fiolkę należy przechowywać w zewnętrznym opakowaniu kartonowym w celu ochrony przed światłem. Nie należy stosować leku ImmunoGam, jeżeli roztwór wydaje się mętny lub zawiera osad. Leków nie należy wyrzucać do kanalizacji ani domowych pojemników na odpadki. Wszelkie resztki niewykorzystanego produktu należy usunąć w sposób zgodny z lokalnymi przepisami. Takie postępowanie pomoże chronić środowisko. 6. INNE INFORMACJE Co zawiera lek ImmunoGam - Substancją czynną leku jest immunoglobulina ludzka przeciw wirusowi zapalenia wątroby typu B. Lek ImmunoGam dostępny jest w fiolkach o pojemności 1 ml lub 5 ml, zawierających mg/ml białka osocza ludzkiego, w którym 96% (312 j.m./ml) to immunoglobulina typu G (IgG). - Inne składniki to maltoza i polisorbat 80. Jak wygląda lek ImmunoGam i co zawiera opakowanie Lek ImmunoGam ma postać roztworu do wstrzykiwań w szklanej fiolce. Jest to przezroczysty lub lekko opalizujący, bezbarwny lub jasnożółty płyn. Wielkość opakowania: 1 fiolka. Podmiot odpowiedzialny i wytwórca Podmiot odpowiedzialny Cangene Europe Limited Parkshot House 5 Kew Road Richmond, Surrey TW9 2PR Wielka Brytania Tel.: +44 (0) Faks: +44 (0) Wytwórca Cangene Corporation 155 Innovation Drive Winnipeg, MA R3T 5Y3 Kanada 22
23 Data zatwierdzenia ulotki Szczegółowa informacja o tym leku jest dostępna na stronie internetowej Europejskiej Agencji ds. Produktów Leczniczych: Poniższe informacje przeznaczone są wyłącznie dla personelu medycznego lub pracowników służby zdrowia: Dawkowanie - Zapobieganie wirusowemu zapaleniu wątroby typu B w razie przypadkowego kontaktu z wirusem u pacjentów niezaszczepionych: Co najmniej 500 j.m., w zależności od intensywności narażenia, jak najszybciej po narażeniu, najlepiej w ciągu godzin. - Immunoprofilaktyka wirusowego zapalenia wątroby typu B u pacjentów hemodializowanych: 8 12 j.m./kg, maksymalnie 500 j.m., co 2 miesiące, do czasu uzyskania serokonwersji po szczepieniu. - Zapobieganie wirusowemu zapaleniu wątroby typu B u noworodków, których matki są nosicielkami wirusa zapalenia wątroby typu B, zaraz po urodzeniu lub jak najszybciej po urodzeniu: j.m./kg. Podanie immunoglobuliny przeciw wirusowi zapalenia wątroby typu B może wymagać powtarzania do czasu uzyskania serokonwersji po szczepieniu. We wszystkich tych przypadkach zdecydowanie zaleca się szczepienie przeciw wirusowi zapalenia wątroby typu B. Pierwszą dawkę szczepionki można wstrzyknąć tego samego dnia co immunoglobulinę ludzką przeciw wirusowi zapalenia wątroby typu B, ale w inne miejsce. U pacjentów niewykazujących odpowiedzi immunologicznej (poziom brak mierzalnego poziomu przeciwciał przeciw wirusowi zapalenia wątroby typu B) po szczepieniu oraz u pacjentów, u których konieczna jest ciągła profilaktyka, można rozważyć podawanie 500 j.m. w przypadku dorosłych i 8 j.m./kg w przypadku dzieci co 2 miesiące, biorąc pod uwagę, że minimalne ochronne miano przeciwciał wynosi 10 mj.m./ml. Należy również uwzględniać dawki i schematy dawkowania dla immunoglobuliny ludzkiej przeciw wirusowi zapalenia wątroby typu B podawanej domięśniowo, zalecane w innych oficjalnych wytycznych. Sposób podawania Lek ImmunoGam należy podawać domięśniowo. Jeżeli konieczne jest podanie dużej objętości leku (>2 ml u dzieci lub >5 ml u dorosłych), zaleca się podanie podzielonych dawek w różne miejsca. Jeżeli niezbędne jest jednoczesne szczepienie, immunoglobulinę i szczepionkę należy podać w dwa różne miejsca. Instrukcja dotycząca przygotowania leku do stosowania i usuwania Przed użyciem lek ImmunoGam powinien osiągnąć temperaturę pokojową (około 20ºC do 25ºC). Roztwór powinien być przezroczysty lub lekko opalizujący, bezbarwny lub jasnożółty. Nie wolno stosować roztworów mętnych lub zawierających osad. Wszelkie resztki niewykorzystanego produktu lub jego odpady należy usunąć w sposób zgodny z lokalnymi przepisami. 23
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA
 ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA GAMMA anty-hbs 200 Roztwór do wstrzykiwań Immunoglobulinum humanum hepatitidis B Immunoglobulina ludzka przeciw wirusowemu zapaleniu wątroby typu B Należy
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA GAMMA anty-hbs 200 Roztwór do wstrzykiwań Immunoglobulinum humanum hepatitidis B Immunoglobulina ludzka przeciw wirusowemu zapaleniu wątroby typu B Należy
Immunoglobulinum humanum hepatitidis B Immunoglobulina ludzka przeciw wirusowemu zapaleniu wątroby typu B
 ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA GAMMA anty-hbs 200 Roztwór do wstrzykiwań Immunoglobulinum humanum hepatitidis B Immunoglobulina ludzka przeciw wirusowemu zapaleniu wątroby typu B Należy
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA GAMMA anty-hbs 200 Roztwór do wstrzykiwań Immunoglobulinum humanum hepatitidis B Immunoglobulina ludzka przeciw wirusowemu zapaleniu wątroby typu B Należy
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA. Immunoglobulina ludzka przeciw wirusowemu zapaleniu wątroby typu B
 ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA GAMMA anty-hbs 1000 Immunoglobulinum humanum hepatitidis B Immunoglobulina ludzka przeciw wirusowemu zapaleniu wątroby typu B Roztwór do wstrzykiwań Należy
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA GAMMA anty-hbs 1000 Immunoglobulinum humanum hepatitidis B Immunoglobulina ludzka przeciw wirusowemu zapaleniu wątroby typu B Roztwór do wstrzykiwań Należy
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA
 ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA GAMMA anty-d 50 Roztwór do wstrzykiwań Immunoglobulinum humanum anti-d Immunoglobulina ludzka anty-d Należy zapoznać się z treścią ulotki przed zastosowaniem
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA GAMMA anty-d 50 Roztwór do wstrzykiwań Immunoglobulinum humanum anti-d Immunoglobulina ludzka anty-d Należy zapoznać się z treścią ulotki przed zastosowaniem
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO Strona 1 z 8 1. NAZWA PRODUKTU LECZNICZEGO, 180 j.m./ml Roztwór do wstrzykiwań 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Immunoglobulina ludzka przeciw wirusowemu zapaleniu wątroby
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO Strona 1 z 8 1. NAZWA PRODUKTU LECZNICZEGO, 180 j.m./ml Roztwór do wstrzykiwań 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Immunoglobulina ludzka przeciw wirusowemu zapaleniu wątroby
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Tetabulin S/D 250 j.m./ml roztwór do wstrzykiwań 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Immunoglobulina ludzka przeciw tężcowi Jedna dawka (1ml)
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Tetabulin S/D 250 j.m./ml roztwór do wstrzykiwań 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Immunoglobulina ludzka przeciw tężcowi Jedna dawka (1ml)
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA
 ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA GAMMA anty-d 150 Roztwór do wstrzykiwań Immunoglobulinum humanum anti-d Immunoglobulina ludzka anty-d Należy zapoznać się z treścią ulotki przed zastosowaniem
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA GAMMA anty-d 150 Roztwór do wstrzykiwań Immunoglobulinum humanum anti-d Immunoglobulina ludzka anty-d Należy zapoznać się z treścią ulotki przed zastosowaniem
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Hepatect CP 50 j.m./ml; roztwór do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Immunoglobulina ludzka przeciw wirusowemu zapaleniu wątroby
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Hepatect CP 50 j.m./ml; roztwór do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Immunoglobulina ludzka przeciw wirusowemu zapaleniu wątroby
Ulotka dołączona do opakowania: informacja dla użytkownika. Synagis 100 mg/ml roztwór do wstrzykiwań Substancja czynna: paliwizumab
 Ulotka dołączona do opakowania: informacja dla użytkownika Synagis 100 mg/ml roztwór do wstrzykiwań Substancja czynna: paliwizumab Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem tego
Ulotka dołączona do opakowania: informacja dla użytkownika Synagis 100 mg/ml roztwór do wstrzykiwań Substancja czynna: paliwizumab Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem tego
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO SUBCUVIA 160 g/l roztwór do wstrzykiwań 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Immunoglobulina ludzka normalna (Ig s.c./i.m.) 1 l roztworu zawiera:
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO SUBCUVIA 160 g/l roztwór do wstrzykiwań 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Immunoglobulina ludzka normalna (Ig s.c./i.m.) 1 l roztworu zawiera:
Igantet j.m./ml, roztwór do wstrzykiwań, Immunoglobulina ludzka przeciwtężcowa
 ULOTKA DOŁĄCZONA DO OPAKOWANIA: INFORMACJA DLA PACJENTA Igantet 250 250 j.m./ml, roztwór do wstrzykiwań, Immunoglobulina ludzka przeciwtężcowa Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem
ULOTKA DOŁĄCZONA DO OPAKOWANIA: INFORMACJA DLA PACJENTA Igantet 250 250 j.m./ml, roztwór do wstrzykiwań, Immunoglobulina ludzka przeciwtężcowa Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO GAMMA anty-d 150 Roztwór do wstrzykiwań Immunoglobulinum humanum anti-d Immunoglobulina ludzka anty-d 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO GAMMA anty-d 150 Roztwór do wstrzykiwań Immunoglobulinum humanum anti-d Immunoglobulina ludzka anty-d 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY
Ulotka dołączona do opakowania: informacja dla użytkownika
 Ulotka dołączona do opakowania: informacja dla użytkownika Hepatect CP 50 j.m./ml, roztwór do infuzji Immunoglobulina ludzka przeciw wirusowemu zapaleniu wątroby typu B do podania dożylnego Należy uważnie
Ulotka dołączona do opakowania: informacja dla użytkownika Hepatect CP 50 j.m./ml, roztwór do infuzji Immunoglobulina ludzka przeciw wirusowemu zapaleniu wątroby typu B do podania dożylnego Należy uważnie
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Hepatect CP 50 j.m./ml; roztwór do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Immunoglobulina ludzka przeciw wirusowemu zapaleniu wątroby
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Hepatect CP 50 j.m./ml; roztwór do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Immunoglobulina ludzka przeciw wirusowemu zapaleniu wątroby
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO GAMMA anty-hbs 200 Roztwór do wtrzykiwań Immunoglobulinum humanum hepatitidis B Immunoglobulina ludzka przeciw wirusowemu zapaleniu wątroby
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO GAMMA anty-hbs 200 Roztwór do wtrzykiwań Immunoglobulinum humanum hepatitidis B Immunoglobulina ludzka przeciw wirusowemu zapaleniu wątroby
Ulotka dołączona do opakowania: informacja dla użytkownika
 Ulotka dołączona do opakowania: informacja dla użytkownika Pseudovac, roztwór do wstrzykiwań Szczepionka poliwalentna przeciwko pałeczce ropy błękitnej Pseudomonas aeruginosa 1 ml szczepionki zawiera antygeny
Ulotka dołączona do opakowania: informacja dla użytkownika Pseudovac, roztwór do wstrzykiwań Szczepionka poliwalentna przeciwko pałeczce ropy błękitnej Pseudomonas aeruginosa 1 ml szczepionki zawiera antygeny
Nieoficjalne tłumaczenie niemieckiej ulotki dla pacjenta
 Nieoficjalne tłumaczenie niemieckiej ulotki dla pacjenta Ulotka dla pacjenta:informacja dla użytkownika Medivitan iv ampułko-strzykawka 5 mg, 1 mg, 1,05 mg roztwór do wstrzykiwań Substancje czynne: pirydoksyny
Nieoficjalne tłumaczenie niemieckiej ulotki dla pacjenta Ulotka dla pacjenta:informacja dla użytkownika Medivitan iv ampułko-strzykawka 5 mg, 1 mg, 1,05 mg roztwór do wstrzykiwań Substancje czynne: pirydoksyny
1. NAZWA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Igantet 250, 250 j.m./ml, roztwór do wstrzykiwań Immunoglobulinum humanum tetanicum 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera:
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Igantet 250, 250 j.m./ml, roztwór do wstrzykiwań Immunoglobulinum humanum tetanicum 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera:
Ulotka dołączona do opakowania: informacja dla użytkownika. Woda do wstrzykiwań Baxter rozpuszczalnik do sporządzania leków pareneteralnych
 Ulotka dołączona do opakowania: informacja dla użytkownika Woda do wstrzykiwań Baxter rozpuszczalnik do sporządzania leków pareneteralnych Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem
Ulotka dołączona do opakowania: informacja dla użytkownika Woda do wstrzykiwań Baxter rozpuszczalnik do sporządzania leków pareneteralnych Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem
Ulotka dołączona do opakowania: informacja dla użytkownika
 Ulotka dołączona do opakowania: informacja dla użytkownika D - Szczepionka błonicza adsorbowana zawiesina do wstrzykiwań Szczepionka przeciw błonicy, adsorbowana Nie mniej niż 30 j.m. toksoidu błoniczego/0,5
Ulotka dołączona do opakowania: informacja dla użytkownika D - Szczepionka błonicza adsorbowana zawiesina do wstrzykiwań Szczepionka przeciw błonicy, adsorbowana Nie mniej niż 30 j.m. toksoidu błoniczego/0,5
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. 1,5 ml roztworu zawiera: Immunoglobulinę ludzką przeciw wirusowemu zapaleniu wątroby typu B 1000 j.m.
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO GAMMA anty-hbs 1000 Roztwór do wtrzykiwań Immunoglobulinum humanum hepatitidis B Immunoglobulina ludzka przeciw wirusowemu zapaleniu wątroby
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO GAMMA anty-hbs 1000 Roztwór do wtrzykiwań Immunoglobulinum humanum hepatitidis B Immunoglobulina ludzka przeciw wirusowemu zapaleniu wątroby
Nieoficjalne tłumaczenie niemieckiej ulotki dla pacjenta
 Nieoficjalne tłumaczenie niemieckiej ulotki dla pacjenta Ulotka dla pacjenta: Informacja dla użytkownika Medivitan iv ampułki 5 mg, 1 mg, 1,05 mg roztwór do wstrzykiwań Substancje czynne: pirydoksyny chlorowodorek
Nieoficjalne tłumaczenie niemieckiej ulotki dla pacjenta Ulotka dla pacjenta: Informacja dla użytkownika Medivitan iv ampułki 5 mg, 1 mg, 1,05 mg roztwór do wstrzykiwań Substancje czynne: pirydoksyny chlorowodorek
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Woodward s Gripe Water, płyn doustny, (0,46 mg + 10,5 mg)/ml 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Substancje czynne zawartość w 5 ml (1 łyżeczka)
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Woodward s Gripe Water, płyn doustny, (0,46 mg + 10,5 mg)/ml 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Substancje czynne zawartość w 5 ml (1 łyżeczka)
ASMAG FORTE 34 mg jonów magnezu, tabletki Magnesii hydroaspartas
 Ulotka dołączona do opakowania: informacja dla użytkownika ASMAG FORTE 34 mg jonów magnezu, tabletki Magnesii hydroaspartas Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ
Ulotka dołączona do opakowania: informacja dla użytkownika ASMAG FORTE 34 mg jonów magnezu, tabletki Magnesii hydroaspartas Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Fluarix, zawiesina do wstrzykiwań w ampułko-strzykawce. Szczepionka przeciw grypie (rozszczepiony wirion), inaktywowana 2. SKŁAD JAKOŚCIOWY
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Fluarix, zawiesina do wstrzykiwań w ampułko-strzykawce. Szczepionka przeciw grypie (rozszczepiony wirion), inaktywowana 2. SKŁAD JAKOŚCIOWY
Ulotka dołączona do opakowania: informacja dla użytkownika. Synagis 100 mg/ml roztwór do wstrzykiwań Substancja czynna: paliwizumab
 Ulotka dołączona do opakowania: informacja dla użytkownika Synagis 100 mg/ml roztwór do wstrzykiwań Substancja czynna: paliwizumab Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem tego
Ulotka dołączona do opakowania: informacja dla użytkownika Synagis 100 mg/ml roztwór do wstrzykiwań Substancja czynna: paliwizumab Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem tego
INFORMACJE ZAMIESZCZANE NA OPAKOWANIACH BEZPOŚREDNICH
 INFORMACJE ZAMIESZCZANE NA OPAKOWANIACH BEZPOŚREDNICH BUTELKA Z POLIETYLENU Z DOZOWNIKIEM I NAKRĘTKĄ 1. NAZWA PRODUKTU LECZNICZEGO (9,8 mg + 9,8 mg + 245 mg)/g (Benzocainum + Mentholum + Zinci oxidum),
INFORMACJE ZAMIESZCZANE NA OPAKOWANIACH BEZPOŚREDNICH BUTELKA Z POLIETYLENU Z DOZOWNIKIEM I NAKRĘTKĄ 1. NAZWA PRODUKTU LECZNICZEGO (9,8 mg + 9,8 mg + 245 mg)/g (Benzocainum + Mentholum + Zinci oxidum),
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Ty - Szczepionka durowa, zawiesina do wstrzykiwań Szczepionka przeciw durowi brzusznemu. Szczepionka 20 - dawkowa 2. SKŁAD JAKOŚCIOWY
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Ty - Szczepionka durowa, zawiesina do wstrzykiwań Szczepionka przeciw durowi brzusznemu. Szczepionka 20 - dawkowa 2. SKŁAD JAKOŚCIOWY
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Rhesonativ 1250 j.m. 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Po odtworzeniu w 2 ml wody do wstrzykiwań (dołączono) produkt zawiera: w ml w fiolce
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Rhesonativ 1250 j.m. 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Po odtworzeniu w 2 ml wody do wstrzykiwań (dołączono) produkt zawiera: w ml w fiolce
Diosminum. Należy przeczytać uważnie całą ulotkę, ponieważ zawiera ona informacje ważne dla pacjenta.
 ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA Diohespan max, 1000 mg, tabletki Diosminum Należy przeczytać uważnie całą ulotkę, ponieważ zawiera ona informacje ważne dla pacjenta. Lek ten jest dostępny
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA Diohespan max, 1000 mg, tabletki Diosminum Należy przeczytać uważnie całą ulotkę, ponieważ zawiera ona informacje ważne dla pacjenta. Lek ten jest dostępny
Ulotka dla pacjenta: Informacja dla użytkownika Neuro-Medivitan tabletki powlekane
 Nieoficjalne tłumaczenie niemieckiej ulotki dla pacjenta Ulotka dla pacjenta: Informacja dla użytkownika Neuro-Medivitan tabletki powlekane Substancje czynne: tiaminy chlorku chlorowodorek / pirydoksyny
Nieoficjalne tłumaczenie niemieckiej ulotki dla pacjenta Ulotka dla pacjenta: Informacja dla użytkownika Neuro-Medivitan tabletki powlekane Substancje czynne: tiaminy chlorku chlorowodorek / pirydoksyny
Aneks III. Zmiany, które należy wprowadzić w odpowiednich punktach charakterystyki produktu leczniczego i ulotkach dla pacjenta
 Aneks III Zmiany, które należy wprowadzić w odpowiednich punktach charakterystyki produktu leczniczego i ulotkach dla pacjenta Uwaga: Ta Charakterystyka Produktu Leczniczego, oznakowanie opakowań i ulotka
Aneks III Zmiany, które należy wprowadzić w odpowiednich punktach charakterystyki produktu leczniczego i ulotkach dla pacjenta Uwaga: Ta Charakterystyka Produktu Leczniczego, oznakowanie opakowań i ulotka
Ulotka dołączona do opakowania: informacja dla pacjenta. Essentiale VITAL, 600 mg, pasta doustna. Phospholipidum essentiale
 Ulotka dołączona do opakowania: informacja dla pacjenta Essentiale VITAL, 600 mg, pasta doustna Phospholipidum essentiale Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ
Ulotka dołączona do opakowania: informacja dla pacjenta Essentiale VITAL, 600 mg, pasta doustna Phospholipidum essentiale Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ
Flexbumin 200 g/l, roztwór do infuzji Albumina ludzka
 Ulotka dołączona do opakowania: informacja dla użytkownika Flexbumin 200 g/l, roztwór do infuzji Albumina ludzka Należy zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje
Ulotka dołączona do opakowania: informacja dla użytkownika Flexbumin 200 g/l, roztwór do infuzji Albumina ludzka Należy zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO 1. NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO Mucosiffa liofilizat i rozpuszczalnik do sporządzania zawiesiny do wstrzykiwań dla bydła 2. SKŁAD JAKOŚCIOWY
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO 1. NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO Mucosiffa liofilizat i rozpuszczalnik do sporządzania zawiesiny do wstrzykiwań dla bydła 2. SKŁAD JAKOŚCIOWY
Ulotka dołączona do opakowania: informacja dla pacjenta
 Ulotka dołączona do opakowania: informacja dla pacjenta Miacalcic, 50 j.m./ml, roztwór do wstrzykiwań Miacalcic, 100 j.m./ml, roztwór do wstrzykiwań Calcitoninum salmonis Należy zapoznać się z treścią
Ulotka dołączona do opakowania: informacja dla pacjenta Miacalcic, 50 j.m./ml, roztwór do wstrzykiwań Miacalcic, 100 j.m./ml, roztwór do wstrzykiwań Calcitoninum salmonis Należy zapoznać się z treścią
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO TYPHIM Vi, roztwór do wstrzykiwań w ampułko-strzykawce Vaccinum febris typhoidis polysaccharidicum Szczepionka przeciw durowi brzusznemu,
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO TYPHIM Vi, roztwór do wstrzykiwań w ampułko-strzykawce Vaccinum febris typhoidis polysaccharidicum Szczepionka przeciw durowi brzusznemu,
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 NAZWA PRODUKTU LECZNICZEGO GAMMANORM, 165 mg/ml, roztwór do wstrzykiwań 2 SKŁAD JAKOŚCIOWY I ILOŚCIOWY Immunoglobulina ludzka normalna (s.c./i.m.) Immunoglobulina
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 NAZWA PRODUKTU LECZNICZEGO GAMMANORM, 165 mg/ml, roztwór do wstrzykiwań 2 SKŁAD JAKOŚCIOWY I ILOŚCIOWY Immunoglobulina ludzka normalna (s.c./i.m.) Immunoglobulina
Ulotka dołączona do opakowania: informacja dla pacjenta
 Ulotka dołączona do opakowania: informacja dla pacjenta tabletki powlekane 100 mg Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje ważne dla pacjenta.
Ulotka dołączona do opakowania: informacja dla pacjenta tabletki powlekane 100 mg Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje ważne dla pacjenta.
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA. Proszek i rozpuszczalnik do sporządzania roztworu do stosowania miejscowego, 400 j.m., 200 j.m.
 ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA BioTrombina 400 Thrombinum bovine Proszek i rozpuszczalnik do sporządzania roztworu do stosowania miejscowego, 400 j.m., 200 j.m./ml Należy zapoznać się
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA BioTrombina 400 Thrombinum bovine Proszek i rozpuszczalnik do sporządzania roztworu do stosowania miejscowego, 400 j.m., 200 j.m./ml Należy zapoznać się
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO
 ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO 1 1. NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO RESPIPORC FLUpan H1N1 zawiesina do wstrzykiwań dla świń 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Dawka
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO 1 1. NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO RESPIPORC FLUpan H1N1 zawiesina do wstrzykiwań dla świń 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Dawka
ULOTKA DLA PACJENTA 1
 ULOTKA DLA PACJENTA 1 Ulotka dołączona do opakowania: informacja dla użytkownika Supremin MAX, 1,5 mg/ml, syrop Butamirati citras Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku,
ULOTKA DLA PACJENTA 1 Ulotka dołączona do opakowania: informacja dla użytkownika Supremin MAX, 1,5 mg/ml, syrop Butamirati citras Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku,
Ulotka dołączona do opakowania: informacja dla użytkownika. UNIBEN 1,5 mg/ml, aerozol do stosowania w jamie ustnej (Benzydamini hydrochloridum)
 Ulotka dołączona do opakowania: informacja dla użytkownika UNIBEN 1,5 mg/ml, aerozol do stosowania w jamie ustnej (Benzydamini hydrochloridum) Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem
Ulotka dołączona do opakowania: informacja dla użytkownika UNIBEN 1,5 mg/ml, aerozol do stosowania w jamie ustnej (Benzydamini hydrochloridum) Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem
Ulotka dołączona do opakowania: informacja dla użytkownika VESSEL DUE F. 250 LSU kapsułki miękkie. Sulodexidum
 Ulotka dołączona do opakowania: informacja dla użytkownika VESSEL DUE F 250 LSU kapsułki miękkie Sulodexidum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona
Ulotka dołączona do opakowania: informacja dla użytkownika VESSEL DUE F 250 LSU kapsułki miękkie Sulodexidum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO POLIORIX, roztwór do wstrzykiwań Vaccinum poliomyelitidis inactivatum Szczepionka przeciw poliomyelitis, inaktywowana 2. SKŁAD JAKOŚCIOWY
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO POLIORIX, roztwór do wstrzykiwań Vaccinum poliomyelitidis inactivatum Szczepionka przeciw poliomyelitis, inaktywowana 2. SKŁAD JAKOŚCIOWY
Ulotka dołączona do opakowania: informacja dla użytkownika. Bendamustine Kabi, 2,5 mg/ml, proszek do sporządzania koncentratu roztworu do infuzji
 Ulotka dołączona do opakowania: informacja dla użytkownika Bendamustine Kabi, 2,5 mg/ml, proszek do sporządzania koncentratu roztworu do infuzji Bendamustini hydrochloridum Należy uważnie zapoznać się
Ulotka dołączona do opakowania: informacja dla użytkownika Bendamustine Kabi, 2,5 mg/ml, proszek do sporządzania koncentratu roztworu do infuzji Bendamustini hydrochloridum Należy uważnie zapoznać się
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA WŁASNA PRODUKTU LECZNICZEGO CROTAMITON FARMAPOL płyn do stosowania na skórę, 100 mg/g 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY SUBSTANCJI CZYNNEJ 1 g płynu do stosowania
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA WŁASNA PRODUKTU LECZNICZEGO CROTAMITON FARMAPOL płyn do stosowania na skórę, 100 mg/g 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY SUBSTANCJI CZYNNEJ 1 g płynu do stosowania
B. ULOTKA INFORMACYJNA
 B. ULOTKA INFORMACYJNA 1 ULOTKA INFORMACYJNA Versifel FeLV 1. NAZWA I ADRES PODMIOTU ODPOWIEDZIALNEGO ORAZ WYTWÓRCY ODPOWIEDZIALNEGO ZA ZWOLNIENIE SERII, JEŚLI JEST INNY Podmiot odpowiedzialny: Zoetis
B. ULOTKA INFORMACYJNA 1 ULOTKA INFORMACYJNA Versifel FeLV 1. NAZWA I ADRES PODMIOTU ODPOWIEDZIALNEGO ORAZ WYTWÓRCY ODPOWIEDZIALNEGO ZA ZWOLNIENIE SERII, JEŚLI JEST INNY Podmiot odpowiedzialny: Zoetis
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA. Glimbax, 0,74 mg/ml (0,074%), roztwór do płukania jamy ustnej i gardła (Diclofenacum)
 ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA Glimbax, 0,74 mg/ml (0,074%), roztwór do płukania jamy ustnej i gardła (Diclofenacum) Należy przeczytać uważnie całą ulotkę, ponieważ zawiera ona ważne informacje
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA Glimbax, 0,74 mg/ml (0,074%), roztwór do płukania jamy ustnej i gardła (Diclofenacum) Należy przeczytać uważnie całą ulotkę, ponieważ zawiera ona ważne informacje
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO 1 1. NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO Gleptosil, 200 mg/ml, roztwór do wstrzykiwań dla świń 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml produktu
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO 1 1. NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO Gleptosil, 200 mg/ml, roztwór do wstrzykiwań dla świń 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml produktu
Ulotka dołączona do opakowania: informacja dla użytkownika. POLIORIX, roztwór do wstrzykiwań
 Ulotka dołączona do opakowania: informacja dla użytkownika POLIORIX, roztwór do wstrzykiwań Szczepionka przeciw poliomyelitis, inaktywowana Szczepionka 1-dawkowa Należy uważnie zapoznać się z treścią ulotki
Ulotka dołączona do opakowania: informacja dla użytkownika POLIORIX, roztwór do wstrzykiwań Szczepionka przeciw poliomyelitis, inaktywowana Szczepionka 1-dawkowa Należy uważnie zapoznać się z treścią ulotki
ASMAG B 20 mg jonów magnezu + 0,25 mg pirydoksyny chlorowodorku, tabletki Magnesii hydroaspartas + Pyridoxini hydrochloridum
 Ulotka dołączona do opakowania: informacja dla użytkownika ASMAG B 20 mg jonów magnezu + 0,25 mg pirydoksyny chlorowodorku, tabletki Magnesii hydroaspartas + Pyridoxini hydrochloridum Należy uważnie zapoznać
Ulotka dołączona do opakowania: informacja dla użytkownika ASMAG B 20 mg jonów magnezu + 0,25 mg pirydoksyny chlorowodorku, tabletki Magnesii hydroaspartas + Pyridoxini hydrochloridum Należy uważnie zapoznać
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Oviderm, 250 mg, krem 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 gram kremu zawiera 250 mg glikolu propylenowego Substancja pomocnicza o znanym
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Oviderm, 250 mg, krem 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 gram kremu zawiera 250 mg glikolu propylenowego Substancja pomocnicza o znanym
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO 1 1. NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO Gleptosil, 200 mg/ml, roztwór do wstrzykiwań dla świń 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Substancja czynna:
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO 1 1. NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO Gleptosil, 200 mg/ml, roztwór do wstrzykiwań dla świń 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Substancja czynna:
Ulotka dołączona do opakowania: informacja dla użytkownika
 Ulotka dołączona do opakowania: informacja dla użytkownika IMOVAX POLIO, zawiesina do wstrzykiwań w ampułko-strzykawce Szczepionka przeciw poliomyelitis, inaktywowana Należy uważnie zapoznać się z treścią
Ulotka dołączona do opakowania: informacja dla użytkownika IMOVAX POLIO, zawiesina do wstrzykiwań w ampułko-strzykawce Szczepionka przeciw poliomyelitis, inaktywowana Należy uważnie zapoznać się z treścią
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA
 ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA SYLIMAROL 35 mg Produkt przeznaczony dla młodzieży powyżej 12 roku życia i dorosłych. Wielkość opakowania: 30 lub 60 sztuk Należy przeczytać uważnie całą
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA SYLIMAROL 35 mg Produkt przeznaczony dla młodzieży powyżej 12 roku życia i dorosłych. Wielkość opakowania: 30 lub 60 sztuk Należy przeczytać uważnie całą
A. OZNAKOWANIE OPAKOWAŃ
 A. OZNAKOWANIE OPAKOWAŃ 1 INFORMACJE ZAMIESZCZANE NA OPAKOWANIACH ZEWNĘTRZNYCH OPAKOWANIE ZAWIERAJĄCE OPAKOWANIE Z 50 FIOLKAMI Z ZAWIESINĄ ORAZ 2 OPAKOWANIA Z 25 FIOLKAMI Z EMULSJĄ 1. NAZWA PRODUKTU LECZNICZEGO
A. OZNAKOWANIE OPAKOWAŃ 1 INFORMACJE ZAMIESZCZANE NA OPAKOWANIACH ZEWNĘTRZNYCH OPAKOWANIE ZAWIERAJĄCE OPAKOWANIE Z 50 FIOLKAMI Z ZAWIESINĄ ORAZ 2 OPAKOWANIA Z 25 FIOLKAMI Z EMULSJĄ 1. NAZWA PRODUKTU LECZNICZEGO
INFORMACJE ZAMIESZCZANE NA OPAKOWANIACH BEZPOŚREDNICH
 INFORMACJE ZAMIESZCZANE NA OPAKOWANIACH BEZPOŚREDNICH {Tuba} 1. NAZWA PRODUKTU LECZNICZEGO PUDER PŁYNNY Z ANESTEZYNĄ (240 mg + 20 mg)/g, zawiesina na skórę (Zinci oxidum + Benzocainum) 2. ZAWARTOŚĆ SUBSTANCJI
INFORMACJE ZAMIESZCZANE NA OPAKOWANIACH BEZPOŚREDNICH {Tuba} 1. NAZWA PRODUKTU LECZNICZEGO PUDER PŁYNNY Z ANESTEZYNĄ (240 mg + 20 mg)/g, zawiesina na skórę (Zinci oxidum + Benzocainum) 2. ZAWARTOŚĆ SUBSTANCJI
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. 1 ml roztworu do wstrzykiwań zawiera 10 mg fitomenadionu (Phytomenadionum) - witaminy K 1.
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO VITACON, 10 mg/ml, roztwór do wstrzykiwań 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu do wstrzykiwań zawiera 10 mg fitomenadionu (Phytomenadionum)
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO VITACON, 10 mg/ml, roztwór do wstrzykiwań 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu do wstrzykiwań zawiera 10 mg fitomenadionu (Phytomenadionum)
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO 1. NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO Gletvax 6 zawiesina do wstrzykiwań dla świń 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY SUBSTANCJI CZYNNEJ(-YCH) Subastancje
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO 1. NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO Gletvax 6 zawiesina do wstrzykiwań dla świń 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY SUBSTANCJI CZYNNEJ(-YCH) Subastancje
Ulotka dołączona do opakowania: informacja dla pacjenta. LORATADYNA GALENA, 10 mg, tabletki Loratadinum
 Ulotka dołączona do opakowania: informacja dla pacjenta LORATADYNA GALENA, 10 mg, tabletki Loratadinum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje
Ulotka dołączona do opakowania: informacja dla pacjenta LORATADYNA GALENA, 10 mg, tabletki Loratadinum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO
 ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO 1 1. NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO ECOPORC SHIGA zawiesina do wstrzykiwań dla świń 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każda dawka
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO 1 1. NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO ECOPORC SHIGA zawiesina do wstrzykiwań dla świń 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każda dawka
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA
 ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA Karbis, 4 mg, tabletki Karbis, 8 mg, tabletki Karbis, 16 mg, tabletki Karbis, 32 mg, tabletki Candesartanum cilexetilum Należy zapoznać się z treścią ulotki
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA Karbis, 4 mg, tabletki Karbis, 8 mg, tabletki Karbis, 16 mg, tabletki Karbis, 32 mg, tabletki Candesartanum cilexetilum Należy zapoznać się z treścią ulotki
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA VERTIX, 24 MG, TABLETKI (BETAHISTINI DIHYDROCHLORIDUM)
 ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA VERTIX, 24 MG, TABLETKI (BETAHISTINI DIHYDROCHLORIDUM) Należy zapoznać się z treścią ulotki przez zastosowaniem leku. - Należy zachować tę ulotkę, aby w
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA VERTIX, 24 MG, TABLETKI (BETAHISTINI DIHYDROCHLORIDUM) Należy zapoznać się z treścią ulotki przez zastosowaniem leku. - Należy zachować tę ulotkę, aby w
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO. PRIMENE 10% roztwór do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO PRIMENE 10% roztwór do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 100 ml roztworu do infuzji zawiera: L-Izoleucyna... L-Leucyna... L-Walina...
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO PRIMENE 10% roztwór do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 100 ml roztworu do infuzji zawiera: L-Izoleucyna... L-Leucyna... L-Walina...
Ulotka dołączona do opakowania: informacja dla pacjenta Linomag, 200 mg/g krem (Lini oleum virginale)
 Ulotka dołączona do opakowania: informacja dla pacjenta Linomag, 200 mg/g krem (Lini oleum virginale) Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje
Ulotka dołączona do opakowania: informacja dla pacjenta Linomag, 200 mg/g krem (Lini oleum virginale) Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Cholinex Intense, 2,5 mg + 1,2 mg, tabletki do ssania 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jedna tabletka do ssania zawiera 2,5 mg heksylorezorcynolu
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Cholinex Intense, 2,5 mg + 1,2 mg, tabletki do ssania 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jedna tabletka do ssania zawiera 2,5 mg heksylorezorcynolu
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Syrop tymiankowy Labima, 110 mg/ml, syrop 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Płynny wyciąg z ziela tymianku (Thymi extractum fluidum).
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Syrop tymiankowy Labima, 110 mg/ml, syrop 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Płynny wyciąg z ziela tymianku (Thymi extractum fluidum).
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. adsorbowany na wodorotlenku glinu, uwodnionym nie więcej niż 0,7 mg Al 3+
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO D - Szczepionka błonicza adsorbowana, zawiesina do wstrzykiwań Szczepionka przeciw błonicy, adsorbowana Szczepionka 20 - dawkowa 2. SKŁAD
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO D - Szczepionka błonicza adsorbowana, zawiesina do wstrzykiwań Szczepionka przeciw błonicy, adsorbowana Szczepionka 20 - dawkowa 2. SKŁAD
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO 1. NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO Parvoruvax, zawiesina do wstrzykiwań dla świń 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY SUBSTANCJI CZYNNEJ(-YCH)
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO 1. NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO Parvoruvax, zawiesina do wstrzykiwań dla świń 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY SUBSTANCJI CZYNNEJ(-YCH)
Klimakt-HeelT. tabletki
 Ulotka dołączona do opakowania: informacja dla pacjenta Klimakt-HeelT tabletki Należy uważnie zapoznać się z treścią ulotki przed zażyciem leku, ponieważ zawiera ona informacje ważne dla pacjenta. Lek
Ulotka dołączona do opakowania: informacja dla pacjenta Klimakt-HeelT tabletki Należy uważnie zapoznać się z treścią ulotki przed zażyciem leku, ponieważ zawiera ona informacje ważne dla pacjenta. Lek
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. Gaviscon o smaku mięty Saszetki, (500 mg + 267 mg + 160 mg)/10 ml, zawiesina doustna
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Gaviscon o smaku mięty Saszetki, (500 mg + 267 mg + 160 mg)/10 ml, zawiesina doustna 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Gaviscon o smaku
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Gaviscon o smaku mięty Saszetki, (500 mg + 267 mg + 160 mg)/10 ml, zawiesina doustna 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Gaviscon o smaku
Ulotka dołączona do opakowania: informacja dla pacjenta. Terbilum 10 mg/g krem Terbinafini hydrochloridum
 Ulotka dołączona do opakowania: informacja dla pacjenta Terbilum 10 mg/g krem Terbinafini hydrochloridum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje
Ulotka dołączona do opakowania: informacja dla pacjenta Terbilum 10 mg/g krem Terbinafini hydrochloridum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje
A. OZNAKOWANIE OPAKOWAŃ
 A. OZNAKOWANIE OPAKOWAŃ 34 INFORMACJE ZAMIESZCZANE NA OPAKOWANIACH ZEWNĘTRZNYCH PUDEŁKO KARTONOWE NA STRZYKAWKĘ 1. NAZWA PRODUKTU LECZNICZEGO Focetria zawiesina do wstrzykiwań w ampułkostrzykawce Szczepionka
A. OZNAKOWANIE OPAKOWAŃ 34 INFORMACJE ZAMIESZCZANE NA OPAKOWANIACH ZEWNĘTRZNYCH PUDEŁKO KARTONOWE NA STRZYKAWKĘ 1. NAZWA PRODUKTU LECZNICZEGO Focetria zawiesina do wstrzykiwań w ampułkostrzykawce Szczepionka
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA. HIRUDOID, 0,3 g/100 g maść (Mucopolisaccharidum polisulphatum)
 ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA HIRUDOID, 0,3 g/100 g maść (Mucopolisaccharidum polisulphatum) Należy przeczytać uważnie całą ulotkę, ponieważ zawiera ona informacje ważne dla pacjenta.
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA HIRUDOID, 0,3 g/100 g maść (Mucopolisaccharidum polisulphatum) Należy przeczytać uważnie całą ulotkę, ponieważ zawiera ona informacje ważne dla pacjenta.
Ulotka dołączona do opakowania: informacja dla użytkownika. Flexbumin 200 g/l, roztwór do infuzji Albumina ludzka
 Ulotka dołączona do opakowania: informacja dla użytkownika Flexbumin 200 g/l, roztwór do infuzji Albumina ludzka Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera
Ulotka dołączona do opakowania: informacja dla użytkownika Flexbumin 200 g/l, roztwór do infuzji Albumina ludzka Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO 1. NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO ERYSIN SINGLE SHOT, emulsja do wstrzykiwań dla świń 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY SUBSTANCJI CZYNNEJ(-YCH)
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO 1. NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO ERYSIN SINGLE SHOT, emulsja do wstrzykiwań dla świń 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY SUBSTANCJI CZYNNEJ(-YCH)
Ulotka dołączona do opakowania: informacja dla użytkownika. Mucofluid, 50 mg/ml, aerozol do nosa, roztwór. Mesnum
 Ulotka dołączona do opakowania: informacja dla użytkownika Mucofluid, 50 mg/ml, aerozol do nosa, roztwór Mesnum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona
Ulotka dołączona do opakowania: informacja dla użytkownika Mucofluid, 50 mg/ml, aerozol do nosa, roztwór Mesnum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO PNEUMO 23, roztwór do wstrzykiwań w ampułko-strzykawce Vaccinum pneumococcale polysaccharidicum Szczepionka przeciw pneumokokom, polisacharydowa
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO PNEUMO 23, roztwór do wstrzykiwań w ampułko-strzykawce Vaccinum pneumococcale polysaccharidicum Szczepionka przeciw pneumokokom, polisacharydowa
INFORMACJE ZAMIESZCZANE NA OPAKOWANIACH BEZPOŚREDNICH
 WOREK 10 KG 1. NAZWA PRODUKTU LECZNICZEGO CIECHOCIŃSKI SZLAM LECZNICZY proszek do sporządzania roztworu na skórę produkt złożony 2. ZAWARTOŚĆ SUBSTANCJI CZYNNYCH Co zawiera Ciechociński szlam leczniczy
WOREK 10 KG 1. NAZWA PRODUKTU LECZNICZEGO CIECHOCIŃSKI SZLAM LECZNICZY proszek do sporządzania roztworu na skórę produkt złożony 2. ZAWARTOŚĆ SUBSTANCJI CZYNNYCH Co zawiera Ciechociński szlam leczniczy
ULOTKA DLA PACJENTA 1
 ULOTKA DLA PACJENTA 1 ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA EUVAX B, 20 mikrogramów, zawiesina do wstrzykiwań Vaccinum hepatitidis B (ADNr) Szczepionka przeciw wirusowemu zapaleniu wątroby typu
ULOTKA DLA PACJENTA 1 ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA EUVAX B, 20 mikrogramów, zawiesina do wstrzykiwań Vaccinum hepatitidis B (ADNr) Szczepionka przeciw wirusowemu zapaleniu wątroby typu
Ulotka dołączona do opakowania: informacja dla pacjenta. DISTREPTAZA Streptokinaza + Streptodornaza j.m j.m. Czopki doodbytnicze
 Ulotka dołączona do opakowania: informacja dla pacjenta DISTREPTAZA Streptokinaza + Streptodornaza 15 000 j.m. + 1250 j.m. Czopki doodbytnicze Należy zapoznać się z treścią ulotki przed zastosowaniem leku,
Ulotka dołączona do opakowania: informacja dla pacjenta DISTREPTAZA Streptokinaza + Streptodornaza 15 000 j.m. + 1250 j.m. Czopki doodbytnicze Należy zapoznać się z treścią ulotki przed zastosowaniem leku,
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO 1 1. NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO Rispoval 3 BRSV PI3 BVD Liofilizat i zawiesina do sporządzania zawiesiny do wstrzykiwań dla bydła. 2.
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO 1 1. NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO Rispoval 3 BRSV PI3 BVD Liofilizat i zawiesina do sporządzania zawiesiny do wstrzykiwań dla bydła. 2.
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO 1/18
 ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO 1/18 1. NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO Nobivac Piro 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY PRODUKTU LECZNICZEGO W dawce 1 ml: Substancja
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO 1/18 1. NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO Nobivac Piro 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY PRODUKTU LECZNICZEGO W dawce 1 ml: Substancja
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO 1. NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO Leukocell 2 zawiesina do wstrzykiwań dla kotów 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY PRODUKTU LECZNICZEGO Substancja
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO 1. NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO Leukocell 2 zawiesina do wstrzykiwań dla kotów 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY PRODUKTU LECZNICZEGO Substancja
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Uro-Vaxom 6 mg, kapsułki, twarde 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 kapsułka twarda zawiera: liofilizat OM-89 w tym: liofilizowany lizat
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Uro-Vaxom 6 mg, kapsułki, twarde 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 kapsułka twarda zawiera: liofilizat OM-89 w tym: liofilizowany lizat
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO VAXIGRIP JUNIOR, zawiesina do wstrzykiwań w ampułko-strzykawce Szczepionka przeciw grypie (rozszczepiony wirion), inaktywowana 2. SKŁAD
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO VAXIGRIP JUNIOR, zawiesina do wstrzykiwań w ampułko-strzykawce Szczepionka przeciw grypie (rozszczepiony wirion), inaktywowana 2. SKŁAD
Ulotka dołączona do opakowania: informacja dla pacjenta. LORATADYNA PYLOX 10 mg, tabletki Loratadinum
 Ulotka dołączona do opakowania: informacja dla pacjenta LORATADYNA PYLOX 10 mg, tabletki Loratadinum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje
Ulotka dołączona do opakowania: informacja dla pacjenta LORATADYNA PYLOX 10 mg, tabletki Loratadinum Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje
Stodal syrop jest lekiem stosowanym w leczeniu kaszlu różnego pochodzenia, towarzyszącego infekcjom górnych dróg oddechowych.
 Ulotka dołączona do opakowania: informacja dla pacjenta Stodal, syrop Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje ważne dla pacjenta. Lek ten
Ulotka dołączona do opakowania: informacja dla pacjenta Stodal, syrop Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje ważne dla pacjenta. Lek ten
Aneks I. Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu
 Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
Aneks I Wnioski naukowe i podstawy zmiany warunków pozwolenia (pozwoleń) na dopuszczenie do obrotu 1 Wnioski naukowe Uwzględniając raport oceniający komitetu PRAC w sprawie okresowych raportów o bezpieczeństwie
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA
 ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA UMAN BIG 180 j.m./ml roztwór do wstrzykiwań Immunoglobulina ludzka przeciw wirusowemu zapaleniu wątroby typu B Należy zapoznać się z treścią ulotki przed
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA UMAN BIG 180 j.m./ml roztwór do wstrzykiwań Immunoglobulina ludzka przeciw wirusowemu zapaleniu wątroby typu B Należy zapoznać się z treścią ulotki przed
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA. Ropimol 2 mg/ml, roztwór do wstrzykiwań. Ropivacaini hydrochloridum
 ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA Ropimol 2 mg/ml, roztwór do wstrzykiwań Ropivacaini hydrochloridum Należy zapoznać się z treścią ulotki przed zastosowaniem leku. - Należy zachować tę ulotkę,
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA Ropimol 2 mg/ml, roztwór do wstrzykiwań Ropivacaini hydrochloridum Należy zapoznać się z treścią ulotki przed zastosowaniem leku. - Należy zachować tę ulotkę,
100 ml syropu zawiera 825 mg suchego wyciągu z liści bluszczu (Hedera helix L., folium) (4-8:1). Ekstrahent: etanol 30% (m/m).
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Hedussin, 33 mg/4 ml, syrop 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 100 ml syropu zawiera 825 mg suchego wyciągu z liści bluszczu (Hedera helix
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Hedussin, 33 mg/4 ml, syrop 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 100 ml syropu zawiera 825 mg suchego wyciągu z liści bluszczu (Hedera helix
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO 1 1. NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO Vanguard Plus 5, liofilizat i rozpuszczalnik do sporządzania zawiesiny do wstrzykiwań dla psów 2. SKŁAD
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO 1 1. NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO Vanguard Plus 5, liofilizat i rozpuszczalnik do sporządzania zawiesiny do wstrzykiwań dla psów 2. SKŁAD
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO ESPUMISAN, 40 mg, kapsułki 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każda kapsułka zawiera 40 mg symetykonu. Substancje pomocnicze o znanym działaniu:
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO ESPUMISAN, 40 mg, kapsułki 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każda kapsułka zawiera 40 mg symetykonu. Substancje pomocnicze o znanym działaniu:
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY SUBSTANCJI CZYNNYCH
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA WŁASNA PRODUKTU LECZNICZEGO SOLUVIT N, proszek do sporządzania roztworu do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY SUBSTANCJI CZYNNYCH 1 fiolka zawiera: Substancje
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA WŁASNA PRODUKTU LECZNICZEGO SOLUVIT N, proszek do sporządzania roztworu do infuzji 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY SUBSTANCJI CZYNNYCH 1 fiolka zawiera: Substancje
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO AVAXIM 160 U, zawiesina do wstrzykiwań w ampułko-strzykawce Vaccinum hepatitidis A inactivatum adsorbatum Szczepionka przeciw wirusowemu
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO AVAXIM 160 U, zawiesina do wstrzykiwań w ampułko-strzykawce Vaccinum hepatitidis A inactivatum adsorbatum Szczepionka przeciw wirusowemu
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Oilatum 700 mg/g, żel 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 g żelu zawiera 700 mg parafiny ciekłej, lekkiej (Paraffinum perliquidum). Pełny
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Oilatum 700 mg/g, żel 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 g żelu zawiera 700 mg parafiny ciekłej, lekkiej (Paraffinum perliquidum). Pełny
CHA RAKTERYSTYKA PRODUKTU LECZNICZEGO. Ampułko-strzykawka po 1 ml zawiera 250 j.m. immunoglobuliny ludzkiej przeciwtężcowej.
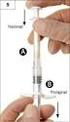 CHA RAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA WŁASNA PRODUKTU LECZNICZEGO Igantet 250, 250j.m./ml, roztwór do wstrzykiwań Immunoglobulinum humanum tetanicum 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY SUBSTANCJI
CHA RAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA WŁASNA PRODUKTU LECZNICZEGO Igantet 250, 250j.m./ml, roztwór do wstrzykiwań Immunoglobulinum humanum tetanicum 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY SUBSTANCJI
Ulotka dołączona do opakowania: informacja dla pacjenta Oscillococcinum, granulki w pojemniku jednodawkowym
 Ulotka dołączona do opakowania: informacja dla pacjenta Oscillococcinum, granulki w pojemniku jednodawkowym Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje
Ulotka dołączona do opakowania: informacja dla pacjenta Oscillococcinum, granulki w pojemniku jednodawkowym Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem leku, ponieważ zawiera ona informacje
