1. NAZWA PRODUKTU LECZNICZEGO ^015-08" 2 6 ^
|
|
|
- Agata Grabowska
- 5 lat temu
- Przeglądów:
Transkrypt
1 Sprawdzono M pc cl wgtędem merytorycznym 1. NAZWA PRODUKTU LECZNICZEGO ^015-08" 2 6 ^ PRIORIX, proszek i rozpuszczalnik do sporządzania roztworu do wstrzykiwań Szczepionka przeciw odrze, śwince i różyczce, żywa 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 dawka (0,5 ml) szczepionki po rekonstytucji zawiera: Żywy atenuowany wirus odry 1 (szczep Schwarz) Żywy atenuowany wirus świnki' (szczep RIT 4385, pochodzący od szczepu Jeryl Lynn) Żywy atenuowany wirus różyczki 2 (szczep Wistar RA 27/3) nie mniej niż CCID 50 3 nie mniej niż 10 3 ' 7 CCID 50 3 nie mniej niż CCID namnażany w hodowli komórek zarodków kurzych 2 namnażany w hodowli ludzkich komórek diploidalnych MRC-5 3 CCIDso- wyznaczona statystycznie ilość wirusa mogąca w wyniku zaszczepienia zakazić 50% hodowli komórkowej Ta szczepionka zawiera śladowe ilości neomycyny. Patrz punkt 4.3. Substancje pomocnicze o znanym działaniu: Szczepionka zawiera 9 mg sorbitolu, patrz punkt 4.4. Pełny wykaz substancji pomocniczych, patrz punkt 6.1, 3. POSTAĆ FARMACEUTYCZNA Proszek i rozpuszczalnik do sporządzania roztworu do wstrzykiwań. Liofilizowane komponenty odry, świnki i różyczki (MMR) mają postać proszku barwy białej do lekko różowej. Rozpuszczalnik jest przezroczystym i bezbarwnym roztworem. 4. SZCZEGÓŁOWE DANE KLINICZNE 4.1 Wskazania do stosowania PRIORIX jest przeznaczony do czynnego uodparniania przeciwko odrze, śwince i różyczce dzieci po ukończeniu 9. miesiąca życia, młodzieży oraz osób dorosłych. W celu uzyskania informacji dotyczącej stosowania u dzieci w wieku od 9 do 12 miesięcy, patrz punkty 4.2, 4.4 i Dawkowanie i sposób podawania Dawkowanie Szczepionka PRIORIX powinna być stosowana zgodnie z oficjalnymi zaleceniami. Osoby w wieku 12 miesięcy i starsze Zaleca się podanie jednej dawki (0,5 ml) szczepionki. Druga dawka powinna zostać podana zgodnie z oficjalnymi zaleceniami. 2
2 Szczepionka PRIORIX może być stosowana u osób, które zostały uprzednio zaszczepione inną monowalentną lub skojarzoną szczepionką przeciw odrze, śwince i różyczce. Niemowlęta w wieku od 9 do 12 miesięcy Niemowlęta w pierwszym roku życia mogą nie wytworzyć wystarczającej odpowiedzi na składniki szczepionki. W przypadku, gdy sytuacja epidemiologiczna wymaga szczepienia niemowląt w pierwszym roku ich życia (np. wybuch epidemii lub podróż w rejony endemiczne), druga dawka szczepionki PRIORIX powinna zostać podana w drugim roku życia, najlepiej w ciągu 3 miesięcy od podania pierwszej dawki. W żadnym przypadku odstęp pomiędzy dawkami nie powinien być krótszy niż 4 tygodnie (patrz punkty 4.4 i 5.1). Niemowlęta w wieku poniżej 9 miesięcy Nie określono bezpieczeństwa stosowania ani skuteczności szczepionki PRIORIX u niemowląt w wieku poniżej 9 miesięcy. Sposób podawania PRIORIX podaje się podskórnie, jakkolwiek można także podać domięśniowo (patrz punkty 4.4 i 5.1). Szczepionka powinna zostać podana podskórnie u pacjentów z trombocytopenią lub u których występują zaburzenia krzepnięcia (patrz punkt 4.4). Instrukcja dotycząca rekonstytucji produktu leczniczego przed podaniem, patrz punkt Przeciwwskazania Nadwrażliwość na substancje czynne lub na którąkolwiek substancję pomocniczą wymienioną w punkcie 6.1, lub neomycynę. Stwierdzone w wywiadzie kontaktowe zapalenie skóry wywołane przez neomycynę nie jest przeciwwskazaniem do szczepienia. W celu uzyskania informacji dotyczących reakcji nadwrażliwości na białko jaja kurzego, patrz punkt 4.4. Ciężki humoralny lub komórkowy (pierwotny lub nabyty) niedobór odporności, np. ciężki, złożony niedobór odporności, agammaglobulinemia lub AIDS lub objawowe zakażenie wirusem HIV, lub właściwy dla wieku odsetek limfocytów T CD4+ u dzieci w wieku poniżej 12 miesięcy z CD4+ <25%; w wieku między 12 a 35 miesięcy z CD4+ <20%; w wieku między 36 a 59 miesięcy z CD4+ <15% (patrz punkt 4.4). Ciąża. Ponadto, należy unikać zajścia w ciążę przez 1 miesiąc po zaszczepieniu (patrz punkt 4.6). Tak jak w przypadku innych szczepionek, u osób w okresie ostrych i ciężkich chorób przebiegających z gorączką podanie szczepionki powinno być odroczone. Łagodna infekcja, taka jak przeziębienie, nie jest przeciwwskazaniem do szczepienia. 4.4 Specjalne ostrzeżenia i środki ostrożności dotyczące stosowania Podobnie jak w przypadku wszystkich szczepionek podawanych w iniekcji, istnieje możliwość wystąpienia rzadkiej reakcji anafilaktycznej, dlatego należy zapewnić możliwość fachowej opieki medycznej bezpośrednio po szczepieniu. Alkohol, a także inne środki dezynfekujące powinny wyparować ze skóry przed podaniem szczepionki, ponieważ mogą unieczynnić atenuowane wirusy znajdujące się w szczepionce. 3
3 Niemowlęta szczepione w pierwszym roku życia mogą nie wytworzyć wystarczającej odpowiedzi immunologicznej na składniki szczepionki, w związku z możliwą obecnością przeciwciał matczynych w ich organizmie (patrz punkty 4.2 i 5.1) Szczególna ostrożność powinna zostać zachowana w przypadku podawania szczepionki PRIORIX osobom z zaburzeniami ośrodkowego układu nerwowego, u których istnieje ryzyko występowania drgawek gorączkowych lub u osób z drgawkami w wywiadzie rodzinnym. Osoby z przebytymi drgawkami gorączkowymi, powinny być ściśle monitorowane. Zawarte w szczepionce wirusy odry i świnki są uzyskiwane z hodowli komórek zarodka kurzego i z tego powodu mogą zawierać śladowe ilości białka jaja. Osoby z reakcjami anafilaktycznymi, anafilaktoidalnymi lub innymi reakcjami typu natychmiastowego w wywiadzie (np. uogólniona pokrzywka, obrzęk jamy ustnej i gardła, trudności w oddychaniu, obniżenie ciśnienia tętniczego lub wstrząs) występującymi po spożyciu jaj mogą być bardziej narażone na wystąpienie reakcji typu natychmiastowego po szczepieniu, chociaż jak wykazano, reakcje te są bardzo rzadkie. Podczas szczepienia tych osób, należy zachować szczególną ostrożność oraz zapewnić dostępność odpowiednich środków leczniczych na wypadek wystąpienia reakcji nadwrażliwości. Pacjenci z rzadkimi dziedzicznymi problemami dotyczącymi nietolerancji fruktozy, nie powinni być szczepieni szczepionką PRIORIX, gdyż zawiera ona sorbitol. Ograniczona ochrona przeciw odrze może zostać uzyskana przez zaszczepienie w ciągu 72 godzin od momentu narażenia na zarażenie naturalnie występującą odrą. Utrata przytomności (omdlenie) może wystąpić po podaniu lub nawet przed podaniem szczepionki, szczególnie u młodzieży, jako reakcja psychogenna na ukłucie igłą. Mogą temu towarzyszyć objawy neurologiczne, takie jak przemijające zaburzenia widzenia, parestezje oraz toniczno-kloniczne ruchy kończyn podczas odzyskiwania przytomności. Ważne jest zachowanie odpowiednich procedur, aby uniknąć urazów podczas omdleń. Tak jak w przypadku wszystkich szczepionek, nie wszystkie zaszczepione osoby mogą wytworzyć ochronny poziom przeciwciał. PRIORIX W ŻADNYM PRZYPADKU NIE MOŻE BYĆ PODAWANY DONACZYNIOWO Trombocytopenia Przypadki nasilenia lub nawrotu trombocytopenii u osób chorujących na tę chorobę były zgłaszane po podaniu pierwszej dawki żywych szczepionek przeciwko odrze, śwince, różyczce. Trombocytopenia związana ze szczepieniem szczepionką MMR jest rzadka i zasadniczo samoograniczająca. U pacjentów z istniejącą trombocytopenią lub historią trombocytopenii po szczepieniu przeciw odrze, śwince i różyczce należy dokładnie ocenić stosunek korzyści do ryzyka wynikający ze szczepienia szczepionką PRIORIX. Tych pacjentów należy szczepić z zachowaniem ostrożności i wykorzystując podskórną drogę podania. Pacjenci z upośledzoną odpornością Można rozważyć szczepienie pacjentów z wybranymi rodzajami niedoborów odporności w przypadku, gdy korzyści przewyższają ryzyko (np. pacjenci z bezobjawowym zakażeniem HIV, niedobór podklas IgG, wrodzona neutropenia, przewlekła choroba ziarniakowa oraz choroby przebiegające z niedoborem dopełniacza). Pacjenci z niedoborami odporności, u których nie stwierdza się przeciwwskazań do szczepienia (patrz punkt 4.3), mogą zareagować słabiej niż pacjenci z prawidłową czynnością układu immunologicznego; dlatego w przypadku kontaktu z patogenami niektóre z tych osób mogą zachorować na odrę, świnkę lub różyczkę pomimo prawidłowego podania szczepionki. Tych pacjentów należy starannie monitorować pod kątem występowania objawów odry, świnki i różyczki.
4 Przenoszenie Przeniesienie wirusów odry i świnki ze szczepionki na osoby podatne na zachorowanie nie zostało nigdy udokumentowane. Wydalanie wirusów różyczki i odry do gardła występuje około 7 do 28 dni po szczepieniu, ze szczytową ilością wydalania około 11 dnia. Jednakże brak jest dowodów transmisji tych wydalonych wirusów na osoby podatne na zachorowanie. Przeniesienie wirusa różyczki na niemowlęta poprzez mleko matki oraz transmisja wirusa przez łożysko zostały udokumentowane, bez żadnego dowodu na wystąpienie klinicznych objawów choroby. 4.5 Interakcje z innymi produktami leczniczymi i inne rodzaje interakcji Szczepionka PRIORIX może zostać podana jednocześnie (ale w inne miejsce wstrzyknięcia) z każdą z następujących monowalentnych lub skojarzonych szczepionek [w tym sześciowalentnymi szczepionkami (DTPa-HBV-IPV/Hib)]: szczepionką przeciwko błonicy, tężcowi, krztuścowi (bezkomórkowa) (DTPa), szczepionką przeciw Haemophilus influenzae typu B (Hib), inaktywowaną szczepionką przeciw polio (IPV), szczepionką przeciw Hepatitis B (HBV), szczepionką przeciw Hepatitis A (HAV), szczepionką przeciw meningokokom grupy C, koniugowaną (MenC), szczepionką przeciw ospie (VZV), doustną szczepionką przeciw polio (OPV) oraz 10-walentną skoniugowaną szczepionką przeciw pneumokokom, zgodnie z oficjalnymi zaleceniami. Jeżeli PRIORIX nie może być podany w tym samym czasie, co inne szczepionki zawierające żywe, atenuowane wirusy, należy zachować odstęp co najmniej jednego miesiąca pomiędzy szczepieniami. Brak danych, które mogłyby poprzeć jednoczesne podawanie szczepionki PRIORIX z jakimikolwiek innymi szczepionkami. Jeżeli istnieje konieczność przeprowadzenia testów tuberkulinowych, należy je wykonać przed lub równocześnie z podaniem szczepionki, ponieważ istnieją doniesienia, że szczepionki przeciw odrze, śwince i różyczce mogą spowodować przejściowe obniżenie wrażliwości skórnej na tuberkulinę. Anergia ta może utrzymywać się do 6 tygodni po szczepieniu i w tym okresie nie należy przeprowadzać prób tuberkulinowych, aby uniknąć fałszywie ujemnych wyników. U pacjentów, którzy otrzymywali ludzką immunoglobulinę lub transfuzję krwi należy wstrzymać się z podawaniem szczepionki przez okres trzech miesięcy lub dłużej (aż do 11 miesięcy) w zależności od dawki ludzkiej immunoglobuliny jaka została podana, z powodu możliwości nie wytworzenia u nich odporności na skutek obecności biernie nabytych przeciwciał przeciwko śwince, odrze lub różyczce. 4.6 Wpływ na płodność, ciążę i laktację Płodność Szczepionka PRIORIX nie była oceniana w badaniach dotyczących płodności. Ciąża Kobiety w okresie ciąży nie powinny być szczepione szczepionką Priorix. Nie udokumentowano jednak przypadków uszkodzenia płodu po podaniu szczepionki przeciwko odrze, śwince lub różyczce kobietom w okresie ciąży. Chociaż teoretycznie nie można wykluczyć takiego ryzyka, nie zgłoszono żadnego przypadku zespołu różyczki wrodzonej u ponad 3500 nieświadomych wczesnej ciąży, podatnych na zakażenie kobiet, którym podano szczepionkę zawierającą komponentę różyczki. Z tego względu nieumyślne podanie szczepionki zawierającej komponentę odry, świnki i różyczki nieświadomej ciąży kobiecie nie powinno być powodem przerwania ciąży. 5
5 Należy unikać zajścia w ciążę przez okres 1 miesiąca od zaszczepienia. Kobiety, które planują ciążę powinny zostać pouczone o konieczności opóźnienia tej decyzji. Karmienie piersią Istnieją tylko ograniczone doniesienia dotyczące stosowania szczepionki PRIORIX w okresie karmienia piersią. Badania wykazały, ze kobiety karmiące piersią po porodzie, zaszczepione żywą, atenuowaną szczepionką przeciw różyczce mogą wydzielać wirusy wraz z mlekiem i przenosić je na dziecko karmione piersią, bez dowodu na wystąpienie klinicznych objawów choroby. Jedynie w przypadku, gdy zostanie potwierdzone lub gdy przypuszcza się, iż dziecko ma obniżoną odporność, należy przeprowadzić analizę korzyści i ryzyka wynikającego ze szczepienia matki (patrz punkt 4.3). 4.7 Wpływ na zdolność prowadzenia pojazdów i obsługiwania maszyn PRIORIX nie ma wpływu lub wywiera nieistotny wpływ na zdolność prowadzenia pojazdów i obsługiwania maszyn. 4.8 Działania niepożądane Podsumowanie profilu bezpieczeństwa Przedstawiony profil bezpieczeństwa oparty jest na danych uzyskanych z badań klinicznych, w których uczestniczyło około osób zaszczepionych szczepionką PRIORIX. Działania niepożądane, które mogą wystąpić po podaniu skojarzonej szczepionki przeciw odrze, śwince i różyczce są takie same, jak objawy obserwowane po podaniu szczepionek monowalentnych osobno lub w formie skojarzonej. W kontrolowanych badaniach klinicznych aktywnie monitorowano objawy występujące po szczepieniu w czasie 42 dniowej obserwacji. Osoby zaszczepione były również proszone o odnotowywanie wszelkich zdarzeń klinicznych pojawiających się w trakcie trwania badania. Najczęstszymi działaniami niepożądanymi występującym po podaniu szczepionki PRIORIX były zaczerwienienie w miejscu podania oraz gorączka > 38 C (mierzona w odbytnicy) lub > 37,5 C (temperatura mierzona pod pachą lub w ustach). Lista działań niepożądanych Działania niepożądane wymienione są zgodnie z częstością występowania: Bardzo często: >1/10 Często: > 1/100 do <1/10 Niezbyt często: > 1/1000 do <1/100 Rzadko: > 1/ do <1/1000 Dane pochodzące z badań klinicznych Zakażenia i zarażenia pasożytnicze: Często: zakażenie górnych dróg oddechowych Niezbyt często: zapalenia ucha środkowego Zaburzenia krwi i układu chłonnego: Niezbyt często: uogólnione powiększenie węzłów chłonnych
6 Zaburzenia układu immunologicznego: Rzadko: reakcje alergiczne Zaburzenia metabolizmu i odżywiania: Niezbyt często: jadłowstręt Zaburzenia psychiczne: Niezbyt często: nerwowość, nietypowy płacz, bezsenność Zaburzenia układu nerwowego: Rzadko: drgawki gorączkowe Zaburzenia oka: Niezbyt często: zapalenie spojówek Zaburzenia układu oddechowego, klatki piersiowej i śródpiersia: Niezbyt często: zapalenie oskrzeli, kaszel Zaburzenia układu pokarmowego: Niezbyt często: obrzęk ślinianki przyusznej, biegunka, wymioty Zaburzenia skóry i tkanki podskórnej: Często: wysypka Zaburzenia ogólne i stany w miejscu podania: Bardzo często: zaczerwienienie w miejscu podania, gorączka (mierzona w odbytnicy > 38 C; mierzona pod pachą lub w ustach > 37,5 C) Często: ból i obrzęk w miejscu podania, gorączka (mierzona w odbytnicy > 39,5 C; mierzona pod pachą lub w ustach > 39 C) Kategorie częstości występowania działań niepożądanych były podobne po podaniu pierwszej i drugiej dawki szczepionki, z wyjątkiem bólu w miejscu wstrzyknięcia, który występował często po pierwszej dawce szczepionki i bardzo często po drugiej dawce szczepionki. Dane pochodzące z okresu po wprowadzeniu do obrotu Poniższe działania niepożądane odnotowywano sporadycznie w ramach monitorowania po wprowadzeniu do obrotu. Ponieważ te działania niepożądane były zgłaszane dobrowolnie i dotyczyły populacji o nieokreślonej wielkości, nie jest możliwe określenie częstości ich występowania. Zakażenia i zarażenia pasożytnicze: Zapalenie opon mózgowo-rdzeniowych, objawy przypominające odrę, objawy przypominające świnkę (w tym zapalenie jąder, zapalenie najądrzy i zapalenie przyusznic) Zaburzenia krwi i układu chłonnego: Małopłytkowość (trombocytopenia), plamica małopłytkowa Zaburzenia układu immunologicznego: Reakcje anafilaktyczne Zaburzenia układu nerwowego: Zapalenie mózgu*, zapalenie móżdżku i objawy przypominające zapalenie móżdżku (w tym przejściowe zaburzenia chodu i przejściowa ataksja), zespół Guillain-Barre, poprzeczne zapalenie rdzenia, zapalenie nerwów obwodowych 7
7 Zaburzenia naczyniowe: Zapalenie naczyń Zaburzenia skóry i tkanki podskórnej: Rumień wielopostaciowy Zaburzenia mieśniowo-szkieletowe i tkanki Łącznej Ból stawów, zapalenie stawów *Zapalenie mózgu było zgłaszane z częstością mniejszą niż 1 na 10 milionów dawek. Ryzyko wystąpienia zapalenia mózgu w następstwie podania szczepionki jest znacznie niższe niż ryzyko wystąpienia zapalenia mózgu spowodowanego przez choroby, przeciw którym szczepionka uodparnia (odra: 1 na do przypadków; świnka: 2-4 na 1000 przypadków, różyczka około 1 na przypadków). Przypadkowe donaczyniowe podanie szczepionki może wywołać ciężką reakcję, a nawet wstrząs. Natychmiastowe działania lecznicze, które należy podjąć, zależą od ciężkości reakcji (patrz punkt 4.4). Zgłaszanie podejrzewanych działań niepożądanych Po dopuszczeniu produktu leczniczego do obrotu istotne jest zgłaszanie podejrzewanych działań niepożądanych. Umożliwia to nieprzerwane monitorowanie stosunku korzyści do ryzyka stosowania produktu leczniczego. Osoby należące do fachowego personelu medycznego powinny zgłaszać wszelkie podejrzewane działania niepożądane za pośrednictwem Departamentu Monitorowania Niepożądanych Działań Produktów Leczniczych Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych: Al. Jerozolimskie 181C Warszawa Tel.: Faks: ndl@urpl.goy.pl 4.9 Przedawkowanie Przypadki przedawkowania (podania dawki do dwukrotnie większej niż zalecana) były zgłaszane podczas monitorowania działań niepożądanych po wprowadzeniu szczepionki do obrotu. Nie były one powiązane z wystąpieniem żadnych działań niepożądanych. 5. WŁAŚCIWOŚCI FARMAKOLOGICZNE 5.1 Właściwości farmakodynamiczne Grupa farmakoterapeutyczna: szczepionka przeciwwirusowa, kod ATC: J07BD52 Odpowiedź immunologiczna u dzieci w wieku 12 miesięcy i starszych W badaniach klinicznych z udziałem dzieci w wieku od 12 miesięcy do 2 lat wykazano, iż szczepionka PRIORIX jest wysoce immunogenna. Szczepienie pojedynczą dawką szczepionki PRIORIX indukowało wytwarzanie przeciwciał przeciw odrze u 98,1%, przeciwko śwince u 94,4% oraz przeciwko różyczce u 100% uprzednio seronegatywnych zaszczepionych. 8
8 Dwa lata po szczepieniu pierwotnym wskaźniki serokonwersji wynosiły 93,4% dla odry, 94,4% dla świnki oraz 100% dla różyczki. Mimo iż brak danych dotyczących skuteczności ochronnej szczepionki PRIORIX, immunogenność jest akceptowana jako wskaźnik skuteczności ochronnej. Jednakże, niektóre z badań wskazują, iż efektywność ochrony przed świnką może być niższa niż obserwowane wskaźniki serokonwersji wobec świnki. Odpowiedź immunologiczna u dzieci w wieku od 9 do 10 miesięcy Do udziału w badaniu klinicznym zakwalifikowano 300 zdrowych dzieci w wieku od 9 do 10 miesięcy, w czasie otrzymywania pierwszej dawki szczepionki. 147 dzieci z tej grupy otrzymało równocześnie szczepionki PRIORIX i VARILRIX. Wskaźniki serokonwersji dla odry, świnki i różyczki wynosiły odpowiednio 92,6%, 91,5% oraz 100%. Wskaźniki serokonwersji po podaniu drugiej dawki, podanej 3 miesiące po pierwszej dawce wynosiły 100% dla odry, 99,2% dla świnki oraz 100% dla różyczki. W związku z tym, aby zapewnić optymalną odpowiedź immunologiczną, druga dawka szczepionki PRIORIX powinna zostać podana w ciągu 3 miesięcy. Młodzież i osoby dorosłe Bezpieczeństwo i immunogenność szczepionki PRIORIX u młodzieży i osób dorosłych nie były szczegółowo badane w badaniach klinicznych. Domięśniowa droga podania Ograniczona liczba pacjentów otrzymała w trakcie badań klinicznych szczepionkę PRIORIX domięśniowo. Wskaźniki serokonwersji wobec 3 składników były porównywalne do tych obserwowanych w przypadku podskórnej drogi podania. 5.2 Właściwości farmakokinetyczne Ocena właściwości farmakokinetycznych nie jest wymagana dla szczepionek. 5.3 Przedkliniczne dane o bezpieczeństwie Dane niekliniczne, opierające się na ogólnych badaniach bezpieczeństwa, nie wykazują żadnego ryzyka dla ludzi. 6. DANE FARMACEUTYCZNE 6.1 Wykaz substancji pomocniczych Proszek: Aminokwasy Laktoza (bezwodna) Mannitol Sorbitol Rozpuszczalnik: Woda do wstrzykiwań. 6.2 Niezgodności farmaceutyczne Nie mieszać szczepionki z innymi produktami leczniczymi, ponieważ nie wykonano badań dotyczących zgodności. 9
9 6.3 Okres ważności 2 lata Po rekonstytucji szczepionkę należy zużyć natychmiast. Jeśli nie jest to możliwe, powinna być przechowywana w temperaturze 2 C - 8 C i zużyta w ciągu 8 godzin od jej rekonstytucji. 6.4 Specjalne środki ostrożności podczas przechowywania Przechowywać i przewozić w stanie schłodzonym (2 C - 8 C). Nie zamrażać. Przechowywać w oryginalnym opakowaniu w celu ochrony przed światłem. Warunki przechowywania produktu leczniczego po rekonstytucji, patrz punkt Rodzaj i zawartość opakowania Proszek w fiolce (szkło typu I) z gumowym korkiem. 0,5 ml roztworu w ampułce (szkło typu I) - opakowania po 1, 10, 20, 25, 40 lub 100 sztuk. Nie wszystkie wielkości opakowań muszą znajdować się w obrocie. 6.6 Specjalne środki ostrożności dotyczące usuwania i przygotowywania produktu leczniczego do stosowania Przed podaniem rozpuszczalnik oraz szczepionkę poddaną rekonstytucji należy obejrzeć pod kątem obecności obcych cząstek i (lub) zmian fizycznych. W przypadku stwierdzenia nieprawidłowości w wyglądzie, należy wyrzucić rozpuszczalnik lub szczepionkę poddaną rekonstytucji. Szczepionkę należy poddać rekonstytucji poprzez dodanie do fiolki z proszkiem całej objętości rozpuszczalnika z ampułki. Następnie należy energicznie wstrząsnąć, do momentu całkowitego rozpuszczenia proszku. Zależnie od niewielkich wahań ph, szczepionka po rekonstytucji może przybierać barwę od brzoskwiniowej do różowej o odcieniu fuksji, co pozostaje bez wpływu na jej skuteczność. Należy pobrać z powrotem całą zawartość fiolki i następnie wstrzyknąć. Do podania szczepionki należy użyć nowej igły. Należy unikać kontaktu szczepionki ze środkami dezynfekującymi (patrz punkt 4.4). Wszelkie niewykorzystane resztki produktu leczniczego lub jego odpady należy usunąć zgodnie z lokalnymi przepisami. 7. PODMIOT ODPOWIEDZIALNY POSIADAJĄCY POZWOLENIE NA DOPUSZCZENIE DO OBROTU GlaxoSmithKline Biologicals S.A. rue de l'institut Rixensart, Belgia Tel.: +32(0) Fax.: +32(0)
10 8. NUMER POZWOLENIA NA DOPUSZCZENIE DO OBROTU Pozwolenie Nr DATA WYDANIA PIERWSZEGO POZWOLENIA NA DOPUSZCZENIE DO OBROTU I DATA PRZEDŁUŻENIA POZWOLENIA Data wydania pierwszego pozwolenia na dopuszczenie do obrotu: Data ostatniego przedłużenia pozwolenia: DATA ZATWIERDZENIA LUB CZĘŚCIOWEJ ZMIANY TEKSTU CHARAKTERYSTYKI PRODUKTU LECZNICZEGO
1. NAZWA PRODUKTU LECZNICZEGO PRIORIX. 1 dawka (0,5 ml) szczepionki po rekonstytucji zawiera: CCID 50. szczepu Jeryl Lynn) hodowli komórkowej
 1. NAZWA PRODUKTU LECZNICZEGO PRIORIX, 2. 1 dawka (0,5 ml) szczepionki po rekonstytucji zawiera: 1 (szczep Schwarz) 3,0 3 CCID 50 1 3,7 3 CCID 50 szczepu Jeryl Lynn) 2 (szczep Wistar RA 27/3) 3,0 3 CCID
1. NAZWA PRODUKTU LECZNICZEGO PRIORIX, 2. 1 dawka (0,5 ml) szczepionki po rekonstytucji zawiera: 1 (szczep Schwarz) 3,0 3 CCID 50 1 3,7 3 CCID 50 szczepu Jeryl Lynn) 2 (szczep Wistar RA 27/3) 3,0 3 CCID
1. NAZWA PRODUKTU LECZNICZEGO
 1. NAZWA PRODUKTU LECZNICZEGO PRIORIX, proszek i rozpuszczalnik do sporządzania roztworu do wstrzykiwań Szczepionka przeciw odrze, śwince i różyczce, żywa 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 dawka (0,5 ml)
1. NAZWA PRODUKTU LECZNICZEGO PRIORIX, proszek i rozpuszczalnik do sporządzania roztworu do wstrzykiwań Szczepionka przeciw odrze, śwince i różyczce, żywa 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 dawka (0,5 ml)
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO PRIORIX, proszek i rozpuszczalnik do sporządzania roztworu do wstrzykiwań Vaccinum morbillorum, parotitidis et rubellae vivum Szczepionka
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO PRIORIX, proszek i rozpuszczalnik do sporządzania roztworu do wstrzykiwań Vaccinum morbillorum, parotitidis et rubellae vivum Szczepionka
1. NAZWA PRODUKTU LECZNICZEGO
 1. NAZWA PRODUKTU LECZNICZEGO PRIORIX, proszek i rozpuszczalnik do sporządzania roztworu do wstrzykiwań Szczepionka przeciw odrze, śwince i różyczce, żywa 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 dawka (0,5 ml)
1. NAZWA PRODUKTU LECZNICZEGO PRIORIX, proszek i rozpuszczalnik do sporządzania roztworu do wstrzykiwań Szczepionka przeciw odrze, śwince i różyczce, żywa 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 dawka (0,5 ml)
Charakterystyka Produktu Leczniczego, Oznakowanie Opakowań i Ulotka dla Pacjenta
 Aneks III Charakterystyka Produktu Leczniczego, Oznakowanie Opakowań i Ulotka dla Pacjenta Uwaga: Ta wersja Charakterystyki Produktu Leczniczego uzyskuje ważność w momencie wydania Dezycji Komisji Europejskiej.
Aneks III Charakterystyka Produktu Leczniczego, Oznakowanie Opakowań i Ulotka dla Pacjenta Uwaga: Ta wersja Charakterystyki Produktu Leczniczego uzyskuje ważność w momencie wydania Dezycji Komisji Europejskiej.
UWAGA: W składzie szczepionki podano minimalne miana wirusów odry, świnki i różyczki oznaczane pod koniec terminu ważności preparatu.
 ULOTKA DLA PACJENTA Należy zapoznać się z właściwościami leku przed zastosowaniem PRIORIX (Vaccinum morbillorum, parotitidis et rubellae vivum) Liofilizat i rozpuszczalnik do sporządzania roztworu do wstrzykiwań
ULOTKA DLA PACJENTA Należy zapoznać się z właściwościami leku przed zastosowaniem PRIORIX (Vaccinum morbillorum, parotitidis et rubellae vivum) Liofilizat i rozpuszczalnik do sporządzania roztworu do wstrzykiwań
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO POLIORIX, roztwór do wstrzykiwań Vaccinum poliomyelitidis inactivatum Szczepionka przeciw poliomyelitis, inaktywowana 2. SKŁAD JAKOŚCIOWY
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO POLIORIX, roztwór do wstrzykiwań Vaccinum poliomyelitidis inactivatum Szczepionka przeciw poliomyelitis, inaktywowana 2. SKŁAD JAKOŚCIOWY
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Oviderm, 250 mg, krem 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 gram kremu zawiera 250 mg glikolu propylenowego Substancja pomocnicza o znanym
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Oviderm, 250 mg, krem 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 gram kremu zawiera 250 mg glikolu propylenowego Substancja pomocnicza o znanym
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO TYPHIM Vi, roztwór do wstrzykiwań w ampułko-strzykawce Vaccinum febris typhoidis polysaccharidicum Szczepionka przeciw durowi brzusznemu,
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO TYPHIM Vi, roztwór do wstrzykiwań w ampułko-strzykawce Vaccinum febris typhoidis polysaccharidicum Szczepionka przeciw durowi brzusznemu,
Ulotka dołączona do opakowania: informacja dla użytkownika
 Ulotka dołączona do opakowania: informacja dla użytkownika Priorix, proszek i rozpuszczalnik do sporządzania roztworu do wstrzykiwań Szczepionka przeciw odrze, śwince i różyczce, żywa Należy uważnie zapoznać
Ulotka dołączona do opakowania: informacja dla użytkownika Priorix, proszek i rozpuszczalnik do sporządzania roztworu do wstrzykiwań Szczepionka przeciw odrze, śwince i różyczce, żywa Należy uważnie zapoznać
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Hiberix, proszek i rozpuszczalnik do sporządzania zawiesiny do wstrzykiwań. Vaccinum haemophili stirpi b coniugatum Szczepionka przeciwko
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Hiberix, proszek i rozpuszczalnik do sporządzania zawiesiny do wstrzykiwań. Vaccinum haemophili stirpi b coniugatum Szczepionka przeciwko
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Ty - Szczepionka durowa, zawiesina do wstrzykiwań Szczepionka przeciw durowi brzusznemu. Szczepionka 20 - dawkowa 2. SKŁAD JAKOŚCIOWY
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Ty - Szczepionka durowa, zawiesina do wstrzykiwań Szczepionka przeciw durowi brzusznemu. Szczepionka 20 - dawkowa 2. SKŁAD JAKOŚCIOWY
Ulotka dołączona do opakowania: informacja dla użytkownika
 Ulotka dołączona do opakowania: informacja dla użytkownika Priorix-Tetra, proszek i rozpuszczalnik do sporządzania roztworu do wstrzykiwań Szczepionka przeciw odrze, śwince, różyczce i ospie wietrznej,
Ulotka dołączona do opakowania: informacja dla użytkownika Priorix-Tetra, proszek i rozpuszczalnik do sporządzania roztworu do wstrzykiwań Szczepionka przeciw odrze, śwince, różyczce i ospie wietrznej,
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Priorix-Tetra proszek i rozpuszczalnik do sporządzania roztworu do wstrzykiwań w ampułkostrzykawce Szczepionka przeciw odrze, śwince,
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Priorix-Tetra proszek i rozpuszczalnik do sporządzania roztworu do wstrzykiwań w ampułkostrzykawce Szczepionka przeciw odrze, śwince,
1. NAZWA PRODUKTU LECZNICZEGO
 1. NAZWA PRODUKTU LECZNICZEGO Priorix-Tetra proszek i rozpuszczalnik do sporządzania roztworu do wstrzykiwań Szczepionka przeciw odrze, śwince, różyczce i ospie wietrznej, żywa 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY
1. NAZWA PRODUKTU LECZNICZEGO Priorix-Tetra proszek i rozpuszczalnik do sporządzania roztworu do wstrzykiwań Szczepionka przeciw odrze, śwince, różyczce i ospie wietrznej, żywa 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO PNEUMO 23, roztwór do wstrzykiwań w ampułko-strzykawce Vaccinum pneumococcale polysaccharidicum Szczepionka przeciw pneumokokom, polisacharydowa
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO PNEUMO 23, roztwór do wstrzykiwań w ampułko-strzykawce Vaccinum pneumococcale polysaccharidicum Szczepionka przeciw pneumokokom, polisacharydowa
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO IMOVAX POLIO, zawiesina do wstrzykiwań w ampułko-strzykawce Vaccinum poliomyelitidis inactivatum Szczepionka przeciw poliomyelitis, inaktywowana
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO IMOVAX POLIO, zawiesina do wstrzykiwań w ampułko-strzykawce Vaccinum poliomyelitidis inactivatum Szczepionka przeciw poliomyelitis, inaktywowana
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Woodward s Gripe Water, płyn doustny, (0,46 mg + 10,5 mg)/ml 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Substancje czynne zawartość w 5 ml (1 łyżeczka)
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Woodward s Gripe Water, płyn doustny, (0,46 mg + 10,5 mg)/ml 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Substancje czynne zawartość w 5 ml (1 łyżeczka)
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Priorix-Tetra proszek i rozpuszczalnik do sporządzania roztworu do wstrzykiwań w ampułkostrzykawce Szczepionka przeciw odrze, śwince,
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Priorix-Tetra proszek i rozpuszczalnik do sporządzania roztworu do wstrzykiwań w ampułkostrzykawce Szczepionka przeciw odrze, śwince,
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. adsorbowany na wodorotlenku glinu, uwodnionym nie więcej niż 0,7 mg Al 3+
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO D - Szczepionka błonicza adsorbowana, zawiesina do wstrzykiwań Szczepionka przeciw błonicy, adsorbowana Szczepionka 20 - dawkowa 2. SKŁAD
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO D - Szczepionka błonicza adsorbowana, zawiesina do wstrzykiwań Szczepionka przeciw błonicy, adsorbowana Szczepionka 20 - dawkowa 2. SKŁAD
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Priorix-Tetra proszek i rozpuszczalnik do sporządzania roztworu do wstrzykiwań w ampułkostrzykawce Szczepionka przeciw odrze, śwince,
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Priorix-Tetra proszek i rozpuszczalnik do sporządzania roztworu do wstrzykiwań w ampułkostrzykawce Szczepionka przeciw odrze, śwince,
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Fluarix, zawiesina do wstrzykiwań w ampułko-strzykawce. Szczepionka przeciw grypie (rozszczepiony wirion), inaktywowana 2. SKŁAD JAKOŚCIOWY
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Fluarix, zawiesina do wstrzykiwań w ampułko-strzykawce. Szczepionka przeciw grypie (rozszczepiony wirion), inaktywowana 2. SKŁAD JAKOŚCIOWY
Ulotka dołączona do opakowania: informacja dla użytkownika
 Ulotka dołączona do opakowania: informacja dla użytkownika Priorix-Tetra, proszek i rozpuszczalnik do sporządzania roztworu do wstrzykiwań w ampułkostrzykawce Szczepionka przeciw odrze, śwince, różyczce
Ulotka dołączona do opakowania: informacja dla użytkownika Priorix-Tetra, proszek i rozpuszczalnik do sporządzania roztworu do wstrzykiwań w ampułkostrzykawce Szczepionka przeciw odrze, śwince, różyczce
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. CIECHOCIŃSKI SZLAM LECZNICZY, proszek do sporządzania roztworu na skórę
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO CIECHOCIŃSKI SZLAM LECZNICZY, proszek do sporządzania roztworu na skórę 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 kg proszku do sporządzania roztworu
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO CIECHOCIŃSKI SZLAM LECZNICZY, proszek do sporządzania roztworu na skórę 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 kg proszku do sporządzania roztworu
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO 1. NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO Mucosiffa liofilizat i rozpuszczalnik do sporządzania zawiesiny do wstrzykiwań dla bydła 2. SKŁAD JAKOŚCIOWY
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO 1. NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO Mucosiffa liofilizat i rozpuszczalnik do sporządzania zawiesiny do wstrzykiwań dla bydła 2. SKŁAD JAKOŚCIOWY
Ulotka dołączona do opakowania: informacja dla użytkownika. POLIORIX, roztwór do wstrzykiwań
 Ulotka dołączona do opakowania: informacja dla użytkownika POLIORIX, roztwór do wstrzykiwań Szczepionka przeciw poliomyelitis, inaktywowana Szczepionka 1-dawkowa Należy uważnie zapoznać się z treścią ulotki
Ulotka dołączona do opakowania: informacja dla użytkownika POLIORIX, roztwór do wstrzykiwań Szczepionka przeciw poliomyelitis, inaktywowana Szczepionka 1-dawkowa Należy uważnie zapoznać się z treścią ulotki
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO NERVOMIX Forte, kapsułka twarda 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 kapsułka zawiera: Substancje czynne: Valerianae radix 210 mg, Lupuli
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO NERVOMIX Forte, kapsułka twarda 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 kapsułka zawiera: Substancje czynne: Valerianae radix 210 mg, Lupuli
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Syrop tymiankowy Labima, 110 mg/ml, syrop 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Płynny wyciąg z ziela tymianku (Thymi extractum fluidum).
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Syrop tymiankowy Labima, 110 mg/ml, syrop 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Płynny wyciąg z ziela tymianku (Thymi extractum fluidum).
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO ESPUMISAN, 40 mg, kapsułki 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każda kapsułka zawiera 40 mg symetykonu. Substancje pomocnicze o znanym działaniu:
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO ESPUMISAN, 40 mg, kapsułki 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każda kapsułka zawiera 40 mg symetykonu. Substancje pomocnicze o znanym działaniu:
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO VAXIGRIP JUNIOR, zawiesina do wstrzykiwań w ampułko-strzykawce Szczepionka przeciw grypie (rozszczepiony wirion), inaktywowana 2. SKŁAD
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO VAXIGRIP JUNIOR, zawiesina do wstrzykiwań w ampułko-strzykawce Szczepionka przeciw grypie (rozszczepiony wirion), inaktywowana 2. SKŁAD
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO VAXIGRIP JUNIOR, zawiesina do wstrzykiwań w ampułko-strzykawce Szczepionka przeciw grypie (rozszczepiony wirion), inaktywowana 2. SKŁAD
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO VAXIGRIP JUNIOR, zawiesina do wstrzykiwań w ampułko-strzykawce Szczepionka przeciw grypie (rozszczepiony wirion), inaktywowana 2. SKŁAD
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Uro-Vaxom 6 mg, kapsułki, twarde 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 kapsułka twarda zawiera: liofilizat OM-89 w tym: liofilizowany lizat
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Uro-Vaxom 6 mg, kapsułki, twarde 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 kapsułka twarda zawiera: liofilizat OM-89 w tym: liofilizowany lizat
1. NAZWA PRODUKTU LECZNICZEGO
 1. NAZWA PRODUKTU LECZNICZEGO Infanrix-IPV, zawiesina do wstrzykiwań w ampułkostrzykawce Szczepionka przeciw błonicy, tężcowi, krztuścowi (bezkomórkowa, złożona) i poliomyelitis (inaktywowana), adsorbowana
1. NAZWA PRODUKTU LECZNICZEGO Infanrix-IPV, zawiesina do wstrzykiwań w ampułkostrzykawce Szczepionka przeciw błonicy, tężcowi, krztuścowi (bezkomórkowa, złożona) i poliomyelitis (inaktywowana), adsorbowana
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. Gaviscon o smaku mięty Saszetki, (500 mg + 267 mg + 160 mg)/10 ml, zawiesina doustna
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Gaviscon o smaku mięty Saszetki, (500 mg + 267 mg + 160 mg)/10 ml, zawiesina doustna 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Gaviscon o smaku
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Gaviscon o smaku mięty Saszetki, (500 mg + 267 mg + 160 mg)/10 ml, zawiesina doustna 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Gaviscon o smaku
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Inflexal V Zawiesina do wstrzykiwań Szczepionka przeciw grypie (antygen powierzchniowy), inaktywowana, wirosomalna Sezon 2012/2013 2.
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Inflexal V Zawiesina do wstrzykiwań Szczepionka przeciw grypie (antygen powierzchniowy), inaktywowana, wirosomalna Sezon 2012/2013 2.
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO VAXIGRIP, zawiesina do wstrzykiwań w ampułko-strzykawce Szczepionka przeciw grypie (rozszczepiony wirion), inaktywowana 2. SKŁAD JAKOŚCIOWY
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO VAXIGRIP, zawiesina do wstrzykiwań w ampułko-strzykawce Szczepionka przeciw grypie (rozszczepiony wirion), inaktywowana 2. SKŁAD JAKOŚCIOWY
100 ml syropu zawiera 825 mg suchego wyciągu z liści bluszczu (Hedera helix L., folium) (4-8:1). Ekstrahent: etanol 30% (m/m).
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Hedussin, 33 mg/4 ml, syrop 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 100 ml syropu zawiera 825 mg suchego wyciągu z liści bluszczu (Hedera helix
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Hedussin, 33 mg/4 ml, syrop 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 100 ml syropu zawiera 825 mg suchego wyciągu z liści bluszczu (Hedera helix
Tradycyjny produkt leczniczy roślinny przeznaczony do stosowania w określonych wskazaniach wynikających wyłącznie z jego długotrwałego stosowania.
 1. NAZWA PRODUKTU LECZNICZEGO Avioplant 250 mg kapsułki twarde 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 kapsułka zawiera 250 mg sproszkowanego kłącza imbiru (Zingiber officinale Roscoe, rhizoma). Substancja pomocnicza
1. NAZWA PRODUKTU LECZNICZEGO Avioplant 250 mg kapsułki twarde 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 kapsułka zawiera 250 mg sproszkowanego kłącza imbiru (Zingiber officinale Roscoe, rhizoma). Substancja pomocnicza
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Septofar Miód i Cytryna, 0,6 mg + 1,2 mg, pastylki twarde 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każda pastylka twarda zawiera: Amylometakrezol
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Septofar Miód i Cytryna, 0,6 mg + 1,2 mg, pastylki twarde 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każda pastylka twarda zawiera: Amylometakrezol
INFORMACJA O LEKU DLA PACJENTA Należy zapoznać się z właściwościami leku przed zastosowaniem
 INFORMACJA O LEKU DLA PACJENTA Należy zapoznać się z właściwościami leku przed zastosowaniem Hiberix Vaccinum haemophili influenzae stripe b conjugatum Proszek i rozpuszczalnik do sporządzenia zawiesiny
INFORMACJA O LEKU DLA PACJENTA Należy zapoznać się z właściwościami leku przed zastosowaniem Hiberix Vaccinum haemophili influenzae stripe b conjugatum Proszek i rozpuszczalnik do sporządzenia zawiesiny
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Patentex Oval N, 75 mg, globulki dopochwowe 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 globulka (3,15 g) zawiera: Nonoksynol-9 (INN) 75 mg Pełny
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Patentex Oval N, 75 mg, globulki dopochwowe 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 globulka (3,15 g) zawiera: Nonoksynol-9 (INN) 75 mg Pełny
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO AVAXIM 160 U, zawiesina do wstrzykiwań w ampułko-strzykawce Szczepionka przeciw wirusowemu zapaleniu wątroby typu A, inaktywowana, adsorbowana
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO AVAXIM 160 U, zawiesina do wstrzykiwań w ampułko-strzykawce Szczepionka przeciw wirusowemu zapaleniu wątroby typu A, inaktywowana, adsorbowana
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Hiberix, proszek i rozpuszczalnik do sporządzania zawiesiny do wstrzykiwań Vaccinum haemophili stirpi b coniugatum Szczepionka przeciwko
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Hiberix, proszek i rozpuszczalnik do sporządzania zawiesiny do wstrzykiwań Vaccinum haemophili stirpi b coniugatum Szczepionka przeciwko
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO VARILRIX, proszek i rozpuszczalnik do sporządzania roztworu do wstrzykiwań Szczepionka przeciw ospie wietrznej, żywa 2. SKŁAD JAKOŚCIOWY
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO VARILRIX, proszek i rozpuszczalnik do sporządzania roztworu do wstrzykiwań Szczepionka przeciw ospie wietrznej, żywa 2. SKŁAD JAKOŚCIOWY
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Oilatum 700 mg/g, żel 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 g żelu zawiera 700 mg parafiny ciekłej, lekkiej (Paraffinum perliquidum). Pełny
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Oilatum 700 mg/g, żel 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 g żelu zawiera 700 mg parafiny ciekłej, lekkiej (Paraffinum perliquidum). Pełny
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. sodu glutaminian (E 621)
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Broncho-Vaxom dla dzieci, 3,5 mg, granulat do sporządzania zawiesiny doustnej 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 dawka (saszetka) zawiera:
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Broncho-Vaxom dla dzieci, 3,5 mg, granulat do sporządzania zawiesiny doustnej 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 dawka (saszetka) zawiera:
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO AVAXIM 160 U, zawiesina do wstrzykiwań w ampułko-strzykawce Vaccinum hepatitidis A inactivatum adsorbatum Szczepionka przeciw wirusowemu
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO AVAXIM 160 U, zawiesina do wstrzykiwań w ampułko-strzykawce Vaccinum hepatitidis A inactivatum adsorbatum Szczepionka przeciw wirusowemu
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO POLCROM, 20 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 20 mg sodu kromoglikanu (Natrii cromoglicas).
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO POLCROM, 20 mg/ml, krople do oczu, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 ml roztworu zawiera 20 mg sodu kromoglikanu (Natrii cromoglicas).
Ulotka dołączona do opakowania: informacja dla użytkownika
 Ulotka dołączona do opakowania: informacja dla użytkownika Pseudovac, roztwór do wstrzykiwań Szczepionka poliwalentna przeciwko pałeczce ropy błękitnej Pseudomonas aeruginosa 1 ml szczepionki zawiera antygeny
Ulotka dołączona do opakowania: informacja dla użytkownika Pseudovac, roztwór do wstrzykiwań Szczepionka poliwalentna przeciwko pałeczce ropy błękitnej Pseudomonas aeruginosa 1 ml szczepionki zawiera antygeny
B. ULOTKA INFORMACYJNA
 B. ULOTKA INFORMACYJNA 1 ULOTKA INFORMACYJNA Versifel FeLV 1. NAZWA I ADRES PODMIOTU ODPOWIEDZIALNEGO ORAZ WYTWÓRCY ODPOWIEDZIALNEGO ZA ZWOLNIENIE SERII, JEŚLI JEST INNY Podmiot odpowiedzialny: Zoetis
B. ULOTKA INFORMACYJNA 1 ULOTKA INFORMACYJNA Versifel FeLV 1. NAZWA I ADRES PODMIOTU ODPOWIEDZIALNEGO ORAZ WYTWÓRCY ODPOWIEDZIALNEGO ZA ZWOLNIENIE SERII, JEŚLI JEST INNY Podmiot odpowiedzialny: Zoetis
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Szczepionka tężcowa adsorbowana (T), zawiesina do wstrzykiwań Szczepionka przeciw tężcowi, adsorbowana 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Szczepionka tężcowa adsorbowana (T), zawiesina do wstrzykiwań Szczepionka przeciw tężcowi, adsorbowana 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO 1. NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO Parvoruvax, zawiesina do wstrzykiwań dla świń 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY SUBSTANCJI CZYNNEJ(-YCH)
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO 1. NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO Parvoruvax, zawiesina do wstrzykiwań dla świń 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY SUBSTANCJI CZYNNEJ(-YCH)
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Neurolipon-MIP 600, 600 mg, kapsułki miękkie 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 kapsułka miękka zawiera 600 mg kwasu tioktynowego (Acidum
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Neurolipon-MIP 600, 600 mg, kapsułki miękkie 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 kapsułka miękka zawiera 600 mg kwasu tioktynowego (Acidum
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA WŁASNA PRODUKTU LECZNICZEGO Encepur Adults, zawiesina do wstrzykiwań Vaccinum encephalitidis ixodibus advectae inactivatum Szczepionka przeciw kleszczowemu
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA WŁASNA PRODUKTU LECZNICZEGO Encepur Adults, zawiesina do wstrzykiwań Vaccinum encephalitidis ixodibus advectae inactivatum Szczepionka przeciw kleszczowemu
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO VARILRIX, proszek i rozpuszczalnik do sporządzania roztworu do wstrzykiwań Vaccinum varicellae vivum Szczepionka przeciw ospie wietrznej,
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO VARILRIX, proszek i rozpuszczalnik do sporządzania roztworu do wstrzykiwań Vaccinum varicellae vivum Szczepionka przeciw ospie wietrznej,
Ulotka dołączona do opakowania: informacja dla użytkownika
 Ulotka dołączona do opakowania: informacja dla użytkownika D - Szczepionka błonicza adsorbowana zawiesina do wstrzykiwań Szczepionka przeciw błonicy, adsorbowana Nie mniej niż 30 j.m. toksoidu błoniczego/0,5
Ulotka dołączona do opakowania: informacja dla użytkownika D - Szczepionka błonicza adsorbowana zawiesina do wstrzykiwań Szczepionka przeciw błonicy, adsorbowana Nie mniej niż 30 j.m. toksoidu błoniczego/0,5
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. Antygeny powierzchniowe wirusa grypy (hemaglutynina i neuraminidaza) odpowiadające
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Influvac Zawiesina do wstrzykiwań Vaccinum influenzae inactivatum ex corticis antigeniis praeparatum Szczepionka przeciw grypie (antygen
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Influvac Zawiesina do wstrzykiwań Vaccinum influenzae inactivatum ex corticis antigeniis praeparatum Szczepionka przeciw grypie (antygen
Silny niepożądany odczyn poszczepienny u rocznego dziecka. Dr n. med. Ewa Duszczyk Pediatria przez przypadki, Warszawa, r.
 Silny niepożądany odczyn poszczepienny u rocznego dziecka Dr n. med. Ewa Duszczyk Pediatria przez przypadki, Warszawa, 18.11.2016 r. 2 Co to jest niepożądany odczyn poszczepienny Niepożądany odczyn poszczepienny
Silny niepożądany odczyn poszczepienny u rocznego dziecka Dr n. med. Ewa Duszczyk Pediatria przez przypadki, Warszawa, 18.11.2016 r. 2 Co to jest niepożądany odczyn poszczepienny Niepożądany odczyn poszczepienny
Produktu nie należy stosować pod opatrunkiem okluzyjnym lub w postaci okładów.
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Amol, produkt złożony, płyn doustny, płyn na skórę 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 g produktu zawiera: Mentholum (mentol) 17,23 mg Citronellae
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Amol, produkt złożony, płyn doustny, płyn na skórę 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 g produktu zawiera: Mentholum (mentol) 17,23 mg Citronellae
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO 1. NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO ERYSIN SINGLE SHOT, emulsja do wstrzykiwań dla świń 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY SUBSTANCJI CZYNNEJ(-YCH)
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO 1. NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO ERYSIN SINGLE SHOT, emulsja do wstrzykiwań dla świń 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY SUBSTANCJI CZYNNEJ(-YCH)
Jedna dawka (0,5 ml) po rekonstytucji, zawiera: Polisacharyd otoczkowy Haemophilus influenzae typ b.. 10 mikrogramów
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Act-HIB, 10 mikrogramów/0,5 ml, proszek i rozpuszczalnik do sporządzania roztworu do wstrzykiwań Vaccinum haemophili stirpi b coniugatum
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Act-HIB, 10 mikrogramów/0,5 ml, proszek i rozpuszczalnik do sporządzania roztworu do wstrzykiwań Vaccinum haemophili stirpi b coniugatum
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO CROTAMITON FARMAPOL płyn do stosowania na skórę, 100 mg/g 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 g płynu do stosowania na skórę zawiera 100
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO CROTAMITON FARMAPOL płyn do stosowania na skórę, 100 mg/g 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 g płynu do stosowania na skórę zawiera 100
Szczepienia ochronne. Dr hab. med. Agnieszka Szypowska Dr med. Anna Taczanowska Lek. Katarzyna Piechowiak
 Szczepienia ochronne Dr hab. med. Agnieszka Szypowska Dr med. Anna Taczanowska Lek. Katarzyna Piechowiak Klinika Pediatrii Warszawski Uniwersytet Medyczny Szczepienie (profilaktyka czynna) Podanie całego
Szczepienia ochronne Dr hab. med. Agnieszka Szypowska Dr med. Anna Taczanowska Lek. Katarzyna Piechowiak Klinika Pediatrii Warszawski Uniwersytet Medyczny Szczepienie (profilaktyka czynna) Podanie całego
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. nie mniej niż 30 j.m. nie mniej niż 40 j.m.
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO DT - Szczepionka błoniczo - tężcowa adsorbowana, zawiesina do wstrzykiwań Szczepionka przeciw błonicy i tężcowi, adsorbowana 2. SKŁAD
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO DT - Szczepionka błoniczo - tężcowa adsorbowana, zawiesina do wstrzykiwań Szczepionka przeciw błonicy i tężcowi, adsorbowana 2. SKŁAD
Ulotka dołączona do opakowania: informacja dla użytkownika
 Ulotka dołączona do opakowania: informacja dla użytkownika IMOVAX POLIO, zawiesina do wstrzykiwań w ampułko-strzykawce Szczepionka przeciw poliomyelitis, inaktywowana Należy uważnie zapoznać się z treścią
Ulotka dołączona do opakowania: informacja dla użytkownika IMOVAX POLIO, zawiesina do wstrzykiwań w ampułko-strzykawce Szczepionka przeciw poliomyelitis, inaktywowana Należy uważnie zapoznać się z treścią
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO - 1 - 1. NAZWA PRODUKTU LECZNICZEGO INFANRIX-DTPa, zawiesina do wstrzykiwań Vaccinum diphtheriae, tetani, pertussis sine cellulis ex elementis praeparatum adsorbatum
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO - 1 - 1. NAZWA PRODUKTU LECZNICZEGO INFANRIX-DTPa, zawiesina do wstrzykiwań Vaccinum diphtheriae, tetani, pertussis sine cellulis ex elementis praeparatum adsorbatum
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA WŁASNA PRODUKTU LECZNICZEGO Feminon PMS, 4 mg, kapsułki twarde 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY SUBSTANCJI CZYNNYCH Każda kapsułka twarda Feminon PMS zawiera
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA WŁASNA PRODUKTU LECZNICZEGO Feminon PMS, 4 mg, kapsułki twarde 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY SUBSTANCJI CZYNNYCH Każda kapsułka twarda Feminon PMS zawiera
ULOTKA DLA PACJENTA. nie mniej niż 2 j.m.
 ULOTKA DLA PACJENTA Należy zapoznać się z treścią ulotki przed zastosowaniem szczepionki. - Należy zachować tę ulotkę, aby w razie potrzeby móc ją ponownie przeczytać - Należy zwrócić się do lekarza lub
ULOTKA DLA PACJENTA Należy zapoznać się z treścią ulotki przed zastosowaniem szczepionki. - Należy zachować tę ulotkę, aby w razie potrzeby móc ją ponownie przeczytać - Należy zwrócić się do lekarza lub
Ulotka dołączona do opakowania: informacja dla użytkownika. VARILRIX, proszek i rozpuszczalnik do sporządzania roztworu do wstrzykiwań
 Ulotka dołączona do opakowania: informacja dla użytkownika VARILRIX, proszek i rozpuszczalnik do sporządzania roztworu do wstrzykiwań Szczepionka przeciw ospie wietrznej, żywa Należy uważnie zapoznać się
Ulotka dołączona do opakowania: informacja dla użytkownika VARILRIX, proszek i rozpuszczalnik do sporządzania roztworu do wstrzykiwań Szczepionka przeciw ospie wietrznej, żywa Należy uważnie zapoznać się
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO ISMIGEN tabletki podjęzykowe 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każda tabletka zawiera 7 mg lizatu bakterii: Staphylococcus aureus
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO ISMIGEN tabletki podjęzykowe 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każda tabletka zawiera 7 mg lizatu bakterii: Staphylococcus aureus
Charakterystyka produktu leczniczego. 1 NAZWA PRODUKTU LECZNICZEGO Tdap Szczepionka SSI, zawiesina do wstrzykiwań w ampułko-strzykawce.
 Charakterystyka produktu leczniczego 1 NAZWA PRODUKTU LECZNICZEGO Tdap Szczepionka SSI, zawiesina do wstrzykiwań w ampułko-strzykawce. Szczepionka przeciw błonicy, tężcowi i krztuścowi (bezkomórkowa, złożona),
Charakterystyka produktu leczniczego 1 NAZWA PRODUKTU LECZNICZEGO Tdap Szczepionka SSI, zawiesina do wstrzykiwań w ampułko-strzykawce. Szczepionka przeciw błonicy, tężcowi i krztuścowi (bezkomórkowa, złożona),
ODRA, ŚWINKA, RÓŻYCZKA (MMR)
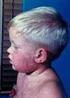 ODRA, ŚWINKA, RÓŻYCZKA (MMR) CO POWINIENEŚ WIEDZIEĆ NA TEN TEMAT? CZY JESTEŚ PEWIEN, ŻE JESTEŚ CHRONIONY PRZED MMR? ZDOBĄDŹ INFORMACJE! ZASZCZEP SIĘ! ZDOBĄDŹ OCHRONĘ! szczepionka przeciw MMR CZY WIESZ,
ODRA, ŚWINKA, RÓŻYCZKA (MMR) CO POWINIENEŚ WIEDZIEĆ NA TEN TEMAT? CZY JESTEŚ PEWIEN, ŻE JESTEŚ CHRONIONY PRZED MMR? ZDOBĄDŹ INFORMACJE! ZASZCZEP SIĘ! ZDOBĄDŹ OCHRONĘ! szczepionka przeciw MMR CZY WIESZ,
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO HAVRIX Adult, zawiesina do wstrzykiwań Szczepionka przeciw wirusowemu zapaleniu wątroby typu A, inaktywowana, adsorbowana 2. SKŁAD JAKOŚCIOWY
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO HAVRIX Adult, zawiesina do wstrzykiwań Szczepionka przeciw wirusowemu zapaleniu wątroby typu A, inaktywowana, adsorbowana 2. SKŁAD JAKOŚCIOWY
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Syrop z bluszczu Labima 5,4 mg/ml, syrup 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Suchy wyciąg z liści bluszczu (Hedera helix L., folium). 1 ml
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Syrop z bluszczu Labima 5,4 mg/ml, syrup 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Suchy wyciąg z liści bluszczu (Hedera helix L., folium). 1 ml
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO M-M-RVAXPRO proszek i rozpuszczalnik do sporządzania zawiesiny do wstrzykiwań Szczepionka przeciw odrze, śwince i różyczce (żywa).
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO M-M-RVAXPRO proszek i rozpuszczalnik do sporządzania zawiesiny do wstrzykiwań Szczepionka przeciw odrze, śwince i różyczce (żywa).
Miejscowe oczyszczanie skóry: Wetrzeć niewielką ilość emulsji do kąpieli w zwilżoną uprzednio skórę, a następnie spłukać wodą i osuszyć ręcznikiem.
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Oilatum 634 mg/g, emulsja do kąpieli 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 g emulsji do kąpieli zawiera 634 mg parafiny ciekłej, lekkiej (Paraffinum
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Oilatum 634 mg/g, emulsja do kąpieli 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 g emulsji do kąpieli zawiera 634 mg parafiny ciekłej, lekkiej (Paraffinum
Ulotka dołączona do opakowania: informacja dla pacjenta
 Ulotka dołączona do opakowania: informacja dla pacjenta Hiberix, proszek i rozpuszczalnik do sporządzania zawiesiny do wstrzykiwań Szczepionka przeciwko zakażeniom haemophilus typ b, skoniugowana Należy
Ulotka dołączona do opakowania: informacja dla pacjenta Hiberix, proszek i rozpuszczalnik do sporządzania zawiesiny do wstrzykiwań Szczepionka przeciwko zakażeniom haemophilus typ b, skoniugowana Należy
Act-HIB 10 mikrogramów/0,5 ml, proszek i rozpuszczalnik do sporządzania roztworu do wstrzykiwań Szczepionka przeciw haemophilus typ b, skoniugowana
 Ulotka dołączona do opakowania: informacja dla użytkownika Act-HIB 10 mikrogramów/0,5 ml, proszek i rozpuszczalnik do sporządzania roztworu do wstrzykiwań Szczepionka przeciw haemophilus typ b, skoniugowana
Ulotka dołączona do opakowania: informacja dla użytkownika Act-HIB 10 mikrogramów/0,5 ml, proszek i rozpuszczalnik do sporządzania roztworu do wstrzykiwań Szczepionka przeciw haemophilus typ b, skoniugowana
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO 1. NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO Ingelvac MycoFLEX zawiesina do wstrzykiwań dla świń 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Inaktywowana Mycoplasma
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO 1. NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO Ingelvac MycoFLEX zawiesina do wstrzykiwań dla świń 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Inaktywowana Mycoplasma
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA
 ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA GAMMA anty-hbs 200 Roztwór do wstrzykiwań Immunoglobulinum humanum hepatitidis B Immunoglobulina ludzka przeciw wirusowemu zapaleniu wątroby typu B Należy
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA GAMMA anty-hbs 200 Roztwór do wstrzykiwań Immunoglobulinum humanum hepatitidis B Immunoglobulina ludzka przeciw wirusowemu zapaleniu wątroby typu B Należy
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO 1 1. NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO CEVAC MASS L liofilizat do sporządzania zawiesiny do podania na oczy i nozdrza dla kur 2. SKŁAD JAKOŚCIOWY
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO 1 1. NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO CEVAC MASS L liofilizat do sporządzania zawiesiny do podania na oczy i nozdrza dla kur 2. SKŁAD JAKOŚCIOWY
Pełny wykaz substancji pomocniczych, patrz punkt 6.1 Charakterystyki Produktu Leczniczego (ChPL).
 Nazwa produktu leczniczego i nazwa powszechnie stosowana: Aerius 0,5 mg/ml, roztwór doustny, desloratadyna Skład jakościowy i ilościowy w odniesieniu do substancji czynnych oraz tych substancji pomocniczych,
Nazwa produktu leczniczego i nazwa powszechnie stosowana: Aerius 0,5 mg/ml, roztwór doustny, desloratadyna Skład jakościowy i ilościowy w odniesieniu do substancji czynnych oraz tych substancji pomocniczych,
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA HANDLOWA LEKU GOTOWEGO SALICYLOL 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY SUBSTANCJI CZYNNYCH (W PRZELICZENIU NA 100g)
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA HANDLOWA LEKU GOTOWEGO SALICYLOL 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY SUBSTANCJI CZYNNYCH (W PRZELICZENIU NA 100g)
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Polyvaccinum submite, Polyvaccinum mite, Polyvaccinum forte Zawiesina do wstrzykiwań. Nieswoista szczepionka bakteryjna. 2. SKŁAD JAKOŚCIOWY
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Polyvaccinum submite, Polyvaccinum mite, Polyvaccinum forte Zawiesina do wstrzykiwań. Nieswoista szczepionka bakteryjna. 2. SKŁAD JAKOŚCIOWY
VARILRIX (Vaccinum varicellae vivum) Liofilizat i rozpuszczalnik do sporządzenia roztworu do wstrzykiwań podskórnych.
 INFORMACJA O LEKU DLA PACJENTA Należy zapoznać się z właściwościami leku przed zastosowaniem VARILRIX (Vaccinum varicellae vivum) Liofilizat i rozpuszczalnik do sporządzenia roztworu do wstrzykiwań podskórnych.
INFORMACJA O LEKU DLA PACJENTA Należy zapoznać się z właściwościami leku przed zastosowaniem VARILRIX (Vaccinum varicellae vivum) Liofilizat i rozpuszczalnik do sporządzenia roztworu do wstrzykiwań podskórnych.
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Debridat, 100 mg, tabletki powlekane 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 tabletka zawiera 100 mg trimebutyny maleinianu (Trimebutini maleas).
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Debridat, 100 mg, tabletki powlekane 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 tabletka zawiera 100 mg trimebutyny maleinianu (Trimebutini maleas).
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Cholinex Intense, 2,5 mg + 1,2 mg, tabletki do ssania 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jedna tabletka do ssania zawiera 2,5 mg heksylorezorcynolu
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO Cholinex Intense, 2,5 mg + 1,2 mg, tabletki do ssania 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jedna tabletka do ssania zawiera 2,5 mg heksylorezorcynolu
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO VAXIGRIP, zawiesina do wstrzykiwań w ampułko-strzykawce Szczepionka przeciw grypie (rozszczepiony wirion), inaktywowana 2. SKŁAD JAKOŚCIOWY
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO VAXIGRIP, zawiesina do wstrzykiwań w ampułko-strzykawce Szczepionka przeciw grypie (rozszczepiony wirion), inaktywowana 2. SKŁAD JAKOŚCIOWY
Ulotka dołączona do opakowania: informacja dla użytkownika. Synagis 100 mg/ml roztwór do wstrzykiwań Substancja czynna: paliwizumab
 Ulotka dołączona do opakowania: informacja dla użytkownika Synagis 100 mg/ml roztwór do wstrzykiwań Substancja czynna: paliwizumab Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem tego
Ulotka dołączona do opakowania: informacja dla użytkownika Synagis 100 mg/ml roztwór do wstrzykiwań Substancja czynna: paliwizumab Należy uważnie zapoznać się z treścią ulotki przed zastosowaniem tego
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY. Antygen powierzchniowy wirusa zapalenia wątroby typu B (HBsAg)*
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Hepavax Gene TF, 20 mikrogramów, zawiesina do wstrzykiwań Szczepionka przeciw wirusowemu zapaleniu wątroby typu B (rdna) 2. SKŁAD JAKOŚCIOWY
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Hepavax Gene TF, 20 mikrogramów, zawiesina do wstrzykiwań Szczepionka przeciw wirusowemu zapaleniu wątroby typu B (rdna) 2. SKŁAD JAKOŚCIOWY
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. POLCROM 2%, 20 mg/ml (2,8 mg/dawkę donosową), aerozol do nosa, roztwór
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO POLCROM 2%, 20 mg/ml (2,8 mg/dawkę donosową), aerozol do nosa, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każdy ml roztworu zawiera 20 mg
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO POLCROM 2%, 20 mg/ml (2,8 mg/dawkę donosową), aerozol do nosa, roztwór 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Każdy ml roztworu zawiera 20 mg
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1.NAZWA PRODUKTU LECZNICZEGO Transpulmin S, (10 g + 3 g)/100 g, krem 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 g kremu zawiera 100 mg olejku eukaliptusowego (Eucalypti aetheroleum)
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1.NAZWA PRODUKTU LECZNICZEGO Transpulmin S, (10 g + 3 g)/100 g, krem 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY 1 g kremu zawiera 100 mg olejku eukaliptusowego (Eucalypti aetheroleum)
Immunoglobulinum humanum hepatitidis B Immunoglobulina ludzka przeciw wirusowemu zapaleniu wątroby typu B
 ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA GAMMA anty-hbs 200 Roztwór do wstrzykiwań Immunoglobulinum humanum hepatitidis B Immunoglobulina ludzka przeciw wirusowemu zapaleniu wątroby typu B Należy
ULOTKA DLA PACJENTA: INFORMACJA DLA UŻYTKOWNIKA GAMMA anty-hbs 200 Roztwór do wstrzykiwań Immunoglobulinum humanum hepatitidis B Immunoglobulina ludzka przeciw wirusowemu zapaleniu wątroby typu B Należy
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO 1 1. NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO Rispoval 3 BRSV PI3 BVD Liofilizat i zawiesina do sporządzania zawiesiny do wstrzykiwań dla bydła. 2.
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO 1 1. NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO Rispoval 3 BRSV PI3 BVD Liofilizat i zawiesina do sporządzania zawiesiny do wstrzykiwań dla bydła. 2.
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO PROSPAN, 26 mg, pastylki miękkie 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jedna pastylka miękka zawiera 26 mg wyciągu (w postaci suchego wyciągu)
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO PROSPAN, 26 mg, pastylki miękkie 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jedna pastylka miękka zawiera 26 mg wyciągu (w postaci suchego wyciągu)
Ulotka dołączona do opakowania: informacja dla użytkownika
 Ulotka dołączona do opakowania: informacja dla użytkownika Polio Sabin oral, zawiesina doustna Vaccinum poliomyelitidis perorale Szczepionka przeciwko poliomyelitis, doustna Należy uważnie zapoznać się
Ulotka dołączona do opakowania: informacja dla użytkownika Polio Sabin oral, zawiesina doustna Vaccinum poliomyelitidis perorale Szczepionka przeciwko poliomyelitis, doustna Należy uważnie zapoznać się
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Quintanrix, proszek i zawiesina do sporządzenia zawiesiny do wstrzykiwań Szczepionka przeciwko błonicy, tężcowi, krztuścowi (pełnokomórkowa),
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1. NAZWA PRODUKTU LECZNICZEGO Quintanrix, proszek i zawiesina do sporządzenia zawiesiny do wstrzykiwań Szczepionka przeciwko błonicy, tężcowi, krztuścowi (pełnokomórkowa),
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. NAZWA PRODUKTU LECZNICZEGO Polyvaccinum mite, krople do nosa, zawiesina. Nieswoista szczepionka bakteryjna.. SKŁAD JAKOŚCIOWY I ILOŚCIOWY ml szczepionki zawiera inaktywowane
CHARAKTERYSTYKA PRODUKTU LECZNICZEGO. NAZWA PRODUKTU LECZNICZEGO Polyvaccinum mite, krople do nosa, zawiesina. Nieswoista szczepionka bakteryjna.. SKŁAD JAKOŚCIOWY I ILOŚCIOWY ml szczepionki zawiera inaktywowane
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO
 ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO M-M-RVAXPRO proszek i rozpuszczalnik do sporządzania zawiesiny do wstrzykiwań Szczepionka przeciw odrze, śwince i różyczce (żywa).
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO 1 1. NAZWA PRODUKTU LECZNICZEGO M-M-RVAXPRO proszek i rozpuszczalnik do sporządzania zawiesiny do wstrzykiwań Szczepionka przeciw odrze, śwince i różyczce (żywa).
