GŁÓWNY INSPEKTORAT FARMACEUTYCZNY Departament Inspekcji ds. Wytwarzania
|
|
|
- Kazimiera Kasprzak
- 8 lat temu
- Przeglądów:
Transkrypt
1 GŁÓWNY INSPEKTORAT FARMACEUTYCZNY Departament Inspekcji ds. Wytwarzania Na podstawie uzupełnionej zgodnie z poniższymi wskazówkami, Informacji o zakresie wytwarzania lub importu, stanowiącej część Wniosku o wydanie zezwolenia bądź Wniosku o zmianę zezwolenia przygotowana zostanie treść zezwolenia na wytwarzanie lub import. INFORMACJA O ZAKRESIE WYTWARZANIA LUB IMPORTU PRODUKTÓW LECZNICZYCH: - stanowiąca punkt 2*, a w przypadku badanych produktów leczniczych punkt 3* Wniosku o wydanie zezwolenia bądź punkt 3**, a w przypadku badanych produktów leczniczych punkt 4** Wniosku o zmianę zezwolenia, powinna być przygotowana odrębnie dla każdego miejsca wytwarzania (CZĘŚĆ 1*) lub importu (CZĘŚĆ 2*), * numeracja w odniesieniu do Rozporządzenia MZ z dnia 10 marca 2015 r. w sprawie wzoru wniosku o wydanie zezwolenia na wytwarzanie lub import produktów leczniczych (Dz. U. z 2015 r., poz. 365) ** numeracja w odniesieniu do Rozporządzenia MZ z dnia 10 marca 2015 r. w sprawie wzoru wniosku o zmianę zezwolenia na wytwarzanie lub import produktów leczniczych (Dz. U. z 2015 r., poz. 368) - powinna być przygotowana odrębnie w przypadku wytwarzania produktów leczniczych przeznaczonych dla ludzi i wytwarzania produktów leczniczych weterynaryjnych, z zastosowaniem poniższych informacji. Wypełniając Informację o zakresie wytwarzania lub importu produktów leczniczych, należy wykreślić punkty, które nie dotyczą. CZĘŚĆ 1 Zakres operacji wytwórczych prowadzony przez posiadacza zezwolenia powinien zostać zaznaczony w Informacji o zakresie wytwarzania lub importu produktów leczniczych z uwzględnieniem poniższych wyjaśnień: Operacje procesowe (punkty z pominięciem punktów dotyczących certyfikacji serii) Pakowanie w opakowania bezpośrednie (punkty z uwzględnieniem komentarza pod punktem ) Pakowanie w opakowania zewnętrzne (punkty ) Certyfikacja serii obejmuje poszczególne lub wszystkie etapy procesu wytwarzania produktu leczniczego do etapu pakowania w opakowania bezpośrednie (włącznie) z uwzględnieniem komentarza pod punktem obejmuje umieszczenie i zamknięcie produktu leczniczego wewnątrz materiału opakowaniowego produktu końcowego, mającego bezpośredni kontakt z produktem leczniczym. - obejmuje umieszczenie i zamknięcie w zewnętrznym materiale opakowaniowym produktu leczniczego, zapakowanego uprzednio w opakowanie bezpośrednie; - obejmuje również operacje etykietowania lub dołączenie innych elementów, wymienionych w pozwoleniu na dopuszczenie do obrotu lub w podstawowej dokumentacji produktu w przypadku badanych produktów leczniczych. obejmuje certyfikację serii produktu końcowego przez Osobę Wykwalifikowaną. Certyfikacja serii odnosi się do wszystkich postaci farmaceutycznych w danej sekcji (1.1.3 Certyfikacja serii dla produktów sterylnych lub Certyfikacja serii dla produktów niesterylnych), chyba że wprowadzone zostały wyłączenia/ 3 Oct 2014; EMA/572454/2014 Rev 17 Strona 1 z 7
2 Kontrola jakości restrykcje w Zastrzeżeniach lub uwagach wyjaśniających dotyczących operacji wytwórczych/importowych. Dla biologicznych produktów leczniczych pkt Certyfikacja serii oznacza ostatnią certyfikację końcowej postaci farmaceutycznej produktu; należy zaznaczyć również odpowiednie punkty i/lub 1.2.2, aby wskazać rodzaj produktu, którego dotyczy. Etap przepakowania produktów leczniczych w ramach importu równoległego lub dystrybucji równoległej, po którym wystawiane jest potwierdzenie zgodności przeprowadzonego etapu z wymaganiami GMP, wymaga zaznaczenia punktów 1.1.3, bądź oraz wpisania Zastrzeżeń lub uwag wyjaśniających dotyczących operacji wytwórczych o następującej przykładowej treści: Punkt tylko w zakresie certyfikacji serii produktów leczniczych przepakowywanych w ramach importu równoległego i dystrybucji równoległej. obejmuje rodzaj kontroli laboratoryjnej wytwarzanych produktów leczniczych wykonywanej w miejscu wytwarzania. Kontrola laboratoryjna produktów leczniczych przeznaczonych dla ludzi powinna odbywać się u wytwórców posiadających zezwolenie na wytwarzanie produktów leczniczych przeznaczonych dla ludzi. Analogicznie należy postępować w stosunku do produktów leczniczych weterynaryjnych, badanych oraz produktów leczniczych importowanych. Wszystkie informacje, restrykcje lub wyłączenia (np. jeżeli produkt leczniczy musi być wytwarzany w dedykowanych obszarach), powinny zostać zawarte w Zastrzeżeniach lub uwagach wyjaśniających dotyczących operacji wytwórczych z odniesieniem do konkretnego punktu w tabeli lub postaci farmaceutycznej. Informacje dotyczące prowadzenia wszystkich etapów wytwarzania, podczas których mamy do czynienia z otwartym produktem***, uważanym za wysoce uczulający, wysoce toksyczny, silnie działający lub mogący stanowić zagrożenie z innych powodów, bądź zawierającym substancje o takim działaniu, np. z grup: antybiotyki β-laktamowe, inne wysoko uczulające antybiotyki, żywe komórki, patogeny (poziom bezpieczeństwa 3 i 4), radiofarmaceutyki, produkty lecznicze zawierające priony, genotoksyny albo teratogenny, produkty ekto-pasożytobójcze, inne (np. produkty wysoko toksyczne) powinna zostać umieszczona w Zastrzeżeniach lub uwagach wyjaśniających dotyczących operacji wytwórczych z odniesieniem do konkretnego punktu w tabeli. *** w odniesieniu do punktów 1.1.1, 1.1.2, 1.2.1, 1.3.1, 1.4.2, wskazanych w załączniku do Rozporządzenia MZ z dnia 10 marca 2015 r. w sprawie wzoru wniosku o zmianę zezwolenia na wytwarzanie lub import produktów leczniczych (Dz. U. z 2015 r., poz. 368) Magazynowanie - dla każdego miejsca wytwarzania posiadającego zezwolenie na wytwarzanie lub import produktów leczniczych, w którym prowadzone są operacje procesowe lub pakowanie produktów leczniczych, automatycznie zezwolenie obejmuje również magazynowanie, bez 3 Oct 2014; EMA/572454/2014 Rev 17 Strona 2 z 7
3 konieczności dodatkowego wpisywania tej operacji. Jeżeli w miejscu wytwarzania prowadzone są inne operacje, z których magazynowanie nie wynika automatycznie, np. certyfikacja serii, wówczas operacja magazynowania powinna zostać zawarta w punkcie <inne>. Dystrybucja - dla każdego miejsca wytwarzania objętego zezwoleniem na wytwarzanie lub import produktów leczniczych, w którym prowadzone są operacje procesowe lub pakowanie serii produktów leczniczych, zezwolenie automatycznie obejmuje dystrybucję własnych produktów leczniczych, chyba że wprowadzone zostały wyłączenia/restrykcje w Zastrzeżeniach lub uwagach wyjaśniających dotyczących operacji wytwórczych. CZĘŚĆ 1: Operacje wytwórcze (Manufacturing Operations) 1.1 Produkty sterylne (Sterile products) Aseptycznie wytwarzane (Aseptically prepared) Postaci płynne o dużej objętości (Large volume liquids) Liofilizaty (Lyophilisates) Postaci półstałe (Semi-solids) Postaci płynne o małej objętości (Small volume liquids) Postaci stałe i implanty (Solids and implants) Inne produkty aseptycznie wytwarzane: wymienić (Other aseptically prepared products <free text>) Sterylizowane końcowo (Terminally sterilised) Uwaga: Gdy sterylizacja końcowa nie jest prowadzona w miejscu wytwarzania formy farmaceutycznej, tylko zlecana innemu wytwórcy, w Zastrzeżeniach lub uwagach wyjaśniających dotyczących operacji wytwórczych powinna znajdować się informacja o zleceniu etapu sterylizacji w odniesieniu do konkretnych punktów z formami farmaceutycznymi z tabeli Postaci płynne o dużej objętości (Large volume liquids) Postaci półstałe (Semi-solids) Postaci płynne o małej objętości (Small volume liquids) Postaci stałe i implanty (Solids and implants) Inne produkty sterylizowane końcowo: wymienić (Other terminalny sterilised prepared products <free text>) Certyfikacja serii (Batch Certification) 1.2 Produkty niesterylne (Non-sterile products) Produkty niesterylne (Non-sterile products) Kapsułki, twarda powłoka (Capsules, hard shell) Kapsułki, miękka powłoka (Capsules, soft shell) Lecznicze gumy do żucia (Chewing gums) Impregnowane matryce (Impregnated matrices) Płyn do użytku zewnętrznego (Liquids for external use) Płyn do użytku wewnętrznego (Liquids for internal use) Gazy medyczne (Medicinal gases) Inne postaci stałe (Other solid dosage forms) Produkty lecznicze w pojemnikach pod ciśnieniem (Pressurised preparations) Generatory radionuklidów (Radionuclide generators) Postaci półstałe (Semi-solids) Czopki (Suppositories) Tabletki (Tablets) Systemy transdermalne (Transdermal patches) Systemy dożwaczowe (Intraruminal devices) 3 Oct 2014; EMA/572454/2014 Rev 17 Strona 3 z 7
4 Premiksy weterynaryjne (Veterinary premixes) Inne niesterylne produkty: wymienić (Other non-sterile medicinal product <free text>) Punkt Produkty lecznicze w pojemnikach pod ciśnieniem - dotyczy produktów w specjalnych pojemnikach pod ciśnieniem gazu. Natomiast w przypadku, gdy wydozowanie produktu odbywa się za pomocą mechanicznej pompki, bez zastosowania gazu wytłaczającego, wtedy taka postać farmaceutyczna produktu leczniczego zostaje sklasyfikowana odpowiednio jako: Płyn do użytku zewnętrznego lub Płyn do użytku wewnętrznego. W punkcie Inne niesterylne produkty: wymienić - należy wyszczególnić np. wytwarzanie produktów pośrednich (podać rodzaj produktów) Certyfikacja serii (Batch Certification) 1.3 Biologiczne produkty lecznicze (Biological medicinal products) Poniższe kategorie biologicznych produktów leczniczych powinny być stosowane do określenia czy Wytwórca prowadzi jakiekolwiek etapy procesu związane z wytwarzaniem produktów biologicznych. Wytwarzanie substancji biologicznej może być częścią ciągłych etapów procesu w wytwarzaniu końcowego produktu biologicznego i te operacje powinny być także ujęte w tej sekcji, jeżeli dotyczy. Gdy operacje wytwórcze obejmują wytwarzanie końcowej postaci farmaceutycznej biologicznych produktów leczniczych, powinna zostać zaznaczona również odpowiednia postać farmaceutyczna (np Liofilizaty) Biologiczne produkty lecznicze (Biological medicinal products) Produkty krwiopochodne (Blood products) Produkty immunologiczne (Immunological products) Produkty terapii komórkowej (Cell therapy products) Produkty terapii genowej (Gene therapy products) Produkty biotechnologiczne (Biotechnology products) Produkty pochodzenia ludzkiego lub zwierzęcego (Human or animal extracted products) Produkty inżynierii tkankowej (Tissue engineered products) Inne biologiczne produkty lecznicze: wymienić (Other biological medicinal products <free text>) Certyfikacja serii (Batch certification) Należy zaznaczyć również odpowiednio punkty i/lub Produkty krwiopochodne (Blood products) Produkty immunologiczne (Immunological products) Produkty terapii komórkowej (Cell therapy products) Produkty terapii genowej (Gene therapy products) Produkty biotechnologiczne (Biotechnology products) Produkty pochodzenia ludzkiego lub zwierzęcego (Human or animal extracted products) Produkty inżynierii tkankowej (Tissue engineered products) Inne biologiczne produkty lecznicze: wymienić (Other biological medicinal products <free text>) 3 Oct 2014; EMA/572454/2014 Rev 17 Strona 4 z 7
5 1.4 Inne produkty lub operacje wytwórcze (Other products or manufacturing activity) Jeżeli wytwarzanie obejmuje m.in. produkty roślinne lub homeopatyczne, należy zaznaczyć odpowiednią postać farmaceutyczną w sekcji 1.1. i/lub 1.2. oraz odpowiedni rodzaj produktów w sekcji Jeżeli wytwarzane są jedynie produkty roślinne lub homeopatyczne, należy to wykazać w Zastrzeżeniach lub uwagach wyjaśniających dotyczących operacji wytwórczych w odniesieniu do punktów z odpowiedniej sekcji 1.1. i/lub 1.2 Przykład: Tabletki Produkty lecznicze roślinne Zastrzeżenia lub uwagi wyjaśniające dotyczące operacji wytwórczych : Pkt dotyczy tylko produktów roślinnych Wytwarzanie (Manufacture of) Produkty lecznicze roślinne (Herbal products) Produkty lecznicze homeopatyczne (Homoeopathic products) Inne: wymienić (Other) Sterylizacja substancji czynnej lub składnika, lub produktu gotowego (Sterilisation of active substances / excipients / finished product) Ten punkt powinien być zaznaczany przez Zleceniobiorcę, w przypadku gdy proces sterylizacji nie jest prowadzony przez wytwórcę formy farmaceutycznej np. wykonawca, któremu zlecono naświetlanie promieniami gamma formy farmaceutycznej, wytworzonej przez innego wytwórcę Filtracja (Filtration) Sterylizacja suchym gorącym powietrzem (Dry heat) Sterylizacja nasyconą parą wodną (Moist heat) Sterylizacja chemiczna (Chemical) Naświetlanie promieniami gamma (Gamma irradiation) Sterylizacja strumieniami elektronów (Electron beam) Inne : wymienić (Other <free text>) 1.5 Pakowanie (Packaging) Pakowanie w opakowania bezpośrednie (Primary packing) Pakowanie w opakowania bezpośrednie produktów sterylnych, włączone jest do części operacji procesowych, zawartych w punkcie 1.1. pod warunkiem, że brak jest innego komentarza w Zastrzeżeniach lub uwagach wyjaśniających dotyczących operacji wytwórczych w odniesieniu do konkretnej postaci farmaceutycznej sterylnego produktu leczniczego Kapsułki, twarda powłoka (Capsules, hard shell) Kapsułki, miękka powłoka (Capsules, soft shell) Lecznicze gumy do żucia (Chewing gums) Impregnowane matryce (Impregnated matrices) Płyn do użytku zewnętrznego (Liquids for external use) Płyn do użytku wewnętrznego (Liquids for internal use) Gazy medyczne (Medicinal gases) Inne postaci stałe (Other solid dosage forms) Produkty lecznicze w pojemnikach pod ciśnieniem (Pressurised preparations) Generatory radionuklidów (Radionuclide generators) Postaci półstałe (Semi-solids) Czopki (Suppositories) Tabletki (Tablets) Systemy transdermalne (Transdermal patches) 3 Oct 2014; EMA/572454/2014 Rev 17 Strona 5 z 7
6 Systemy dożwaczowe (Intraruminal devices) Premiksy weterynaryjne (Veterinary premixes) Inne niesterylne produkty: wymienić (Other non-sterile medicinal product <free text>) Jeżeli wytwórca prowadzi tylko pakowanie w opakowania bezpośrednie produktów, które następnie są sterylizowane końcowo, ale nie jest wytwórcą formy farmaceutycznej (np. implanty), powinien wpisać w punkcie Inne niesterylne produkty lecznicze, komentarz: Pakowanie w opakowania bezpośrednie (nazwa postaci farmaceutycznej), które podlegają sterylizacji końcowej Pakowanie w opakowania zewnętrzne (Secondary packing) Punkt Pakowanie w opakowania zewnętrzne obejmuje pakowanie wszystkich postaci farmaceutycznych, chyba że wprowadzone zostały wyłączenia/restrykcje w Zastrzeżeniach lub uwagach wyjaśniających dotyczących operacji wytwórczych. Wytwórca, którego jedyną operacją wytwórczą będzie oznakowywanie produktów leczniczych etykietą próbka bezpłatna, produktów wykorzystywanych w celach marketingowych powinien mieć zaznaczony pkt i wprowadzoną restrykcję tylko oznakowanie: próbka bezpłatna. 1.6 Badania w kontroli jakości (Quality control testing) Badania mikrobiologiczne: produkty sterylne (Microbiological: sterility) Badania mikrobiologiczne: produkty niesterylne (Microbiological: non-sterility) Badania fizykochemiczne (Chemical / Physical) Badania biologiczne (Biological) CZĘŚĆ 2: Import produktów leczniczych (Importation of medicinal products) 2.1 Badania w kontroli jakości importowanych produktów leczniczych (Quality control testing of imported medicinal products) Kontrola jakości importowanych produktów leczniczych obejmuje rodzaj kontroli laboratoryjnej importowanych końcowych produktów leczniczych, wykonywanej w miejscu importu; Gdy w miejscu importu prowadzone są badania w Kontroli Jakości w odniesieniu do wytwarzanych produktów leczniczych, kategorie badań objęte zezwoleniem powinny zostać określone w odpowiednich sekcjach CZĘŚCI 1 (punkt 1.6) oraz CZĘŚCI 2 (punkt 2.1) Badania mikrobiologiczne: produkty sterylne (Microbiological: sterility) Badania mikrobiologiczne: produkty niesterylne (Microbiological: non-sterility) Badania fizykochemiczne (Chemical / Physical) Badania biologiczne (Biological) 2.2 Certyfikacja serii importowanych produktów leczniczych (Batch certification of imported medicinal products) Punkt 2.2. powinien zostać zaznaczony w przypadku certyfikacji produktu końcowego. Jeżeli wytwórca jest również fizycznym miejscem importu powinien zaznaczyć także punkt Dla importerów badanych produktów leczniczych, zezwolenie na certyfikację importowanych produktów porównawczych powinno być wskazane przez uwagi wyjaśniające w odniesieniu do odpowiedniej kategorii produktów z punktów , , i/lub Produkty sterylne (Sterile Products) Wytwarzane aseptycznie (Aseptically prepared) Sterylizowane końcowo (Terminally sterilised) 3 Oct 2014; EMA/572454/2014 Rev 17 Strona 6 z 7
7 2.2.2 Produkty niesterylne (Non-sterile products) Biologiczne produkty lecznicze (Biological medicinal products) Zaznaczona kategoria biologicznych produktów leczniczych powinna zostać uzupełniona poprzez zaznaczenie odpowiednich punktów i/lub Produkty krwiopochodne (Blood products) Produkty immunologiczne (Immunological products) Produkty terapii komórkowej (Cell therapy products) Produkty terapii genowej (Gene therapy products) Produkty biotechnologiczne (Biotechnology products) Produkty pochodzenia ludzkiego lub zwierzęcego (Human or animal extracted products) Produkty inżynierii tkankowej (Tissue engineered products) Inne biologiczne produkty lecznicze: wymienić (Other biological medicinal products <free text>) Inna działalność importowa -inne aktywności związane z importem, które nie zostały 2.3 zawarte powyżej(other importation activities) Fizyczne miejsce importu (Site of physical importation) Zaznaczenie tego punktu oznacza, że miejsce importu posiada zezwolenie na otrzymywanie i przechowywanie importowanych końcowych produktów oczekujących na certyfikację przez Osobę Wykwalifikowaną. Certyfikacja musi być zaznaczona osobno w odniesieniu do odpowiedniej kategorii produktów w sekcji Import produktów pośrednich poddawanych dalszym operacjom wytwórczym: wymienić (Importation of intermediate which undergoes further processing <free text>) Powinien zostać określony rodzaj produktu pośredniego lub produktu luzem Biologiczne substancje czynne (Biological active substance) Inne: wymienić (Other <free text>) 3 Oct 2014; EMA/572454/2014 Rev 17 Strona 7 z 7
Warszawa, dnia 17 marca 2015 r. Poz. 365 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 10 marca 2015 r.
 DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ Warszawa, dnia 17 marca 2015 r. Poz. 365 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 10 marca 2015 r. w sprawie wzoru wniosku o wydanie zezwolenia na wytwarzanie
DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ Warszawa, dnia 17 marca 2015 r. Poz. 365 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 10 marca 2015 r. w sprawie wzoru wniosku o wydanie zezwolenia na wytwarzanie
Warszawa, dnia 13 sierpnia 2013 r. Poz. 922
 Warszawa, dnia 13 sierpnia 2013 r. Poz. 922 OBWIESZCZENIE MINISTRA ZDROWIA z dnia 18 kwietnia 2013 r. w sprawie ogłoszenia jednolitego tekstu rozporządzenia Ministra Zdrowia w sprawie wzoru wniosku o wydanie
Warszawa, dnia 13 sierpnia 2013 r. Poz. 922 OBWIESZCZENIE MINISTRA ZDROWIA z dnia 18 kwietnia 2013 r. w sprawie ogłoszenia jednolitego tekstu rozporządzenia Ministra Zdrowia w sprawie wzoru wniosku o wydanie
ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 12 stycznia 2011 r.
 Dziennik Ustaw Nr 20 1480 Poz. 109 109 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 12 stycznia 2011 r. w sprawie wzoru wniosku o wydanie zezwolenia na wytwarzanie produktów leczniczych i badanych produktów
Dziennik Ustaw Nr 20 1480 Poz. 109 109 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 12 stycznia 2011 r. w sprawie wzoru wniosku o wydanie zezwolenia na wytwarzanie produktów leczniczych i badanych produktów
Zofia Ulz. wedhig rozdzielnika. Warszawa, dnia...2.01.4.-12-.. 1 5 GIF-P-L-0210/3-15/MO/14
 RPW/95442/2014 P Data:2014-12-17 Glowny Impektor Farmaceutyczny Zofia Ulz Warszawa, dnia...2.01.4.-12-.. 1 5 GIF-P-L-0210/3-15/MO/14 wedhig rozdzielnika Na podstawie upowaznien wydanych przez Ministra
RPW/95442/2014 P Data:2014-12-17 Glowny Impektor Farmaceutyczny Zofia Ulz Warszawa, dnia...2.01.4.-12-.. 1 5 GIF-P-L-0210/3-15/MO/14 wedhig rozdzielnika Na podstawie upowaznien wydanych przez Ministra
Komunikat Nr 8 I 04 G³ównego Inspektora Farmaceutycznego
 ~..{æ._-~:::---~~::::::::::~ G ÓWNY INSPEKTOR FARMACEUTYCZNY Warszawa, dnia 29 wrzeœnia 2004r. Dorota Duliban GIF-P-O21-15/D/AK/O4 Komunikat Nr 8 I 04 G³ównego Inspektora Farmaceutycznego W zwi¹zku z licznymi
~..{æ._-~:::---~~::::::::::~ G ÓWNY INSPEKTOR FARMACEUTYCZNY Warszawa, dnia 29 wrzeœnia 2004r. Dorota Duliban GIF-P-O21-15/D/AK/O4 Komunikat Nr 8 I 04 G³ównego Inspektora Farmaceutycznego W zwi¹zku z licznymi
ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 29 czerwca 2011 r.
 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 29 czerwca 2011 r. w sprawie wzoru wniosku o wydanie zgody na wytwarzanie Na podstawie art. 38a ust. 6 pkt 1 ustawy z dnia 6 września 2001 r. Prawo farmaceutyczne
ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 29 czerwca 2011 r. w sprawie wzoru wniosku o wydanie zgody na wytwarzanie Na podstawie art. 38a ust. 6 pkt 1 ustawy z dnia 6 września 2001 r. Prawo farmaceutyczne
1. Dane dotyczące produktu leczniczego, który zostanie wprowadzony do obrotu na terytorium Rzeczypospolitej Polskiej w ramach importu równoległego
 Załącznik nr 1 WZÓR WNIOSEK O WYDANIE POZWOLENIA NA IMPORT RÓWNOLEGŁY produkt leczniczy produkt leczniczy weterynaryjny (Wypełnia pracownik Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych
Załącznik nr 1 WZÓR WNIOSEK O WYDANIE POZWOLENIA NA IMPORT RÓWNOLEGŁY produkt leczniczy produkt leczniczy weterynaryjny (Wypełnia pracownik Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych
Kwalifikacja wykonawców różnych etapów wytwarzania
 Kwalifikacja wykonawców różnych etapów wytwarzania Dorota Prokopczyk Warszawskie Zakłady Farmaceutyczne Polfa S.A. wytwarzaniem produktów leczniczych -jest każde działanie prowadzące do powstania produktu
Kwalifikacja wykonawców różnych etapów wytwarzania Dorota Prokopczyk Warszawskie Zakłady Farmaceutyczne Polfa S.A. wytwarzaniem produktów leczniczych -jest każde działanie prowadzące do powstania produktu
Pytania dotyczące Rejestru Wytwórców, Importerów i Dystrybutorów Substancji Czynnych
 Pytania dotyczące Rejestru Wytwórców, Importerów i Dystrybutorów Substancji Czynnych 1. Czy są dostępne, a jeżeli tak to gdzie, wersje edytowalne (word) wzorów wniosków o zmianę zezwolenia na wytwarzanie
Pytania dotyczące Rejestru Wytwórców, Importerów i Dystrybutorów Substancji Czynnych 1. Czy są dostępne, a jeżeli tak to gdzie, wersje edytowalne (word) wzorów wniosków o zmianę zezwolenia na wytwarzanie
Warszawa, dnia 11 czerwca 2014 r. Poz. 775 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 3 czerwca 2014 r.
 DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ Warszawa, dnia 11 czerwca 2014 r. Poz. 775 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 3 czerwca 2014 r. w sprawie wzoru wniosku o wydanie pozwolenia na import równoległy
DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ Warszawa, dnia 11 czerwca 2014 r. Poz. 775 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 3 czerwca 2014 r. w sprawie wzoru wniosku o wydanie pozwolenia na import równoległy
4) badanie zanieczyszczeń: mineralnych, biologicznych lub botanicznych innych niż opisanych dla homeopatycznej substancji czynnej; 5) oznaczenie
 Załącznik nr 4 Sposób przedstawiania dokumentacji dotyczącej jakości dołączanej do wniosku o dopuszczenie do obrotu produktów leczniczych homeopatycznych z użyciem formatu CTD Celem tego załącznika jest
Załącznik nr 4 Sposób przedstawiania dokumentacji dotyczącej jakości dołączanej do wniosku o dopuszczenie do obrotu produktów leczniczych homeopatycznych z użyciem formatu CTD Celem tego załącznika jest
FSP Galena. Jest prężnie rozwijającą się polską firmą o 65-letniej tradycji i doświadczeniu, zajmującą się: produkcją farmaceutyczną,
 Wiarygodny partner FSP Galena Jest prężnie rozwijającą się polską firmą o 65-letniej tradycji i doświadczeniu, zajmującą się: - produkcją farmaceutyczną, - produkcją suplementów diety, - konfekcjonowaniem,
Wiarygodny partner FSP Galena Jest prężnie rozwijającą się polską firmą o 65-letniej tradycji i doświadczeniu, zajmującą się: - produkcją farmaceutyczną, - produkcją suplementów diety, - konfekcjonowaniem,
Wiarygodny partner do najważniejszych zadań
 Wiarygodny partner do najważniejszych zadań FSP Galena Jest prężnie rozwijającą się polską firmą o 65-letniej tradycji i doświadczeniu, zajmującą się : - produkcją farmaceutyczną, - produkcją suplementów
Wiarygodny partner do najważniejszych zadań FSP Galena Jest prężnie rozwijającą się polską firmą o 65-letniej tradycji i doświadczeniu, zajmującą się : - produkcją farmaceutyczną, - produkcją suplementów
Wiarygodny partner do najważniejszych zadań
 Wiarygodny partner do najważniejszych zadań FSP Galena Jest prężnie rozwijającą się polską firmą o 70-letniej tradycji i doświadczeniu, zajmującą się : - produkcją farmaceutyczną, - produkcją suplementów
Wiarygodny partner do najważniejszych zadań FSP Galena Jest prężnie rozwijającą się polską firmą o 70-letniej tradycji i doświadczeniu, zajmującą się : - produkcją farmaceutyczną, - produkcją suplementów
Warszawa, dnia 14 grudnia 2017 r. Poz. 2337
 Warszawa, dnia 14 grudnia 2017 r. Poz. 2337 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 5 grudnia 2017 r. w sprawie wzoru wniosku o dopuszczenie do obrotu surowca farmaceutycznego do sporządzania leków recepturowych
Warszawa, dnia 14 grudnia 2017 r. Poz. 2337 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 5 grudnia 2017 r. w sprawie wzoru wniosku o dopuszczenie do obrotu surowca farmaceutycznego do sporządzania leków recepturowych
DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ
 DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ Warszawa, dnia 15 lipca 2015 r. Poz. 988 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 8 lipca 2015 r. w sprawie sposobu ustalania i uiszczania opłat związanych z dopuszczeniem
DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ Warszawa, dnia 15 lipca 2015 r. Poz. 988 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 8 lipca 2015 r. w sprawie sposobu ustalania i uiszczania opłat związanych z dopuszczeniem
Badania kliniczne doświadczenie Polski
 URZĄD REJESTRACJI PRODUKTÓW LECZNICZYCH, WYROBÓW MEDYCZNYCH I PRODUKTÓW BIOBÓJCZYCH Badania kliniczne doświadczenie Polski Michał Gryz Dyrektor Departamentu Inspekcji Produktów Leczniczych i Wyrobów Medycznych
URZĄD REJESTRACJI PRODUKTÓW LECZNICZYCH, WYROBÓW MEDYCZNYCH I PRODUKTÓW BIOBÓJCZYCH Badania kliniczne doświadczenie Polski Michał Gryz Dyrektor Departamentu Inspekcji Produktów Leczniczych i Wyrobów Medycznych
Badania kliniczne w Polsce
 Badania kliniczne w Polsce Michał Gryz Dyrektor Departamentu Inspekcji Produktów Leczniczych i Wyrobów Medycznych www.urpl.gov.pl 1 60 dni na ocenę projektu badania URZĄD REJESTRACJI PRODUKTÓW LECZNICZYCH,
Badania kliniczne w Polsce Michał Gryz Dyrektor Departamentu Inspekcji Produktów Leczniczych i Wyrobów Medycznych www.urpl.gov.pl 1 60 dni na ocenę projektu badania URZĄD REJESTRACJI PRODUKTÓW LECZNICZYCH,
Certyfikacja i zwalnianie serii produktów leczniczych do obrotu. 2 Kongres Świata Przemysłu Farmaceutycznego Rzeszów, 10 11 czerwca 2010
 Certyfikacja i zwalnianie serii produktów leczniczych do obrotu 2 Kongres Świata Przemysłu Farmaceutycznego Rzeszów, 10 11 czerwca 2010 Kim jestem? Agnieszka Szwocer Absolwentka UW, Wydział Biologii Absolwentka
Certyfikacja i zwalnianie serii produktów leczniczych do obrotu 2 Kongres Świata Przemysłu Farmaceutycznego Rzeszów, 10 11 czerwca 2010 Kim jestem? Agnieszka Szwocer Absolwentka UW, Wydział Biologii Absolwentka
20 czerwca 2016r., Warszawa
 20 czerwca 2016r., Warszawa CERTYFIKACJA I ZWALNIANIE SERII NOWY ANEKS 16 GMP Najważniejsze zmiany w prawie i ich skutki dla wytwórcy produktów leczniczych Wymagania Aneksu 16 GMP nowe obowiązki, uprawnienia
20 czerwca 2016r., Warszawa CERTYFIKACJA I ZWALNIANIE SERII NOWY ANEKS 16 GMP Najważniejsze zmiany w prawie i ich skutki dla wytwórcy produktów leczniczych Wymagania Aneksu 16 GMP nowe obowiązki, uprawnienia
Rola Osoby Wykwalifikowanej wstrzymanie, wycofanie serii produktu leczniczego
 Rola Osoby Wykwalifikowanej wstrzymanie, wycofanie serii produktu leczniczego 2 Kongres Świata Przemysłu Farmaceutycznego Rzeszów, 10 11 czerwca 2010 Rozporządzenie Rozporządzenie Ministra Zdrowia z dnia
Rola Osoby Wykwalifikowanej wstrzymanie, wycofanie serii produktu leczniczego 2 Kongres Świata Przemysłu Farmaceutycznego Rzeszów, 10 11 czerwca 2010 Rozporządzenie Rozporządzenie Ministra Zdrowia z dnia
Kancelaria Sejmu s. 1/33. Dz.U. 2015 poz. 28. USTAWA z dnia 19 grudnia 2014 r. o zmianie ustawy Prawo farmaceutyczne oraz niektórych innych ustaw
 Kancelaria Sejmu s. 1/33 Dz.U. 2015 poz. 28 USTAWA z dnia 19 grudnia 2014 r. 1), 2) o zmianie ustawy Prawo farmaceutyczne oraz niektórych innych ustaw Art. 1. W ustawie z dnia 6 września 2001 r. Prawo
Kancelaria Sejmu s. 1/33 Dz.U. 2015 poz. 28 USTAWA z dnia 19 grudnia 2014 r. 1), 2) o zmianie ustawy Prawo farmaceutyczne oraz niektórych innych ustaw Art. 1. W ustawie z dnia 6 września 2001 r. Prawo
GMP - Dobra Praktyka Wytwarzania (ang. Good Manufacturing Prac:ce)
 GMP - Dobra Praktyka Wytwarzania (ang. Good Manufacturing Prac:ce) GMP definicja GMP to system oparty na procedurach produkcyjnych, kontrolnych oraz zapewnienia jakości, gwarantujących, że wytworzone produkty
GMP - Dobra Praktyka Wytwarzania (ang. Good Manufacturing Prac:ce) GMP definicja GMP to system oparty na procedurach produkcyjnych, kontrolnych oraz zapewnienia jakości, gwarantujących, że wytworzone produkty
WZÓR WNIOSEK O PRZEDŁUŻENIE OKRESU WAŻNOŚCI POZWOLENIA NA DOPUSZCZENIE DO OBROTU PRODUKTU LECZNICZEGO
 Dziennik Ustaw Nr 80 4927 Poz. 436 Załączniki do rozporządzenia Ministra Zdrowia z dnia 23 marca 2011 r. (poz. 436) Załącznik nr 1 WZÓR WNIOSEK O PRZEDŁUŻENIE OKRESU WAŻNOŚCI POZWOLENIA NA DOPUSZCZENIE
Dziennik Ustaw Nr 80 4927 Poz. 436 Załączniki do rozporządzenia Ministra Zdrowia z dnia 23 marca 2011 r. (poz. 436) Załącznik nr 1 WZÓR WNIOSEK O PRZEDŁUŻENIE OKRESU WAŻNOŚCI POZWOLENIA NA DOPUSZCZENIE
GMP w przemyśle farmaceutycznym
 GMP w przemyśle farmaceutycznym Jadwiga Marczewska, Krystyna Mysłowska* GMP (ang. Good Manufacturing Practice) Dobra Praktyka Wytwarzania, to połączenie efektywnych procedur produkcyjnych oraz skutecznej
GMP w przemyśle farmaceutycznym Jadwiga Marczewska, Krystyna Mysłowska* GMP (ang. Good Manufacturing Practice) Dobra Praktyka Wytwarzania, to połączenie efektywnych procedur produkcyjnych oraz skutecznej
2) sposób prowadzenia dokumentacji wytwarzania i obrotu, a także sposób transportu pasz leczniczych;
 ROZPORZĄDZENIE MINISTRA ROLNICTWA I ROZWOJU WSI1) z dnia 17 grudnia 2002 r. w sprawie pasz leczniczych (Dz. U. z dnia 15 stycznia 2003 r.) Na podstawie art. 45 ust. 5 ustawy z dnia 6 września 2001 r. -
ROZPORZĄDZENIE MINISTRA ROLNICTWA I ROZWOJU WSI1) z dnia 17 grudnia 2002 r. w sprawie pasz leczniczych (Dz. U. z dnia 15 stycznia 2003 r.) Na podstawie art. 45 ust. 5 ustawy z dnia 6 września 2001 r. -
Uwaga iii. Niniejszy aneks ma zastosowanie również w przypadku radiofarmaceutyków używanych do badań klinicznych.
 Załącznik nr 2 ANEKS 3 WYTWARZANIE PRODUKTÓW RADIOFARMACEUTYCZNYCH Reguła Wytwarzanie radiofarmaceutyków powinno być prowadzone zgodnie z zasadami Dobrej Praktyki Wytwarzania dla Produktów Leczniczych
Załącznik nr 2 ANEKS 3 WYTWARZANIE PRODUKTÓW RADIOFARMACEUTYCZNYCH Reguła Wytwarzanie radiofarmaceutyków powinno być prowadzone zgodnie z zasadami Dobrej Praktyki Wytwarzania dla Produktów Leczniczych
GMP w wytwarzaniu produktu chemicznego
 GMP w wytwarzaniu produktu chemicznego Good Manufacturing Practice - GMP Good Manufacturing Practice - GMP (Dobra Praktyka Wytwarzania/Produkcji) połączenie efektywnych procedur produkcyjnych oraz skutecznej
GMP w wytwarzaniu produktu chemicznego Good Manufacturing Practice - GMP Good Manufacturing Practice - GMP (Dobra Praktyka Wytwarzania/Produkcji) połączenie efektywnych procedur produkcyjnych oraz skutecznej
Wniosek o dopuszczenie do obrotu produktu leczniczego wymienionego w art. 20 ust. 1 pkt 1-5 ustawy z dnia 6 września 2001 r. - Prawo farmaceutyczne
 (Wypełnia pracownik Urzędu) ---------------- numer wniosku... kod ATC, jeŝeli został nadany ---------------- ------------------------------ data złoŝenia wniosku podpis i pieczęć pracownika Wniosek o dopuszczenie
(Wypełnia pracownik Urzędu) ---------------- numer wniosku... kod ATC, jeŝeli został nadany ---------------- ------------------------------ data złoŝenia wniosku podpis i pieczęć pracownika Wniosek o dopuszczenie
Przedsiębiorstwo Farmaceutyczne Okoniewscy VETOS-FARMA. Polski producent farmaceutyczny Firma rodzinna Zaufany partner
 Przedsiębiorstwo Farmaceutyczne Okoniewscy VETOS-FARMA Polski producent farmaceutyczny Firma rodzinna Zaufany partner P.F.O. VETOS-FARMA Przedsiębiorstwo Farmaceutyczne Okoniewscy Vetos-Farma jest polską,
Przedsiębiorstwo Farmaceutyczne Okoniewscy VETOS-FARMA Polski producent farmaceutyczny Firma rodzinna Zaufany partner P.F.O. VETOS-FARMA Przedsiębiorstwo Farmaceutyczne Okoniewscy Vetos-Farma jest polską,
DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ
 DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ Warszawa, dnia 8 stycznia 2015 r. Poz. 28 USTAWA z dnia 19 grudnia 2014 r. 1), 2) o zmianie ustawy Prawo farmaceutyczne oraz niektórych innych ustaw Art. 1. W ustawie
DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ Warszawa, dnia 8 stycznia 2015 r. Poz. 28 USTAWA z dnia 19 grudnia 2014 r. 1), 2) o zmianie ustawy Prawo farmaceutyczne oraz niektórych innych ustaw Art. 1. W ustawie
POMAGAMY ZREALIZOWAĆ TWÓJ CEL LOGISTYKA BADAŃ KLINICZNYCH
 POMAGAMY ZREALIZOWAĆ TWÓJ CEL LOGISTYKA BADAŃ KLINICZNYCH O FIRMIE Jesteśmy działającą od 2006 roku firmą typu CRO (Contract Research Organization), obejmującą swoim zasięgiem teren całej Polski oraz obszar
POMAGAMY ZREALIZOWAĆ TWÓJ CEL LOGISTYKA BADAŃ KLINICZNYCH O FIRMIE Jesteśmy działającą od 2006 roku firmą typu CRO (Contract Research Organization), obejmującą swoim zasięgiem teren całej Polski oraz obszar
ZAŁĄCZNIK Nr 2 WZÓR WNIOSEK O DOPUSZCZENIE DO OBROTU PRODUKTU HOMEOPATYCZNEGO, W TYM PRODUKTU HOMEOPATYCZNEGO WETERYNARYJNEGO
 ZAŁĄCZNIK Nr 2 WZÓR WNIOSEK O DOPUSZCZENIE DO OBROTU PRODUKTU HOMEOPATYCZNEGO, W TYM PRODUKTU HOMEOPATYCZNEGO WETERYNARYJNEGO 2. DOKUMENTY DOŁĄCZONE DO WNIOSKU Wypełnia pracownik przyjmujący wniosek,
ZAŁĄCZNIK Nr 2 WZÓR WNIOSEK O DOPUSZCZENIE DO OBROTU PRODUKTU HOMEOPATYCZNEGO, W TYM PRODUKTU HOMEOPATYCZNEGO WETERYNARYJNEGO 2. DOKUMENTY DOŁĄCZONE DO WNIOSKU Wypełnia pracownik przyjmujący wniosek,
Warszawa, dnia 23 kwietnia 2013 r. Poz. 491 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 10 kwietnia 2013 r.
 DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ Warszawa, dnia 23 kwietnia 2013 r. Poz. 491 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 10 kwietnia 2013 r. w sprawie kontroli seryjnej wstępnej produktów leczniczych
DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ Warszawa, dnia 23 kwietnia 2013 r. Poz. 491 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 10 kwietnia 2013 r. w sprawie kontroli seryjnej wstępnej produktów leczniczych
FARMACJA PRZEMYSŁOWA Studia podyplomowe 3-semestralne
 FARMACJA PRZEMYSŁOWA Studia podyplomowe 3-semestralne Wydział Farmaceutyczny GDAŃSKI UNIWERSYTET MEDYCZNY Absolwent studiów podyplomowych Farmacja przemysłowa uzyska szczególne kwalifikacje do: pełnienia
FARMACJA PRZEMYSŁOWA Studia podyplomowe 3-semestralne Wydział Farmaceutyczny GDAŃSKI UNIWERSYTET MEDYCZNY Absolwent studiów podyplomowych Farmacja przemysłowa uzyska szczególne kwalifikacje do: pełnienia
o rządowym projekcie ustawy o uchyleniu ustawy o wyrobach stosowanych w medycynie weterynaryjnej oraz o zmianie innych ustaw (druk nr 2732).
 SEJM RZECZYPOSPOLITEJ POLSKIEJ VI kadencja Druk nr 2790 S P R A W O Z D A N I E KOMISJI ROLNICTWA I ROZWOJU WSI ORAZ KOMISJI ZDROWIA o rządowym projekcie ustawy o uchyleniu ustawy o wyrobach stosowanych
SEJM RZECZYPOSPOLITEJ POLSKIEJ VI kadencja Druk nr 2790 S P R A W O Z D A N I E KOMISJI ROLNICTWA I ROZWOJU WSI ORAZ KOMISJI ZDROWIA o rządowym projekcie ustawy o uchyleniu ustawy o wyrobach stosowanych
Certificate of Pharmaceutical Product (CPP)
 Certificate of Pharmaceutical Product (CPP) Informacje dla Wytwórcy, Eksportera lub organu uprawnionego w sprawach dopuszczenia do obrotu w kraju importera, dotyczące zasad wydawania certyfikatu Certificate
Certificate of Pharmaceutical Product (CPP) Informacje dla Wytwórcy, Eksportera lub organu uprawnionego w sprawach dopuszczenia do obrotu w kraju importera, dotyczące zasad wydawania certyfikatu Certificate
ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 2009 r. zmieniające rozporządzenie w sprawie wymagań Dobrej Praktyki Wytwarzania
 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 2009 r. zmieniające rozporządzenie w sprawie wymagań Dobrej Praktyki Wytwarzania Na podstawie art. 39 ust. 4 pkt 1 ustawy z dnia 6 września 2001 r. - Prawo farmaceutyczne
ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 2009 r. zmieniające rozporządzenie w sprawie wymagań Dobrej Praktyki Wytwarzania Na podstawie art. 39 ust. 4 pkt 1 ustawy z dnia 6 września 2001 r. - Prawo farmaceutyczne
Dyrektywa 90/385/EWG
 Dyrektywa 90/385/EWG Załącznik nr 1 Załącznik nr 1 Polskie Normy zharmonizowane opublikowane do 31.12.2013 Wykaz norm z dyrektywy znajduje się również na www.pkn.pl Według Dziennika Urzędowego UE (20013/C
Dyrektywa 90/385/EWG Załącznik nr 1 Załącznik nr 1 Polskie Normy zharmonizowane opublikowane do 31.12.2013 Wykaz norm z dyrektywy znajduje się również na www.pkn.pl Według Dziennika Urzędowego UE (20013/C
SZKOLENIE OKRESOWE GMP zmiany, nowości WARSZTATY
 10 października 2016r., Warszawa SZKOLENIE OKRESOWE GMP Aktualne wymagania GMP - wpływ na system jakości wytwórcy Implementacja wymagań do systemu jakości wytwórcy w zakresie substancji czynnej i substancji
10 października 2016r., Warszawa SZKOLENIE OKRESOWE GMP Aktualne wymagania GMP - wpływ na system jakości wytwórcy Implementacja wymagań do systemu jakości wytwórcy w zakresie substancji czynnej i substancji
Wiarygodny partner do najważniejszych zadań
 Wiarygodny partner do najważniejszych zadań FSP Galena Jest prężnie rozwijającą się polską firmą o 70-letniej tradycji i doświadczeniu, zajmującą się : - produkcją farmaceutyczną, - produkcją suplementów
Wiarygodny partner do najważniejszych zadań FSP Galena Jest prężnie rozwijającą się polską firmą o 70-letniej tradycji i doświadczeniu, zajmującą się : - produkcją farmaceutyczną, - produkcją suplementów
Badania mikrobiologiczne wg PN-EN ISO 11737
 Badania mikrobiologiczne wg PN-EN ISO 11737 mgr Agnieszka Wąsowska Specjalistyczne Laboratorium Badawcze ITA-TEST Z-ca Dyrektora ds. Badań Kierownik Zespołu Badań Mikrobiologicznych i Chemicznych Tel.022
Badania mikrobiologiczne wg PN-EN ISO 11737 mgr Agnieszka Wąsowska Specjalistyczne Laboratorium Badawcze ITA-TEST Z-ca Dyrektora ds. Badań Kierownik Zespołu Badań Mikrobiologicznych i Chemicznych Tel.022
ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 23 marca 2011 r. w sprawie wzoru wniosków o przedłużenie lub skrócenie okresu ważności pozwolenia
 436 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 23 marca 2011 r. w sprawie wzoru wniosków o przedłużenie lub skrócenie okresu ważności pozwolenia na dopuszczenie do obrotu produktu leczniczego Na podstawie
436 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 23 marca 2011 r. w sprawie wzoru wniosków o przedłużenie lub skrócenie okresu ważności pozwolenia na dopuszczenie do obrotu produktu leczniczego Na podstawie
SZKOLENIE OKRESOWE GMP zmiany, nowości
 Firma szkoleniowa 2015 roku TOP 3 w rankingu firm szkoleniowych zaprasza na szkolenie: SZKOLENIE OKRESOWE GMP zmiany, nowości WARSZTATY 20 maja 2016r. Centrum Konferencyjne Golden Floor, Al. Jerozolimskie
Firma szkoleniowa 2015 roku TOP 3 w rankingu firm szkoleniowych zaprasza na szkolenie: SZKOLENIE OKRESOWE GMP zmiany, nowości WARSZTATY 20 maja 2016r. Centrum Konferencyjne Golden Floor, Al. Jerozolimskie
Interpretacja nowych polskich rozporządzeń dotyczących substancji i mieszanin niebezpiecznych
 Interpretacja nowych polskich rozporządzeń dotyczących substancji i mieszanin niebezpiecznych SYGOS IX Ustroń, 29.11-01.12.2012 r. Dorota Dominiak dorota.dominiak@chemikalia.gov.pl Ustawa Ustawa z dnia
Interpretacja nowych polskich rozporządzeń dotyczących substancji i mieszanin niebezpiecznych SYGOS IX Ustroń, 29.11-01.12.2012 r. Dorota Dominiak dorota.dominiak@chemikalia.gov.pl Ustawa Ustawa z dnia
Załączniki do rozporządzenia Ministra Zdrowia z dnia 28 marca 2012 r. Załącznik nr 1 ROZDZIAŁ 4 DOKUMENTACJA
 ROZDZIAŁ 4 DOKUMENTACJA Załączniki do rozporządzenia Ministra Zdrowia z dnia 28 marca 2012 r. Załącznik nr 1 Reguła Dobra dokumentacja jest zasadniczym elementem Systemu Zapewnienia Jakości. Wytwórca powinien
ROZDZIAŁ 4 DOKUMENTACJA Załączniki do rozporządzenia Ministra Zdrowia z dnia 28 marca 2012 r. Załącznik nr 1 Reguła Dobra dokumentacja jest zasadniczym elementem Systemu Zapewnienia Jakości. Wytwórca powinien
SPOSÓB PRZEDSTAWIANIA DOKUMENTACJI DOŁĄCZANEJ DO WNIOSKU O DOPUSZCZENIE DO OBROTU PRODUKTU LECZNICZEGO WETERYNARYJNEGO IMMUNOLOGICZNEGO
 Załącznik nr 2 SPOSÓB PRZEDSTAWIANIA DOKUMENTACJI DOŁĄCZANEJ DO WNIOSKU O DOPUSZCZENIE DO OBROTU PRODUKTU LECZNICZEGO WETERYNARYJNEGO IMMUNOLOGICZNEGO CZĘŚĆ I - STRESZCZENIE DOKUMENTACJI I A IB I B 1 I
Załącznik nr 2 SPOSÓB PRZEDSTAWIANIA DOKUMENTACJI DOŁĄCZANEJ DO WNIOSKU O DOPUSZCZENIE DO OBROTU PRODUKTU LECZNICZEGO WETERYNARYJNEGO IMMUNOLOGICZNEGO CZĘŚĆ I - STRESZCZENIE DOKUMENTACJI I A IB I B 1 I
VI. Wydawanie Certyfikatu CPP (Certificate of Pharmaceutical Product)
 Źródło: http://www.gif.gov.pl/pl/nadzor/wytwarzanie-i-import-pr/certyfikaty-cpp/549,wydawanie-certyfikatu-cpp-certificate-of- Pharmaceutical-Product.html Wygenerowano: Wtorek, 2 lutego 2016, 17:21 VI.
Źródło: http://www.gif.gov.pl/pl/nadzor/wytwarzanie-i-import-pr/certyfikaty-cpp/549,wydawanie-certyfikatu-cpp-certificate-of- Pharmaceutical-Product.html Wygenerowano: Wtorek, 2 lutego 2016, 17:21 VI.
Magdalena Szymaniak EMA, Biologics Working Party
 Magdalena Szymaniak EMA, Biologics Working Party Punkty prezentacji Biologiczne produkty lecznicze, w tym referencyjne i biopodobne Sposoby rejestracji leków biologicznych Wymagania rejestracyjne dla leków
Magdalena Szymaniak EMA, Biologics Working Party Punkty prezentacji Biologiczne produkty lecznicze, w tym referencyjne i biopodobne Sposoby rejestracji leków biologicznych Wymagania rejestracyjne dla leków
ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 2 marca 2011 r.
 314 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 2 marca 2011 r. zmieniające rozporządzenie w sprawie sposobu ustalania i uiszczania opłat związanych z dopuszczeniem do obrotu produktu leczniczego Na podstawie
314 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 2 marca 2011 r. zmieniające rozporządzenie w sprawie sposobu ustalania i uiszczania opłat związanych z dopuszczeniem do obrotu produktu leczniczego Na podstawie
ROZPORZĄDZENIE MINISTRA ZDROWIA1)
 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia r. w sprawie wymagań, jakim powinna odpowiadać osoba wykwalifikowana odpowiedzialna za jakość i kontrolę serii produktu leczniczego przed wprowadzeniem na rynek
ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia r. w sprawie wymagań, jakim powinna odpowiadać osoba wykwalifikowana odpowiedzialna za jakość i kontrolę serii produktu leczniczego przed wprowadzeniem na rynek
DYREKTYWA KOMISJI 2003/94/WE. z dnia 8 października 2003 r.
 DYREKTYWA KOMISJI 2003/94/WE z dnia 8 października 2003 r. ustanawiająca zasady i wytyczne dobrej praktyki wytwarzania w odniesieniu do produktów leczniczych stosowanych u ludzi oraz produktów leczniczych
DYREKTYWA KOMISJI 2003/94/WE z dnia 8 października 2003 r. ustanawiająca zasady i wytyczne dobrej praktyki wytwarzania w odniesieniu do produktów leczniczych stosowanych u ludzi oraz produktów leczniczych
Powyższy artykuł określa kto jest odpowiedzialny za wprowadzenie do obrotu produktu kosmetycznego. Może to być producent, dystrybutor lub importer.
 Wprowadzanie produktów kosmetycznych do obrotu Przepisy prawa dotyczące wprowadzania kosmetyków do obrotu w Polsce reguluje ustawa z dnia 30 marca 2001 roku o kosmetykach (Dz.U. Nr 42, poz. 473 ze zm.).
Wprowadzanie produktów kosmetycznych do obrotu Przepisy prawa dotyczące wprowadzania kosmetyków do obrotu w Polsce reguluje ustawa z dnia 30 marca 2001 roku o kosmetykach (Dz.U. Nr 42, poz. 473 ze zm.).
ROZPORZĄDZENIE MINISTRA ROLNICTWA I ROZWOJU WSI 1)
 Pasze lecznicze nieprzeznaczone do obrotu. Dz.U.2007.24.157 z dnia 2007.02.14 Status: Akt obowiązujący Wersja od: 14 lutego 2007 r. ROZPORZĄDZENIE MINISTRA ROLNICTWA I ROZWOJU WSI 1) z dnia 1 lutego 2007
Pasze lecznicze nieprzeznaczone do obrotu. Dz.U.2007.24.157 z dnia 2007.02.14 Status: Akt obowiązujący Wersja od: 14 lutego 2007 r. ROZPORZĄDZENIE MINISTRA ROLNICTWA I ROZWOJU WSI 1) z dnia 1 lutego 2007
Obrót i stosowanie produktów leczniczych przez lekarzy weterynarii przy wykonywaniu praktyki lekarsko-weterynaryjnej
 Obrót i stosowanie produktów leczniczych przez lekarzy weterynarii przy wykonywaniu praktyki lekarsko-weterynaryjnej I. Zasady ogólne Obrót produktami leczniczymi jest obrotem cywilnoprawnym, polegającym
Obrót i stosowanie produktów leczniczych przez lekarzy weterynarii przy wykonywaniu praktyki lekarsko-weterynaryjnej I. Zasady ogólne Obrót produktami leczniczymi jest obrotem cywilnoprawnym, polegającym
Safety features znakowanie produktów leczniczych spotkanie z przedstawicielami przemysłu farmaceutycznego
 Safety features znakowanie produktów leczniczych spotkanie z przedstawicielami przemysłu farmaceutycznego Anna Ryszczuk Dyrektor Departamentu Inspekcji ds. Wytwarzania Główny Inspektorat Farmaceutyczny
Safety features znakowanie produktów leczniczych spotkanie z przedstawicielami przemysłu farmaceutycznego Anna Ryszczuk Dyrektor Departamentu Inspekcji ds. Wytwarzania Główny Inspektorat Farmaceutyczny
LEKI CHEMICZNE A LEKI BIOLOGICZNE
 LEKI CHEMICZNE A LEKI BIOLOGICZNE PRODUKT LECZNICZY - DEFINICJA Art. 2 pkt.32 Ustawy - Prawo farmaceutyczne Substancja lub mieszanina substancji, przedstawiana jako posiadająca właściwości: zapobiegania
LEKI CHEMICZNE A LEKI BIOLOGICZNE PRODUKT LECZNICZY - DEFINICJA Art. 2 pkt.32 Ustawy - Prawo farmaceutyczne Substancja lub mieszanina substancji, przedstawiana jako posiadająca właściwości: zapobiegania
WNIOSEK O DOKONANIE ZMIAN W POZWOLENIU I DOKUMENTACJI DOTYCZĄCEJ WPROWADZANIA DO OBROTU PRODUKTU LECZNICZEGO
 Załącznik nr 1 WZÓR WNIOSEK O DOKONANIE ZMIAN W POZWOLENIU I DOKUMENTACJI DOTYCZĄCEJ WPROWADZANIA DO OBROTU PRODUKTU LECZNICZEGO Numer wniosku 1) : złożenia 1) :. (zaznaczyć wszystkie punkty mające zastosowanie)
Załącznik nr 1 WZÓR WNIOSEK O DOKONANIE ZMIAN W POZWOLENIU I DOKUMENTACJI DOTYCZĄCEJ WPROWADZANIA DO OBROTU PRODUKTU LECZNICZEGO Numer wniosku 1) : złożenia 1) :. (zaznaczyć wszystkie punkty mające zastosowanie)
WZÓR WNIOSEK O WYDANIE POZWOLENIA NA DOPUSZCZENIE DO OBROTU PRODUKTU LECZNICZEGO HOMEOPATYCZNEGO
 Załącznik nr 3 WZÓR WNIOSEK O WYDANIE POZWOLENIA NA DOPUSZCZENIE DO OBROTU PRODUKTU LECZNICZEGO HOMEOPATYCZNEGO Numer wniosku: Data złożenia wniosku (rrrr-mm-dd): Podpis i pieczęć pracownika: (w przypadku
Załącznik nr 3 WZÓR WNIOSEK O WYDANIE POZWOLENIA NA DOPUSZCZENIE DO OBROTU PRODUKTU LECZNICZEGO HOMEOPATYCZNEGO Numer wniosku: Data złożenia wniosku (rrrr-mm-dd): Podpis i pieczęć pracownika: (w przypadku
Katedra Technologii Postaci Leku i Biofaramcji. W zakresie wiedzy:
 Sylabus modułów kształcenia Nazwa Wydziału Nazwa jednostki prowadzącej moduł Nazwa modułu kształcenia modułu Język kształcenia Efekty kształcenia dla modułu kształcenia Typ modułu kształcenia (obowiązkowy/fakultatywny)
Sylabus modułów kształcenia Nazwa Wydziału Nazwa jednostki prowadzącej moduł Nazwa modułu kształcenia modułu Język kształcenia Efekty kształcenia dla modułu kształcenia Typ modułu kształcenia (obowiązkowy/fakultatywny)
REGULACJE PRAWNE W ZAKRESIE UŻYTKOWANIA WYROBÓW MEDYCZNYCH. Małgorzata Nowicka
 REGULACJE PRAWNE W ZAKRESIE UŻYTKOWANIA WYROBÓW MEDYCZNYCH Małgorzata Nowicka Regulacje prawne w zakresie użytkowania wyrobów medycznych znajdują się w trzech aktach prawnych: Ustawa o wyrobach medycznych
REGULACJE PRAWNE W ZAKRESIE UŻYTKOWANIA WYROBÓW MEDYCZNYCH Małgorzata Nowicka Regulacje prawne w zakresie użytkowania wyrobów medycznych znajdują się w trzech aktach prawnych: Ustawa o wyrobach medycznych
do ustawy z dnia 5 grudnia 2014 r. o zmianie ustawy Prawo farmaceutyczne oraz niektórych innych ustaw (druk nr 787)
 BIURO LEGISLACYJNE/ Materiał porównawczy M A T E R I A Ł P O R Ó W N AW C Z Y do ustawy z dnia 5 grudnia 2014 r. o zmianie ustawy Prawo farmaceutyczne oraz niektórych innych ustaw (druk nr 787) U S T A
BIURO LEGISLACYJNE/ Materiał porównawczy M A T E R I A Ł P O R Ó W N AW C Z Y do ustawy z dnia 5 grudnia 2014 r. o zmianie ustawy Prawo farmaceutyczne oraz niektórych innych ustaw (druk nr 787) U S T A
SPOSÓB PRZEDSTAWIANIA DOKUMENTACJI DOŁĄCZANEJ DO WNIOSKU O DOPUSZCZENIE DO OBROTU PRODUKTU LECZNICZEGO WETERYNARYJNEGO IMMUNOLOGICZNEGO
 Załącznik nr 2 SPOSÓB PRZEDSTAWIANIA DOKUMENTACJI DOŁĄCZANEJ DO WNIOSKU O DOPUSZCZENIE DO OBROTU PRODUKTU LECZNICZEGO WETERYNARYJNEGO IMMUNOLOGICZNEGO CZĘŚĆ I STRESZCZENIE DOKUMENTACJI I A Wniosek o dopuszczenie
Załącznik nr 2 SPOSÓB PRZEDSTAWIANIA DOKUMENTACJI DOŁĄCZANEJ DO WNIOSKU O DOPUSZCZENIE DO OBROTU PRODUKTU LECZNICZEGO WETERYNARYJNEGO IMMUNOLOGICZNEGO CZĘŚĆ I STRESZCZENIE DOKUMENTACJI I A Wniosek o dopuszczenie
Dotyczy: Zakup i dostawa opatrunków [350/100/2012]
![Dotyczy: Zakup i dostawa opatrunków [350/100/2012] Dotyczy: Zakup i dostawa opatrunków [350/100/2012]](/thumbs/56/39089645.jpg) Poznań, dnia 14-09-2012 EZ/350/100/2012/ 1172 Wg rozdzielnika Do wszystkich zainteresowanych postępowaniem o zamówienie publiczne Dotyczy: Zakup i dostawa opatrunków [350/100/2012] Wielkopolskie Centrum
Poznań, dnia 14-09-2012 EZ/350/100/2012/ 1172 Wg rozdzielnika Do wszystkich zainteresowanych postępowaniem o zamówienie publiczne Dotyczy: Zakup i dostawa opatrunków [350/100/2012] Wielkopolskie Centrum
Warszawa, dnia 3 stycznia 2014 r. Poz. 10 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 12 grudnia 2013 r.
 DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ Warszawa, dnia 3 stycznia 2014 r. Poz. 10 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 12 grudnia 2013 r. w sprawie wzoru wniosków o przedłużenie lub skrócenie okresu
DZIENNIK USTAW RZECZYPOSPOLITEJ POLSKIEJ Warszawa, dnia 3 stycznia 2014 r. Poz. 10 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 12 grudnia 2013 r. w sprawie wzoru wniosków o przedłużenie lub skrócenie okresu
z dnia 12 marca 2008 r. (Dz.U. Nr 57, poz. 347)
 Rozporządzenie Ministra Zdrowia w sprawie określenia szczegółowych zasad i trybu wstrzymywania i wycofywania z obrotu produktów leczniczych i wyrobów medycznych z dnia 12 marca 2008 r. (Dz.U. Nr 57, poz.
Rozporządzenie Ministra Zdrowia w sprawie określenia szczegółowych zasad i trybu wstrzymywania i wycofywania z obrotu produktów leczniczych i wyrobów medycznych z dnia 12 marca 2008 r. (Dz.U. Nr 57, poz.
Od czystego do sterylnego - filtracja procesowa
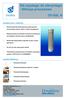 Od czystego do sterylnego - filtracja procesowa GŁÓWNE CECHY I KORZYŚCI: Wysoka zdolność zatrzymywania zanieczyszczeń przy wysokiej różnicy ciśnień i dużych przepływach Regenerowalne przy płukaniu w kierunku
Od czystego do sterylnego - filtracja procesowa GŁÓWNE CECHY I KORZYŚCI: Wysoka zdolność zatrzymywania zanieczyszczeń przy wysokiej różnicy ciśnień i dużych przepływach Regenerowalne przy płukaniu w kierunku
AKTUALNE WYMAGANIA GMP 2015 zmiany, nowości
 Firma szkoleniowa 2014 roku. TOP 3 w rankingu firm szkoleniowych zaprasza na szkolenie: AKTUALNE WYMAGANIA GMP 2015 zmiany, nowości WARSZTATY 26 października 2015 r. Centrum Konferencyjne Golden Floor,
Firma szkoleniowa 2014 roku. TOP 3 w rankingu firm szkoleniowych zaprasza na szkolenie: AKTUALNE WYMAGANIA GMP 2015 zmiany, nowości WARSZTATY 26 października 2015 r. Centrum Konferencyjne Golden Floor,
Warszawa, dnia 11 grudnia 2013 r. Poz. 1512
 Warszawa, dnia 11 grudnia 2013 r. Poz. 1512 Rozporządzenie Ministra Rolnictwa i Rozwoju Wsi 1) z dnia 27 listopada 2013 r. w sprawie pobierania próbek środków ochrony roślin do badań laboratoryjnych Na
Warszawa, dnia 11 grudnia 2013 r. Poz. 1512 Rozporządzenie Ministra Rolnictwa i Rozwoju Wsi 1) z dnia 27 listopada 2013 r. w sprawie pobierania próbek środków ochrony roślin do badań laboratoryjnych Na
Nadzór nad pracowniami chemicznymi w szkołach. Oddział Higieny Dzieci i Młodzieży Wojewódzkiej Stacji Sanitarno-Epidemiologicznej w Opolu
 Nadzór nad pracowniami chemicznymi w szkołach Uregulowania prawne: - Ustawa z dnia 25.02.2011 r. o substancjach chemicznych i ich mieszaninach (t. j. Dz. U. 2018, poz. 143) - Ustawa z dnia 26.06.1974 r.
Nadzór nad pracowniami chemicznymi w szkołach Uregulowania prawne: - Ustawa z dnia 25.02.2011 r. o substancjach chemicznych i ich mieszaninach (t. j. Dz. U. 2018, poz. 143) - Ustawa z dnia 26.06.1974 r.
Zarządzanie ryzykiem wystąpienia zanieczyszczeń krzyżowych cz. I
 Zarządzanie ryzykiem wystąpienia zanieczyszczeń krzyżowych cz. I Marek Skowronek TEVA Operations Poland Sp. z o.o. Fot.: photogenica.pl, I.E.S. International Polska Sp. z o.o Wytwarzanie i stosowanie ów
Zarządzanie ryzykiem wystąpienia zanieczyszczeń krzyżowych cz. I Marek Skowronek TEVA Operations Poland Sp. z o.o. Fot.: photogenica.pl, I.E.S. International Polska Sp. z o.o Wytwarzanie i stosowanie ów
Firma szkoleniowa 2015 roku. TOP 3 w rankingu firm szkoleniowych zaprasza na szkolenie:
 Firma szkoleniowa 2015 roku. TOP 3 w rankingu firm szkoleniowych zaprasza na szkolenie: NOWE WYMAGANIA PRAWNE DLA WYTWÓRCÓW I IMPORTERÓW PRODUKTÓW LECZNICZYCH WARSZTATY 1 kwietnia 2016 r., Centrum Konferencyjne
Firma szkoleniowa 2015 roku. TOP 3 w rankingu firm szkoleniowych zaprasza na szkolenie: NOWE WYMAGANIA PRAWNE DLA WYTWÓRCÓW I IMPORTERÓW PRODUKTÓW LECZNICZYCH WARSZTATY 1 kwietnia 2016 r., Centrum Konferencyjne
KOMISJI EUROPEJSKIEJ
 22.1.2010 Dziennik Urzędowy Unii Europejskiej C 17/1 (Komunikaty) KOMUNIKATY INSTYTUCJI, ORGANÓW I JEDNOSTEK ORGANIZACYJNYCH UN EUROPEJSKIEJ KOMISJI EUROPEJSKIEJ Komunikat Komisji wytyczne dotyczące szczegółów
22.1.2010 Dziennik Urzędowy Unii Europejskiej C 17/1 (Komunikaty) KOMUNIKATY INSTYTUCJI, ORGANÓW I JEDNOSTEK ORGANIZACYJNYCH UN EUROPEJSKIEJ KOMISJI EUROPEJSKIEJ Komunikat Komisji wytyczne dotyczące szczegółów
Załącznik nr 3 ANEKS 13 WYTWARZANIE BADANYCH PRODUKTÓW LECZNICZYCH
 Załącznik nr 3 ANEKS 13 WYTWARZANIE BADANYCH PRODUKTÓW LECZNICZYCH Reguła Badane produkty lecznicze powinny być produkowane zgodnie z zasadami oraz szczegółowymi wytycznymi Dobrej Praktyki Wytwarzania
Załącznik nr 3 ANEKS 13 WYTWARZANIE BADANYCH PRODUKTÓW LECZNICZYCH Reguła Badane produkty lecznicze powinny być produkowane zgodnie z zasadami oraz szczegółowymi wytycznymi Dobrej Praktyki Wytwarzania
DYREKTYWY. (Tekst mający znaczenie dla EOG)
 L 238/44 DYREKTYWY DYREKTYWA KOMISJI (UE) 2017/1572 z dnia 15 września 2017 r. uzupełniająca dyrektywę 2001/83/WE Parlamentu Europejskiego i Rady w odniesieniu do zasad i wytycznych dobrej praktyki wytwarzania
L 238/44 DYREKTYWY DYREKTYWA KOMISJI (UE) 2017/1572 z dnia 15 września 2017 r. uzupełniająca dyrektywę 2001/83/WE Parlamentu Europejskiego i Rady w odniesieniu do zasad i wytycznych dobrej praktyki wytwarzania
ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 30 maja 2003 r.
 Dz.U.03.105.996 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 30 maja 2003 r. w sprawie sposobu przedstawiania dokumentacji oraz wzoru wniosku o dopuszczenie do obrotu produktu homeopatycznego i produktu homeopatycznego
Dz.U.03.105.996 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 30 maja 2003 r. w sprawie sposobu przedstawiania dokumentacji oraz wzoru wniosku o dopuszczenie do obrotu produktu homeopatycznego i produktu homeopatycznego
II. Zestawienie wykonanych kontroli w roku 2015.
 II. Zestawienie wykonanych kontroli w roku 2015. Lp. Placówki podlegające nadzorowi i kontroli Plan kontroli Wykonanie kontroli Rodzaj wg stanu na dzień 31.12.2015 Ogółem w tym planowych Planowe Sprawdzające
II. Zestawienie wykonanych kontroli w roku 2015. Lp. Placówki podlegające nadzorowi i kontroli Plan kontroli Wykonanie kontroli Rodzaj wg stanu na dzień 31.12.2015 Ogółem w tym planowych Planowe Sprawdzające
wwww.shl.org.pl Wymagania merytoryczno-prawne w zakresie realizacji procesów dekontaminacji wyrobów medycznych
 Wymagania merytoryczno-prawne w zakresie realizacji procesów dekontaminacji wyrobów medycznych Sesja Warsztatowa SKSSiD Stanisław Świtalski Stare Jabłonki 04-07 października 2009 Wymagania merytoryczno-prawne
Wymagania merytoryczno-prawne w zakresie realizacji procesów dekontaminacji wyrobów medycznych Sesja Warsztatowa SKSSiD Stanisław Świtalski Stare Jabłonki 04-07 października 2009 Wymagania merytoryczno-prawne
sporządzoną zgodnie z wzorem stanowiącym załącznik nr 9 do rozporządzenia, lub
 ROZPORZĄDZENIE MINISTRA ZDROWIA z dnia 5 sierpnia 2008 r. w sprawie wzoru wniosku o wydanie zezwolenia na wytwarzanie produktów leczniczych i wzoru wniosku o wydanie zezwolenia na import produktów leczniczych
ROZPORZĄDZENIE MINISTRA ZDROWIA z dnia 5 sierpnia 2008 r. w sprawie wzoru wniosku o wydanie zezwolenia na wytwarzanie produktów leczniczych i wzoru wniosku o wydanie zezwolenia na import produktów leczniczych
Podstawy sterylizacji parą wodną
 Podstawy sterylizacji parą wodną Grzegorz Cacko Getinge Poland Sp. z o.o. Page 1 O czym będzie mowa... Sterylizacja wstęp teoretyczny Kilka słów o parze nasyconej Przebieg procesu sterylizacji parowej
Podstawy sterylizacji parą wodną Grzegorz Cacko Getinge Poland Sp. z o.o. Page 1 O czym będzie mowa... Sterylizacja wstęp teoretyczny Kilka słów o parze nasyconej Przebieg procesu sterylizacji parowej
USTAWA. z dnia 6 września 2001 r. Prawo farmaceutyczne. (tekst jednolity) Rozdział 1. Przepisy ogólne
 Dz.U.2008.45.271 2013.01.01 zm. Dz.U.2012.1342 art. 10 zm. Dz.U.2012.1544 art. 10 USTAWA z dnia 6 września 2001 r. Prawo farmaceutyczne (tekst jednolity) Rozdział 1 Przepisy ogólne Art. 1. 1. Ustawa określa:
Dz.U.2008.45.271 2013.01.01 zm. Dz.U.2012.1342 art. 10 zm. Dz.U.2012.1544 art. 10 USTAWA z dnia 6 września 2001 r. Prawo farmaceutyczne (tekst jednolity) Rozdział 1 Przepisy ogólne Art. 1. 1. Ustawa określa:
Ustawa prawo farmaceutyczne
 Ustawa prawo farmaceutyczne Ustawa z dnia 6 września 2001 r. Prawo farmaceutyczne. Ustawa opublikowana w Dzienniku Ustaw 2001 nr 126 poz. 1381. Tekst ujednolicony ustawy do pobrania w naszym dziale plików
Ustawa prawo farmaceutyczne Ustawa z dnia 6 września 2001 r. Prawo farmaceutyczne. Ustawa opublikowana w Dzienniku Ustaw 2001 nr 126 poz. 1381. Tekst ujednolicony ustawy do pobrania w naszym dziale plików
Spis treści. Wykaz skrótów. Słowo wstępne Prezesa Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych.
 Spis treści Wykaz skrótów Słowo wstępne Prezesa Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych Od Redaktora Rozdział I Rynek farmaceutyczny 1. Założenia wstępne 2.
Spis treści Wykaz skrótów Słowo wstępne Prezesa Urzędu Rejestracji Produktów Leczniczych, Wyrobów Medycznych i Produktów Biobójczych Od Redaktora Rozdział I Rynek farmaceutyczny 1. Założenia wstępne 2.
DR ŻANETA PACUD Zdolność patentowa roślin
 DR ŻANETA PACUD Zdolność patentowa roślin czyli rzecz o brokułach i pomidorach Sposoby ochrony prawnej roślin wprowadzenie Ochrona prawna odmian roślin - Międzynarodowa konwencja o ochronie nowych odmian
DR ŻANETA PACUD Zdolność patentowa roślin czyli rzecz o brokułach i pomidorach Sposoby ochrony prawnej roślin wprowadzenie Ochrona prawna odmian roślin - Międzynarodowa konwencja o ochronie nowych odmian
1. Liczba produktów leczniczych i wyrobów medycznych pobranych w ramach planowej kontroli: - 35 analiz pozytywnych - 35 w trakcie badania - 0
 III. Jakość leków. 1. Liczba produktów leczniczych i wyrobów medycznych pobranych w ramach planowej kontroli: 35 analiz pozytywnych 35 w trakcie badania 0 IV. Ustalenia kontroli oraz wydane na ich podstawie
III. Jakość leków. 1. Liczba produktów leczniczych i wyrobów medycznych pobranych w ramach planowej kontroli: 35 analiz pozytywnych 35 w trakcie badania 0 IV. Ustalenia kontroli oraz wydane na ich podstawie
Dyrektywa 98/79/WE. Polskie Normy zharmonizowane opublikowane do 31.12.2013 Wykaz norm z dyrektywy znajduje się również na www.pkn.
 Dyrektywa 98/79/WE Załącznik nr 23 Załącznik nr 23 Polskie Normy zharmonizowane opublikowane do 31.12.2013 Wykaz norm z dyrektywy znajduje się również na www.pkn.pl Według Dziennika Urzędowego UE (2013/C
Dyrektywa 98/79/WE Załącznik nr 23 Załącznik nr 23 Polskie Normy zharmonizowane opublikowane do 31.12.2013 Wykaz norm z dyrektywy znajduje się również na www.pkn.pl Według Dziennika Urzędowego UE (2013/C
2) szczegółowe zasady i sposób sprawowania nadzoru przez powiatowych lekarzy weterynarii nad obrotem paszami leczniczymi;
 ROZPORZĄDZENIE MINISTRA ROLNICTWA I ROZWOJU WSI z dnia 10 stycznia 2003 r. w sprawie nadzoru nad obrotem produktami leczniczymi weterynaryjnymi, wyrobami medycznymi przeznaczonymi wyłącznie dla zwierząt
ROZPORZĄDZENIE MINISTRA ROLNICTWA I ROZWOJU WSI z dnia 10 stycznia 2003 r. w sprawie nadzoru nad obrotem produktami leczniczymi weterynaryjnymi, wyrobami medycznymi przeznaczonymi wyłącznie dla zwierząt
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO 1/18
 ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO 1/18 1. NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO Nobivac Piro 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY PRODUKTU LECZNICZEGO W dawce 1 ml: Substancja
ANEKS I CHARAKTERYSTYKA PRODUKTU LECZNICZEGO WETERYNARYJNEGO 1/18 1. NAZWA PRODUKTU LECZNICZEGO WETERYNARYJNEGO Nobivac Piro 2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY PRODUKTU LECZNICZEGO W dawce 1 ml: Substancja
Wytwarzanie wyrobów sterylnych w szpitalu w świetle aktualnych przepisów. Mgr Jarosław Czapliński Wojewódzki Szpital Zespolony w Elblągu
 Wytwarzanie wyrobów sterylnych w szpitalu w świetle aktualnych przepisów. Mgr Jarosław Czapliński Wojewódzki Szpital Zespolony w Elblągu HISTORIA - PRL Produkcja opatrunków podstawy prawne. Ustawa z dnia
Wytwarzanie wyrobów sterylnych w szpitalu w świetle aktualnych przepisów. Mgr Jarosław Czapliński Wojewódzki Szpital Zespolony w Elblągu HISTORIA - PRL Produkcja opatrunków podstawy prawne. Ustawa z dnia
Audity w branży farmaceutycznej Elżbieta Bętkowska-Ożóg
 Audity w branży farmaceutycznej Elżbieta Bętkowska-Ożóg Ożarów Mazowiecki, 15 listopada 2016 roku Audity WYMAGANIA NORMY PN-EN ISO 19011:2011 Wytyczne dotyczące auditowania systemów zarządzania ISO 9000
Audity w branży farmaceutycznej Elżbieta Bętkowska-Ożóg Ożarów Mazowiecki, 15 listopada 2016 roku Audity WYMAGANIA NORMY PN-EN ISO 19011:2011 Wytyczne dotyczące auditowania systemów zarządzania ISO 9000
DYREKTYWA KOMISJI (UE) / z dnia r.
 KOMISJA EUROPEJSKA Bruksela, dnia 15.9.2017 r. C(2017) 6127 final DYREKTYWA KOMISJI (UE) / z dnia 15.9.2017 r. uzupełniająca dyrektywę 2001/83/WE Parlamentu Europejskiego i Rady w odniesieniu do zasad
KOMISJA EUROPEJSKA Bruksela, dnia 15.9.2017 r. C(2017) 6127 final DYREKTYWA KOMISJI (UE) / z dnia 15.9.2017 r. uzupełniająca dyrektywę 2001/83/WE Parlamentu Europejskiego i Rady w odniesieniu do zasad
ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 2 kwietnia 2010 r.
 Dziennik Ustaw Nr 82 6988 Poz. 538 538 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 2 kwietnia 2010 r. w sprawie sposobu przedstawiania dokumentacji dołączanej do wniosku o dopuszczenie do obrotu produktu
Dziennik Ustaw Nr 82 6988 Poz. 538 538 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 2 kwietnia 2010 r. w sprawie sposobu przedstawiania dokumentacji dołączanej do wniosku o dopuszczenie do obrotu produktu
1. Jestem posiadaczem pozwolenia na dopuszczenie do obrotu z siedzibą w Zjednoczonym Królestwie. Co należy zrobić?
 KOMISJA EUROPEJSKA DYREKCJA GENERALNA DS. ZDROWIA I BEZPIECZEŃSTWA ŻYWNOŚCI Rev 04, 1 lutego 2019 r. Pytania i odpowiedzi w kontekście wystąpienia Zjednoczonego Królestwa z Unii Europejskiej dotyczące
KOMISJA EUROPEJSKA DYREKCJA GENERALNA DS. ZDROWIA I BEZPIECZEŃSTWA ŻYWNOŚCI Rev 04, 1 lutego 2019 r. Pytania i odpowiedzi w kontekście wystąpienia Zjednoczonego Królestwa z Unii Europejskiej dotyczące
W całym aneksie, jeżeli inaczej nie określono produkt leczniczy roślinny zawiera tradycyjny roślinny produkt leczniczy.
 Załącznik nr 3 ANEKS 7 WYTWARZANIE PRODUKTÓW LECZNICZYCH ROŚLINNYCH Reguła Kontrola materiałów wyjściowych, sposób ich przechowywania i przetwarzania ma ogromne znaczenie w wytwarzaniu produktów leczniczych
Załącznik nr 3 ANEKS 7 WYTWARZANIE PRODUKTÓW LECZNICZYCH ROŚLINNYCH Reguła Kontrola materiałów wyjściowych, sposób ich przechowywania i przetwarzania ma ogromne znaczenie w wytwarzaniu produktów leczniczych
22. Międzynarodowy Kongres Ogólnopolskiego Systemu Ochrony Zdrowia "Innowacyjna Ochrona Zdrowia".
 22. Międzynarodowy Kongres Ogólnopolskiego Systemu Ochrony Zdrowia "Innowacyjna Ochrona Zdrowia". KATOWICE 4-5 KWIETNIA 2017 Radca Prawny Krystian Szulc Śląska Izba Aptekarska Prawne aspekty obrotu produktem
22. Międzynarodowy Kongres Ogólnopolskiego Systemu Ochrony Zdrowia "Innowacyjna Ochrona Zdrowia". KATOWICE 4-5 KWIETNIA 2017 Radca Prawny Krystian Szulc Śląska Izba Aptekarska Prawne aspekty obrotu produktem
ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 12 marca 2008 r.
 ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 12 marca 2008 r. w sprawie określenia szczegółowych zasad i trybu wstrzymywania i wycofywania z obrotu produktów leczniczych i wyrobów medycznych (Dz. U. z dnia
ROZPORZĄDZENIE MINISTRA ZDROWIA 1) z dnia 12 marca 2008 r. w sprawie określenia szczegółowych zasad i trybu wstrzymywania i wycofywania z obrotu produktów leczniczych i wyrobów medycznych (Dz. U. z dnia
USTAWA z dnia 6 września 2001 r. Prawo farmaceutyczne. Rozdział 1 Przepisy ogólne
 Kancelaria Sejmu s. 1/132 USTAWA z dnia 6 września 2001 r. Prawo farmaceutyczne Rozdział 1 Przepisy ogólne Art. 1. 1. Ustawa określa: 1) zasady i tryb dopuszczania do obrotu produktów leczniczych, z uwzględnieniem
Kancelaria Sejmu s. 1/132 USTAWA z dnia 6 września 2001 r. Prawo farmaceutyczne Rozdział 1 Przepisy ogólne Art. 1. 1. Ustawa określa: 1) zasady i tryb dopuszczania do obrotu produktów leczniczych, z uwzględnieniem
USTAWA. z dnia 13 września 2002 r. o produktach biobójczych. (Dz. U. z dnia 21 października 2002 r.) [wyciąg] Rozdział 1.
![USTAWA. z dnia 13 września 2002 r. o produktach biobójczych. (Dz. U. z dnia 21 października 2002 r.) [wyciąg] Rozdział 1. USTAWA. z dnia 13 września 2002 r. o produktach biobójczych. (Dz. U. z dnia 21 października 2002 r.) [wyciąg] Rozdział 1.](/thumbs/24/2454590.jpg) Dz.U.02.175.1433 z późn. zm. USTAWA z dnia 13 września 2002 r. o produktach biobójczych. (Dz. U. z dnia 21 października 2002 r.) [wyciąg] Rozdział 1 Przepisy ogólne Art. 1. 1. Ustawa określa warunki wprowadzania
Dz.U.02.175.1433 z późn. zm. USTAWA z dnia 13 września 2002 r. o produktach biobójczych. (Dz. U. z dnia 21 października 2002 r.) [wyciąg] Rozdział 1 Przepisy ogólne Art. 1. 1. Ustawa określa warunki wprowadzania
Dz.U. 2001 Nr 126 poz. 1381. Prawo farmaceutyczne. Rozdział 1 Przepisy ogólne
 Kancelaria Sejmu s. 1/131 Dz.U. 2001 Nr 126 poz. 1381 USTAWA z dnia 6 września 2001 r. Prawo farmaceutyczne Rozdział 1 Przepisy ogólne Art. 1. 1. Ustawa określa: 1) zasady i tryb dopuszczania do obrotu
Kancelaria Sejmu s. 1/131 Dz.U. 2001 Nr 126 poz. 1381 USTAWA z dnia 6 września 2001 r. Prawo farmaceutyczne Rozdział 1 Przepisy ogólne Art. 1. 1. Ustawa określa: 1) zasady i tryb dopuszczania do obrotu
Nowe obowiązki dla przedsiębiorców. -wdrażanie dyrektywy fałszywkowej
 1 Ewa Warmińska Nowe obowiązki dla przedsiębiorców -wdrażanie dyrektywy fałszywkowej Akty prawne Dyrektywa Parlamentu Europejskiego i Rady 2011/62/UE z dnia 8 czerwca 2011 r. zmieniająca dyrektywę 2001/83/WE
1 Ewa Warmińska Nowe obowiązki dla przedsiębiorców -wdrażanie dyrektywy fałszywkowej Akty prawne Dyrektywa Parlamentu Europejskiego i Rady 2011/62/UE z dnia 8 czerwca 2011 r. zmieniająca dyrektywę 2001/83/WE
